一种肿瘤靶向多肽、多肽偶联药物及其应用的制作方法
1.本发明涉及癌症治疗,特别是胰腺癌和三阴性乳腺癌的治疗过程中所涉及的产品领域,具体涉及一种肿瘤靶向多肽、多肽偶联药物及其应用。
背景技术:
2.2021年初,世界卫生组织国际癌症研究机构(iarc)发布了2020年全球最新癌症负担数据。2020年全球男性新发癌症1007万例,而女性新发癌症923万例。根据数据显示,中国新发癌症人数及癌症死亡人数均位居全球第一。
3.目前,癌症的治疗方法,主要有手术治疗、化疗、放疗等,其中化疗是目前治疗癌症主要手段之一。但是在治疗的过程中,患者存在明显的恶心、呕吐、脱发、消瘦等副作用,给患者带来很大的不适感。
4.目前用于癌症化疗的小分子药物,往往在杀伤肿瘤细胞的同时,也会杀伤大量的人体正常细胞,导致患者的免疫力快速下降,毒副作用大。
5.相比于小分子药物,目前正在兴起的单抗药物在癌症治疗方面无疑具有靶向性强的优点。但是,与传统的小分子药物相比,抗体药物的靶点数量相对较少,限制了其在各类疾病治疗中的应用。
6.多肽分子量相对较小,相比于抗体药物,在生产制造过程中,不仅成本较低,而且获得的产品纯度比抗体药物要高很多,相应的药物副作用也比较小,同时生产成本要远远低于抗体药物。多肽药物组织渗透性更强,联合抗癌药物用于肿瘤靶向治疗,具有更好药物靶向传递途径和疗效。目前多肽偶联药物已经成为肿瘤靶向治疗一个新的研究热点。
7.肿瘤靶向肽(tumor homing peptides,thps)是指能够特异的结合到肿瘤细胞和肿瘤血管的多肽,通常是由5~31个氨基酸构成的分子量很小的活性肽。小分子多肽具有如下优点:与抗体相比,克服了抗体会存在异源性问题;分子量较小,易通过生理屏障,有效渗透组织,亲和力高,确保可以高效的浓聚配体;易化学合成,成本低。
8.吉西他滨、紫杉醇、阿霉素是目前癌症治疗较为常用的化疗药物。但是因为没有实现靶向性治疗,本身对正常细胞的损害较大,因此用药量受到了很大的限制,患者的耐药性以及治疗效果也均不是很理想。
技术实现要素:
9.为了解决现有技术中的不足,本发明的主要目的是提供一种肿瘤靶向多肽、多肽偶联药物及其应用。
10.本发明第一方面提供一种肿瘤靶向多肽,其多肽序列为:
11.x-arg-arg-arg-arg-arg-arg-arg-arg-d-glu-peg
4-cyclo(lys-arg-gly-asp-d-phe),所述d-phe-主链羧基与lys主链氨基形成酰胺环,peg4与lys侧链氨基连接;
12.其中,x表示氨基酸残基为cys或者没有。
13.本发明第二方面提供所述肿瘤靶向多肽在制备多肽偶联药物中的应用。
14.本发明第三方面提供一种多肽偶联药物,其包括所述肿瘤靶向多肽、细胞毒性药物和连接子,所述连接子将所述肿瘤靶向多肽与所述细胞毒性药物相连接。
15.进一步地,所述细胞毒性药物为肿瘤化疗药物;
16.优选地,所述肿瘤化疗药物为吉西他滨、阿霉素或紫杉醇。
17.进一步地,所述连接子为琥珀酰亚胺-4-(n-马来酰亚胺)环已烷-1-1羟酸酯或γ-氨基丁酸。
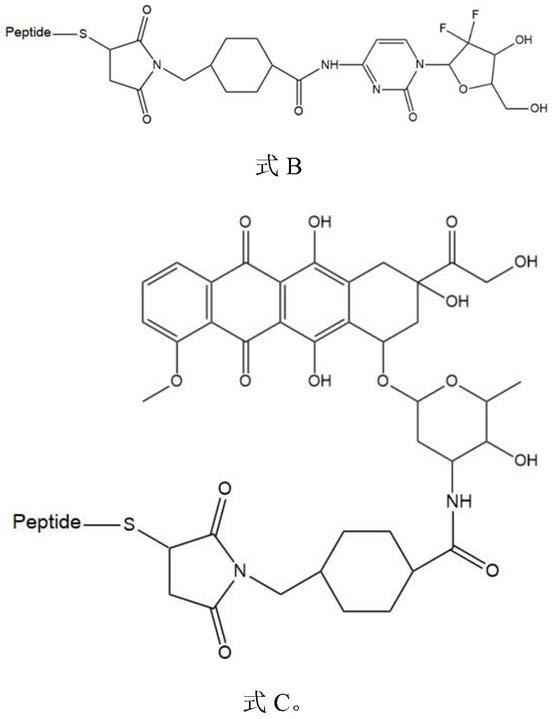
18.进一步地,所述多肽偶联药物具有如式a、b或c所示结构:
19.其中,peptide表示权利要求1所述肿瘤靶向多肽;
20.[0021][0022]
本发明提供所述多肽偶联药物的制备方法,包括如下步骤:
[0023]
(1)采用fmoc固相多肽合成技术,将fmoc-asp-odmab偶联到wang树脂上,然后依次偶联fmoc-gly-oh、fmoc-arg(pbf)-oh、fmoc-lys(alloc)-oh、fmoc-d-phe-oh,偶联完成后,脱除asp残基主链的dmab保护基团,加入缩合剂,完成环化反应;
[0024]
(2)步骤(1)环化反应完成后,进行步骤2-a或2-b
[0025]
步骤2-a:脱除lys侧链的alloc保护基团,然后依次偶联fmoc-peg
4-ch2ch
2-cooh、fmoc-d-glu(otbu)-oh、8个fmoc-arg(pbf)-oh,得到arg-arg-arg-arg-arg-arg-arg-arg-d-glu-peg
4-cyclo(lys-arg-gly-asp-d-phe)(d-phe-主链羧基与lys主链氨基形成酰胺环,peg4与lys侧链氨基连接)的肽树脂;
[0026]
步骤2-b:脱除lys侧链的alloc保护基团,然后依次偶联fmoc-peg
4-ch2ch
2-cooh、fmoc-d-glu(otbu)-oh、8个fmoc-arg(pbf)-oh,boc-cys(stbu)-oh,偶联完成后,脱除cys残基侧链的stbu保护基团,得到cys侧链裸露的cys-arg-arg-arg-arg-arg-arg-arg-arg-d-glu-peg
4-cyclo(lys-arg-gly-asp-d-phe)(d-phe-主链羧基与lys主链氨基形成酰胺环,peg4与lys侧链氨基连接)的肽树脂;
[0027]
(3)使用连接子将步骤(2)得到的肽树脂与细胞毒性药物相连接,得到多肽偶联药物树脂,用tfa裂解多肽偶联药物树脂,经过纯化,即得所述多肽偶联药物。
[0028]
进一步地,所述细胞毒性药物为紫杉醇时,步骤(3)中所述多肽偶联药物树脂的制备具体为:在步骤2-a所得肽树脂上偶联fmoc-γ-氨基丁酸,然后加入氯甲酸-4-硝基苯酯反应完成酰化,然后加入dmap和紫杉醇,偶联反应,得到所述多肽偶联药物树;
[0029]
所述细胞毒性药物为吉西他滨或阿霉素时,步骤(3)中所述多肽偶联药物树脂的
resin共26克,检测替代度为0.25mmol/g。
[0047]
然后称取上述fmoc-asp-odmab-wang resin共16克(4mmol),根据fmoc固相多肽合成的常规方法,按照序列依次偶联fmoc-gly-oh、fmoc-arg(pbf)-oh、fmoc-lys(alloc)-oh、fmoc-d-phe-oh,脱除fmoc-d-phe-oh上的fmoc保护基团。
[0048]
偶联完成后,用5%水合肼的dmf溶液,脱除asp残基主链羧基上的dmab保护基团。然后用加入hatu/hoat/diea(4mmol/4.8mmol/6.0mmol),在dmf中反应4小时,在固相上完成相应的环化反应。
[0049]
上述环化完成的肽树脂,用dcm清洗3次。称取2.6克的二甲胺硼烷,量取80ml的dcm,加入反应柱中,反应10分钟之后,加入0.2克的pd0(ph3p)4,反应2小时。然后用dcm清洗3次树脂,用0.2m铜试剂的dmf溶液清洗肽树脂30分钟,dmf清洗树脂3次,再用dcm清洗树脂3次,得到选择性脱除alloc的肽树脂。
[0050]
上述脱除alloc的肽树脂,按照fmoc固相多肽合成的标准方法,依次偶联fmoc-peg
4-ch2ch
2-cooh、fmoc-d-glu(otbu)-oh,然后再依次偶联8个fmoc-arg(pbf)-oh,脱除fmoc保护基团,用甲醇清洗肽树脂10分钟,真空干燥4小时,得到干燥的h-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-d-glu(otbu)-peg
4-cyclo(lys-arg(pbf)-gly-asp-d-phe)-wang resin(其中:d-phe-主链羧基与lys主链氨基形成酰胺环;peg4与lys侧链氨基连接;wang resin与asp侧链羧基连接)的肽树脂20.8g,备用。
[0051]
实施例2:多肽序列的合成(x为cys)
[0052]
通过实施例1得到肽树脂,称取10.4g(三分之二,2mmol)加入固相反应柱中,加入dmf溶胀30分钟,然后按照fmoc固相肽合成的标准方法,继续偶联boc-cys(stbu)-oh,偶联完成后,加入含有10mmol(5eq)三丁基膦的dmf溶液,反应1小时,选择性脱除cys残基侧链的stbu保护基团,dmf清洗5次后,用甲醇清洗10分钟,真空干燥4小时,得到cys侧链巯基裸露的boc-cys-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-arg(pbf)-d-glu(otbu)-peg
4-cyclo(lys-arg(pbf)-gly-asp-d-phe)-wang resin(其中:d-phe-主链羧基与lys主链氨基形成酰胺环;peg4与lys侧链氨基连接;wang resin与asp侧链羧基连接)的肽树脂共10.8g,备用。
[0053]
实施例3:紫杉醇(ptx)与多肽的偶联
[0054]
称取实施例1得到的肽树脂5.2g(1mmol),加入带有夹套的固相反应柱,dmf溶胀树脂30分钟之后,按照fmoc固相多肽合成的标准方法,继续在树脂上偶联fmoc-gaba-oh(fmoc-γ-氨基丁酸),脱除fmoc保护基团,然后加入dmf溶剂,加入5mmol(5eq)的4-nitrophenyl chloroformate(氯甲酸-4-硝基苯酯),加入2ml的吡啶,通过夹套加热反应温度到60℃,相反应6小时,dmf清洗树脂5次。
[0055]
上述清洗后的肽树脂,加入12mmol的hobt(12eq)、1mol的dmap(1eq)、15mmol的dic(15eq)和10mmol的紫杉醇(10eq),加入dcm作为反应溶剂,室温下反应4小时,得到紫杉醇与多肽序列偶联的肽树脂6.8g。
[0056]
将上述6.8克肽树脂加入到100ml单口烧瓶中,预先配制裂解液140ml的tfa:tis:edt:phoh:h2o=90:3:3:2:2(体积比),将裂解液加入到烧瓶中,室温反应2.5小时,滤掉树脂,滤液加入到14000ml无水乙醚中析出白色固体,离心,无水乙醚洗涤固体,真空干燥的到
白色固体的多肽偶联药物a的粗品3.23克。多肽偶联药物a,结构如下:
[0057][0058]
合成得到的多肽偶联药物a的粗品3.23g,采用hplc纯化得到相应的纯品。
[0059]
多肽偶联药物a纯品的ms分析谱图和hplc分析谱图如图1和2。
[0060]
实施例4:吉西他滨(gem)与多肽的偶联
[0061]
在四氢呋喃溶剂中,加入3.35g(10mmol)琥珀酰亚胺-4-(n-马来酰亚胺)环已烷-1-1羟酸酯(smcc),使用三乙胺调节反应液的ph值为7.0,然后逐滴加入含有1.58g(6mmol)吉西他滨的dmf溶液,1小时滴加完成,继续反应1小时,停止反应,重结晶后得到smcc与吉西他滨偶联的化合物1,结构如下:
[0062][0063]
称取实施例2合成得到的肽树脂5.4g(1mmol)与固相反应柱中,dmf溶胀30分钟,然后加入上述得到的化合物1,加入dmf作为反应溶剂,用三乙胺调节ph值为7.6,室温下反应4小时,完成化合物1与肽序中cys侧链巯基的反应,dmf清洗树脂5次之后,甲醇清洗树脂10分钟,真空干燥4小时,得到多肽偶联药物b的肽树脂5.82g。
[0064]
将上述5.82克肽树脂加入到100ml单口烧瓶中,预先配制裂解液120ml的tfa:tis:edt:phoh:h2o=90:3:3:2:2(体积比),将裂解液加入到烧瓶中,室温反应2.5小时,滤掉树脂,滤液加入到12000ml无水乙醚中析出白色固体,离心,无水乙醚洗涤固体,真空干燥的到白色固体的多肽偶联药物b的粗品2.76克。多肽偶联药物b,结构如下:
[0065][0066]
合成得到的多肽偶联药物b的粗品2.76g,采用hplc纯化得到相应的纯品。
[0067]
多肽偶联药物b纯品的ms分析谱图和hplc分析谱图如图3和4。
[0068]
实施例5:阿霉素(dox)与多肽的偶联
[0069]
采用与实施例4完全相同的方法,在液相中完成smcc与阿霉素的偶联;得到的化合物2结构如下:
[0070][0071]
然后采用与实施例4完全相同的方法得到2.97g多肽偶联药物c,结构如下:
[0072]
[0073]
合成得到的多肽偶联药物c的粗品2.97g,采用hplc纯化得到相应的纯品。
[0074]
多肽偶联药物c纯品的ms分析谱图和hplc分析谱图如图5和6。
[0075]
实施例6:fitc-多肽与癌细胞特异性靶向结合能力的体外鉴定
[0076]
fitc-多肽的合成:实施例1得到的肽树脂,按照固相fmoc多肽合成的标准合成以及裂解方法,继续偶联fmoc-ahx-oh(fmoc-6-氨基己酸),然后偶联荧光标记fitc,用tfa裂解后,用hplc纯化,得到完成荧光标记的多肽序列:fitc-ahx-arg-arg-arg-arg-arg-arg-arg-arg-d-glu-peg
4-cyclo(lys-arg-gly-asp-d-phe)(d-phe-主链羧基与lys主链氨基形成酰胺环,peg4与lys侧链氨基连接)。
[0077]
将正常胰腺导管上皮细胞pc-1、正常乳腺细胞bc-1,胰腺癌细胞pcc-1、pcc-2,三阴性乳腺癌细胞tnbcc-1、tnbcc-2(内部命名)细胞铺于带有载玻片的24孔板中,放入细胞孵化箱培养细胞贴壁并铺满单层。24小时后,弃去培养基用pbs洗3次,每次5min。4%多聚甲醛固定10min。pbs洗2次,每次5min。用含0.5%的triton x-100的pbs透化10min。pbs洗2次,每次3min。加3%bsa封闭,室温静置20min。加入3μm的fitc-多肽,37℃静置15min。pbs洗2次,每次3min。加入dab染液,37度静置15min。将24孔板中的载玻片取出,倒扣在加有抗荧光淬灭封片剂的载玻片上,通过激光共聚焦显微镜定位fitc-多肽偶联药物在细胞的位置,并鉴定胰腺癌细胞的特异性靶向作用。
[0078]
上述检测的结果显示,在pcc-1、pcc-2和tnbcc-1、tnbcc-2细胞上观察到强荧光信号,而在pc-1、bc-1细胞上检测到较弱的荧光信号。检测结果说明上述多肽有较强的胰腺癌和三阴性乳腺癌特异性靶向作用。
[0079]
实施例7:在动物模型上进行多肽偶联药物a的抗肿瘤药效测定
[0080]
(1)构建裸鼠三阴性乳腺癌动物模型,具体操作方式为:将三阴性乳腺癌细胞tnbcc-1通过皮下注射进入裸鼠皮下(每支注射数量为4
×
108个),总共24只裸鼠。
[0081]
(2)待肿瘤长大只150mm3左右,把裸鼠分为3组,每组8只。
[0082]
(3)分别对每组老鼠进行为静脉给药,给药剂量为1.0mg/kg。每周一次,连续4周。每组分别注射药物为:多肽偶联药物a、紫杉醇、空白对照溶剂。其中,所述空白溶剂与多肽偶联药物a和紫杉醇的溶剂相同,具体为含10%丙二醇的生理盐水。
[0083]
(4)每周两次测量肿瘤大小和裸鼠模型体重,统计结果参见表1和表2。
[0084]
表1:多肽偶联药物a药效测定肿瘤大小变化表
[0085][0086]
表2:多肽偶联药物a药效测定裸鼠模型体重变化表
[0087][0088]
从表1的数据可以看出,多肽偶联药物a对皮下移植三阴性乳腺癌细胞(tnbcc-1)的裸鼠模型具有明显的肿瘤生长抑制作用。说明多肽偶联药物a具有明显的抗肿瘤活性。
[0089]
从表2可以看出,在相同的给药剂量下,单纯注射紫杉醇,裸鼠样本体重下降较为迅速,并且后期全部死亡。而多肽偶联药物a的样本小鼠体重下降缓慢,基本没有太大下降,这说明多肽偶联药物a具有较低的毒副作用。
[0090]
实施例8:在动物模型上进行多肽偶联药物b和c的抗肿瘤药效测定
[0091]
(1)构建裸鼠胰腺癌动物模型,具体操作方式为:将胰腺癌细胞pcc-1通过皮下注射进入裸鼠皮下(每支注射数量为4
×
108个),总共24只裸鼠。
[0092]
(2)待肿瘤长大只150mm3左右,把裸鼠分为3组,每组8只。
[0093]
(3)分别对每组老鼠进行为静脉给药,给药剂量为1.0mg/kg。每周一次,连续4周。每组分别注射药物为:多肽偶联药物b、多肽偶联药物c、空白对照溶剂。其中,所述空白溶剂与多肽偶联药物b和多肽偶联药物c的溶剂相同,具体为含10%丙二醇的生理盐水。
[0094]
(4)每周两次测量肿瘤大小和裸鼠模型体重,统计结果参见表3和表4。
[0095]
表3:多肽偶联药物b和c药效测定肿瘤大小变化表
[0096][0097]
表4:多肽偶联药物a药效测定裸鼠模型体重变化表
[0098][0099]
从表3的数据可以看出,多肽偶联药物b和多肽偶联药物c对皮下移植胰腺癌细胞(pcc-1)的裸鼠模型具有明显的肿瘤生长抑制作用。说明多肽偶联药物b和多肽偶联药物c均具有明显的抗肿瘤活性。
[0100]
从表4可以看出,在相同的给药剂量下,多肽偶联药物b的样本小鼠体重下降缓慢,基本没有太大下降,这说明多肽偶联药物b具有较低的毒副作用。而多肽偶联药物c的样本小鼠体重下降比b要快一些,说明药物c比药物b具有稍微高的毒副作用,但是从整体体重下降情况下,仍处于可以接受的范围内。
[0101]
实施例9:癌细胞对多肽偶联药物的耐药性
[0102]
将多肽偶联药物a、b、c分别对癌细胞进行耐药性实验,实验方法为本领域常规的
一些实验方法,结果显示该肽具有不诱导快速的耐药过程。
[0103]
以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明的内容进行一些稍微的变更,或直接或间接运用在相关的技术领域,均同理包括在本发明的专利保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1