一种橙红光长余辉荧光粉及其制备方法与流程
本发明涉及荧光粉,尤其是涉及一种橙红光长余辉荧光粉及其制备方法。
背景技术:
长余辉材料作为一种储能材料,具有能够在激发光源停止以后持续发光的特性而被人们广泛关注,自20世纪末被研究者关注并研究以来,蓝色和绿色长余辉材料得到了较好的发展,并且大都以铝酸盐作为基质为主。比如商用的蓝色长余辉(CaAl2O4:Eu2+,Nd3+)和绿色长余辉(SrAl2O4:Eu2+,Dy3+)材料的余辉时间都能够超过10h(参照文献1和2)。而更长波长的长余辉材料,如红光以及红外光的长余辉材料则相对种类较少,并且长余辉发光性能相对较差,再者由于红光以及红外光长余辉材料近年来在生物成像等方面表现出了强有力的竞争力。所以开发和研制长波长的长余辉材料具有重要意义。
从发光原理上来讲,想要得到红色长余辉发光材料,激活离子一般可以为Eu2+,Eu3+,Pr3+和Cr3+等。比如文献3报道的Eu2+激活的CaS材料,在紫外光照射储能之后,能够表现出峰值为650nm的持续红光余辉性质。再如文献4中报道的在Y2O2S:Eu3+,Ti4+,Mg2+中同样能够得到长余辉为Eu3+的特征发射的长余辉现象。在文献5中,峰值为611nm红光长余辉现象可在La2Ti2O7:Pr3+中实现,并且余辉时间能够超过1h。以上均为稀土离子掺杂的红色长余辉材料。近年来,过渡金属激活的红光长余辉发光材料同样得到了一些的发展,且在生物光学成像等领域得到了一定的应用,如文献6中得到的红光长余辉材料Zn3Ga2Ge2O10:Cr3+,在紫外光(254nm)照射之后,能够表现出Cr3+特征发射的长余辉性质。尽管有部分红色长余辉材料得到了一些发展,但还是种类相对缺乏,再者由于如文献3和4中分别报道的Y2O2S:Eu3+,Ti4+,Mg2+和CaS:Eu2+红光长余辉材料都属于硫化物,而耐水性差和不稳定的性质制约其发展。因此开发性质稳定的长余辉发光材料具有重要意义。而氮氧化物作为发光材料通常表现出优异的稳定性。此外,开发新的发光中心的红光长余辉材料对于长余辉发光材料的发展也很重要,而以Yb2+作为发光中心的长余辉发光材料的专利文献则很少有报道。
参考文献:
1:Koen Van den Eeckhout,Philippe F.Smet,Dirk Poelman,Materials,Vol.3,No.4,2536-2566,2010.
2:T.Matsuzawa,Y.Aoki,N.Takeuchi,Y.Murayama,Journal of the Electrochemical Society,Vol.143,No.8,2670-2673,1996.
3:Philippe F.Smet,Iwan Moreels,Zeger Hens,Dirk Poelman,Materials,Vol.3,No.4,2834-2883,2010.
4:Chia-Cheng Kang,Ru-Shi Liu,Jiin-Chyuan Chang,Biing-Jye Lee,Chemistry of Materials,Vol.15,No.21,3966-3968,2003.
5:Ming-Hui Chu,Da-Peng Jiang,Cheng-Jiu Zhao,Bin Li,Chinese Physics Letters,Vol.27,No.4,047203-1-047203-4,2010.
6:Zhengwei Pan,Yi-Ying Lu,Feng Liu,Nature Materials,Vol.11,No.1,58-63,2012.
技术实现要素:
本发明的目的是提供简单、效率高且有利于工业化生产的适用于白光LED和太阳能电池的一种橙红光长余辉荧光粉及其制备方法。
所述橙红光长余辉荧光粉的结构式如下:
M1-x-yAlSi5O2N7:Ybx,Lny;
其中,0.001≤x≤0.1,0≤y≤0.1;M至少包含Ba,以及Mg、Ca、Sr、Ba等中的至少一种;Ln是Pr、Nd、Sm、Gd、Tb、Dy、Ho、Er、Tm等中的至少一种。
所述橙红光长余辉荧光粉的制备方法如下:
将M前驱体、Yb前驱体、Ln前躯体、Al前驱体与Si前驱体在还原气氛中于1200~1800℃下煅烧;或
先在还原气氛下烧结得到Yb2+和Ln3+掺杂的M金属的硅酸盐化合物,再与Si前驱体和Al前驱体在还原气氛下于1200~1800℃再次烧结。
所述M前驱体可选自M的碳酸盐、M的氧化物、M的草酸盐与M的硝酸盐等中的至少一种;
所述Yb前驱体可选自Yb的碳酸盐、Yb的氧化物、Yb的草酸盐与Yb的硝酸盐等中的至少一种;
所述Ln前驱体可选自Ln的碳酸盐、Ln的氧化物、Ln的草酸盐与Ln的硝酸盐等中的至少一种;
所述Al前驱体可选自Al的氧化物与Al的硝酸盐等中的至少一种;
所述Si前驱体可选自Si的氧化物、Si的氮化物等中的至少一种;
所述还原气氛可选自氨气或氮氢混合气体。
所述先在还原气氛下烧结的温度可为1200~1800℃,烧结的时间可为3~15h。
本发明提供了一种橙红光长余辉材料及其制备方法。该长余辉荧光粉具有全新的化学组成,以Yb2+作为激活剂。通过三价稀土离子的掺杂可以提高M1-x-yAlSi5O2N7:Yb2+的余辉强度和时间。该荧光粉能被200~480nm波长范围内的光激发而发射出峰值波长位于615~625nm范围的橙红光,停止该波段的激发光照后,能够产生长余辉发光,从而使该荧光材料可存储紫外光及紫蓝光转化为橙红光。本发明提供的长余辉荧光粉制备方法简单、化学性能稳定,适用于白光LED、太阳能电池或者生物标记的应用场景。
附图说明
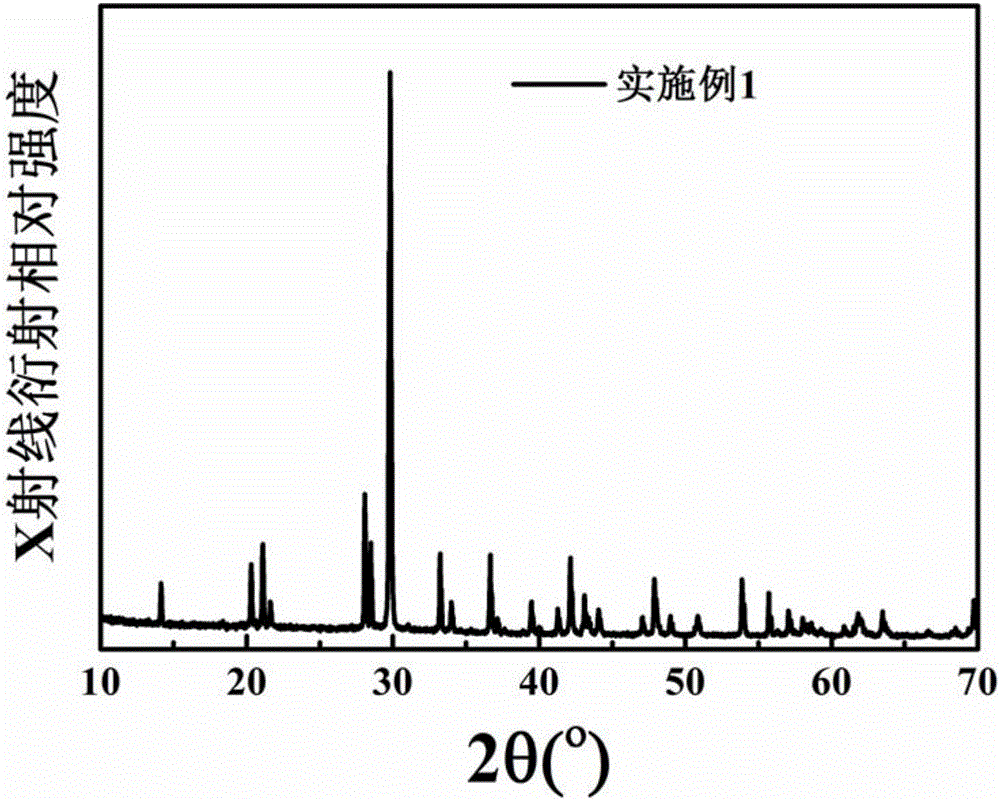
图1为本发明实施例1中得到的长余辉发光材料的X射线衍射图谱;
图2为本发明实施例2中得到的长余辉发光材料在300nm激发下的光致发光谱图;
图3为本发明实施例2中得到的长余辉发光材料在254nm激发停止后不同时间的长余辉发射光谱图;
图4是通过实施例1和实施例8获得的长余辉发光材料,经过254nm紫外线照射2min后,测得的长余辉衰减曲线。
具体实施方式
下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,以下实施例仅是本发明的部分实施例。
实施例1
按照BaCO3(分析纯)、SiO2(分析纯)和Yb2O3(分析纯)摩尔比为1.94︰1︰0.03,分别取料将上述原料研磨混匀、干燥后再装入刚玉坩埚,在高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1300℃烧结3h,随炉冷却到室温,得到Yb2+掺杂的Ba2SiO4前驱体材料。然后将此前躯体与Si3N4和AlN按照摩尔比为1︰3︰2的量混合,研磨混匀、干燥后再装入氮化硼坩埚中,放入高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1600℃烧结6h,随炉冷却到室温取出后研磨后得到所需的长余辉发光材料。
利用X射线衍射对实施例1中得到的材料进行分析,得到其X射线衍射图谱,如图1所示。在国际晶体学数据库中查询,确认此图谱与属于正交晶系空间群为Imm2的且化学组成为BaAlSi5O2N7的标准图谱(ICSD 240276)一致,没有观察到明显的杂峰。
利用荧光光谱仪对实施例1中得到的荧光材料进行分析,在300nm紫外光激发下的发射峰位于615nm,在254nm紫外光激发下,能够表现出长余辉发光特性。可见该荧光粉能被紫外光激发而发射橙红光,从而使该荧光材料可将紫外光转化为橙红光。
实施例2
按照BaCO3(分析纯)、SrCO3(分析纯)、SiO2(分析纯)和Yb2O3(分析纯)摩尔比为1.54︰0.4︰1︰0.03,分别取料将上述原料研磨混匀、干燥后再装入刚玉坩埚,在高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1300℃烧结3h,随炉冷却到室温,得到Yb2+掺杂的Ba1.6Sr0.4SiO4前驱体材料。然后将此前躯体与Si3N4和AlN按照摩尔比为1︰3︰2的量混合,研磨混匀、干燥后再装入氮化硼坩埚中,放入高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1600℃烧结6h,随炉冷却到室温取出后研磨后得到所需的长余辉发光材料。
利用X射线衍射对实施例2中得到的材料进行分析,确认此样品的衍射图谱与BaAlSi5O2N7的标准图谱(ICSD 240276)一致,没有观察到明显的杂峰。
利用荧光光谱仪对实施例2中得到的荧光材料进行分析,在300nm紫外光激发下得到其发射光谱图,如图2所示。可见该荧光粉能被紫外光激发而发射橙红光,从而使该荧光材料可将紫外光转化为橙红光。此外,将该样品在254nm紫外线激发2min后,移除掉激发光源,测试样品不同时间的余辉发射光谱。如图3所示,在1,3和5min后的余辉发射光谱。余辉发射光谱和光致发光光谱(图2)形状并无明显区别。
实施例3~6
按照BaCO3(分析纯)、SrCO3(分析纯)、SiO2(分析纯)、Yb2O3(分析纯)和Ln2O3(分析纯)摩尔比为1.92︰1︰0.03︰0.01,实施例3~6中的Ln2O3分别对应于Nd2O3,Dy2O3,Ho2O3,Tm2O3。分别取料将上述原料研磨混匀、干燥后再装入刚玉坩埚,放入高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1300℃烧结3h,随炉冷却到室温,得到Yb2+和Ln3+掺杂的Ba1.6Sr0.4SiO4前驱体材料。然后将此前躯体与Si3N4和AlN按照摩尔比为1︰3︰2的量混合,研磨混匀、干燥后再装入氮化硼坩埚中,在高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1600℃烧结6h,随炉冷却到室温取出后研磨后得到所需的长余辉发光材料。
利用X射线衍射对实施例3~6中得到的材料进行分析,确认此样品的衍射图谱与BaAlSi5O2N7的标准图谱(ICSD 240276)一致,没有观察到明显的杂峰。
利用荧光光谱仪对实施例3~6中得到的荧光材料进行分析,在300nm紫外光激发下得到其发射光谱。除共掺三价稀土离子的实施例3的发射光谱中存在Nd3+的特征吸收外,实施例4、实施例5和实施例6的发光光谱图形状与图2相比无明显变化。并且实施例3~6都具有长余辉性质。
实施例7
按照BaCO3(分析纯)、SrCO3(分析纯)、Yb2O3(分析纯)和Tb4O7(分析纯)摩尔比为1.52︰0.4︰0.03︰0.005,分别取料将上述原料研磨混匀、干燥后再装入刚玉坩埚,在高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1300℃烧结3h,随炉冷却到室温,得到Yb2+和Tb3+掺杂的Ba1.6Sr0.4SiO4前驱体材料。然后将此前躯体与Si3N4和AlN按照摩尔比为1︰3︰2的量混合,研磨混匀、干燥后再装入氮化硼坩埚中,放入高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1600℃烧结6h,随炉冷却到室温取出后研磨后得到所需的长余辉发光材料。
利用X射线衍射对实施例7中得到的材料进行分析,确认此样品的衍射图谱与BaAlSi5O2N7的标准图谱(ICSD 240276)一致,没有观察到明显的杂峰。
利用荧光光谱仪对实施例7中得到的荧光材料进行分析,在300nm紫外光激发下得到其发射光谱与图2相比无明显变化。在停止254nm紫外光激发后,比实施例1样品有更强的余辉强度和更长的余辉时间。
实施例8
按照BaCO3(分析纯)、SrCO3(分析纯)、Yb2O3(分析纯)和Er2O3(分析纯)摩尔比为1.52︰0.4︰0.03︰0.01,分别取料将上述原料研磨混匀、干燥后再装入刚玉坩埚,放入高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1300℃烧结3h,随炉冷却到室温,得到Yb2+和Er3+掺杂的Ba1.6Sr0.4SiO4前驱体材料。然后将此前躯体与Si3N4和AlN按照摩尔比为1︰3︰2的量混合,研磨混匀、干燥后再装入氮化硼坩埚中,放入高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1600℃烧结6h,随炉冷却到室温取出后研磨后得到所需的长余辉发光材料。
利用X射线衍射对实施例8中得到的材料进行分析,确认此样品的衍射图谱与BaAlSi5O2N7的标准图谱(ICSD 240276)一致,没有观察到明显的杂峰。
利用荧光光谱仪对实施例8中得到的荧光材料进行分析,在300nm紫外光激发下得到其发射光谱与图2相比,除了在523nm处有Er3+的f-f特征吸收以外,无其他明显变化。在254nm紫外光激发2min并停止后,实施例8具有更强的余辉强度和更长的余辉时间。如图4所示,实施例8与实施例1的衰减曲线。
实施例9
按照BaCO3(分析纯)、SrCO3(分析纯)、Si3N4(分析纯)、AlN(分析纯)、Yb2O3(分析纯)和Tb4O7(分析纯)摩尔比为1.52︰0.4︰3︰2︰0.03︰0.005,分别取料将上述原料研磨混匀、干燥后再装入氮化硼坩埚,放入高温炉内,在H2/N2混合气(气体含量比例为H2︰N2=5︰95,气体流速为100mL/min)中1600℃烧结6h,随炉冷却到室温取出后研磨后得到所需的长余辉发光材料。
利用X射线衍射对实施例9中得到的材料进行分析,确认此样品的衍射图谱与BaAlSi5O2N7的标准图谱(ICSD 240276)一致,没有观察到明显的杂峰。
利用荧光光谱仪对实施例9中得到的荧光材料进行分析,在300nm紫外光激发下得到其发射光谱与图2相比,无明显变化。在停止254nm紫外光激发后,实施例9同样展现出橙红色长余辉性质。
- 还没有人留言评论。精彩留言会获得点赞!