一种绿色氮氧化物荧光材料及其制造方法与流程
本发明涉发光材料,尤其是涉及一种绿色氮氧化物荧光材料及其制造方法。
背景技术:
首先,led照明作为当前最为主流的照明技术,具有效率高、结构坚固、节能、体积小巧等诸多优点。荧光粉是led照明技术中不可或缺的材料,通过荧光粉的光色转换,可以获得包括白光在内的各种光谱类型。
其次,绿色光是三原色之一,而商业上最为成熟的照明芯片产品是蓝光芯片。因此,在蓝光芯片的激发下,通过绿色荧光粉和红色荧光粉的光色转换,一定可以获得高品质的白光。目前红色荧光粉有如,caalsin3:eu和sr2si5n8:eu等。而可供使用的、商业化的绿色荧光粉包括sr2sio4:eu(专利文献1,朱达川,罗林龄,涂铭旌,一种led用共掺杂的硅酸盐绿色荧光粉的制备方法,cn103468250a)、lu3al5o12:ce(专利文献二,t·于斯特尔,w·布泽尔特,p·施密德特,w·迈尔,包括辐射源和荧光材料的照明系统,cn1761835a)和β-sialon:eu(专利文献三,naotohirosaki,hideyukiemoto,masahiroibukiyama,β-typesialonfluorescentsubstance,wo2006121083a1)等。但是sr2sio4:eu热淬灭特性较差,而lu3al5o12:ce的原料成本较高,而β-sialon:eu的合成温度超过1850℃,一般设备难以达到。
最后,氮氧化物是新型荧光材料的重要基质材料。许多氮氧化物通过掺杂稀土离子可以获得优异的发光性能,虽然上述发光性能是不可预测的,但是包含了创造性劳动。但目前很少有基于氯氧氮化合物作为荧光材料机制的公开文献。这是因为含氯的材料,熔点较低,合成的时候,挥发较多,较难控制材料的最终组成和发光性能。
技术实现要素:
为此,本发明的第一目的在于提供一种绿色氮氧化物荧光材料。该材料以eu2+为激活剂,该发光材料热淬灭特性较好,原料成本低廉,合成温度相对较低,能被蓝光激发而发射绿光,从而使该发光材料应用于白光led器件。
为实现上述目的,本发明采用如下技术方案:
一种绿色氮氧化物荧光材料,该材料的化学通式为:
ba6-xeuxsi12o21+0.5ycl3-yn5
其中,0<x<0.5,0<y<3。
优选的,该x可为0.24,所述y可以为2。
本发明的第二目的在于提供一种绿色氮氧化物荧光材料的制造方法。所述制造方法包含如下步骤:
a)将ba前驱体、eu前驱体、si前驱体、cl前驱体和n前驱体混合,在氮气气氛下,进行高温高压固相反应,得到一种中间体;
b)将该中间体、ba前驱体、si前驱体和n前驱体混合,在还原气氛下,进行高温固相反应,得到一种绿色氮氧化物荧光材料。
优选的,该步骤a)中,ba前驱体、eu前驱体、si前驱体、cl前驱体和n前驱体中ba、eu、si、cl和n的摩尔比是(4-x):x:2:(3-y):1,所得中间体的化学通式为:ba4-xeuxsi2o5+0.5ycl3-yn,其中,0<x<0.5,0<y<3。
优选的,该步骤b)中,中间体、ba前驱体、si前驱体和n前驱体,中间体、ba、si与n的摩尔比为1:2:10:4。
优选的,该步骤a)中,ba前驱体选自ba的碳酸盐、ba的氧化物、ba的草酸盐、bacl2和ba的硝酸盐中的至少两种,其中bacl2是必须的;eu前驱体可选自eu的碳酸盐、eu的氧化物、eu的草酸盐和eu的硝酸盐中的至少一种;cl前驱体来自bacl2;si前驱体选自二氧化硅及氮化硅;n前驱体来自氮化硅。
优选的,该步骤b)中,ba前驱体选自ba的碳酸盐、ba的氧化物、ba的草酸盐和ba的硝酸盐中的至少一种;所述si前驱体选自二氧化硅及氮化硅;所述n前驱体来自氮化硅。
优选的,该ba前驱体、eu前驱体、si前驱体、cl前驱体和n前驱体的纯度均不低于99.5%。
优选的,该述步骤a)中,高温高压固相反应的温度介于1000~1200℃,气氛为氮气,压力介于0.5mpa~1mpa,高温高压固相反应的时间介于4~10h。
优选的,该步骤b)中,还原气氛为氨气或氮氢混合气体;高温固相的温度介于为1500~1700℃,高温固相的时间介于4~10h。
有益效果
与现有技术相比,依据本发明实施方法制造的绿色氮氧化物荧光材料具有全新的化学组成,以eu2+为激活剂,该发光材料热淬灭特性较好,原料成本低廉,合成温度相对较低,能被蓝光激发而发射绿光,从而使该发光材料应用于白光led器件。该发光材料的化学成为ba6-xeuxsi12o21+0.5ycl3-yn5,其中,0<x<0.5,0<y<3。
附图说明
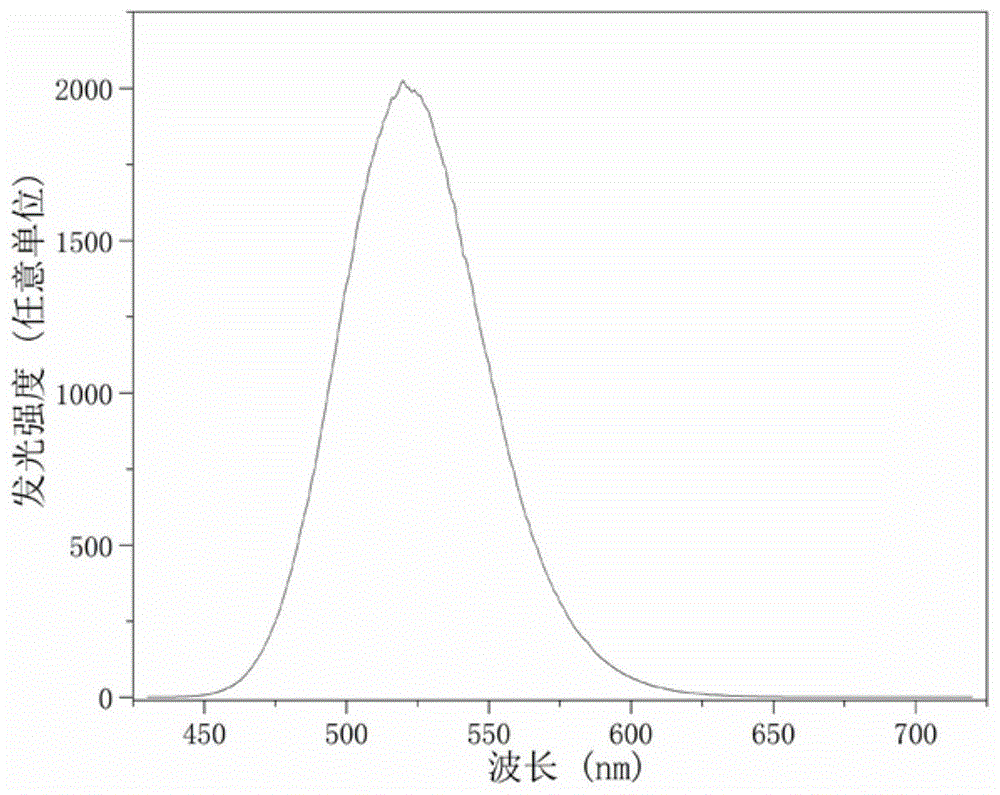
图1为本发明实施例1中得到的发光材料的发射光谱图。
具体实施方式
下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述。
本申请提出一种绿色氮氧化物荧光材料,其化学通式如下:
ba6-xeuxsi12o21+0.5ycl3-yn5
其中,0<x<0.5,0<y<3,优选为0.1<x<0.4,1.5<y<2.5,更优选为0.2<x<0.3,1.8<y<2.2。在本申请一实施例中,该x优选为0.01,y优选为0.01;在本申请一实施例中,该x优选为0.05,y优选为0.5;在本申请一实施例中,该x优选为0.24,y优选为2;在本申请一实施例中,该x优选为0.3,y优选为2.1;在本申请另一实施例中,该x优选为0.4,y优选为2.5。
本申请提出还提供一种绿色氮氧化物荧光材料的制造方法,其步骤如下:
a)将ba前驱体、eu前驱体、si前驱体、cl前驱体和n前驱体混合,在氮气气氛下,进行高温高压固相反应,得到一种中间体;
b)将中间体、ba前驱体、si前驱体和n前驱体混合,在还原气氛下,进行高温固相反应,得到一种绿色氮氧化物荧光材料。
上述步骤a)中,ba前驱体、eu前驱体、si前驱体、cl前驱体和n前驱体中ba、eu、si、cl和n的摩尔比是(4-x):x:2:(3-y):1,所得中间体的化学通式为:ba4-xeuxsi2o5+0.5ycl3-yn,其中,0<x<0.5,0<y<3。
上述步骤a)中,ba前驱体为本领域熟知的包含ba的化合物即可,并无特殊的限制,本发明中优选为ba前驱体选自ba的碳酸盐、ba的氧化物、ba的草酸盐、bacl2和ba的硝酸盐中的至少两种,其中bacl2是必须的,更优选为ba的碳酸盐(即碳酸钡)和bacl2;eu前驱体可选自eu的碳酸盐、eu的氧化物、eu的草酸盐和eu的硝酸盐中的至少一种,更优选为eu的氧化物,即氧化铕;cl前驱体来自bacl2;si前驱体选自二氧化硅及氮化硅;n前驱体来自氮化硅。
上述步骤b)中,中间体、ba前驱体、si前驱体和n前驱体,中间体、ba、si与n的摩尔比为1:2:10:4。
上述步骤b)中,ba前驱体为本领域熟知的包含ba的化合物即可,并无特殊的限制,本发明中优选为ba前驱体选自ba的碳酸盐、ba的氧化物、ba的草酸盐和ba的硝酸盐中的至少一种,更优选为碳酸钡;所述si前驱体选自二氧化硅及氮化硅;上述n前驱体来自氮化硅。
上述ba前驱体、eu前驱体、si前驱体、cl前驱体和n前驱体的纯度均不低于99.5%,纯度越高,得到的发光材料的杂质越少。
上述步骤a)中,高温高压固相反应的温度为1000~1200℃,气氛为氮气,压力为0.5mpa~1mpa,高温高压固相反应的时间为4~10h。
上述步骤b)中,还原气氛为氨气或氮氢混合气体;高温固相的温度为1500~1700℃,高温固相的时间为4~10h。
上述步骤a)中高温高压固相的温度优选为1000~1200℃,气氛为氮气,压力为0.5mpa~1mpa;在本发明提供的一实施例中,该高温固相的温度优选为1100℃,压力为0.8mpa。
上述步骤a)中高温高压固相的时间优选为4~10h,更优选为5~8h;在本发明提供的一些实施例中,该高温固相的时间优选为6h。
上述步骤b)中高温固相的温度优选为1500~1700℃;在本发明提供的一些实施例中,所述高温固相的温度优选为1600℃。
上述步骤b)中高温固相的时间优选为4~10h,更优选为5~8h;在本发明提供的一些实施例中,该高温固相的时间优选为6h。
上述步骤b)中还原气氛为本领域技术人员熟知的干燥气氛即可,并无特殊的限制,本发明中优选为氨气;
上述高温(高压)固反应相优选在高温炉内进行;经历先后步骤a)和步骤b)实施反应后,随炉冷却至室温,即可得到一种一种绿色氮氧化物荧光材料。
本申请实施方式采用高温(高压)固相反应,成功制造一种绿色氮氧化物荧光材料。
为了进一步说明本发明,以下结合实施例对本发明提供的一种绿色氮氧化物荧光材料及其制造方法进行详细描述。
以下对比例和实施例中所用的试剂均为市售。
对比例1
原料为srco3(分析纯)、eu2o3(分析纯)和sio2(分析纯),摩尔比为1.96︰0.02︰1,将上述原料研磨混匀后,装入坩埚,氨气还原气氛下,在高温炉内,1500℃烧结6h,随炉冷却到室温,得到理论化学成分为sr1.96eu0.04sio4的发光材料。
利用荧光光谱仪对对比例1中得到荧光材料进行分析。可见该材料能被蓝光激发,发射光谱的主峰位于525nm附近,室温下光谱发光峰最高的强度及150℃下光谱发光峰最高的强度(即热淬灭特性)见表格1。可见对比例1对应荧光材料的热淬灭特性较差,150℃时,其发光强度仅为室温时的10%
实施例1
原料为bacl2(分析纯)、baco3(分析纯)、eu2o3(分析纯)、si3n4(分析纯)和sio2(分析纯),摩尔比为1.495:2.495:0.005:0.25:1.25,将上述原料研磨混匀后,装入坩埚,在高温炉内,压力为0.8mpa氮气压力下,1100℃烧结6h,随炉冷却到室温,得到理论化学成分为ba3.99eu0.01si2o5.005cl2.99n的中间体。将中间体、baco3(分析纯)、sio2(分析纯)和si3n4(分析纯)按照摩尔比1:2:10:4配料,研磨混匀后,装入坩埚,氨气还原气氛下,在高温炉内,1600℃烧结6h,随炉冷却到室温,即可得到一种绿色氮氧化物荧光材料,化学成分为ba5.99eu0.01si12o21.005cl2.99n5。
利用荧光光谱仪对实施例1中得到荧光材料进行分析,得到其发射光谱图,如图1所示。可见该材料能被蓝光激发,发射光谱的主峰位于528nm附近,室温下光谱发光峰最高的强度及150℃下光谱发光峰最高的强度(即热淬灭特性)见表格1。可见与对比例1相比,实施例1对应荧光材料的热淬灭特性较好,150℃时,其发光强度为室温时的92%。
实施例2
原料为bacl2(分析纯)、baco3(分析纯)、eu2o3(分析纯)、si3n4(分析纯)和sio2(分析纯),摩尔比为1.25:2.7:0.025:0.25:1.25,将上述原料研磨混匀后,装入坩埚,在高温炉内,压力为0.8mpa氮气压力下,1100℃烧结6h,随炉冷却到室温,得到理论化学成分为ba3.95eu0.05si2o5.25cl2.5n的中间体。将中间体、baco3(分析纯)、sio2(分析纯)和si3n4(分析纯)按照摩尔比1:2:10:4配料,研磨混匀后,装入坩埚,氨气还原气氛下,在高温炉内,1600℃烧结6h,随炉冷却到室温,即可得到一种绿色氮氧化物荧光材料,化学成分为ba5.95eu0.05si12o21.25cl2.5n5。
利用荧光光谱仪对实施例2中得到荧光材料进行分析。可见该材料能被蓝光激发,发射光谱的主峰位于529nm附近,室温下光谱发光峰最高的强度及150℃下光谱发光峰最高的强度(即热淬灭特性)见表格1。可见与对比例1相比,实施例2对应荧光材料的热淬灭特性较好,150℃时,其发光强度为室温时的93%。
实施例3
原料为bacl2(分析纯)、baco3(分析纯)、eu2o3(分析纯)、si3n4(分析纯)和sio2(分析纯),摩尔比为0.5:3.26:0.12:0.25:1.25,将上述原料研磨混匀后,装入坩埚,在高温炉内,压力为0.8mpa氮气压力下,1100℃烧结6h,随炉冷却到室温,得到理论化学成分为ba3.76eu0.24si2o6cln的中间体。将中间体、baco3(分析纯)、sio2(分析纯)和si3n4(分析纯)按照摩尔比1:2:10:4配料,研磨混匀后,装入坩埚,氨气还原气氛下,在高温炉内,1600℃烧结6h,随炉冷却到室温,即可得到一种绿色氮氧化物荧光材料,化学成分为ba5.76eu0.24si12o22cln5。
利用荧光光谱仪对实施例3中得到荧光材料进行分析。可见该材料能被蓝光激发,发射光谱的主峰位于532nm附近,室温下光谱发光峰最高的强度及150℃下光谱发光峰最高的强度(即热淬灭特性)见表格1。可见与对比例1相比,实施例3对应荧光材料的热淬灭特性较好,150℃时,其发光强度为室温时的91%。
实施例4
原料为bacl2(分析纯)、baco3(分析纯)、eu2o3(分析纯)、si3n4(分析纯)和sio2(分析纯),摩尔比为0.45:3.25:0.15:0.25:1.25,将上述原料研磨混匀后,装入坩埚,在高温炉内,压力为0.8mpa氮气压力下,1100℃烧结6h,随炉冷却到室温,得到理论化学成分为ba3.7eu0.3si2o6.05cl0.9n的中间体。将中间体、baco3(分析纯)、sio2(分析纯)和si3n4(分析纯)按照摩尔比1:2:10:4配料,研磨混匀后,装入坩埚,氨气还原气氛下,在高温炉内,1600℃烧结6h,随炉冷却到室温,即可得到一种绿色氮氧化物荧光材料,化学成分为ba5.7eu0.3si12o22.05cl0.9n5。
利用荧光光谱仪对实施例4中得到荧光材料进行分析。可见该材料能被蓝光激发,发射光谱的主峰位于530nm附近,室温下光谱发光峰最高的强度及150℃下光谱发光峰最高的强度(即热淬灭特性)见表格1。可见与对比例1相比,实施例4对应荧光材料的热淬灭特性较好,150℃时,其发光强度为室温时的90%。
实施例5
原料为bacl2(分析纯)、baco3(分析纯)、eu2o3(分析纯)、si3n4(分析纯)和sio2(分析纯),摩尔比为0.25:3.15:0.2:0.25:1.25,将上述原料研磨混匀后,装入坩埚,在高温炉内,压力为0.8mpa氮气压力下,1100℃烧结6h,随炉冷却到室温,得到理论化学成分为ba3.6eu0.4si2o6.25cl0.5n的中间体。将中间体、baco3(分析纯)、sio2(分析纯)和si3n4(分析纯)按照摩尔比1:2:10:4配料,研磨混匀后,装入坩埚,氨气还原气氛下,在高温炉内,1600℃烧结6h,随炉冷却到室温,即可得到一种绿色氮氧化物荧光材料,化学成分为ba5.6eu0.4si12o22.25cl0.5n5。
利用荧光光谱仪对实施例1中得到荧光材料进行分析,得到其发射光谱图,如图1所示。可见该材料能被蓝光激发,发射光谱的主峰位于528nm附近,室温下光谱发光峰最高的强度及150℃下光谱发光峰最高的强度(即热淬灭特性)见表格1。可见与对比例1相比,实施例5对应荧光材料的热淬灭特性较好,150℃时,其发光强度为室温时的94%。
表格1
上述的实施例仅用来举例说明本发明的实施方式,以及阐释本发明的技术特征,并非用来限制本发明的保护范围。任何熟悉此技术者可轻易完成的改变或等同性的安排均属于本发明所主张的范围,本发明的权利保护范围应以权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!