一种高通量毒品检测的微流控芯片及应用的制作方法
本发明属违禁药品的检测领域,涉及一种高通量毒品检测的微流控芯片装置及其应用技术。
背景技术:
吗啡(morphine)、冰毒(methamphetamine)、摇头丸(mdma)等化学品虽然问世之初是为了治疗人类疾病,缓解人类疼痛的,但因其在使用后具有严重的副作用,并且具有成瘾性,因此也被列入了毒品名单。毒品的滥用,给人们的生活和生命安全都带来了极大的影响和危害。
目前毒品检测的方法主要包括前期的胶体金试纸检测与后期法庭检测所用的气相色谱-质谱和液相色谱-质谱等方法。胶体金试纸检测方法虽然可以快速现场检测,但是单张试纸只能进行单个样本单一毒品的检测,且每张只能读取单一试纸的检测结果。同时,由于毒品种类的繁多,对于样本的需求量也很大。
微流控芯片由于其消耗样本少、成本低、操作简单等优点,日益受到重视,被应用到了多种检测当中。聚二甲基硅氧烷(polydimethylsiloxane,pdms)、多聚赖氨酸、玻璃等材料的简单易得,为毒品检测提供了很好的方法。检测对象只需提供少量样本,即可实现多种毒品的检测。同时,单张芯片上可以有多个检测区域,并且可以同时检测结果,大大方便了样本的采集与检测的进行。
技术实现要素:
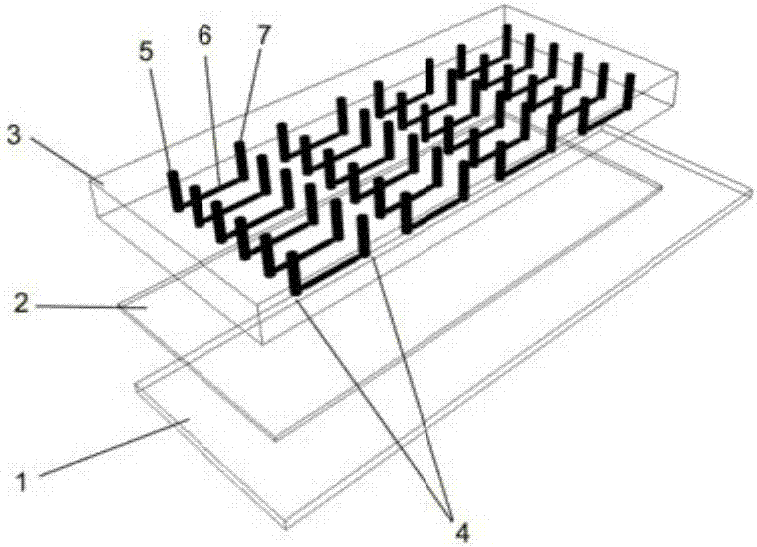
本发明的目的是提供一种高通量毒品检测的微流控芯片,由衬底层1、修饰层2、反应层3构成,反应层3由n(n≥1)个完全相同的反应模块4组成,每个反应模块4由入口5、反应通道6及出口7构成。
该发明装置利用多层软光刻技术制作出具有入口5,反应通道6以及出口7的反应模块4,多个反应模块4构成了反应层3。载玻片构成的衬底层1、多聚赖氨酸构成的修饰层2与pdms制作的反应层3组成了整个芯片装置。
反应通道6的尺寸以及每个反应模块4之间的距离设计时可以调节以改变反应模块4的分布密度与总个数,实现不同数量样本的同时检测。反应通道6宽度优选500μm,高度优选300μm。
衬底层1使用载玻片,材料简单易得。厚度优选1mm,长度优选77mm,宽度优选25mm。
修饰层2为多聚赖氨酸涂层。可以直接选用市面上的多聚赖氨酸载玻片,也可选择普通载玻片自己包被多聚赖氨酸。多聚赖氨酸具有良好的生物相容性,常用作细胞培养,能够形成亲水的表面,利于待测样本在芯片中的流动。
反应层3选用聚二甲基硅氧烷(pdms)为材料,pdms具有生物兼容性好,本身荧光背景低,加工简单、价格低廉等优点,同时pdms具有很强的蛋白吸附作用,这一吸附作用不需要特殊的表面处理,通过预先吸附特定的抗原或抗体,即可实现对毒品的特异性检测。反应层3的厚度可根据实际需要调节,优选3–5mm。
反应层3与涂有修饰层2的衬底层1之间封接采用等离子体处理反应层3,同时在反应层3底面涂敷甲苯与pdms的混合液的方式实现封接。
毒品对应的完全抗原首先使用移液枪从入口5加入反应通道6中。37℃烘干超过12h。之后使用同样的方法,在反应通道6中加入含有体积分数0.05%的tween-20的磷酸盐缓冲液(pbst)封闭液,在湿盒中,37℃保持45min–1h30min。之后,在每个入口5添加15μlpbst封闭液,从出口7抽出,直到抽干芯片内的液体。
本发明的另一个目的是提供所述微流控芯片在高通量毒品检测中的应用。
芯片使用时,先将待测样本与荧光乳胶微球溶液混合,之后添加在入口5。在出口7施加负压,将混合溶液吸入反应通道6中。室温下保持1h。之后从出口7把反应通道6中的液体都抽出。在每个入口5添加15μlpbst封闭液,从出口7加负压,将芯片内液体都抽出。
将芯片放在紫外凝胶成像仪或其他有紫外光源的设备中成像,一次成像可以获得所有反应通道6的荧光情况,分析每个通道的荧光强度与标准曲线对比即可获得毒品的检测结果。
本发明的特点:(1)修饰层为多聚赖氨酸,修饰后的芯片具有亲水性,便于待测样品流入芯片,同时也具有对毒品完全抗原的吸附作用;反应层材质为pdms,对毒品完全抗原具有很强的吸附能力。(2)多聚赖氨酸与pdms的配合使用,可以将多聚赖氨酸亲水性的特点与pdms高蛋白吸附的特点结合起来,实现更好的检测效果。(3)不同毒品、不同样本的检测发生在不同反应通道中,不会出现互相干扰的现象,降低非特异性吸附。(4)pbst封闭液的使用可以增强结果的荧光强度。(5)单张芯片上有多个反应模块,可以在单张芯片上实现多个样本以及多种毒品的现场同时检测,实现高通量快速结果检测分析。(6)反应模块的尺寸、间隔以及个数可以根据需要调整,满足不同的检测需求。
附图说明
图1是本发明的实施例1、3、5、6的示意图,其中1为衬底层,2为修饰层,3为反应层,4为反应模块,5为入口,6为反应通道,7为出口。
图2是本发明的实施例2示意图,其中5为入口,6为反应通道,7为出口,8为阴性对照区域,9为阳性对照区域。区域10对应为3000ng/ml的冰毒检测区,区域11对应为1000ng/ml的冰毒检测区,区域12对应为750ng/ml的冰毒检测区,区域13对应为500ng/ml的冰毒检测区,区域14对应为250ng/ml的冰毒检测区,区域15对应为100ng/ml的冰毒检测区。
图3是本发明的实施例2的结果图。
图4是本发明的实施例4的示意图,其中5为入口,6为反应通道,7为出口,16为荧光乳胶微球连接区,17为空白对照。
图5是本发明的实施例4的结果图。
具体实施方式
本发明结合附图和实施例作进一步的说明。
实施例1芯片的制作
参见图1,一种可实现高通量毒品检测的微流控芯片,由衬底层1、修饰层2、反应层3构成,反应层3由24个完全相同的反应模块4组成,每个反应模块4由入口5、反应通道6及出口7构成。
衬底层1与修饰层2采用市面上售卖的已经包被了多聚赖氨酸的载玻片,优选厚度1mm,宽度25mm,长度77mm。
反应层3采用pdms为材料,采用多层软光刻技术制作具有微通道结构的模具,在模具上浇注具有透气性质的pdms固化脱模形成。反应层3的厚度可根据实际需要调节,优选3–5mm。
反应层3制作完成后,用直径1mm的打孔器在入口5与出口7处打孔,之后使用甲苯与pdms的混合溶液涂在等离子处理过的反应层3底面,将其与修饰层2封接后,85℃加热至牢固。
实施例2冰毒检测标准曲线的制作(参见图2)
(1)将冰毒的完全抗原使用0.01mol/l,ph7.4的磷酸缓冲液(pbs)稀释至200μg/ml,使用移液枪,从每个入口5加3μl进入到反应通道6中。其中阴性对照区域8内的3个反应模块只通入pbs。芯片37℃烘干过夜。
(2)在pbs中添加体积分数0.05%的tween-20,配置成pbst包被液。将包被液用移液枪从每个入口5加3μl进入反应通道6中。芯片放入湿盒,37℃保持1h。
(3)在每个入口5添加15μlpbst,从出口7使用具有抽拉功能的注射泵,将pbst从出口抽出。
(4)使用pbst配置2.4μg/ml的带有冰毒抗体的荧光乳胶微球溶液。
(5)使用(4)中配置的混合液梯度稀释冰毒标准品,浓度稀释至3000ng/ml,1000ng/ml,750ng/ml,500ng/ml,250ng/ml和100ng/ml。
(6)将(5)中得到的冰毒样本加在入口5,从出口7通过注射泵抽入反应通道6中。其中阴性对照区域8与阳性对照区域9的6个反应模块只通入带有冰毒抗体的乳胶微球溶液。区域10通入浓度为3000ng/ml的冰毒,区域11通入浓度为1000ng/ml的冰毒,区域12通入浓度为750ng/ml的冰毒,区域13通入浓度为500ng/ml的冰毒,区域14通入浓度为250ng/ml的冰毒,区域15通入浓度为100ng/ml的冰毒。芯片放入湿盒中,室温保持1h。
(7)在每个入口5添加15μlpbst,从出口7使用注射泵从出口抽出,完成冲洗。
(8)使用紫外凝胶成像仪对芯片进行结果拍摄,之后采集每一条通道的荧光强度,分析结果。随着冰毒含量的增加,荧光强度会减弱,从而得到标准曲线。检测结果如图3所示。
实施例3冰毒检测
(1)将冰毒的完全抗原使用0.01mol/l,ph7.4的pbs稀释至200μg/ml,使用移液枪,从每个入口5加3μl进入到反应通道6中。芯片37℃烘干过夜。
(2)在pbs中添加体积分数0.05%的tween-20,配置成pbst包被液。将包被液用移液枪从每个入口5加3μl进入反应通道6中。芯片放入湿盒,37℃保持1h。
(3)在每个入口5添加15μlpbst,从出口7使用具有抽拉功能的注射泵,将pbst从出口抽出。
(4)使用pbst配置2.4μg/ml的带有冰毒抗体的荧光乳胶微球溶液。
(5)使用(4)中配置的混合液与冰毒样本混合。
(6)将(5)中得到的冰毒样本加在入口5,从出口7通过注射泵抽入反应通道6中。芯片放入湿盒中,室温保持1h。
(7)在每个入口5添加15μlpbst,从出口7使用注射泵从出口抽出,完成冲洗。
(8)使用紫外凝胶成像仪对芯片进行结果拍摄,之后采集每一条通道的荧光强度,分析结果。没有冰毒存在,则荧光强度会最强,而有冰毒存在,荧光强度则会减弱。通过与标准曲线对比,即可以得到检测结果。
实施例4冰毒完全抗原对连接冰毒抗体的荧光乳胶微球的梯度浓度吸附实验
参见图4、图5:
(1)将冰毒的完全抗原使用0.01mol/l,ph7.4的pbs稀释至200μg/ml,使用移液枪,从每个入口5加3μl进入到反应通道6中。其中空白对照区域17内的3个反应模块只通入pbs。芯片37℃烘干过夜。
(2)在pbs中添加体积分数0.05%的tween-20,配置成pbst包被液。将包被液用移液枪从每个入口5加3μl进入反应通道6中。芯片放入湿盒,37℃保持1h。
(3)在每个入口5添加15μlpbst,从出口7使用具有抽拉功能的注射泵,将pbst从出口抽出。
(4)使用pbst配置2.4μg/ml的带有冰毒抗体的荧光乳胶微球溶液。
(5)使用pbst梯度稀释(4)中配置的带有冰毒抗体的荧光乳胶微球溶液,浓度稀释至10%,30%,50%,70%,100%。
(6)将(5)中得到的带有冰毒抗体的荧光乳胶微球样本加在入口5,从出口7通过注射泵抽入反应通道6中。每个区域16中四个反应模块通入相同浓度的荧光乳胶微球溶液。芯片放入湿盒中,室温保持1h。
(7)在每个入口5添加15μlpbst,从出口7使用注射泵从出口抽出,完成冲洗。
(8)使用紫外凝胶成像仪对芯片进行结果拍摄,之后采集每一条通道的荧光强度,分析结果。荧光强度随着荧光乳胶微球浓度的升高而增强,并且空白区域无荧光。
实施例5吗啡检测
(1)参考实施例2制作吗啡检测标准曲线。
(2)将吗啡的完全抗原使用0.01mol/l,ph7.4的pbs稀释至200μg/ml,使用移液枪,从每个入口5加3μl进入到反应通道6中。芯片37℃烘干过夜。
(3)在pbs中添加体积分数0.05%的tween-20,配置成pbst包被液。将包被液用移液枪从每个入口5加3μl进入反应通道6中。芯片放入湿盒,37℃保持1h。
(4)在每个入口5添加15μlpbst,从出口7使用具有抽拉功能的注射泵,将pbst从出口抽出。
(5)使用pbst配置2.4μg/ml的带有吗啡抗体的荧光乳胶微球溶液。
(6)使用(4)中配置的混合液与吗啡样本混合。
(7)将(5)中得到的吗啡样本加在入口5,从出口7通过注射泵抽入反应通道6中。芯片放入湿盒中,室温保持1h。
(8)在每个入口5添加15μlpbst,从出口7使用注射泵从出口抽出,完成冲洗。
(9)使用紫外凝胶成像仪对芯片进行结果拍摄,之后采集每一条通道的荧光强度,分析结果。没有吗啡存在,则荧光强度会最强,而有吗啡存在,荧光强度则会减弱。通过与标准曲线对比,即可以得到检测结果。
实施例6摇头丸检测
(1)参考实施例2制作摇头丸检测标准曲线。
(2)将摇头丸的完全抗原使用0.01mol/l,ph7.4的pbs稀释至200μg/ml,使用移液枪,从每个入口5加3μl进入到反应通道6中。芯片37℃烘干过夜。
(3)在pbs中添加体积分数0.05%的tween-20,配置成pbst包被液。将包被液用移液枪从每个入口5加3μl进入反应通道6中。芯片放入湿盒,37℃保持1h。
(4)在每个入口5添加15μlpbst,从出口7使用具有抽拉功能的注射泵,将pbst从出口抽出。
(5)使用pbst配置2.4μg/ml的带有摇头丸抗体的荧光乳胶微球溶液。
(6)使用(4)中配置的混合液与摇头丸样本混合。
(7)将(5)中得到的摇头丸样本加在入口5,从出口7通过注射泵抽入反应通道6中。芯片放入湿盒中,室温保持1h。
(8)在每个入口5添加15μlpbst,从出口7使用注射泵从出口抽出,完成冲洗。
(9)使用紫外凝胶成像仪对芯片进行结果拍摄,之后采集每一条通道的荧光强度,分析结果。没有摇头丸存在,则荧光强度会最强,而有摇头丸存在,荧光强度则会减弱。通过与标准曲线对比,即可以得到检测结果。
- 还没有人留言评论。精彩留言会获得点赞!