一种生物检测芯片及其检测方法与流程
本发明涉及显示技术领域,尤其涉及一种生物检测芯片及其检测方法。
背景技术:
当前生物分子的检测是在相应的检测芯片上进行的,如蛋白质检测、抗原抗体检测、酶检测、基因检测等。其检测方法是先将大量不同的探针分子点样固定到芯片的各个检测位点上,再将带有荧光标记的待测分子溶液通入芯片,若待测分子与某一位点的探针发生特异性结合反应,通过检测释放的荧光信号即可确定待测分子的结构或类型。该检测方法的检测结果准确度较高,但需要经过荧光检测过程才能确定待测分子的结构或类型,其直观性不高;且目前现有的生物分子检测芯片一般为单次使用,每次能够检测的待测分子种类较少,这会导致检测的耗材成本大幅提高,不利于生物分子检测技术的普及和推广。
因此,如何简化生物分子的检测过程,降低生物分子检测的成本,是本领域技术人员亟待解决的技术问题。
技术实现要素:
本发明实施例提供了一种生物检测芯片及其检测方法,用以简化生物分子的检测过程,降低生物分子检测的成本。
本发明实施例提供了一种生物检测芯片,包括:相对设置的上基板和下基板、参比电极、驱动电极、第一介电层、第二介电层、第一疏水层、第二疏水层和多个挡墙;其中,
所述参比电极位于所述上基板面向所述下基板的一面;
所述第一介电层位于所述参比电极面向所述下基板的一面;
所述第一疏水层位于所述第一介电层面向所述下基板的一面;
所述驱动电极位于所述下基板面向所述上基板的一面;
所述第二介电层位于所述驱动电极面向所述上基板的一面;
所述第二疏水层位于所述第二介电层面向所述上基板的一面;
各所述挡墙支撑于所述第一疏水层与所述第二疏水层之间,且各所述挡墙将所述上基板与所述下基板之间的空间分割为多个子空间,相邻两个所述挡墙之间具有间隙;各所述子空间填充有多个用于与待检测生物分子特异性结合而发生颜色变化的微囊;其中,所述微囊的直径与所述挡墙的高度相同,且所述微囊的直径大于所述间隙的宽度。
在一种可能的实施方式中,本发明实施例提供的上述生物检测芯片中,所述驱动电极包括呈矩阵排列的多个子电极;所述生物检测芯片还包括:与各所述子电极一一对应的开关,多条沿第一方向延伸的控制线以及多条沿与所述第一方向交叉的第二方向延伸的信号线;其中,
每行所述控制线对应一行所述开关,每条所述信号线对应一列所述开关;
各所述开关的控制端与对应的所述控制线相连,输入端与对应的所述信号线相连,输出端与对应的所述子电极相连;所述开关用于在对应的所述控制线的控制下,将对应的所述信号线上的信号输入到对应的所述子电极。
在一种可能的实施方式中,本发明实施例提供的上述生物检测芯片中,各所述挡墙在所述下基板的正投影图形围绕各所述子电极在所述下基板的正投影图形排列。
在一种可能的实施方式中,本发明实施例提供的上述生物检测芯片中,所述开关为开关晶体管;
所述开关晶体管的栅极与对应的所述控制线相连,源极与对应的所述信号线相连,漏极与对应的所述子电极相连。
在一种可能的实施方式中,本发明实施例提供的上述生物检测芯片中,所述子电极的形状为正六边形。
在一种可能的实施方式中,本发明实施例提供的上述生物检测芯片中,所述微囊表面具有多个微孔;所述微囊内具有多个颜色为白色且带电的微球,所述微球的表面具有多个用于与待检测的生物分子进行特异性结合的接头。
在一种可能的实施方式中,本发明实施例提供的上述生物检测芯片中,所述微囊的直径范围为50~200微米。
在一种可能的实施方式中,本发明实施例提供的上述生物检测芯片中,所述上基板具有一组进样口和出样口;所述进样口用于样本溶液的导入;所述出样口用于样本溶液的导出。
本发明实施例提供了一种本发明实施例提供的上述生物检测芯片的检测方法,包括:
将带有染色标记的待测生物分子的样本溶液导入所述生物检测芯片内;
待所述样本溶液流经各所述微囊后,对所述参比电极和所述驱动电极施加电压信号;
观察所述微囊靠近所述上基板的表面的颜色;
根据发生颜色变化的所述微囊确定所述样本溶液中的生物分子的信息。
在一种可能的实施方式中,本发明实施例提供的上述检测方法中,待所述样本溶液流经各所述微囊后,在对所述参比电极和所述驱动电极施加电压信号之前,还包括:
将所述样本溶液导出所述生物检测芯片。
本发明实施例的有益效果包括:
本发明实施例提供了一种生物检测芯片及其检测方法,该生物检测芯片包括:相对设置的上基板和下基板、参比电极、驱动电极、第一介电层、第二介电层、第一疏水层、第二疏水层和多个挡墙;其中,参比电极位于上基板面向下基板的一面;第一介电层位于参比电极面向下基板的一面;第一疏水层位于第一介电层面向下基板的一面;驱动电极位于下基板面向上基板的一面;第二介电层位于驱动电极面向上基板的一面;第二疏水层位于第二介电层面向上基板的一面;各挡墙支撑于第一疏水层与第二疏水层之间,且各挡墙将上基板与下基板之间的空间分割为多个子空间,相邻两个挡墙之间具有间隙;各子空间填充有多个用于与待检测生物分子特异性结合而发生颜色变化的微囊;其中,微囊的直径与挡墙的高度相同,且微囊的直径大于间隙的宽度。
本发明实施例提供的上述的生物检测芯片中,每个子空间的微囊可与一种待测生物分子发生特异性结合而发生颜色变化,使其变为待测分子的标记色,这样通过对驱动电极与参比电极施加电压使微囊靠近上基板的表面呈现颜色变化,从而可从芯片上方直接观察到微囊的颜色变化,使得生物分子检测可以实现直观的观察检测结果,进而确定待测生物分子的结构或类型信息,相对于现有技术不需要进行荧光检测,简化了生物分子的检测过程。而且本发明的生物检测芯片中的微囊可替换,从而该生物检测芯片可重复使用,降低了检测成本;另外,该生物检测芯片可以采用现有的光刻制作工艺来制作,其制作方法简单。
附图说明
图1为本发明实施例提供的生物检测芯片的结构示意图;
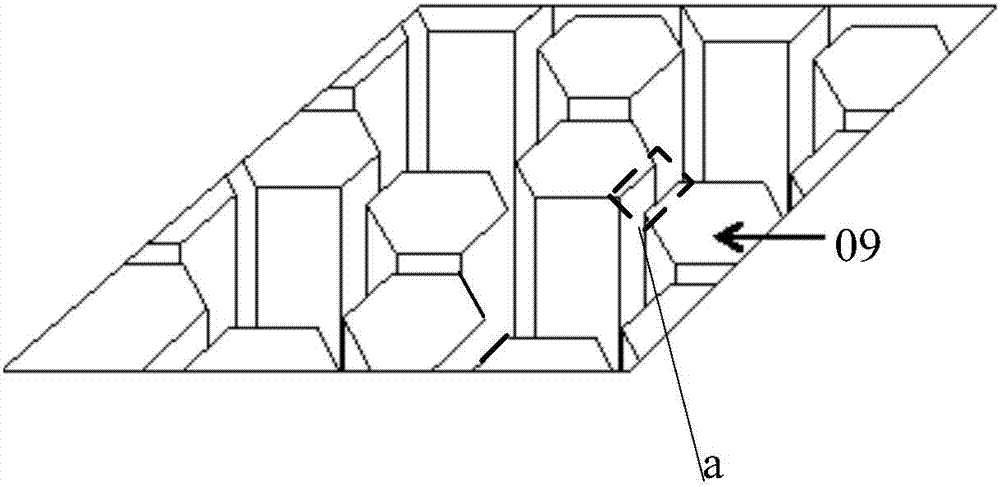
图2为本发明实施例提供的挡墙的排列示意图;
图3为本发明实施例提供的子电极的排列示意图;
图4为本发明实施例提供的微囊的结构示意图;
图5a-图5d分别为本发明实施例提供的生物分子检测过程示意图;
图6为本发明实施例提供的生物检测方法流程图。
具体实施方式
下面结合附图,对本发明实施例提供的生物检测芯片及其检测方法的具体实施方式进行详细的说明。
本发明实施例提供了一种生物检测芯片,如图1所示,包括:相对设置的上基板01和下基板02、参比电极03、驱动电极04、第一介电层05、第二介电层06、第一疏水层07、第二疏水层08和多个挡墙09;其中,
参比电极03位于上基板01面向下基板02的一面;
第一介电层05位于参比电极03面向下基板02的一面;
第一疏水层07位于第一介电层05面向下基板02的一面;
驱动电极04位于下基板02面向上基板01的一面;
第二介电层06位于驱动电极04面向上基板01的一面;
第二疏水层08位于第二介电层06面向上基板01的一面;
各挡墙09支撑于第一疏水层07与第二疏水层08之间,且各挡墙09将上基板01与下基板02之间的空间分割为多个子空间,如图2所示,相邻两个挡墙09之间具有间隙a;各子空间填充有多个用于与待检测生物分子特异性结合而发生颜色变化的微囊10;其中,微囊10的直径与挡墙09的高度相同,且微囊10的直径大于间隙a的宽度,这样挡墙之间的缝隙小于微囊直径,可以保证微囊不能通过缝隙在不同子空间移动,但允许液体可以通过挡墙缝隙。
本发明实施例提供的上述的生物检测芯片中,每个子空间的微囊可与一种待测生物分子发生特异性结合而发生颜色变化,使其变为待测分子的标记色,这样通过对驱动电极与参比电极施加电压使微囊靠近上基板的表面呈现颜色变化,从而可从芯片上方直接观察到微囊的颜色变化,使得生物分子检测可以实现直观的观察检测结果,进而确定待测生物分子的结构或类型信息,相对于现有技术不需要进行荧光检测,简化了生物分子的检测过程。而且本发明的生物检测芯片中的微囊可替换,从而该生物检测芯片可重复使用,降低了检测成本;另外,该生物检测芯片可以采用现有的光刻制作工艺来制作,其制作方法简单。
在具体实施时,本发明实施例提供的上述生物检测芯片中,如图3所示,驱动电极包括呈矩阵排列的多个子电极041;生物检测芯片还可以包括:与各子电极041一一对应的开关11,多条沿第一方向延伸的控制线12以及多条沿与第一方向交叉的第二方向延伸的信号线13;其中,每行控制线12对应一行开关11,每条信号线13对应一列开关11;各开关11的控制端与对应的控制线12相连,输入端与对应的信号线13相连,输出端与对应的子电极041相连;开关11用于在对应的控制线12的控制下,将对应的信号线13上的信号输入到对应的子电极041。
具体地,本发明实施例提供的上述生物检测芯片中,可以将驱动电极分割为多个子电极,进而通过设置与子电极一一对应的开关来控制各区域的生物分子检测,可以实现分区控制。另外,如图3所示,还可以设置各挡墙09在下基板02的正投影图形围绕各子电极041在下基板02的正投影图形排列,即将每个子电极对应的区域规划为一个检测区域,通过设置挡墙的排列,将一个子电极对应的区域由挡墙围绕成一个检测区域,进而通过开关控制对应区域进行生物分子检测,其可以精确到控制每个子电极,进而可以精确控制到每一个检测区域。
在具体实施时,本发明实施例提供的上述生物检测芯片中,开关可以通过开关晶体管来实现,具体地,开关晶体管的栅极与对应的控制线相连,源极与对应的信号线相连,漏极与对应的子电极相连。在进行生物分子检测时,可以通过控制线控制对应区域的开关晶体管打开,进而将信号线上的电压信号输出到对应的子电极,以实现该子电极对应的区域的生物分子检测。
在具体实施时,本发明实施例提供的上述生物检测芯片中,如图3所示,子电极041的形状可以为正六边形,当然也可以设置为其他满足设计需求的形状,例如圆形,矩形等形状,在实际应用时可以相应调整,在此不做限定。相应的,挡墙的截面形状也可以设置为多种多样的形状,如图3所示,挡墙09在下基板上的正投影形状为六边形,在实际应用中,挡墙也可以设置为其他类型的截面形状,在此不做限定。
在具体实施时,本发明实施例提供的上述生物检测芯片中,如图4所示,微囊10表面具有多个微孔101;微囊10内具有多个颜色为白色且带电的微球102,微球102的表面具有多个用于与待检测的生物分子进行特异性结合的接头103。具体地,微囊设置为多孔结构可以允许带有染色标记的待测生物分子自由进出;微囊内包裹的白色带电微球的表面经化学处理,连接不同结构和种类的接头,如抗体、适配体等,这些接头能且仅能与一种未知生物分子特异性结合。如图5a所示,在不施加电压时,带染色标记的待测分子溶液流经所有微囊,如图5b所示,若发生特异性结合,则这些带电微球的表面由白色变为相应待测分子的标记色;如图5c所示,若未发生特异性结合,带电微球表面仍为白色;之后通过施加电压,如图5d所示,微囊内的带电微球会移动到微囊靠近上基板的表面,上基板为透明基板,可直接观察到微球颜色,从而检测出待测生物分子。
在具体实施时,本发明实施例提供的上述生物检测芯片中,微囊的直径范围可以设置为50~200微米。
在具体实施时,本发明实施例提供的上述生物检测芯片中,上基板具有一组进样口和出样口;进样口用于样本溶液的导入;出样口用于样本溶液的导出。具体地,该生物检测芯片在上基板可以设置一对进样口和出样口,用于实现待测溶液的导入和导出。
基于同一发明构思,本发明实施例提供了一种本发明实施例提供的上述生物检测芯片的检测方法,如图6所示,可以包括:
s101、将带有染色标记的待测生物分子的样本溶液导入生物检测芯片内;
s102、待样本溶液流经各微囊后,对参比电极和驱动电极施加电压信号;
s103、观察微囊靠近上基板的表面的颜色;
s104、根据发生颜色变化的微囊确定样本溶液中的生物分子的信息。
本发明实施例提供的上述检测方法中,将染色标记的待测分子溶液流经芯片上的所有微囊,每种待测分子只能与某一微囊发生特异性结合,若结合则变为相应待测分子的标记色;对参比电极和驱动电极施加电压,微囊靠近上基板的表面呈现颜色变化,上基板为透明基板,可直接观察到颜色变化,从而根据发生颜色变化的微囊确定待测生物分子的信息。相对于现有技术不需要进行荧光检测,简化了生物分子的检测过程。
在具体实施时,本发明实施例提供的上述检测方法中,待样本溶液流经各微囊后,在对参比电极和驱动电极施加电压信号之前,还包括:将样本溶液导出生物检测芯片。具体地,待样本溶液流经各微囊后,可以将样本溶液导出,然后再进行加电观察检测结果,这样可以避免未反应的溶液影响检测结果的观察。
本发明实施例提供了一种生物检测芯片及其检测方法,该生物检测芯片包括:相对设置的上基板和下基板、参比电极、驱动电极、第一介电层、第二介电层、第一疏水层、第二疏水层和多个挡墙;其中,参比电极位于上基板面向下基板的一面;第一介电层位于参比电极面向下基板的一面;第一疏水层位于第一介电层面向下基板的一面;驱动电极位于下基板面向上基板的一面;第二介电层位于驱动电极面向上基板的一面;第二疏水层位于第二介电层面向上基板的一面;各挡墙支撑于第一疏水层与第二疏水层之间,且各挡墙将上基板与下基板之间的空间分割为多个子空间,相邻两个挡墙之间具有间隙;各子空间填充有多个用于与待检测生物分子特异性结合而发生颜色变化的微囊;其中,微囊的直径与挡墙的高度相同,且微囊的直径大于间隙的宽度。
本发明实施例提供的上述的生物检测芯片中,每个子空间的微囊可与一种待测生物分子发生特异性结合而发生颜色变化,使其变为待测分子的标记色,这样通过对驱动电极与参比电极施加电压使微囊靠近上基板的表面呈现颜色变化,从而可从芯片上方直接观察到微囊的颜色变化,使得生物分子检测可以实现直观的观察检测结果,进而确定待测生物分子的结构或类型信息,相对于现有技术不需要进行荧光检测,简化了生物分子的检测过程。而且本发明的生物检测芯片中的微囊可替换,从而该生物检测芯片可重复使用,降低了检测成本;另外,该生物检测芯片可以采用现有的光刻制作工艺来制作,其制作方法简单。
显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
- 还没有人留言评论。精彩留言会获得点赞!