一种用于汗液检测的可穿戴传感器及其制备方法与流程
本发明涉及可穿戴设备领域,且特别涉及一种用于汗液检测的可穿戴传感器及其制备方法。
背景技术:
随着人们生活水平的提高,高热量饮食的摄入,导致糖尿病的发病率越来越高。长期存在的高血糖导致患者饱受生理以及心理上的折磨,因此,血糖监测对于人们具有重要作用,如果能够快速、迅捷、非侵入型的传感器监测人体葡萄糖和乳酸含量,就能够实现对人体血糖浓度的动态、连续监测,对监测人体健康具有重要的应用价值。
现有的血糖监测通常采用快速指尖采血的方法对血糖进行检测,这种监测方式需要反复采血,且只能进行定点监测,而无法实现实时监测。汗液是人体代谢的产物,汗液中含有反应人体健康状况的代谢产物,特别是汗液中的葡萄糖和乳酸含量可以在一定程度上反应人体生理状况,因此,精确监测体液中的葡萄糖和乳酸含量尤为重要。目前广泛应用的葡萄糖传感器是基于酶催化的传感器,但是基于酶催化的传感器的稳定性较差、不便携带。
技术实现要素:
本发明的目的在于提供一种用于汗液检测的可穿戴传感器,此可穿戴传感器生物相容性好,检测精度高,检测范围广,使用寿命长久。
本发明的另一目的在于提供一种用于汗液检测的可穿戴传感器的制备方法,工艺简单,各项参数易于控制,可重复性强。
本发明解决其技术问题是采用以下技术方案来实现的。
本发明提出一种用于汗液检测的可穿戴传感器,包括:柔性基底以及形成于所述柔性基底上的工作电极和参比电极,所述柔性基底为蛋白质薄膜,所述工作电极包括从下至上依次设置的金属层、传输层和氧化酶层,所述参比电极包括从下至上依次设置的金属层和ag/agcl层;其中,所述传输层为还原氧化石墨烯/ptnps复合薄膜,所述还原氧化石墨烯/ptnps复合薄膜通过电化学沉积还原法获得。
进一步地,在本发明较佳的实施例中,所述工作电极包括第一电极和第二电极,所述第一电极的氧化酶层为葡萄糖氧化酶层,所述第二电极的氧化酶层为乳酸氧化酶层。
进一步地,在本发明较佳的实施例中,所述氧化酶层上还覆盖有蛋白交联层。
进一步地,在本发明较佳的实施例中,所述还原氧化石墨烯/ptnps复合薄膜包括还原氧化石墨烯片层和掺杂在所述还原氧化石墨烯片层内部及其表面的铂纳米颗粒,其中,铂纳米颗粒的掺杂量为所述还原氧化石墨烯/ptnps复合薄膜的6~12%。
本发明提出一种如上述的用于汗液检测的可穿戴传感器的制备方法,包括以下步骤:
s1,通过磁控溅射法在所述柔性基底上形成至少两个相互分离的金属区域,分别作为所述工作电极和所述参比电极的金属层;
s2,在所述工作电极的金属层上通过电化学沉积还原法沉积得到还原氧化石墨烯/ptnps复合薄膜,形成传输层,然后在所述传输层上形成氧化酶层;
s3,在所述参比电极的金属层上形成银纳米层,并对所述银纳米层进行氯化,得到ag/agcl层。进一步地,在本发明较佳的实施例中,步骤s2中,通过电化学沉积还原法沉积还原氧化石墨烯/ptnps复合薄膜的步骤包括:将具有所述金属层的柔性基底于电解液中,在-1.4v-0.6v之间循环伏安沉积得到所述传输层;其中,所述电解液含有氧化石墨烯、氯铂酸以及pbs缓冲液,且ph值调节至10~11。
进一步地,在本发明较佳的实施例中,所述电解液中,所述氧化石墨烯的浓度为0.1~1mg/ml,所述氯铂酸的浓度为0.1~1mmol/l,所述pbs缓冲液的浓度为0.05~0.2mol/l。
进一步地,在本发明较佳的实施例中,步骤s2中,形成氧化酶层后,还包括以下步骤:在所述氧化酶层上涂覆丝素蛋白溶液,干燥后,在丝素蛋白层表面涂覆戊二醛,形成蛋白交联层。
进一步地,在本发明较佳的实施例中,步骤s3中,形成所述ag/agcl层后,还包括以下步骤:在所述ag/agcl层的表面涂覆聚乙烯醇缩丁醛溶液,然后干燥。
进一步地,在本发明较佳的实施例中,所述工作电极和所述参比电极的间距为0.5~2mm。
本发明实施例的用于汗液检测的可穿戴传感器及其制备方法的有益效果是:
以蛋白薄膜为柔性基底,具有良好的生物相容性,为可穿戴传感器提供基础,可与皮肤直接接触,而不会引起过敏或其他不适反应。
通过电化学沉积还原法获得还原氧化石墨烯/ptnps复合薄膜作为传输层,还原氧化石墨烯具有优良的电催化性能,且能够保持传感器所负载的氧化酶的生物活性,氧化石墨烯残留的氧化基团能够提供与酶共价交联的位点。掺杂在还原石墨烯片层内部和表面的铂颗粒对酶促反应的中间产物过氧化氢具有良好的催化效应,极大提高了传感器的灵敏度。通过本发明制备的传感器,ptnps的负载量高,对葡萄糖的检测灵敏度达到31.02μamm-1cm-2,对乳酸检测的灵敏度达到3.11μamm-1cm-2。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
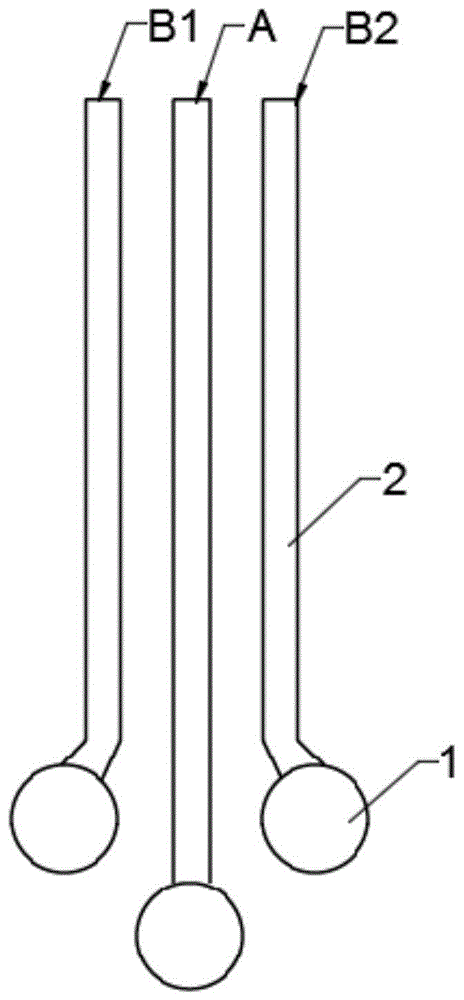
图1为本发明实施例1的用于汗液检测的可穿戴传感器的结构示意图;
图2为本发明实施例1制作的传感器对模拟汗液中不同浓度的葡萄糖的响应电流图;
图3为本发明实施例1制作的传感器对模拟汗液中不同浓度的乳酸的响应电流图。
附图标记汇总如下:a-参比电极,b1-工作电极;b2-工作电极;1-电极区,2-导线。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
下面对本发明实施例的用于汗液检测的可穿戴传感器及其制备方法进行具体说明。
本发明实施例提供一种用于汗液检测的可穿戴传感器,包括:柔性基底以及形成于所述柔性基底上的工作电极和参比电极。
柔性基底为蛋白质薄膜,蛋白质薄膜例如可以是丝素蛋白膜、羊毛角蛋白膜等。在其他实施例中,蛋白质薄膜也可以是蛋白质和聚合物的复合膜,例如将丝素蛋白溶液和聚氨酯溶液混合浇筑成膜得到的复合膜。
在其中一个实施例中,蛋白薄膜按如下步骤制得:将蚕茧进行除杂处理后放进沸腾的浓度为5~8g/l的碳酸氢钠溶液中进行除胶,重复碱洗两次。然后在温清水中漂洗、烘干得到丝素纤维。将丝素纤维置于8~10mol/l的libr溶液中,于60℃烘箱中溶解3~5h。接着将溶解后的丝素蛋白溶液放入截留量为3500d的透析袋中于去离子水中透析3天,最后过滤得到丝素蛋白溶液液。将丝素蛋白液浓缩或稀释至5~10wt%,然后在玻璃基底上浇筑成膜,得到柔性自支撑的蛋白薄膜。
在柔性基底上,设有至少一个工作电极和参比电极。
工作电极和参比的电极的最底层均为金属层。进一步地,该金属层为铂、钯、银、金中的一种或多种。优选地,本实施例中,金属层为au。例如可以通过在柔性基底上通过磁控溅射获得。
进一步地,该金属层包括电极区和导线。优选地,电极区呈圆形,导线呈条状,且沿圆形电极区的边缘引出。更为优选地,电极区的半径为2~4mm。保证有足够的反应位点,保证检测的灵敏度。条状导线的线宽为0.5~1.5mm。
可以理解的是,在其他实施例中,金属层的电极区也可以是方形或其他形状,不局限于此。
在工作电极金属层的电极区上设有传输层。该传输层为还原氧化石墨烯/ptnps复合薄膜,还原氧化石墨烯/ptnps复合薄膜通过电化学沉积还原法获得。在优选的实施例中,还原氧化石墨烯/ptnps复合薄膜包括还原氧化石墨烯片层和掺杂在还原氧化石墨烯片层内部及其表面的铂纳米颗粒,其中,铂纳米颗粒的掺杂量为还原氧化石墨烯/ptnps复合薄膜的6~12%。
以还原氧化石墨烯为传输基底,在还原氧化石墨烯片层的内部和表面嵌入一定量的铂纳米颗粒(ptnps),还原氧化石墨烯的具有良好的导电性和较大的比表面积,能够对ptnps形成良好的负载。利用ptnps对过氧化氢的催化效应,从而极大提高传感器的灵敏度。在ptnps的负载量为6~12%时,传感器对葡萄糖的检测灵敏度达到31.02μamm-1cm-2,对乳酸检测的灵敏度达到3.11μamm-1cm-2。
工作电极的传输层上设有氧化酶层。参比电极的传输层上设有ag/agcl层。优选地,本实施例中,工作电极包括第一电极和第二电极,第一电极的氧化酶层为葡萄糖氧化酶层,第二电极的氧化酶层为乳酸氧化酶层。通过设置两个工作电极,同时实现对葡萄糖和乳酸的实时检测。
进一步地,参比电极设置在第一电极和第二电极的中间位置,三个电极彼此分离。优选地,相邻两个电极之间的间距为0.5~2mm。该间距指从一个电极的电极区的边缘至另一个电极的电极区的边缘的间距。
进一步地,在较佳的实施例中,工作电极的氧化酶层上还覆盖有蛋白交联层。通过蛋白交联层能够对氧化酶进行有效固定,且能够长期保存氧化酶活性,使得传感器具有较长的使用寿命和较高的灵敏度。
参比电极的金属层上设有ag/agcl层。进一步地,在较佳的实施例中,参比电极的ag/agcl层上设有高分子材料保护层,优选地,高分子材料选用聚乙烯醇缩丁醛,进一步提高产品的使用寿命,且通过该保护层提供优良的柔软性和挠曲性。
本发明实施例提出一种如上述的用于汗液检测的可穿戴传感器的制备方法,包括以下步骤:
s1,通过磁控溅射法在柔性基底上形成至少两个相互分离的金属区域,分别作为工作电极和参比电极的金属层。
优选地,本实施例中,柔性基底上形成三个金属区域,分别作为第一电极、第二电极和参比电极的金属层。
s2,在工作电极的金属层上于碱性环境下通过电化学沉积还原法沉积得到还原氧化石墨烯/ptnps复合薄膜,形成传输层;然后在传输层上形成氧化酶层。
进一步地,在较佳的实施例中,该步骤具体为:将具有金属层的柔性基底置于电解液中,在-1.4v-0.6v之间循环伏安沉积一定的圈数得到传输层;其中,电解液含有氧化石墨烯、氯铂酸以及pbs缓冲液,且ph值调节至11~13。将ph值调节至11~13,在碱性条件下,电沉积过程才能够顺利进行,沉积得到30nm左右的复合薄膜。
进一步优选地,电解液中,氧化石墨烯的浓度为0.1~1mg/ml,氯铂酸的浓度为0.1~1mmol/l,pbs缓冲液的浓度为0.05~0.2mol/l。进一步优选为氧化石墨烯的浓度为0.2mg/ml,氯铂酸的浓度为0.2mmol/l。循环伏安沉积的圈数为8~12圈,优选为10圈,扫描速率为25mvs-1。在上述条件下,能够保证沉积过程中,ptnps能够有效沉积,在氯铂酸的浓度为0.2mmol/l的条件下,即可沉积得到6%以上的ptnps,得到致密均匀的复合薄膜。
氧化石墨烯和氯铂酸通过一步法还原得到,制备工艺简单,且通过循环伏安沉积,使得ptnps能够均匀嵌入到原石墨烯片层的内部或表面。在上述条件下,能够保证沉积过程中,ptnps能够有效沉积,在氯铂酸的浓度为0.2mmol/l的条件下,即可沉积得到6%以上ptnps的高负载量,得合薄膜致密均匀。
进一步地,在第一电极的传输层上滴加8~15μl的1.8u/μl的葡萄糖氧化酶后晾干形成葡萄糖氧化酶层,作为葡萄糖检测的工作电极。在第二电极的传输层上滴加8~15μl的0.5u/μl的乳酸氧化酶后晾干形成乳酸氧化酶层;作为乳酸检测的工作电极。
进一步优选地,形成氧化酶层后,还包括以下步骤:在氧化酶层上涂覆丝素蛋白溶液,干燥后,在丝素蛋白层表面涂覆戊二醛溶液,形成蛋白交联层。更为优选地,丝素蛋白溶液和戊二醛溶液的浓度均为1wt%。利用戊二醛和天然丝素蛋白交联形成对氧化酶的保护层,既实现了利用天然蛋白质对葡萄糖氧化酶和乳酸氧化酶进行固定,又能够长期保持维持氧化酶的活性,保证传感器具有较长的使用寿命和较高灵敏度。
s3,在参比电极的金属层上形成银纳米层,并对银纳米层进行氯化,得到ag/agcl层。具体地,在参比电极金属层的电极区上施加8~12μl的银纳米线,干燥后,再在银纳米线表面施加0.05mol/l的氯化铁溶液,维持3~7s,水洗干燥后,得到表面氯化的银纳米线层。
进一步地,在较佳的实施例中,形成ag/agcl层后,还包括以下步骤:在ag/agcl层的表面涂覆聚乙烯醇缩丁醛溶液,然后干燥。进一步优选地,在ag/agcl层的表面滴加10μl的聚乙烯醇缩丁醛溶液(浓度为7~8g/ml)。通过在ag/agcl层表面形成聚乙烯醇缩丁醛高分子材料保护层,保护ag/agcl层免受损伤。
以下结合实施例对本发明的特征和性能作进一步的详细描述。
实施例1
本实施例提供的一种用于汗液检测的可穿戴传感器,其根据以下步骤制得:
(1)以天然丝素蛋白薄膜为柔性基底,在柔性基底上溅射金,获得三个金属区域,分别作为三个电极的金属层,每个金属层包括电极区1和导线2,其中导线线宽为1mm,线长20mm,电极区为半径约为3mm的圆。如图1所示。其中,中间的金属层作为参比电极a,两侧的金属层分别作为葡萄糖检测的工作电极b1和乳酸检测的工作电极b2。
(2)在0.2mg/ml的氧化石墨烯分散液(ph=11,且含有0.1mmol/lpbs缓冲液)中加入氯铂酸,形成0.2mmol/l的氯铂酸氧化石墨烯分散液。将步骤(1)中的溅射有金属层的柔性基底在氯铂酸氧化石墨烯分散液中,于-1.4v-0.6v之间以2525mvs-1的速率循环伏安沉积10圈,在工作电极b1和b2金属层的电极区上形成传输层。
(3)在工作电极b1、b2的两个传输层上分别滴加10μl1.8u/μl的葡萄糖氧化酶和10μl0.5u/μl的乳酸氧化酶,晾干后再滴加5μl1wt%丝素蛋白溶液,再次晾干,滴加5μl1wt%戊二醛,分别得到葡萄糖检测用工作电极b1和乳酸检测用工作电极b2。
(4)在参比电极a金属层的电极区上滴加10μl的银纳米线,晾干后,在其表面滴加10μl0.05mol/l氯化铁氯化5s,水洗晾干,再在表面滴加10μl含有79.1mg的聚乙烯醇缩丁醛溶液晾干。
本实施例获得的传感器,工作电极传输层的ptnps的负载量为6.25%。将实施例1制备得到的用于汗液检测的可穿戴传感器放到不同浓度的葡萄糖溶液中,对其响应电流进行测试,结果如图2所示。从图2可以看出,传感器在2μm-0.4mm有良好的线性关系,灵敏度达到31.02μamm-1cm-2。将实施例1制备得到的用于汗液检测的可穿戴传感器放到不同浓度的乳酸溶液中,对其响应电流进行测试,结果如图3所示。从图3可以看出,传感器在20μm-2mm有良好的线性关系,灵敏度达到3.11μamm-1cm-2。重复使用200次后,对葡萄糖检测的灵敏度保持原有的97%,对乳酸检测的灵敏度保持原有的91%。
实施例2
本实施例中提供了一种用于汗液检测的可穿戴传感器,其与实施例1的区别之处在于:步骤(2)中,氧化石墨烯的浓度为0.4mg/ml。
本实施例获得的传感器,工作电极传输层的ptnps的负载量为6.03%。
实施例3
本实施例中提供了一种用于汗液检测的可穿戴传感器,其与实施例1的区别之处在于:步骤(2)中,氯铂酸的浓度为1mmol/l。
本实施例获得的传感器,工作电极传输层的ptnps的负载量为7.33%。
实施例4
本实施例中提供了一种用于汗液检测的可穿戴传感器,其与实施例1的区别之处在于:步骤(3)中,在工作电极b1的传输层滴加10μl1.8u/μl的葡萄糖氧化酶与10μl质量分数为1wt%的丝素蛋白溶液的混合溶液,晾干后在甘油中浸泡12h,得到葡萄糖检测用工作电极b1。在工作电极b2的传输层滴加10μl0.5u/μl的乳酸氧化酶与10μl质量分数为1wt%的丝素蛋白溶液的混合溶液,晾干后在甘油中浸泡12h,得到乳酸检测用工作电极b2。
本实施例获得的传感器,工作电极传输层的ptnps的负载量为6.25%。重复使用200次后,对葡萄糖检测的灵敏度保持原有的84%,对乳酸检测的灵敏度保持原有的78%。
对比例1
本对比例中提供了一种用于汗液检测的可穿戴传感器,其与实施例1的区别之处在于:步骤(2)中,氧化石墨烯分散液的ph值为7。
对比例1获得的传感器,工作电极传输层的ptnps的负载量为2.45%。
对比例2
本对比例中提供了一种用于汗液检测的可穿戴传感器,其与实施例1的区别之处在于:步骤(2),在0.2mg/ml的氧化石墨烯分散液(ph=11,且含有0.1mmol/lpbs缓冲液)中加入氯金酸,形成0.2mmol/l的氯金酸氧化石墨烯分散液。将步骤(1)中的溅射有金属层的柔性基底在氯金酸氧化石墨烯分散液中,于-1.4v-0.6v之间以2525mvs-1的速率循环伏安沉积10圈,在工作电极b1和b2金属层的电极区上形成传输层。
对比例2获得的传感器,工作电极传输层的aunps的负载量为1.71%。
综上所述,本发明实施例的传感器,以天然丝素蛋白为基底,具有良好的生物相容性,实现可穿戴。以还原氧化石墨烯和铂纳米颗粒的复合薄膜为传输层,灵敏度高。通过蛋白交联层对氧化酶提供保护,多次重复使用仍保持较高的灵敏度。
以上所描述的实施例是本发明一部分实施例,而不是全部的实施例。本发明的实施例的详细描述并非旨在限制要求保护的本发明的范围,而是仅仅表示本发明的选定实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!