MCM-41介孔分子筛修饰碳糊电极的制备及其应用的制作方法
本发明涉及一种测定头孢哌酮的电化学传感器。
背景技术:
头孢哌酮是第三代头孢菌素。该品对阴性杆菌产生的广谱β-内酰胺酶有一定的稳定性,但较某些第三代头孢菌素差,抗阴性杆菌的作用优于第一、二代头孢菌素,但对绿脓杆菌有较好的抗菌活性。抗阳性菌的作用不如第一、二代头孢菌素,但对肺炎球菌、化脓性链球菌均有较好的作用。对厌氧菌的抗菌作用较弱。肠球菌及相当比例的肠杆菌科致病菌对该品耐药,支原体、衣原体、军团菌对头孢哌酮均耐药。抗菌性能与头孢噻肟相似。对革兰阳性菌的作用较弱,仅溶血性链球菌和肺炎链球菌较为敏感。对数的革兰阴性菌,该品的作用略次于头孢噻肟,对绿脓杆菌的作用较强。口服不吸收。对链球菌(肠球菌除外)抗菌作用较强。对革兰阴性菌有较强的抗菌效能。奈瑟菌属、流感杆菌、大肠杆菌、奇异变形杆菌、克雷伯杆菌、沙门杆菌等对该品甚敏感。绿脓杆菌、阴沟杆菌、脆弱拟杆菌等对该品较不敏感。对大多数的革兰阴性菌,作用略次于头孢噻肟,对绿脓杆菌的作用较强。由此可见检测体内头孢哌酮的水平对合理用药具有十分重要的意义。电分析化学由于具有灵敏度高、选择性好、响应时间短、所需仪器设备价格低廉等优点而广泛用于药物的直接电化学检测。开发出高灵敏度,测定头孢哌酮的电化学传感器引起了人们的研究兴趣。
无机介孔材料具有较高的比表面积、大的孔体积、规则有序的孔道和均一的孔径等特点以外,还在材料的柔韧度以及亲/憎水性方面具有可调节性,同时可以衍生出新的活性中心。这种独特的电子特性将使它有望成为新型传感器器件。
技术实现要素:
本发明就是针对上述问题提供一种MCM-41介孔分子筛掺杂的碳糊电极用于头孢哌酮的高灵敏度、高选择性测定。
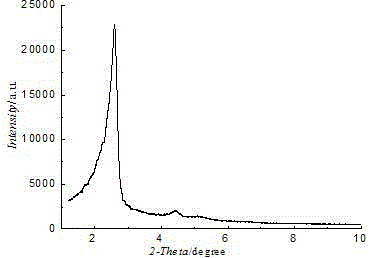
本发明所述的MCM-41介孔分子筛的制备:1.2 g的十六烷基三甲基溴化铵(CTAB)溶于50 mL去离子水、25%的氨水调节pH至10.2,滴加5 mL 正硅酸乙酯(TEOS),搅拌6h,过滤得全硅MCM-41分子筛原粉;250℃烘焙2 h, 600℃下焙烧4 h,得到全硅MCM-41介孔分子筛。最终测定MCM-41介孔分子筛的表征谱线。
本发明所述的MCM-41介孔分子筛掺杂碳糊电极的制备:石墨粉、MCM-41介孔分子筛按90:10研磨混合均匀,加5~6滴硅油进一步研磨,将研磨好的石墨粉末装进8cm的玻璃管中,插入导电铜丝。
本发明的特点在于通过制备MCM-41介孔分子筛掺杂的碳糊电极检测头孢哌酮。MCM-41介孔分子筛一方面有序孔道可以吸附头孢哌酮,增强电信号,因此以MCM-41介孔分子筛掺杂的碳糊电极测定头孢哌酮具有高的灵敏度。
附图说明
图1为MCM-41介孔分子筛的小角XRD衍射图;
图2为不同电极下头孢哌酮的差分脉冲伏安曲线;
图3为头孢哌酮浓度与峰电流的关系曲线。
具体实施方式
实施例1:MCM-41介孔分子筛的制备
用氨水作为碱源调节pH,水热法合成的步骤如下(原料配比按下表):用天平称取1.20 g CTAB于100 mL三口烧瓶中,加入50 mL蒸馏水,60 oC水浴加热,磁力搅拌至CTAB溶解。搅拌条件下加入25%的氨水调节pH至10.2,混匀后,缓慢滴加5 mL TEOS,逐渐生成白色沉淀。继续搅拌6 h后取出,在循环水式多用真空泵上抽滤,并不断用热蒸馏水冲洗,得全硅MCM-41分子筛原粉。室温下干燥后,将所得半成品放入瓷坩埚,置于马弗炉中先以250 oC烘焙2 h,然后在600 oC下焙烧4 h,取出,冷却,得到全硅MCM-41介孔分子筛。
实施例2:裸电极的制备
用天平称量1.0 g石墨粉放入玛瑙研钵中进行研磨,研磨过程中尽可能的朝着一个方向进行,当看到石墨粉不再是细小的粉状的时候滴加5~6滴硅油,继续进行研磨,再次研磨的时候也要尽可能的朝着一个方向进行,同时要避免石墨粉由于用力过大,带出研钵之外。当发现研钵中的石墨粉呈现良好的片状的时候,停止研磨,将研磨好的石墨粉末装进内径五毫米,长8 cm的玻璃管中,用细玻璃棒进行压实,插入铜丝,利用称量纸将电极的另一头打磨光亮,待用。
实施例3:MCM-41介孔分子筛修饰电极的制备
用天平秤取0.10 g MCM-41介孔分子筛白色粉末、0.90 g石墨粉置于玛瑙研钵中,充分研磨待看不到白色粉末后,逐滴加入6滴硅油,混匀后继续研磨,待研磨均匀充分后,装入玻璃管中,用玻璃棒压实。截取一段铜丝,用砂纸打磨掉表面污垢及氧化物至铜丝表面光亮,在1cm处缠上绝缘胶带,使之恰好插入玻璃管的一端,铜丝插入碳粉内,胶带与碳粉表面相接。做好电极后,贴标签待用。
实施例4:磷酸-NaOH 缓冲溶液的配制
配制1 mol/L H3PO4溶液:用移液管量取17.10 mL的分析纯磷酸于500 mL容量瓶中,加二次蒸馏水至刻度线定容,摇匀待用。
配制 1 mol/L NaOH溶液:用托盘天平秤取20.0 g氢氧化钠固体于小烧杯中,加适量二次蒸馏水,搅拌使其溶解,放置冷却,用玻璃棒引流转移至500 mL容量瓶中,二次蒸馏水定容后摇匀待用。
1 mol/L H3PO4 溶液与1 mol/L NaOH 溶液按不同体积比例混合,利用pH计测定溶液的pH,配制一系列不同pH值的H3PO4-NaOH缓冲溶液。
实施例5:头孢哌酮溶液的配制
用分析天平称取头孢哌酮标准品112 mg于小烧杯中,加入去离子水溶解,用玻璃棒搅拌使其溶解,冷却至室温后,用玻璃棒引流移入容量瓶内,用去离子水洗涤烧杯和玻璃棒多次,将洗涤液移入容量瓶,用去离子水定容,摇匀,得1×10-3 mol/L的头孢哌酮溶液。
用移液管取1×10-3 mol/L的头孢哌酮溶液5.0 mL于50 mL的容量瓶中,加pH=1.0的PBS缓冲溶液至刻度线定容,摇匀,贴上标签待用。即得浓度为1×10-4 mol/L的头孢哌酮溶液。
用移液管取1×10-4 mol/L的头孢哌酮溶液5.0 mL于50 mL的容量瓶中,加pH=1.0的PBS缓冲溶液至刻度线定容,摇匀,贴上标签待用。即得浓度为1×10-5 mol/L的头孢哌酮溶液。
用移液管取1×10-4 mol/L的头孢哌酮溶液10.0 mL于50 mL的容量瓶中,加pH=1.0的PBS缓冲溶液至刻度线定容,摇匀,贴上标签待用。即得浓度为2×10-5 mol/L的头孢哌酮溶液。
用移液管取1×10-4 mol/L的头孢哌酮溶液25.0 mL于50 mL的容量瓶中,加pH=1.0的PBS缓冲溶液至刻度线定容,摇匀,贴上标签待用。即得浓度为5×10-5 mol/L的头孢哌酮溶液。
用移液管取1×10-5 mol/L的头孢哌酮溶液5.0 mL于50 mL的容量瓶中,加pH=1.0的PBS缓冲溶液至刻度线定容,摇匀,贴上标签待用。即得浓度为1×10-6 mol/L的头孢哌酮溶液。
用移液管取1×10-5 mol/L的头孢哌酮溶液10.0 mL于50 mL的容量瓶中,加pH=1.0的PBS缓冲溶液至刻度线定容,摇匀,贴上标签待用。即得浓度为2×10-6 mol/L的头孢哌酮溶液。
用移液管取1×10-6 mol/L的头孢哌酮溶液5.0 mL于50 mL的容量瓶中,加pH=1.0的PBS缓冲溶液至刻度线定容,摇匀,贴上标签待用。即得浓度为1×10-7 mol/L的头孢哌酮溶液。
上述溶液配制好后用保鲜膜密封,放于冰箱4℃保存待用。
实施例6:头孢哌酮在不同修饰电极上的电化学响应
分别用裸电极、MCM-41修饰电极、联苯-PMO修饰电极、Co-SBA-15修饰电极做工作电极,对头孢哌酮溶液进行差分脉冲伏安(DPV)扫描,DPV的测定参数为:脉冲幅度0.07 V、脉冲宽度0.02 s。实验中支持电解质为pH为1.0的H3PO4-NaOH 缓冲溶液,头孢哌酮的浓度为1×10-4 mol/L。
头孢哌酮的电流响应在不同电极上强度不同,如图2所示。与使用裸电极相比较,头孢哌酮的电化学响应在使用联苯-PMO修饰电极、Co-SBA-15修饰电极时,无明显改善,均较低。而用MCM-41修饰电极时,头孢哌酮的电化学响应显著性增强。因此本实验所制备的MCM-41修饰电极为测定头孢哌酮的良好电极,具有较好的灵敏度。
实施例7:测定不同浓度甲硝唑的电化学响应
用pH为1.0的缓冲溶液配制一系列不同浓度的头孢哌酮待测液,待测液浓度分别为:1.0×10-7mol/L、1.0×10-6 mol/L、2.0×10-6 mol/L、 2.0×10-5 mol/L、 5.0×10-5 mol/L、1.0×10-4 mol/L、1.0×10-3 mol/L。MCM-41修饰电极为工作电极,对其进行差分脉冲伏安(DPV)测定,DPV的测定参数为:脉冲幅度0.07 V、脉冲宽度0.02 s。峰电流与头孢哌酮浓度间的线性关系,随头孢哌酮浓度的增加,峰电流也逐渐增加。
实验对头孢哌酮钠在MCM-41介孔分子筛修饰电极上的电化学性质进行了分析。头孢哌酮钠在碳糊电极均发生了不可逆的的电化学氧化过程MCM-41介孔分子筛修饰电极可大大提高信号强度。在扫描速度从10 mV/s到1000 mV/s,头孢哌酮钠的峰位发生正移,峰电流逐渐增大。头孢哌酮钠的电流响应随pH值增大而逐渐减小且pH为1.0时,氧化电流最大。可见MCM-41介孔分子筛修饰的碳糊电极为工作电极可以很好的检测头孢哌酮钠。
- 还没有人留言评论。精彩留言会获得点赞!