一种基于酶联免疫法的Septin9检测试剂盒的制作方法
本发明专利是涉及医学临床诊断技术领域,特别是涉及一种基于酶联免疫法的Septin9检测试剂盒。
背景技术:
Septin是一个广泛存在于除植物以外所有真核生物中的基因家族。最初认为septin家族是与酵母细胞胞质分裂相关的基因家族,然而随着研究的深入,人们发现这类基因编码的蛋白在许多生物体内出现了较大的功能分化,尤其是在哺乳动物中,他们不仅成员众多,而且参与了细胞分裂、细胞极化、囊泡运输及胞膜重构等多个过程。更引起研究人员重视的是:最近有大量的数据表明,这一家族的一些成员与肿瘤发生、神经功能障碍和病原微生物感染的过程直接相关。
SEPT9定位于染色体17q25.3,该染色体区段是散发性卵巢癌和乳腺癌的常见杂合性丢失部位。在卵巢癌,约70%的17q等位基因丢失为17q25。Kalikin等以17个微卫星标记确定了卵巢癌17q的最小缺失区,并克隆到了一个候选肿瘤抑制基因,命名为,arian/breast(Ov/Br)septin蛋白(即SEPT9)。但是,新近研究又支持SEPT9为潜在原癌基因。在PyV-mT过渡表达所致的乳腺癌,SKY和CGH检测发现17q25.3区有扩增,RT-PCR证实有SEPT9基因表达上调,9个乳腺癌细胞系中表达也上调。SEPT9表达上调的乳腺癌细胞系Thsp-1和Bax下调,细胞凋亡受抑制。siRNA抑制septin 9表达后,细胞凋亡抑制效应解除。7287例人新鲜组织和292个人细胞系的Affymetrix HG_U133基因芯片检测结果的分析表明,SEPT9在乳腺、中枢神经系统、子宫内膜、肾脏、肝、肺、淋巴、食管、卵巢、胰腺、软组织、皮肤、甲状腺等来源的肿瘤中高表达,RT-PCR与免疫组织化学染色的结果大致与芯片结果一致。最近前列腺癌细胞系体内外实验研究发现,MSF-(SEPT9-vla)可以通过抑制缺氧诱导因子1a(hypo-xia-inducible factor-,HIF1a)的泛素化降解途径,从而促进HIF1a的表达,并促进肿瘤血管形成。该研究为septin家族在肿瘤发生、发展中的作用提供了直接证据。
Septin9蛋白是一个潜在的重要的肿瘤标志物,但是目前检测septin9蛋白的方法复杂且昂贵,因此,需要一种准确快速定量的检测方法满足科学研究已经临床的需要。本发明提供的人septin9酶联免疫试剂盒,可以快速准确的检测人血液、组织液等体液中的septin9的含量。
技术实现要素:
本发明提供一种基于酶联免疫法的Septin9检测试剂盒。该试剂盒具有检测灵敏度高,特异性强,操作简单,稳定性好,无污染,重复性好的特点。
一种人septin9酶联免疫检测试剂盒,主要包括:
(1)包被有septin9特异性抗体的酶标板;
(2)酶标记物(为酶标记的septin9特异性抗体);
(3)Septin9标准品溶液;
(4)底物显色液;
(5)终止液;
(6)浓缩洗涤液。
本发明提供的septin9酶联免疫检测试剂盒,包括包被有septin9特异性抗体I的酶标板,酶标记物(为酶标记的septin9特异性抗体II)。所述septin9特异性I和特异性抗体II可以为多克隆抗体或单克隆抗体。
所述酶标记物的标记酶为辣根过氧化物酶(HRP)或碱性磷酸酯酶(ALP),其中优选HRP;酶标记的septin9特异性抗体II采用戊二醛法或过碘酸钠法将标记酶与抗体偶联得到。
所述试剂盒还包括septin9标准品溶液、底物显色液、终止液和浓缩洗涤液。
所述底物显色液,当标记酶为HRP时,底物显色液由显色液A和显色液B组成,显色液A为过氧化氢或过氧化脲,显色液B为邻苯二胺或四甲基联苯胺(TMB),所述终止液为1-2mol/L硫酸。当标记酶为ALP时,底物显色液为对硝基苯磷酸酯缓冲液,所述终止液为1-2mol/L氢氧化钠。
本发明所述试剂盒中septin9标准品溶液6瓶,0ng/ml,0.3ng/ml,0.9ng/ml,2.7ng/ml,8.1ng/ml,24.3ng/ml,1ml/瓶。
本发明中酶标板的制备过程为:用包被缓冲液将septin9特异性抗体I稀释成0.05-0.1ug/ml,每孔加入100ul,用封板膜封闭,4℃过夜孵育,倒掉包被液,用洗涤液洗2次,拍干,然后每孔中加入150-200ul封闭液,37℃孵育1-2h,倒掉封闭液拍干,37℃烘箱干燥2h,铝箔真空密封保存。
其中酶标板制备过程中所用的包被缓冲液为pH9.6,0.05M碳酸盐缓冲液;所用封闭液为含有BSA 1%,小牛血清20%,叠氮钠0.05%的pH 7.4 0.1M磷酸盐缓冲液。
本发明的septin9酶联免疫检测试剂盒采用双抗体夹心法定量检测人血清、血浆或尿液中的septin9。将标准品和样品加入到酶标板的微孔中,再加入酶标抗体室温下孵育30min,样本中的septin9与微孔中抗体及酶标抗体特异性结合,形成双抗体夹心的结构,之后冲洗。再加入显色底物液,底物在酶标抗体上HRP或ALP作用下,显色15分钟,加入终止液中止反应,在酶标仪下450nm处读取 吸光度,septin9浓度与吸光度高低呈正比。
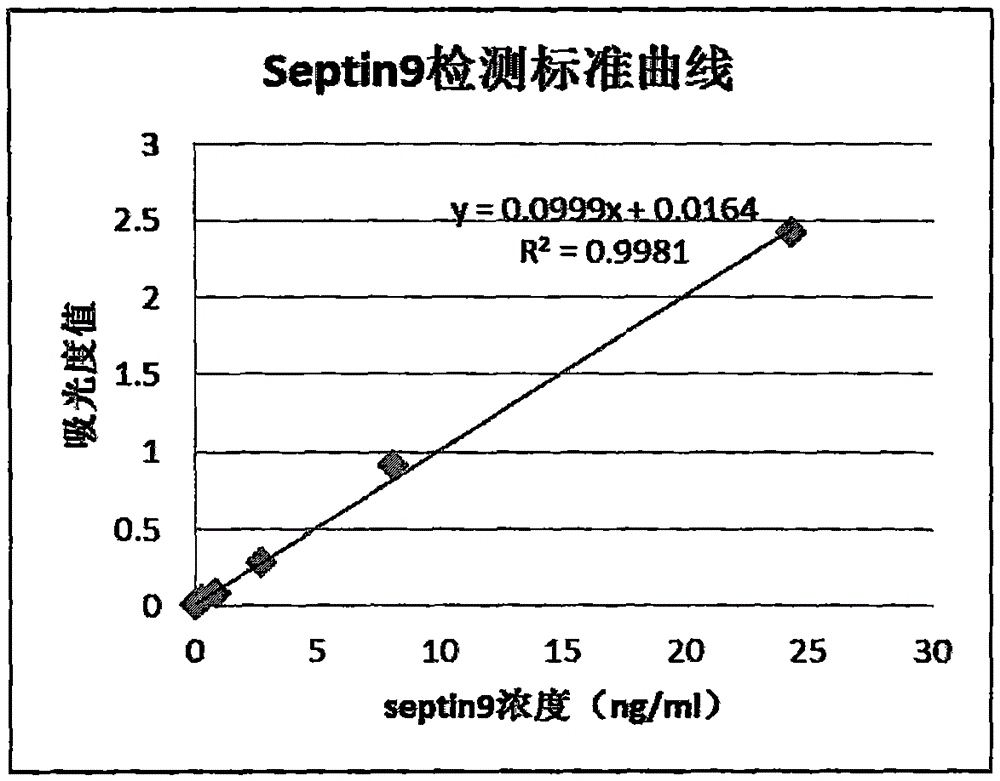
本发明检测结果分析过程为:以标准品浓度和吸光度值做标准曲线,以标准品浓度为X轴,吸光度值为Y轴,绘制标准曲线,相应的,根据每个样品吸光度值即可从标准曲线上读出样本中septin9的含量。
本发明标准曲线绘制也可以采用双对数法,以样品浓度值的对数为X轴,以吸光度值的对数Y为轴,绘制标准曲线,相应的,根据每个样品吸光度值的对数即可从标准曲线上读出样本中septin9浓度值的对数,进而获得其实际浓度。
上述septin9酶联免疫检测试剂盒与目前通常使用的同类检测试剂盒相比,具有明显的优势。首先,免疫反应由两步变为一步,缩短了免疫结合的时间由1h降低为0.5h。其次,HRP或ALP直接标记septin9抗体,由间接法变为直接法,省掉了二抗,降低了生产成本和操作难度。最后,采用单克隆抗体包被微孔板,提高了灵敏度,线性范围大于同类试剂盒,精密度和准确度均在试剂盒要求范围内。血清样本不需稀释,尿液样本不需处理即可直接加样,操作方法比同类试剂盒简单,一般技术人员即可操作。
附图说明
图1:septin9的检测标准曲线。
具体实施方式
下面结合具体的实施例来进一步阐述本发明。应理解,这些实施例仅用于说明本发明,而不用来限制本发明的范围。
实施例1试剂盒制备
1 septin9酶标单抗制备
采用改良过碘酸钠法。以标记20mg单抗为例:准确称取HRP 40mg,加入0.2M pH5.6醋酸缓冲液2ml,溶解后加入0.06MNaIO4溶液2ml,室温反应20min。加入0.16M乙二醇-10%NaCl溶液2ml,室温反应20min,将酶液装入透析袋中,对0.001M pH4.0醋酸盐缓冲液透析过夜;加入2M pH 9.6碳酸盐缓冲液0.8ml,加入septin9特异性单抗II20mg,4℃搅拌反应2h;加入新配制的5mg/ml NaBH4溶液0.4ml,4℃搅拌反应2h;滴加饱和硫酸铵溶液9.2ml,4℃搅拌反应30min,4℃3500rpm离心20min,弃上清,将沉淀溶于2ml 0.02M pH7.4的磷酸盐缓冲液,用0.02M pH7.4的磷酸盐缓冲液透析24h,加2ml甘油,混匀后-20℃保存。
2酶标板制备
将septin9特异性抗体I用pH 9.6 0.02M碳酸盐缓冲液稀释,终浓度为5ug/ml。在96孔酶标板中每孔加入100ul的包被液,2-8℃过夜。用PBST洗涤液洗涤4次,然后每孔加入200ul的封闭液(含BSA 1%,小牛血清20%,叠氮钠0.05%的pH 7.4 0.1M磷酸盐缓冲液),放入37℃烘箱中2h,甩去封闭液,干燥后装入铝箔袋2-8℃保存。
3酶标试剂配制
配制含有20%小牛血清、1%BSA的pH 7.4的0.02M磷酸盐缓冲液,即为酶标稀释液,用酶标稀释液将实施例1中制备的septin9抗体酶复合物按照1∶1500稀释,分装后2-8℃保存。
4标准品配制
称取一定量septin9标准品用空白血清稀释成如下浓度0ng/ml,0.3ng/ml,0.9ng/ml,2.7ng/ml,8.1ng/ml,24.3ng/ml,分装后2-8℃保存。
5显色剂A、B,终止液,20X浓缩洗涤液
显色液A为0.05%的过氧化脲溶液。
显色液B为0.03%的TMB溶液。
20X浓缩洗涤液为0.2M PBST溶液。
终止液为2M硫酸溶液。
实施例2试剂盒检测方法
1准备:将试剂盒放置于室温下平衡20min。
2配液:将50ml浓缩洗涤液(20X)用蒸馏水稀释至1000ml备用。
3加样:分别在相应孔中加入标准品和待测样品50ul,震荡混匀,然后加入50ul酶标二抗,震荡混匀。
4温育:用封板膜封板,37℃温育30min。
5洗涤:温育后将封板膜揭掉,吸干孔内液体,用稀释好的洗涤液洗涤4次。
6显色:每孔加入显色剂A、B液个50ul,轻轻震荡混匀,用封板膜封板后37℃温育避光显色15min。
7终止:每孔加入终止液50ul,轻轻震荡混匀。
8测定:设定酶标仪波长与450/630nm检测,测定各孔0D值。
9绘制标准曲线:以标准品浓度为X轴,吸光度值为Y轴做标准曲线。或者以标准品浓度对数值为X轴,吸光度对数值为Y轴做标准曲线。以标准曲线R2≥0.98,且浓度最高标准品吸光度值大于1.0为合格的标准曲线,否则重复步骤1-8。
实施例3试剂盒最低检出限
本实施例检测本发明试剂盒的检出限。具体操作为:抽取一盒试剂盒,按照实施例2的方法检测样品稀释液,重复检测20次,计算检测0D值的平均值(M)和标准差(SD),计算M-2SD的值,将M-2SD对应的吸光度值代入标准曲线,计算所得到的浓度值即为试剂盒检出限,经过验证本试剂盒的检出限为0.01ng/ml。
实施例4试剂盒特异性
本实施例检测本发明试剂盒的特异性。具体操作为:抽取一盒试剂盒,按照实施例2的方法检测100ng/ml NAGL、100ng/mlC反应蛋白、100ng/ml胱抑素 C,检测结果应小于0.1ng/ml。
实施例5试剂盒重复性
本实施例检测本发明试剂盒的重复性。具体操作为:抽取一盒试剂盒,按照实施例2的方法检测浓度为1.0ng/ml的标准品溶液,重复检测10次。计算测定结果的平均浓度和标准差(S),按照公式(1)计算变异系数(CV),CV应不高于10%。
实施例6试剂盒的剂量-反应曲线的线性
本实施例检测本发明试剂盒的剂量-反应曲线的线性。具体操作为:抽取一盒试剂盒,按照实施例2的方法检测浓度为检测浓度为0ng/ml,0.3ng/ml,0.9ng/ml,2.7ng/ml,8.1ng/ml,24.3ng/ml的septin9测定样品液,每个浓度检测2支,记录各浓度水平的测量结果,并计算各浓度水平两次测量值的平均值(yi),以浓度值(xi)为自变量,以测定结果均值(yi)为因变量求出线性回归方程。按公式(2)计算线性回归的相关系数(r),r应≥0.975。其中为5个浓度值的平均值;为测量值的平均值。
实施例7试剂盒稳定性
本实施例检测本发明试剂盒的稳定性。具体操作为:将试剂盒2-8℃下放置1年,分别在第1、2、3、6、8、12、15个月检测,其检出限、特异性、重复性、剂量-反应曲线的线性应符合要求。
- 还没有人留言评论。精彩留言会获得点赞!
- 用于检测卡巴氧和喹赛多代谢产物的单克隆抗体及酶联免疫方法和试剂盒的制作方法
- 用于检测乙酰甲喹和喹乙醇代谢产物的单克隆抗体及酶联免疫方法与试剂盒的制作方法
- 用于检测硝基咪唑类药物的单克隆抗体及酶联免疫方法与试剂盒的制作方法
- 用于检测苯乙醇胺a的单克隆抗体及酶联免疫方法与试剂盒的制作方法
- 用于检测雄激素类药物的单克隆抗体及酶联免疫方法及试剂盒的制作方法
- 用于检测甲睾酮的单克隆抗体及酶联免疫方法与试剂盒的制作方法
- 用于检测苯二氮卓类药物的单克隆抗体及酶联免疫方法与试剂盒的制作方法
- 用于检测吩噻嗪类药物的单克隆抗体及酶联免疫方法与试剂盒的制作方法
- 抗人胃癌相关蛋白gcrg213的单克隆抗体的制作方法
- 一种百菌清酶联免疫检测方法