生物测定系统以及检测体液内分析物的方法与流程
本发明涉及一种生物测定系统以及一种用于检测体液内分析物的方法。更具体而言,本发明涉及一种包括共振光栅结构的生物测定装置(例如免疫测定装置),以及一种利用上转换纳米颗粒(upconverting nanoparticle)和该共振光栅结构来检测体液中的分析物的方法。
背景技术:
传统上,在生物测定装置中将荧光团用作标记。然而,荧光团随着时间流逝而发生光漂白(photobieaching)。已经进行了各种尝试以使用上转换纳米颗粒(即,直径在1纳米至100纳米之间并且发射光波长短于激发光波长的颗粒)作为生物测定装置中的标记,因为上转换纳米颗粒不会发生光漂白。然而,上转换纳米颗粒的应用引发了其他问题。例如,由于上转换纳米颗粒的量子效率低,并且它们的激发需要相对高的光水平(例如,100mW的980nm聚焦光),所以上转换纳米颗粒的发光相当弱。因为上转换纳米颗粒的量子效率(QE)通常小于0.3%,所以上转换发光弱。相比之下,常规荧光标记明显更亮,因为它们的QE可以大于20%。用于改善上转换发光的一种方法是化学改性纳米颗粒表面,但是该方法的成功具有限制性。
技术实现要素:
上转换纳米颗粒是生物测定中有前景的荧光团和/或标记,因为它们提供了几乎无背景的检测系统,基本上没有光漂白作用。本文所使用的“上转换”是指在比激发光短的波长下发射光。例如,纳米颗粒可以吸收多个近红外(NTR)光子(例如,在约980nm处的两个或三个光子),然后在可见区域发射绿光(约510nm)或红光(约650nm)。在生物样品中很少发生“上转换”过程(即,在比激发光波长短的波长下发光)。利用常规连续波(CW)光源(例如,不需要具有高峰值功率,导致高自体荧光的飞秒脉冲NIR激光器)能够观察到该过程。因此,探测光束将仅触发来自上转换纳米颗粒的发光,并且几乎从不触发来自生物样品的发光。因此,当将NIR CW光用于激发并且对蓝色偏移的发射进行检测时,使用上转换纳米颗粒可以获得几乎无背景的检测。
在生物测定应用中,这样的无背景检测可以使得感测能力得到改进。通常,背景水平决定测定中的检测下限,当背景水平太高时,测量精度受损。特别地,UV光源通常用于生物测定中,其导致来自样品的自体荧光和散射的高背景,并且在体液样品(例如全血)的分析中无法获得分析结果。
因此,需要开发一种新型生物测定装置,其可以解决光漂白的问题、减少背景和光散射(这是常规光源(例如UV光)的特征),并增强来自目标分析物的发光。下面将对上转换纳米颗粒如何用作为标记,以克服发光弱、荧光团漂白和来自样品的背景自体荧光的问题进行更详细地描述。本发明的一个目的在于增强来自上转换纳米颗粒的发光,联合共振光栅结构以实现用于检测分析物(例如但不限于体液中的蛋白质,病原体和电解质)的高灵敏度生物传感平台。上转换纳米颗粒的增强的发光是重要的,因为相对于传统荧光染料、量子点或其他荧光标记而言,上转换纳米颗粒的背景信号更低且灵敏度更高,从而在生物测定中具有测量精度优异的性能,所述生物测定例如但不限于免疫测定应用。
在一个方面中,本发明提供了一种用于检测体液(例如血液、血清、血浆、滑液、脑脊液和尿液)中的目标分析物的生物测定系统。一般而言,生物测定系统包括两个部分:(i)生物传感器,包括:例如包括共振光栅结构的波导,所述共振光栅结构限定增强区域,该增强区域从表面开始并且沿着垂直于所述表面的方向延伸预定距离;以及第二抗体,该第二抗体针对通过连接化学物质结合到所述共振光栅结构表面的所述目标分析物;和(ii)与第一抗体缀合的上转换纳米颗粒,该第一抗体针对所述目标分析物的表位,该表位与第二抗体所针对的表位不同。上转换纳米颗粒包括吸收红外光并响应于红外光的吸收而发射可见光的光学性质。
在本文所述系统的一个实施方案中,目标分析物结合到抗目标分析物抗体上,该抗目标分析物抗体与上转换颗粒缀合,所述上转换颗粒例如为NaYF4:(Yb,Er,Tm)、NaYbF4:(Yb,Er,Tm)、CaF2:(Yb,Er)、La2O3:(Yb,Er)。该目标分析物还结合到第二抗目标分析物抗体(不同于第一抗目标分析物抗体)上,该第二抗目标分析物抗体通过连接化学物质(例如通过链霉亲和素)偶联到共振光栅结构的表面上。因此,目标分析物被纳米颗粒通过第一抗体被“标记”,并被第二抗体“捕获”到共振光栅结构的表面。在共振光栅结构的表面处,光学检测目标分析物。
在一个实施方案中,生物测定传感器还包括设置在共振光栅结构的表面上的高折射层(例如,TiO2和Ta2O5),该高折射层的折射率至少为1.5。共振光栅结构包括光子晶体,其被调谐到预定的共振条件;以及抗体,其通过连接化学物质偶联到所述共振光栅结构。在可替代的实施方案中,本发明提供了一种生物测定传感器,包括:包括共振光栅结构的波导;以及通过连接化学物质偶联到所述共振光栅结构的表面的抗体。
在另一方面中,本发明涉及一种物质组合物,其包含抗体和结合至所述抗体的上转换纳米颗粒。
在一个实施方案中,所述物质组合物还包含结合至抗体结合位点的目标分析物。
在还一方面中,本发明涉及一种免疫测定试剂盒,其包括具有共振光栅结构的装置和通过连接化学物质偶联到共振光栅结构的表面的第二抗体;和具有与第一抗体缀合的上转换纳米颗粒的物质组合物,其中所述第一抗体和所述第二抗体针对相同的目标分析物。
在还一方面中,本发明涉及一种用于检测体液中的目标分析物的方法。提供具有多个捕获位点的共振光栅结构。向共振光栅结构提供光学照射,所述共振光栅结构具有一个或多个目标分析物,该一个或多个目标分析物经由捕获位点的抗体偶联到捕获的上转换纳米颗粒上。检测来自捕获位点的光学反应,并且将其作为在相应的捕获位点是否存在目标分析物的指示。
如本文所使用的术语偶联是指将至少两种要素直接或间接连接在一起。
附图说明
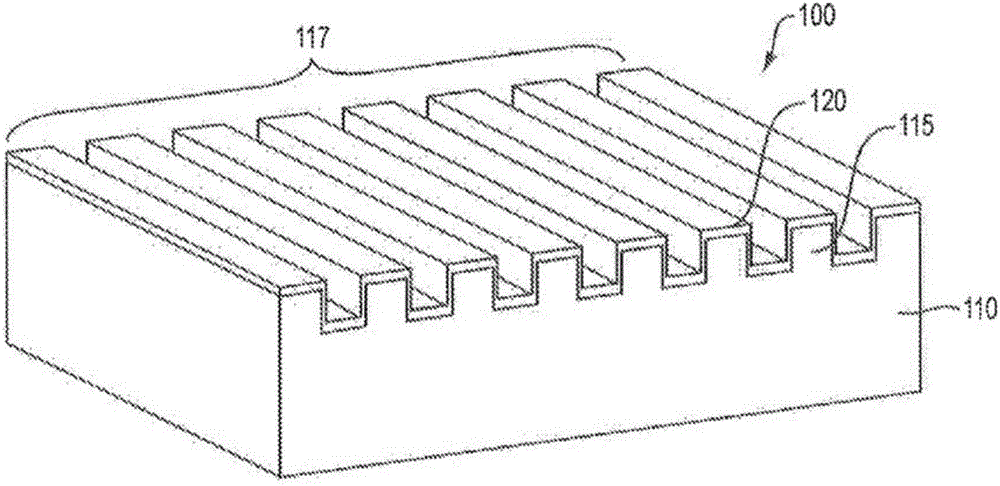
图1A示意性地示出了根据本发明的一个实施方案的具有光栅结构的共振波导的剖视图,图1B示出了其透视图。
图2示意性地示出了根据本发明的一个实施方案,在共振条件下衬底表面上的电场。
图3示意性地示出了根据本发明的一个实施方案,使用生物测定系统(例如免疫测定)感测分析物的方法。
图4示意性地示出了根据本发明的另一个实施方案,使用生物测定系统(例如免疫测定)感测分析物的方法,
具体实施方式
提高生物测定灵敏度的一种方法是通过使用基于聚合物的光栅衬底来增强发光,从而增加照射的光水平,但是这可能导致某些问题,例如高背景和样品温度升高以及样品损伤。例如,在这样的生物测定系统中,由于自体荧光,基于聚合物的光栅衬底开始呈现过量的背景。来自背景的这种干扰不适合用于高灵敏度的生物传感应用,例如免疫测定。虽然已经使用高质量和高纯度的石英衬底来解决这个问题,但是这些材料导致材料成本过高且制造工艺更加复杂。因此,本发明采用吸收近红外激发的上转换纳米颗粒联合共振光栅结构,以在用于检测分析物的生物传感平台中实现高灵敏度。
参见图1A和1B,图1A示出了传感器300的剖视图,图1B示出了传感器300的透视图,该传感器300包括根据本发明的一个实施方案的共振波导100和针对目标分析物的第二抗体320,该第二抗体通过化学连接315结合到共振波导100的表面。在一个实施方案中,化学连接315包括结合蛋白,例如链霉亲和素。
继续参见图1A和1B,共振波导100包括衬底110,其具有形成在衬底110的表面112上的光栅结构115和形成在光栅结构115的表面112上的折射层120。在一个实施方案中,可以在折射层120上形成一个或多个其他的折射层(未示出)。
继续参见图1A,在一个实施方案中,衬底110由光学透明材料或聚合物材料(例如,但不限于聚苯乙烯、紫外线可固化聚合物或玻璃)制成,并且形成这样的光栅结构115,其具有约360nm的光栅周期,深度为约50nm的光栅凹槽以及约36%的占空比。应当理解的是,光栅周期的范围为约200nm至约500nm;光栅凹槽深度的范围为约30nm至约300nm;折射层120(折射率大于1.5)的厚度范围为约30nm至约200nm;并且占空比的范围约30%至约50%。衬底110是透明的并且与近红外(NIR)激发和来自上转换纳米颗粒的发射的可见光检测相容。光栅材料由例如但不限于以下材料制成:SiO2、诸如聚苯乙烯等的聚合物材料、硅酮、热塑性塑料或诸如熔融二氧化硅和石英等的玻璃。
在一个实施方案中,折射层120可由高折射材料(例如,折射率为约2.35的TiO2或折射率为约2.09的Ta2O5)制成。应当理解的是,光栅的各种形式和构造可能产生共振模式,并且可以增强上转换纳米颗粒的激发。例如,在本发明的一个实施方案中,光栅具有多于一层的高折射材料的薄涂层,并且当纳米颗粒接近表面112(在约1至150nm的范围内,优选在约1至2000nm的范围内,更优选在300nm以下)时增强激发光的强度。光栅结构115和折射层120的所得表面表现得非常类似于光栅,但是被调谐到出现增强情况的特定共振模式和波长。在共振波长处,衬底表面112上或上方的易消散的电场非常高(例如,比没有光栅时大50倍),因此诸如上转换纳米颗粒的表面标记物可以强烈发射。虽然在图1A中示出和描述了折射层120,但是应当理解,共振波导100仍然可以构成为光子晶体,而不存在折射层120。
图2示意性地示出了根据本发明的实施方案,在共振条件下衬底110的表面上的电场。如图2所示,光束210从衬底110的与表面112相对的表面114(参见图1A)撞击。多个上转换纳米颗粒350结合到光栅结构115的表面112上,在其上形成折射层120,在一个实施方案中,上转换纳米颗粒350与针对目标分析物(未示出)的抗体(未示出)缀合。该目标分析物结合到纳米颗粒缀合的抗体上,并通过针对目标分析物的第二抗体(未示出)在表面112被捕获。第二抗体通过连接化学物质240(例如但不限于,链霉亲和素,经由反应性官能团(例如氨基、羟基、巯基和羧基)的表面偶联,经修饰的DNA探针以及肽)结合到表面112上。
参见图1A、1B和2,在一个实施方案中,被引导到衬底110的表面114的光束210的波长与构成光子晶体的光栅结构115的共振条件相匹配。作为结果,在衬底110的纹理化表面117上的增强区域230处,极大地增强了光束210的强度。在该实施方案中,纹理化表面117由光栅结构115(平行脊和谷)形成,如图1B所示。应当理解,在其他实施方案中,纹理化表面117可以由突起(例如,柱和杆)阵列或凹陷(例如,圆形凹陷、矩形凹陷和六边形凹陷)阵列形成。在理想的情况下,在不使用光子晶体的条件下,相对于光束210的强度,光束强度的增强可以高达1500倍。在一个实施方案中,增强较小,并且可以达到约50倍。
可用于增强发光的其他材料是(例如)由金属膜制成的等离子体表面结构。在一个实例中,使用等离子体纳米天线(在柱结构上的金点)将上转换纳米颗粒的发光增强差不多300倍。该实施方案的优点是上转换纳米颗粒/标记比常规荧光团更具有鲁棒性且不发生光漂白以及持续很长时间(例如,上转换纳米颗粒/标记为几小时,而常规荧光团为几分钟)。然而,等离子体结构通常更难以制造,并且可能具有若干缺点,例如可引起加热效应的强光吸收。在本发明的又一个实施方案中使用的透明介电材料避免了这个问题。
在一个实施方案中,用于生物医学测定感测应用的高灵敏度系统包括两个部件。例如,第一部件是包括共振光栅结构和二级抗体的传感器,该共振光栅结构由透明介电材料(例如光子晶体波导)制成,该二级抗体针对结合到所述共振光栅结构的表面的目标分析物。在优选的实施方案中,第二部件包括上转换纳米颗粒,其结合到一级抗体上,该一级抗体与二级抗体针对相同的目标分析物。本发明还涵盖除了上转换纳米颗粒以外的缀合物,例如常规的荧光团或下转换纳米颗粒。该系统设计用于高灵敏度测定应用,以提供低的成本并且易于大规模的生产,而且该系统具有最小的背景信号。
继续参见图2,本发明的系统具有改进的灵敏度,在增强区域230处具有增强的场。上转换颗粒350位于共振光栅结构100的增强区域230中,其从衬底110的表面112处开始延伸超过100纳米,应当理解的是,增强区域230在表面112处具有亮线(brightline)边界,但是随着远离表面112逐渐减小的电场而具有相当模糊的边界。在一个实施方案中,可以将模糊的边界定义为轮廓线,其中电场是邻近表面112的最强电场的一半。发光可以被增强约50倍以上,从而提高了测定灵敏度。
本发明的传感器具有优于常规免疫测定系统的许多优点。首先,本发明不会出现来自于自体荧光的强烈背景信号的问题。光栅结构115具有这样的光栅周期、光栅凹槽深度、占空比,使得在本发明的一个实施方案中,光栅115的共振被调谐为上转换纳米颗粒350的吸收峰为980nm,并且照射光源210垂直入射。在该实施方案中,基本上没有来自衬底110的背景,因为980nm的光不会引起来自光栅115或来自待分析的体液样本的自体荧光。
根据本发明的生物测定系统具有优于常规生物测定系统(例如免疫测定系统)的额外优点。例如,本发明的传感器不会出现荧光团的光漂白的问题。已知上转换纳米颗粒350非常稳定,并且不会发生光漂白,并且能够更好地处理邻近表面的高电场。常规的荧光团不是所期望的,并且光漂白快。
另外,本发明的传感器具有增强的局部表面发射。上转换纳米颗粒350在照射强度上具有非线性的吸收依赖性。由于这种非线性特性,仅选择性地激发结合的纳米颗粒或接近表面的纳米颗粒。作为结果,几乎没有来自周围介质的发射。
此外,本发明的传感器适用于均质测定应用。由于结合的纳米颗粒的增强的表面发射,可以消除测定洗涤步骤,从而获得更简单的系统设计。
此外,本发明的传感器不需要聚焦光照射。在此公开的发明中,不需要激光器(或相干光源),因为来自共振光栅的增强效应增加了强度,而不需要聚焦和高功率的激光器。低成本非相干光源(例如但不限于LED、气体放电灯和高强度放电灯)可以用来代替激光器。
图3示意性地示出了使用根据本发明的一个实施方案的生物测定装置检测分析物的方法。在步骤10中,将物质组合物345与体液混合,该物质组合物345包含与靶向目标分析物330的第一抗体340缀合的纳米颗粒350,该体液例如为血液、血清、血浆、滑液、脑脊液或尿液,所述体液中怀疑存在目标分析物330。在一个实施方案中,通过在用于将纳米颗粒与抗体偶联的有机或无机溶剂中,将纳米颗粒350和针对目标分析物的第一抗体340混合,从形成物质组合物345。在其他实施方案中,纳米颗粒标记的抗体是混合在含有待检测的疑似分析物330的流体中的粉末形式。
在下一个步骤,即步骤20中,将结合到分析物330的纳米颗粒标记的抗体345施加到具有共振波导光栅表面112的生物测定传感器300上。在一个实施方案中,生物测定传感器300包括具有光栅结构310的衬底110,形成在光栅结构310的表面上的折射层120,以及第二抗体320,其针对偶联并固定到光栅结构310的表面312的目标分析物330。在一个实施方案中,光栅结构310的每个光栅周期包括与其偶联的抗目标抗体,以构成目标分析物捕获位点305。在一个实施方案中,第二抗体320通过连接化学物质315(例如,链霉亲和素)固定在光栅结构310上,以捕获来自待分析的患者体液中的目标分析物330,该目标分析物330偶联到例如纳米颗粒上,所述纳米颗粒选自由NaYF4:Yb-Er,CaF2:Yb,Er,NaYbF4:Ho,Tm,Er所构成组中。捕获的分析物360与第二抗体320结合,该第二抗体320针对相同的目标分析物330并且偶联到光栅结构300的表面312。在一个实施方案中,利用纯水洗涤生物测定传感器300以从衬底110上去除未捕获的分析物。生物测定传感器300现在准备好可以进行光学检查。
在步骤30中,将光(例如具有约980nm波长的近红外(NIR)光束)施加到衬底110的表面114,该表面114在光栅结构300与表面312相对的衬底110的一侧上,表面312可以包括折射层120。因为选择NIR光束以匹配光栅结构310的共振条件,所以与被定向到目标分析物330的第一抗体340缀合并通过也被定向到目标分析物330的第二抗体320结合到光栅表面312的上转换纳米颗粒350被增强的NIR激发。取决于上转换纳米颗粒350的光学性质,响应于增强的NIR激发而发射光束(例如可见光)。使用光检测器400确定捕获位点350处的是/否存在分析物330。
在一个实施方案中,上转换纳米颗粒350在“夹心”测定中缀合到抗体340上,以在共振光栅结构310表面上的捕获位点305处,检测结合到第二抗体上的捕获的目标分析物330,该第二抗体针对目标分析物330。光栅结构310的共振被调谐到使它们的吸收峰的峰值具有最大的增强效果并使得测定灵敏度得到提高。
在另一个实施方案中,生物测定传感器用于“阻挡测定”应用中,其中颗粒与共振光栅结构310的表面的结合导致共振模式的“失调”并减弱增强效应。表面结合事件导致折射层120的折射率改变,并且足以使共振远离照明波长而失调。例如,具有非常窄的波长带宽的激光和具有高品质因素共振结构的光栅、或具有非常窄和尖锐的共振峰的光栅是用于检测表面处的折射率变化的非常灵敏的布置。随着共振远离激光波长而失调,可以观察到上转换纳米颗粒的增强的发射急剧下降。
在还一个实施方案中,本发明的感测系统利用相对窄的增强区域(在该区域中发生增强)并且可用于检测结合动力学,以及随着时间的推移跟踪目标分析物的量变。不受理论所束缚,但是据信,在光栅结构的表面处捕获的上转换颗粒的发光被限制为邻近光栅表面小于100nm的区域内。在100nm区域外的任何上转换纳米颗粒标记都不会被激发,因此具有比位于更接近光栅结构的表面且在100nm区域内的纳米颗粒少得多的发光。
例如,在一个实施方案中,光栅表面312首先通过预定的连接要素(例如凝血酶)预处理为具有标记(例如荧光团或纳米颗粒),所述连接要素易于通过靶蛋白的作用而裂解。当暴露于凝血酶时,标记在连接要素处裂解并远离增强区域扩散。因此,连接要素的裂解使标记远离光栅结构上方100nm区域内的表面游离,并且该标记不能被检测到。减少的发光使得能够定量测定目标蛋白,例如凝血酶。在另一个实例中,标记可以特异性结合表面312,并增加指示结合事件的信号。
在本发明的另一个实施方案中,如图4所示,生物测定系统以竞争性异质免疫测定模式配置,其中目标分析物330A(例如)结合至上转换纳米颗粒,以形成纳米颗粒标记的缀合分析物360。患者体液样品中的分析物330B未被标记。然后,将纳米颗粒标记的缀合分析物360施加到生物测定传感器300上,这样使捕获位点305结合有缀合的分析物360。此后,将包括经过分析的未标记分析物330B的患者体液施加到所得的“经标记的”生物测定传感器300上。患者的未标记目标分析物330B与纳米颗粒标记的目标分析物360竞争光栅表面偶联的抗目标分析物抗体320上的结合位点305。在引入患者的未标记的体液目标分析物330B时,标记的目标分析物360从光栅表面312释放并且自由地扩散到远离增强区230的溶液中(参见图2)。在存在患者未标记的分析物330B的情况下,由纳米颗粒标记的目标分析物360产生的可检测的光发射减少。这种配置通常用于激素和蛋白质的药物分析和临床生物化学中。在这种模式下,患者样品中的未标记的分析物330B与增强表面312处的经纳米颗粒标记的分析物360竞争。洗去未结合的分析物,并测量结合到光栅表面的剩余的经标记的分析物370。经标记的结合分析物360发光的减少与患者体液样品中的目标分析物的量成一定比例。
尽管已经详细描述了本发明的实施方案,但是应当理解,这些实施方案仅仅是为了示例和说明性的目的。在不脱离所附权利要求中限定的本发明的精神和范围的情况下,本领域技术人员可以进行各种修改和改变。
- 还没有人留言评论。精彩留言会获得点赞!