一种自供能miRNA生物传感器的制备方法与流程
本发明涉及miRNA生物传感器的制备方法,具体地说,设计一种基于酶生物燃料电池的自供能miRNA生物传感器的制备及其超灵敏检测miRNA。
背景技术:
酶生物燃料电池(EBFC)是一种特殊的燃料电池,其能在温和条件下,利用可再生燃料提供可持续能源,受到广泛关注。基于EBFC的自供能生物传感器,是一种以电池性能输出作为分析检测信号的一类传感器,该传感器信号与被检测分析物浓度成比例关系。与传统传感器相比,自供能生物传感器检测过程中无需施加额外电源,其具体优点主要表现在:(1)设备简单。检测过程不同于传统的电化学检测三电极体系,仅需两根电极,即EBFC的阴阳两极,便可实现检测;(2)抗干扰能力强。测试体系未施加额外电源,能有效避免易发生氧化还原的电活性物质在电极表面反应,从而提高了传感器的抗干扰能力;(3)能实现简单、快速、实时检测。检测过程中无需电化学工作站等供电设备,仅需简易电压表便可实现检测,故检测设备易携带,能实现实时监测。
MicroRNA(miRNA),约22个核苷酸大小的内源性非编码RNA,在多种生物过程如细胞分化,凋亡,增殖和免疫反应中具有重要作用,已成为用于检测多种癌症的诊断和预后评估的新生物标志物。目前,检测miRNA表达的方法主要有Northern印迹法、miRNA阵列和实时逆转录聚合酶链反应(RT-PCR)、电化学方法。Northern印迹法方法灵敏度低、费时费力、样品需求量大。微阵列检测法同样存在灵敏度较低的缺点,并且特异性较弱。RT-PCR具有高特异性与高灵敏度,但该方法操作繁琐、RNA需分离纯化。此外,miRNAs小尺寸的特点也限制了传统RT-PCR的直接应用。并且miRNA家庭成员之间高的序列同源性也使定量分析成为挑战。因此,设计制备基于生物燃料电池的自供能生物传感器,实现miRNA简单、方便、高灵敏、高特异性检测非常必要。
本发明针对这一问题,构建了基于EBFC的miRNA生物传感器,核心技术便为EBFC的构建,其中以[Fe(CN)6]3-作为EBFC的电子受体,构建生物阴极;以碳纳米管/纳米金/葡萄糖氧化酶(CNTs/AuNPs/GOx)作为生物阳极催化葡萄糖氧化。首先将电子受体[Fe(CN)6]3-封装在MSN孔中,以目标miRNA的互补链(ssDNA)封孔。当无目标miRNA时,由于互补链将[Fe(CN)6]3-封装于MSN孔中,此时阴极电子受体[Fe(CN)6]3-含量相对较少,电池输出电压低;当目标miRNA存在时,由于DNA互补配对作用,目标miRNA与互补链形成刚性双螺旋结构,远离MSN表面,孔内的[Fe(CN)6]3-释放到体系中得到电子发生还原反应。目标miRNA的引入,达到释放[Fe(CN)6]3-的目的,阴极电子受体[Fe(CN)6]3-量增加,电压输出信号增大,用于定量检测目标miRNA。本发明设计的基于EBFC的自供能miRNA生物传感器,可实现目标物简单、快速、灵敏、高效检测。
技术实现要素:
本发明的目的是提供一种基于EBFC的自供能生物传感器的制备方法,实现miRNA的简单、快速、灵敏、高效检测,有助于癌症早期诊断。
本发明的技术方案如下:
一种互补链封孔的[Fe(CN)6]3-@MSN([Fe(CN)6]3-@MSN@ssDNA)的制备方法如图1,它由下列步骤组成:
步骤1. MSN的制备:浓度为1.5~3.0 mg mL-1水溶液中,加入500~1000 µL 2.0 M NaOH 溶液,在80 ℃下剧烈搅拌10~20 min。随后,将0.5~2 mL的TEOS加入到上述溶液中缓慢搅拌1~3 h直到有白色沉淀产生。将得到的产物过滤,二次水和甲醇多次洗涤,并在空气中晾干。接着取一定量沉淀物在盐酸和甲醇的混合物中回流10 h,以去除表面活性剂模板,制得MSN;
步骤2. 取一定量步骤1中制得的MSN,加入1~2倍于MSN质量的1% PDDA溶液,超声使其溶解,随后,将上述混合物在10000~15000 rpm下离心10~20 min并清洗多次,干燥后得到PDDA修饰的MSN;
步骤3. 取一定量步骤2中制得的PDDA修饰MSN与一定量浓度的[Fe(CN)6]3-混合,室温下缓慢搅拌一夜。随后,10 pM~100 nM ssDNA加入到上述溶液中,并在室温下缓慢搅拌孵育2~6 h。将最终得到的混合物在2000~5000 rpm下离心1~5 min,洗涤,去除未封装在孔内的[Fe(CN)6]3-,制得的[Fe(CN)6]3-@MSN@ssDNA。
一种CNT/AuNPs/GOx生物阳极的制备方法,由下列实验步骤组成:
步骤1. 取一定量CNT分散在1~2倍于CNT质量的1% PDDA的盐溶液中,超声0.5~2 h得到带正电的均匀悬浊液,离心去除剩余的PDDA(10000~15000 rpm,10~20 min),得到CNT/PDDA;
步骤2. 取一定量步骤1中制得的CNT/PDDA与1.0~5.0 mL浓度为10~100 nM的AuNPs相混合,在室温下缓慢搅拌一夜。离心(8000~10000 rpm,10~20 min)去除过量的AuNPs并将最终得到的产物重新分散;
步骤3. 将20~50 µL步骤2中制得的CNT/AuNPs滴在ITO电极表面,在37 ℃下干燥2~4 h,1~10 mg mL-1 EDC和NHS的溶液中浸泡0.5~1 h,随后用二次水冲掉电极表面多余的EDC和NHS;
步骤4. 将步骤3中制得的电极浸泡在500~1000 µL 10~50 mg mL-1的GOx溶液中12~24 h,二次水反复洗涤,置于4 ℃下备用。
一种基于EBFC的自供能miRNA生物传感器的搭建及测量,由下列步骤组成:
步骤1. 在不引入目标miRNA时,一定量[Fe(CN)6]3-@MSN@ssDNA加入到支持电解液中,测量EBFC的EOCV,记为E0OCV;
步骤2. 引入目标micRNA,不同浓度的目标miRNA在37 ℃下与一定量的MSN@ssDNA孵育1~6 h,随后将上述混合物加入到支持电解液,再次测量EBFC的EOCV;
上述搭建的无膜葡萄糖/氧气EBFC的支持电解液为含5 mM 葡萄糖pH 7.4的100 mM Tris−HCl缓冲体系,测量装置如图2。
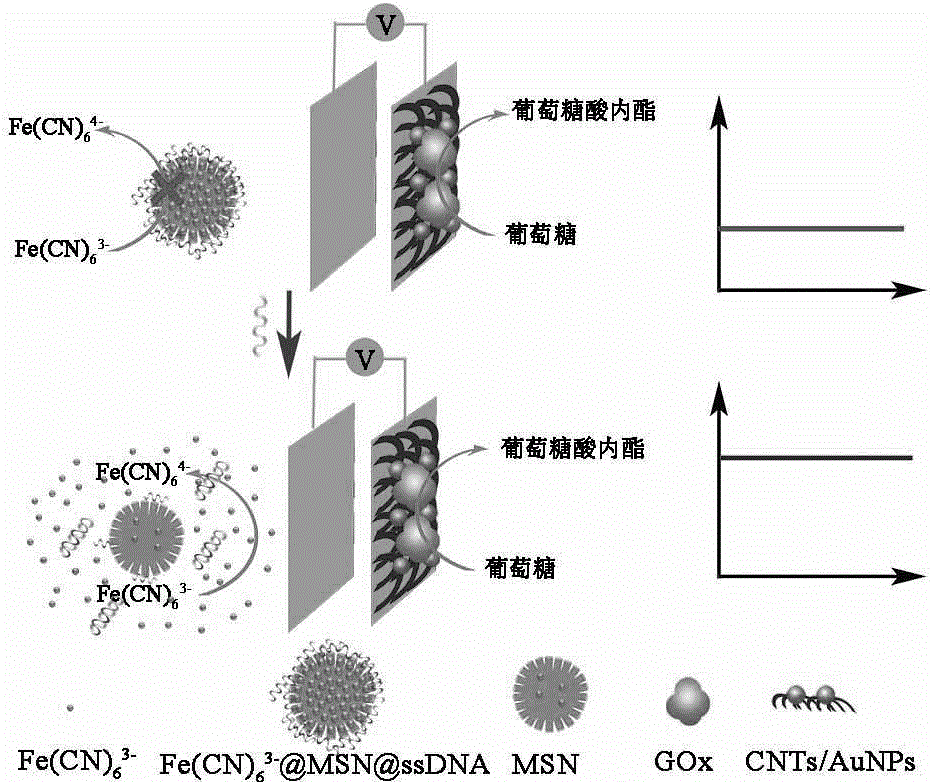
基于EBFC的自供能生物传感器超灵敏检测miRNA的原理如图3所示:
当无目标miRNA时,[Fe(CN)6]3-被互补链封在MSN的孔内,体系内仅含极少量[Fe(CN)6] 3-,生物阴极几乎无电子受体接受电子,此时,EBFC的开路电压较小;当引入目标miRNA时,目标miRNA与其互补链之间由于DNA的杂交配对作用形成的刚性双螺旋结构,使得互补链脱离MSN表面,使孔内的[Fe(CN)6]3-释放到体系中,随着引入miRNA浓度的增加,脱离MSN表面互补链的量增加,释放出来的电子受体[Fe(CN)6]3-的量增加,从而导致EBFC的开路电压增加,通过开路电压增加值与目标miRNA对应关系得出miRNA含量。
本发明与现有技术相比,具有以下特点:
本发明提供了一种基于EBFC的自供能miRNA传感器,实现miRNA简单、方便、快速、灵敏、高效检测,相对现有的miRNA检测方法,具有以下特点:
(1)本发明所述基于EBFC的自供能生物传感器,检测过程中无需外加电源,仅需两根电极,即生物燃料电池的阴阳两极,整个检测设备简单,便是实现现场实时监测;
(2)本发明所述的[Fe(CN)6]3-@MSN@ssDNA电子受体储存器,对[Fe(CN)6]3-储存量大,并且ssDNA封装效果良好,稳定性高,重复性好;
(3)本发明所述的基于EBFC的自供能生物传感器采用DNA杂交配对进行分子识别,不仅具有极高选择性,还具有成本低、操作简单等优点;
(4)本发明所述的基于EBFC的自供能生物传感器中,具有高电化学活性的电子受体[Fe(CN)6]3-在EBFC阴极得电子,同时生物阳极CNTs/AuNPs/GOx对生物燃料葡萄糖具有良好的电催化活性,实现对目标物miRNA的超灵敏检测,大大提高了检测灵敏度;
(5)通过构建无额外供电设备的自供能生物传感器,不需要昂贵的仪器设备,可实现miRNA检测的微型化、便携化和集成化。
附图说明
图1. [Fe(CN)6]3-@MSN@ssDNA组装过程示意图;
图2. 自供能miRNA生物传感器装置示意图;
图3. 基于EBFC的自供能生物传感器超灵敏检测miRNA的原理示意图。
具体实施方式
实施例1:自供能生物传感器用于miRNA-21的检测
(1)介孔硅(MSN)的制备:2.0 mg mL-1的CTAB水溶液中加入875 µL 2.0 M 的NaOH溶液,80 ℃下剧烈搅拌20 min。随后,将1.25 mL的TEOS加入到上述溶液中缓慢搅拌2 h。得到的产物过滤、洗涤、干燥。取160 mg沉淀物在1.5 mL盐酸(37%)和75 mL甲醇的混合物中回流10 h去除表面活性剂模板,制得的MSN过滤,洗涤并在60 ℃下干燥4 h;
(2)PDDA修饰MSN的制备:取16 mg步骤1中制得的MSN,加入8.0 mL浓度为1%的PDDA超声溶解,15000 rpm下离心10 min并清洗3遍,干燥后,得到PDDA修饰的MSN;
(3)Fe(CN)63-@MSN@ssDNA纳米储存器的制备:取10 mg步骤2中制得PDDA修饰的MSN分散于1.0 mL 1.0 M的Fe(CN)63-溶液中,室温下缓慢搅拌一夜。随后,10 µL 10 nM 的ssDNA加入到上述溶液中,并在室温下缓慢搅拌孵育4 h。将最终得到的混合物在3000 rpm下离心2 min,洗涤,去除未被封装在孔内的[Fe(CN)6]3-,得到的[Fe(CN)6]3-@MSN@ssDNA纳米储存器;
(4)CNT/AuNPs/GOx生物阳极的制备:8.0 mg的CNT分散在1% PDDA的盐溶液中,超声30 min得到带正电的均匀悬浊液, 15000 rpm下离心10 min去除剩余的PDDA聚合物,洗涤,得到CNT/PDDA。取一定量上述沉淀物与3.0 mL的AuNPs(10 nM)相混合,室温下缓慢搅拌过夜,8000 rpm下离心10 min去除多余的AuNPs,最终得到的产物重新分散得浓度为1 mg mL-1CNT/AuNPs。将50 µL CNT/AuNPs滴涂在ITO电极表面,在37 ℃下干燥2 h后将电极浸泡在1 mg mL-1 EDC和NHS的溶液中30 min,二次水冲掉电极表面多余的EDC和NHS。将活化电极浸泡在500 µL 10 mg mL-1的GOx溶液中4 °C 孵育12 h,二次水反复洗涤后浸泡在pH 7.4的PBS中,并置于4 ℃下备用;
(5)基于EBFC的miRNA自供能传感器的搭建及测量:当无目标miRNA时,50 µL [Fe(CN)6]3-@MSN@ssDNA加入到支持电解液中,测量EBFC的EOCV,记为E0OCV;引入目标miRNA后,5 µL不同浓度的目标miRNA与50 µL的[Fe(CN)6]3-@MSN@ssDNA 37 ℃下孵育2 h,随后将上述混合物加入到支持电解液,再次测量EBFC的EOCV。
上述搭建的无膜葡萄糖/氧气酶生物燃料电池的支持电解液为含5 mM 葡萄糖的100 mM Tris−HCl缓冲体系,pH= 7.4。
DNA序列miRNA-21:5’-UAG CU U AUC AGA CUG AUG UUG A-3’
ssDNA:5’-TCA ACA TCA GTC TGA TAA GCT A- 3’。
实施案例2:自供能生物传感器用于let-7b的检测
DNA序列let-7b:5’-UGA GGU AGU AGG UUG UGU GGU U-3’
ssDNA:5’-AAC CAC ACA ACC UAC UAC CUC A-3’
其余步骤同实施方案1。
- 还没有人留言评论。精彩留言会获得点赞!