用表面增强拉曼光谱法检测恩诺沙星的活性基底及其制备方法和应用与流程
本发明涉及用表面增强拉曼光谱法检测恩诺沙星的活性基底及其制备方法。
背景技术:
表面增强拉曼光谱法(SERS)是一种能够使分析物分子的拉曼信号得到有力增强的技术。SERS具有高灵敏性,高选择性,高准确性,快速、无损检测的优点。目前,SERS技术已经广泛应用于环境催化、化学和生物传感器、表面科学和材料科学等领域。
恩诺沙星作为喹诺酮类药物的成员,因为它具有能有效控制和杀死动物细菌的能力而受到人们的广泛关注。但这也导致了恩诺沙星这种抗生素的滥用现象变得越来越严重。为了保障人们的健康,许多国家都已经设置了一系列的标准来控制恩诺沙星残留量。欧盟也制定了恩诺沙星在食品中的最大残留量是100μgkg-1(在甲醇溶液中相当于2.20×10-7M)。现有技术中常采用银金属纳米粒子、有机物作为表面增强拉曼光谱法检测恩诺沙星的活性基底。如《拉曼光谱杂志》(Journal of Raman Spectroscopy)的第41卷第7期739–744页的文章《表面增强拉曼光谱法结合树枝状银纳米粒子检测抗生素》(Surface-enhanced Raman spectroscopy coupled with dendritic silver nanosubstrate for detection of restricted antibiotics)公开了一种树枝状银纳米粒子作为SERS基底对三种抗生素(恩诺沙星、环丙沙星、氯霉素)进行快速检测,检测限达到ppb级。该方法虽然很好地检测了药物分子,但是采用原料成本较高,操作较复杂。《食品分析方法》(Food Analytical Methods)在2014年第7卷第6期的1219-1228页公开的文章《使用氨基修饰的甲基丙烯酸缩水甘油酯-乙二醇二甲基丙烯酸酯多孔粉末材料利用表面增强拉曼光谱对鸡肉中的恩诺沙星进行超灵敏检测》(Ultrasensitive Detection of Enrofloxacin in Chicken Muscles by Surface-Enhanced Raman Spectroscopy Using Amino-Modified Glycidyl Methacrylate-Ethylene Dimethacrylate(GMA-EDMA)Powdered Porous Material),该文中以氨基修饰的GMA-EDMA作为SERS基底,对鸡肉中恩诺沙星残留量进行微量快速检测,最低的检测浓度可以达到0.01mgkg-1。该方法采用原料成本较高,并且有毒有害易燃,有着较大的危险性。半导体TiO2作为一种新型的SERS基底具有良好的生物相容性和耐酸耐碱性好等特点,但是它的SERS活性远远低于金属材料,特别是贵金属材料,这也极大的限制了TiO2的发展。
技术实现要素:
本发明是要解决现有的表面增强拉曼光谱法检测恩诺沙星的贵金属活性基底成本高及操作复杂、有机物基底危险性大的技术问题,而提供用表面增强拉曼光谱法检测恩诺沙星的一种新型TiO2活性基底及其制备方法和应用。
本发明的用表面增强拉曼光谱法检测恩诺沙星的活性基底为掺杂镍和锌的二氧化钛,其中镍与钛的摩尔比为(0.5~1.5):100,锌与钛的摩尔比为(0.5~1.5):100。
本发明的用表面增强拉曼光谱法检测恩诺沙星的活性基底的制备方法,按以下步骤进行:
一、将钛酸四丁酯加入到无水乙醇中搅拌均匀,得到溶液A;
二、将硝酸锌、硝酸镍、无水乙醇、水和浓硝酸混合,搅拌均匀,得到溶液B;
三、在搅拌条件下,将溶液A滴加到溶液B中水解,滴加结束后,继续搅拌2~5h,得到透明溶胶;
四、将步骤三制得的溶胶转移至水热釜中,放入烘箱中,在温度为160~180℃的条件下水热反应6~8h,自然冷却至室温,倒掉废液后,将产物干燥,得到前驱物;
五、将前驱物放入研钵中研磨成粉末,然后在450~470℃的条件下焙烧2~3h,得到用表面增强拉曼光谱法检测恩诺沙星的活性基底。
用表面增强拉曼光谱法检测恩诺沙星的活性基底的应用是将该活性基底用于检测恩诺沙星,具体的应用方法如下:
将本发明的活性基底分散到含恩诺沙星待测样品的甲醇溶液中,再调节溶液的pH为6~7.2,搅拌5~11h;然后离心分离出固相物,再用甲醇洗涤,干燥后,得到恩诺沙星分子表面修饰的活性基底,再进行表面增强拉曼光谱法测试。
利用本发明的活性基底,采用标准曲线法,通过表面增强拉曼光谱法可对恩诺沙星进行定量测定。
本发明采用双金属镍和锌掺杂二氧化钛,调控TiO2的表面态(缺陷)能级和金属掺杂能级,制备出一种能级可调控的高性能TiO2SERS活性基底,该活性基底的活性比TiO2基底大大提高,可对恩诺沙星(ENR)药物分子进行SERS检测,实现了采用半导体TiO2作为SERS基底对恩诺沙星药物检测的实际应用。
本发明采用的SERS基底制备方法简单,原料成本低,无毒无害,环境友好,而且具有良好的SERS增强能力,并且能有效的对恩诺沙星药物分子进行检测,检测限低至1×10-9M,能够达到欧盟标准,推进了SERS技术的应用发展。
附图说明
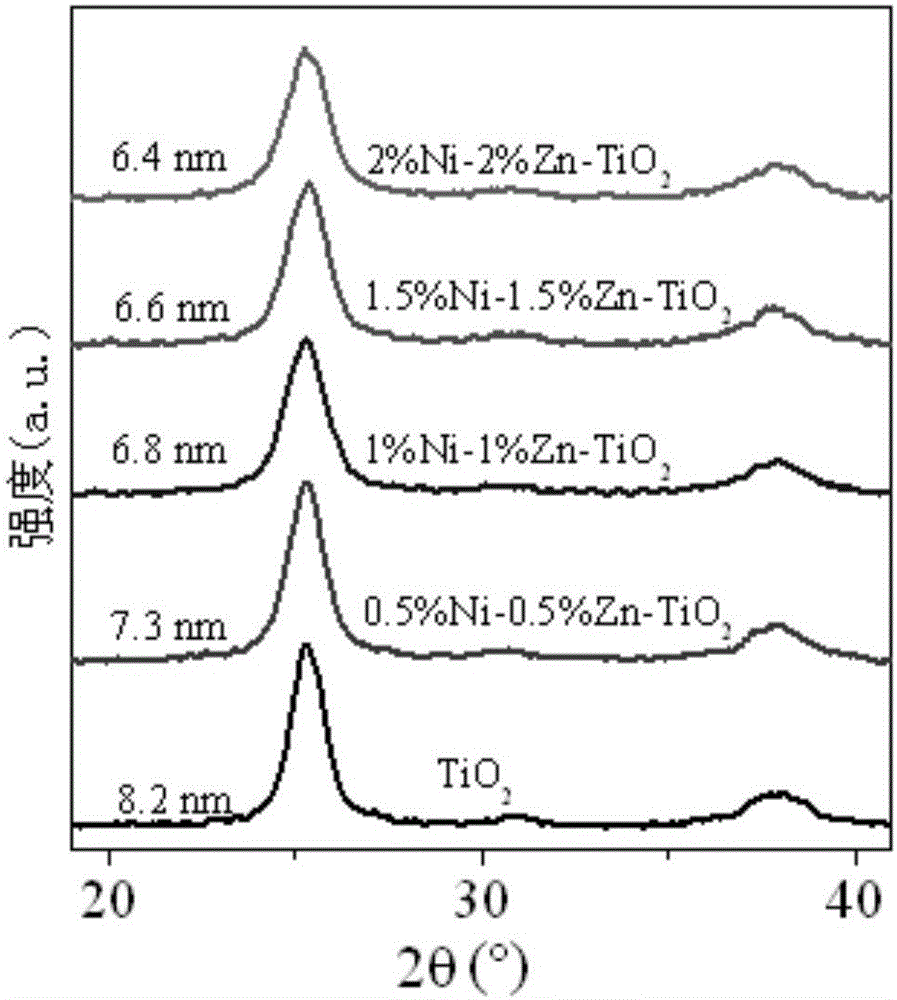
图1是试验1中纯的锐钛矿相TiO2纳米粒子和双金属掺杂的TiO2纳米粒子的XRD谱图;
图2是试验1中吸附在未掺杂和不同金属掺杂TiO2(Zn-TiO2、Ni-TiO2和Ni-Zn-TiO2)纳米粒子上ENR药物分子的SERS光谱图;
图3是不同搅拌时间条件下吸附在1%Ni-1%Zn-TiO2纳米粒子上ENR药物分子的SERS光谱图;
图4是不同的pH值条件下吸附在1%Ni-1%Zn-TiO2纳米粒子上ENR药物分子的SERS光谱图
图5是不同的ENR浓度条件下吸附在1%Ni-1%Zn-TiO2纳米粒子上ENR药物分子的SERS光谱图
图6是ENR浓度及SERS信号强度之间的定量关系曲线图。
具体实施方式
具体实施方式一:本实施方式的用表面增强拉曼光谱法检测恩诺沙星的活性基底为掺杂镍和锌的二氧化钛,其中镍与钛的摩尔比为(0.5~1.5):100,锌与钛的摩尔比为(0.5~1.5):100。
具体实施方式二:具体实施方式一所述的用表面增强拉曼光谱法检测恩诺沙星的活性基底的制备方法,按以下步骤进行:
一、将钛酸四丁酯加入到无水乙醇中搅拌均匀,得到溶液A;
二、将硝酸锌、硝酸镍、无水乙醇、水和浓硝酸混合,搅拌均匀,得到溶液B;
三、在搅拌条件下,将溶液A滴加到溶液B中水解,滴加结束后,继续搅拌2~5h,得到透明溶胶;
四、将步骤三制得的溶胶转移至水热釜中,放入烘箱中,在温度为160~180℃的条件下水热反应6~8h,自然冷却至室温,倒掉废液后,将产物干燥,得到前驱物;
五、将前驱物放入研钵中研磨成粉末,然后在450~470℃的条件下焙烧2~3h,得到用表面增强拉曼光谱法检测恩诺沙星的活性基底;
其中步骤二中硝酸锌与步骤一中钛酸四丁酯的摩尔比为(0.5~1.5):100;步骤二中硝酸镍与步骤一中钛酸四丁酯的摩尔比为(0.5~1.5):100。
具体实施方式三:本实施方式与具体实施方式二不同的是步骤一中钛酸四丁酯与无水乙醇的体积比为1:1;步骤二中无水乙醇、水和浓硝酸与步骤一中钛酸四丁酯的体积比为4:1:0.2:1;其中浓硝酸的质量百分浓度为63%~66%。其它与具体实施方式二相同。
具体实施方式四:本实施方式与具体实施方式二或三不同的是步骤四中,水热反应的温度为160℃,反应时间为6h。其它与具体实施方式二或三相同。
具体实施方式五:本实施方式与具体实施方式二至四之一不同的是步骤五中,焙烧温度为450℃,焙烧时间为2h。其它与具体实施方式二至四之一相同。
具体实施方式六:具体实施方式一所述的用表面增强拉曼光谱法检测恩诺沙星的活性基底的应用是将该活性基底用于检测恩诺沙星,具体的应用方法如下:
将本发明的活性基底分散到含恩诺沙星待测样品的甲醇溶液中,再调节溶液的pH为6~7.2,搅拌5~11h;然后离心分离出固相物,再用甲醇洗涤,干燥后,得到恩诺沙星分子表面修饰的活性基底,再进行表面增强拉曼光谱法测试。
具体实施方式七:本实施方式与具体实施方式六不同的是pH为7.04。其它与具体实施方式六相同。
具体实施方式八:本实施方式与具体实施方式六或七不同的是搅拌时间为7小时。其它与具体实施方式六或七相同。
用以下试验验证本发明的有益效果:
试验1:本试验的用表面增强拉曼光谱法检测恩诺沙星的活性基底的制备方法,按以下步骤进行:
一、将15mL钛酸四丁酯加入到15mL无水乙醇中搅拌5min至均匀,得到溶液A;
二、将a克硝酸锌、b克硝酸镍、60mL无水乙醇、15mL水和3mL质量百分浓度为63%的浓硝酸混合,搅拌均匀,得到溶液B;
三、在搅拌条件下,将溶液A以滴加速度2~3秒1滴的速度滴加到溶液B中水解,滴加结束后,继续搅拌2h,得到淡黄色透明溶胶;
四、将步骤三制得的溶胶转移至水热釜中,放入烘箱中,在温度为160℃的条件下水热反应6h,自然冷却至室温,倒掉废液后,将产物均匀分散到表面皿中,再把表面皿放入烘箱中在80℃下干燥8h,得到前驱物;
五、将前驱物放入研钵中研磨成粉末,然后在450℃的条件下焙烧2h,得到用表面增强拉曼光谱法检测恩诺沙星的活性基底。
其中步骤二中的a、b的取值及对应的活性基底如下表1
本试验第一组得到的是纯的锐钛矿相TiO2纳米粒子,第二组得到的是只掺杂锌的TiO2纳米粒子,第三组得到的是只掺杂镍的TiO2纳米粒子,第四至第七组得到的是双金属掺杂的TiO2纳米粒子。
本试验第一组得到的纯锐钛矿相TiO2纳米粒子和第四至第七组得到的双金属掺杂的TiO2纳米粒子的XRD谱图如图1所示,从图1可以看出,双金属掺杂的TiO2纳米粒子的衍射峰向高角度偏移,这主要归因于掺杂的镍离子不同程度地进入到了TiO2的晶格取代了Ti离子,导致了TiO2的晶格畸变,相应的衍射峰发生了位移。
将20mg第一至第七组的活性基底分别分散到10mL浓度为1×10-3M的恩诺沙星的甲醇溶液(称取35.9mg的恩诺沙星标准品用甲醇定容于100mL容量瓶制得的)中,搅拌均匀,此时该溶液的pH值为7.04,室温下磁力搅拌7h。然后,将混合物放入离心机以9500转/秒速度离心10分钟,之后用甲醇洗涤后再离心。固相物自然干燥后,即得到恩诺沙星分子表面修饰的TiO2纳米粒子。
采用英国雷尼绍公司Renishaw 1000model型共聚焦显微拉曼光谱仪测量拉曼光谱,激发光源的波长为532nm。得到的吸附在未掺杂和不同金属掺杂TiO2(Zn-TiO2、Ni-TiO2和Ni-Zn-TiO2)纳米粒子上ENR药物分子的SERS光谱图如图2所示。从图2可以看出,ENR吸附在不同基底上的增强程度不同,与第一组的纯的锐钛矿相TiO2纳米粒子基底相比,吸附在第二组的单纯掺杂锌的TiO2纳米粒子、第三组的单纯掺杂镍的TiO2纳米粒子基底上的药物分子都表现出较强的SERS增强,活性都比纯TiO2有所提高,但提高的辐度不大,仅为100%~130%。ENR药物分子吸附在第四至第六组制备的双金属掺杂的TiO2纳米粒子上表现出很大的SERS增强,可知,在掺杂量较小时(镍、锌的掺杂量分别小于1.5%时),双金属掺杂大大提高了基底的活性;当镍、锌的掺杂量分别达到2%时,活性反而降低。这表明,适量的双金属(Zn2+和Ni2+)掺杂可以更好地提高TiO2纳米粒子的SERS增强效果。
这是由于适量的Zn2+掺杂可以增加二氧化钛纳米粒子的表面缺陷(表面态能级),从而提高药物分子的SERS信号。通过金属掺杂引起的表面缺陷的增加促进了半导体到药物分子的电荷转移过程。而适量Ni2+掺杂可以进入TiO2晶格取代Ti4+离子,它可以在TiO2的带隙间嵌入一个丰富的金属掺杂能级,进而促进了半导体到药物分子的电荷转移过程和SERS增强效应。因此,丰富的表面态(缺陷)和金属掺杂能级都有利于半导体到药物分子的电荷转移过程。采用Zn和Ni双金属掺杂TiO2,控制金属的掺杂量从而调控表面态(缺陷)能级和金属掺杂能级,使二者同时贡献于TiO2到药物分子的电荷转移过程,得到了更强的药物分子的SERS信号。
以本试验第五组制备的1%Ni-1%Zn-TiO2纳米粒子做为活性基底,改变吸附时间,考察不同吸附时间对吸附在1%Ni-1%Zn-TiO2纳米粒子上恩诺沙星SERS增强的影响。具体步骤是:将20mg 1%Ni-1%Zn-TiO2纳米粒子活性基底分散到10mL浓度为1×10-3M的恩诺沙星的甲醇溶液(称取35.9mg的恩诺沙星标准品用甲醇定容于100mL容量瓶制得的)中,搅拌均匀,此时该溶液的pH值为7.04。上述样品配制六份,室温下分别磁力搅拌1、3、5、7、9和11h。然后,将混合物放入离心机以9500转/秒速度离心10分钟,之后用甲醇洗涤后再离心。固相物自然干燥后,即得到恩诺沙星分子表面修饰的TiO2纳米粒子。采用英国雷尼绍公司Renishaw 1000model型共聚焦显微拉曼光谱仪测量拉曼光谱,激发光源的波长为532nm。得到的吸附在1%Ni-1%Zn-TiO2纳米粒子上ENR药物分子的SERS光谱图如图3所示,从图3可以清楚地看到,吸附在1%Ni-1%Zn-TiO2纳米粒子基底上ENR药物分子的SERS信号强度随着吸附时间的增加明显提高。这是因为随着吸附时间的增加,吸附在纳米TiO2上ENR药物分子的数量也随之增加。当吸附时间为7、9和11h时,ENR药物分子的SERS信号强度几乎彼此相同。这表明,ENR分子吸附时间为7小时时在TiO2表面的吸附量达到饱和状态。
以本试验第五组制备的1%Ni-1%Zn-TiO2纳米粒子做为活性基底,改变pH值,考察不同pH值对吸附在1%Ni-1%Zn-TiO2纳米粒子上恩诺沙星SERS增强的影响。具体步骤是:将20mg 1%Ni-1%Zn-TiO2纳米粒子活性基底分散到10mL浓度为1×10-3M的恩诺沙星的甲醇溶液(称取35.9mg的恩诺沙星标准品用甲醇定容于100mL容量瓶制得的)中,搅拌均匀。上述样品配制六份,用盐酸或氢氧化钠调节溶液的pH值分别为2.97、4.92、7.04、9.02和10.96,磁力搅拌7h。然后,将混合物放入离心机以9500转/秒速度离心10分钟,之后用甲醇洗涤后再离心。固相物自然干燥后,即得到恩诺沙星分子表面修饰的TiO2纳米粒子。采用英国雷尼绍公司Renishaw 1000model型共聚焦显微拉曼光谱仪测量拉曼光谱,激发光源的波长为532nm。得到的吸附在1%Ni-1%Zn-TiO2纳米粒子上ENR药物分子的SERS光谱图如图4所示,从图4可以清楚地看到,当pH值为7.04时,ENR分子表现出最大的SERS增强。这是由于ENR是两性化合物,它的pKa1和pKa2分别为5.88和7.74。因此,ENR离子状态受溶液的pH值和ENR的解离常数(pKa)所控制。当溶液pH值小于6时,ENR的存在形式主要是阳离子状态(ENR+)。当pH值为6~8时,ENR的存在形式主要是两性离子状态(ENR0),这也导致了-COO-基数目的增加。当溶液pH值大于8时,ENR的存在形式主要是阴离子状态(ENR-),ENR的SERS信号增强应该随着-COO-基团增加而增加。但TiO2的等电点(PZC)范围是5.9~7.2,因此当溶液pH值大于7.2时,TiO2表面带负电荷将对吸附产生负面影响,不利于ENR在TiO2表面的吸附。因此pH值为7.04时,ENR分子的SERS信号最强。
以本试验制备的1%Ni-1%Zn-TiO2纳米粒子做为活性基底,改变恩诺沙星浓度,考察不同恩诺沙星浓度对吸附在1%Ni-1%Zn-TiO2纳米粒子上恩诺沙星SERS增强的影响。具体步骤是:将20mg 1%Ni-1%Zn-TiO2纳米粒子活性基底分别分散到10mL浓度为1×10-3、1×10-4、1×10-5、1×10-6、1×10-7、1×10-8、1×10-9、1×10-10M的恩诺沙星的甲醇溶液中,搅拌均匀,调节溶液的pH值分别为7.04,磁力搅拌7h。然后,将混合物放入离心机以9500转/秒速度离心10分钟,之后用甲醇洗涤后再离心。固相物自然干燥后,即得到恩诺沙星分子表面修饰的TiO2纳米粒子。采用英国雷尼绍公司Renishaw 1000model型共聚焦显微拉曼光谱仪测量拉曼光谱,激发光源的波长为532nm。得到的吸附在1%Ni-1%Zn-TiO2纳米粒子上ENR药物分子的SERS光谱图如图5所示,从图5可以看出,拉曼信号强度会随着ENR浓度减小而变弱。当ENR浓度低至10-10M时,难以观察到明显的SERS信号。因此,10-9M是本方法检测ENR的最低浓度。而采用相同的方法测试的单金属掺杂的TiO2,如1%Zn-TiO2和1%Ni-TiO2检测的ENR的最低浓度都为10-7M,对比可知这种双掺杂的能级可调控的TiO2检测恩诺沙星的最低浓度低于单金属掺杂TiO2,能更好地胜任ENR药物检测的工作。将ENR浓度及相对应的SERS信号强度绘于图中,可以看出ENR浓度和SERS信号强度之间的定量关系如图6所示。从图6可以看出,曲线在1×10-4~1×10-9M的浓度范围内有良好的线性关系,线性方程可以表示为:y=21473.66+2306.42C,相应的相关系数R2为0.991。通过该方法,检测限(LOD)可达3×10-10mol/L(对应于3倍信噪比)。这表明该方法可以有效的检测ENR药物分子,并且有较低的检测限可以达到欧盟标准。
- 还没有人留言评论。精彩留言会获得点赞!