孕酮测定试剂盒及制作方法与流程
本发明涉及医学免疫学中荧光免疫层析技术领域,包括蛋白交联技术、膜层析技术、标记免疫分析技术等。具体地说是一种能够快速准确的对血清、血浆和全血等样品中孕酮进行定量分析的孕酮测定试剂盒及制作方法。
背景技术:
:
孕酮(Progesterone,PROG)是一种含21碳的固醇类激素,为类固醇激素合成过程中的中间代谢产物。由胆固醇经孕烯醇酮通过异构酶转化而成。在非妊娠妇女,卵巢中的卵泡膜细胞产生孕酮,妊娠期间,孕酮则主要由胎盘合体滋养细胞层分泌,故血中孕酮水平主要与胎盘重量及血液灌注量相关。孕早期上升较慢,13周后增快,足月时达高峰。在血中,孕酮主要与皮质类固醇结合蛋白(CBG)及白蛋白相结合,血液中绝大部分孕酮为结合型,极少数为游离型。孕酮主要在肝脏降解,被还原成孕二醇,孕二醇再与硫酸或葡萄糖醛酸结合后经肾排出。孕酮对调节月经周期和维持妊娠具有重要的生理作用,可促进子宫内膜分泌期的转化,为受精卵着床做准备;松弛子宫肌,降低对前列腺素和催产素的反应性;抑制输卵管节律性收缩。孕酮还有促乳腺腺泡增生,增加能量代谢,升高基础体温,促进水钠排除的作用。孕酮对下丘脑-垂体系统具有正、负反馈作用,可调控垂体促性腺激素的合成和分泌。排卵前小剂量孕酮协同E3诱发排卵前LH高峰出现,排卵后大剂量孕酮对下丘脑-垂体系统则呈现负反馈作用。
血液中的女性孕酮几乎都是由黄体或胎盘所产生;男性孕酮水平很低,主要由肾上腺皮质产生。孕酮是一个重要的激素,它不仅在月经周期的调节中发挥重要作用,在维持妊娠中也是必不可少的。孕酮在月经周期后期使子宫黏膜内腺体生长,子宫充血,内膜增厚,为受精卵植入作好准备;受精卵植入后则使之产生胎盘,并减少妊娠子宫的兴奋性,抑制其活动,使胎儿安全生长。血清中的孕酮在排卵后浓度迅速升高,因可能发生的流产和异常妊娠的手段。孕酮测定用于确定排卵、孕激素治疗监测和早期妊娠状况的评价,在判断黄体功能状态和方面具有特别重要的意义,是研究卵巢生理和病理生理不可缺少的手段。
免疫分析技术是利用微量抗原与相应的高特异性抗体之间的免疫反应,来检测如激素、药物、蛋白质、多肽、酶、肿瘤相关抗原、微生素、病毒、细菌及金属元素等生物体内活性物质。免疫分析技术包括标记免疫分析、非标记免疫分析和仪器免疫分析。本试剂盒利用的含有稀土元素的羧基乳胶微球标记免疫分析技术是属于标记免疫分析之一种。
荧光免疫分析(FIA)和放射免疫分析(RIA)自问世以来,经历了几十年的发展,但是人们越来越感觉到FIA因自然本地太高,干扰检测结果;RIA采用同位素标记,对人体有极大危害并给实验带来不便。酶免疫分析(EIA)也因酶本身不稳定,受其他影响因素较大,推广应用受到限制。80年代初,人们开始研究用稀土元素代替荧光物质和同位素标记蛋白质或抗体,将时间分辨技术引入到生物检测领域,建立了新型的超微量时间分辨荧光免疫分析技术(Time resolved Fluoroimmunoassay,简称TrFIA)。该技术采用多学科先进技术,集结了其他免疫分析的特点,在免疫学、分子生物学、细胞学和医学等领域,取得长足的发展和广泛应用。
TrFIA利用了具有独特荧光特性的3价稀土离子及螯合物为示踪物代替荧光物质、酶、同位素、化学发光物质,标记抗体、抗原、激素、多肽、蛋白质、核酸探针及生物细胞,待反应体系(如抗原抗体反应、核酸探针杂交、生物素亲和素反应以及靶细胞对效应细胞的杀伤效应等)发生后,用TrFIA检测仪测定反应产物中的荧光强度。根据产物荧光强度和相对荧光强度的比值,判断反应体系中分析物的浓度,从而达到定量分析。在通常的荧光测定中,由于测试样品中含有多种荧光成分,背景荧光(来自样品中的胶体颗粒和溶剂分子引起的散射光以及血清中蛋白质和其他化合物发出的非特异性荧光)强度大、干扰强,成为荧光分析法大范围推广的瓶颈。TrFIA之所以能够成为继EIA、RIA之后一种新的灵敏的检测方法,主要取决于镧系元素独特的荧光特点、检测中采用的波长分辨和时间延迟技术以及解离-增强技术。
镧系元素(lanthanide,Ln)属于稀土元素,共有17中,常用于TrFIA主要有铕(Eu)、钐(Sm)、铽(Tb)、镝(Dy)。镧系元素具有独特的荧光发光特点,与普通荧光相比,镧系离子螯合物荧光衰变时间长,为传统荧光的103-106倍。如镧系离子螯合物的荧光衰变时间在60-900μs,常用的Eu3+荧光衰变时间为714μs,普通荧光免疫分析中荧光团的荧光衰变时间只有1-100μs,样品中一些蛋白质的荧光衰变时间仅为1-10μs,因此利用时间分辨技术,延迟一定时间后测量,便可获得Eu3+特异性荧光信号。同时由于衰变时间长,Eu3+标记物在测量时间里可以反复被激发,每次激发后由激发态很快跃迁到基态,就有荧光发出,然后又可被重新激发,如此每秒可有1000次激发,使得TrFIA荧光标记物的相对比活性很高。镧系元素荧光光谱的最大特征是激发光与发射光之间的Stokes位移较大,Eu3+激发波长为337nm,发射波长为615nm,Stokes位移可达278nm;同时Eu3+被激发的荧光光带极窄,荧光的发射峰非常尖锐,可使仪器调整在极窄的波长范围内测定,这样就几乎完全消除了背景荧光的干扰,继而通过时间延迟和波长分辨,将强特异性荧光和背景荧光辨开(故称为时间分辨),使干扰达到几乎为零。
鉴于以上标记方法及检测技术的应用,本试剂盒具有良好的检测特异性、较高的灵敏度、操作的简便性以及稳定的荧光标记物保证了检测的准确性。
技术实现要素:
:
本发明针对现有技术中存在的缺点和不足,提出了一种利用荧光免疫层析的灵敏性,结合荧光免疫层析分析仪实现的灵敏度高、快捷简便,可以准确定量的孕酮测定试剂盒及制作方法。
本发明可以通过以下措施达到:
一种孕酮测定试剂盒,设有试纸卡,其特征在于所述试纸卡由下至上依次设有:PVC板、样品垫、结合垫、硝酸纤维素膜和吸水垫,其中结合垫上吸附有稀土Eu3+荧光微球标记的抗孕酮单克隆抗体-微球偶联复合物,所述稀土荧光微球的直径为100-250nm,稀土荧光微球含稀土镧系元素中的一种或几种,在基态下稳定,在300-400nm的激发光源作用下发射出波长范围为550-650nm的荧光;所述单克隆抗体为纯化后混合的单克隆抗体,来源于针对2-6个不同的孕酮抗原表位的单克隆抗体细胞株。
本发明所述结合垫的稀土荧光微球的直径优选是120-150nm;所述稀土荧光微球优选含有一种或几种稀土镧系元素;结合垫上稀土荧光微球标记的抗体优选来源于针对2个不同抗原表位的单克隆细胞细胞株。
本发明所述结合垫采用如下步骤制得:将玻璃纤维膜浸泡于150mM Tris-HCL处理液中(含1.0%Triton X-100,2.5%BSA,pH7.4),4℃浸泡2小时,然后取出37℃烘箱烘干4小时,备用,将玻璃纤维膜放在Bio-DotXYZ3050三维喷点平台上,用Bio-Jet Quanti300非接触式微定量喷头将稀土荧光微球标记的抗孕酮单克隆抗体偶联复合物喷到玻璃纤维膜,37℃烘干1小时后制得。
本发明中结合垫上的所述稀土荧光微球标记的抗孕酮单克隆抗体采用如下步骤制得:
步骤1:单克隆抗体细胞株的获得:用孕酮纯品免疫小鼠,采用标准的单克隆抗体制备方法制备特异性高亲和力的单克隆抗体细胞株,对所获得的单抗细胞株进行配对筛选,根据配对结果和亲和力数据优选出用于试剂盒的单抗细胞株;
步骤2:单克隆抗体的制备:采用标准的腹水生产工艺制备并纯化抗孕酮单克隆抗体,分装后保存于-20℃备用;
步骤3:稀土荧光微球的醛基化:取5mg稀土荧光微球,用20mM,pH 9.5的碳酸盐缓冲液,采用离心法洗涤3遍,离心速度为12000rpm,时间为5分钟,最后重悬于100μl的上述碳酸盐缓冲液中,加入500μl醛基化的葡聚糖,混匀,室温下暗反应4小时,采用同样的离心法洗涤和重悬到100μl的上述碳酸盐缓冲液中,置于4℃备用;
步骤4:稀土荧光微球标记的抗孕酮单克隆抗体的制备:选取来自2个不同抗原表位的单克隆细胞细胞株的单克隆抗体,按照质量比1:1将2mg孕酮单克隆抗体用上述碳酸盐缓冲液于4℃透析过夜,然后与上述醛基化的稀土荧光微球混合,4℃反应过夜;然后,加入硼氢化钠至终浓度5mM,4℃反应4小时;再加入等体积的封闭液(50mM Tris-HCL,pH7.4,含2%BSA,5%蔗糖),4℃封闭过夜;然后用50mM Tris-HCL,pH7.4的缓冲液采用离心法洗涤3遍,重悬于100μl的50mM Tris-HCL缓冲液中(含1.2%NaCL,0.5%BSA,0.1%Tween 20),4℃避光保存备用。
本发明所述包被有检测线和质控线的硝酸纤维素膜通过以下步骤制得:
步骤1:采用与结合垫上所用抗孕酮单克隆抗体细胞株不同的细胞株,采用标准的腹水生产工艺制备并纯化抗孕酮单克隆抗体,保存于-20℃备用;
步骤2:分别用包被稀释液将上述鼠源抗孕酮单克隆抗体和羊抗小鼠IgG抗体调整浓度到1-3mg/ml,膜液量为1-3μl/cm,将它们分别作为检测线和质控线平行喷洒于硝酸纤维素膜上进行包被,检测线和质控线间隔为3-7mm,然后置于烘箱中,37℃烘干2小时。
本发明所述样品垫通过以下步骤制得:将玻璃纤维膜浸泡于含有1.0%Triton X-100,2.5%BSA,0.15M Tris缓冲液,pH7.5的处理液中,于4℃浸泡4个小时,然后置于烘箱中,37℃烘干2小时。
本发明还提供了一种如上所述试剂盒实现的孕酮制作方法,其特征在于包括以下步骤:
步骤1:将检测试剂及样本平衡至室温,取出试纸卡,平放;
步骤2:读卡:将IC卡放置在干式荧光免疫分析仪标注位置,读取相关信息,所述荧光免疫层析分析仪是一种光学检测系统,对孕酮的测定范围为0.30-50ng/mL;
步骤3:加样:血清/血浆:取100μL血清/血浆样本垂直滴加至测试卡加样处;全血:取150μL全血样本垂直滴加至测试卡加样处;取样时注意不要吸入气泡;
步骤4:检测,可采用自动测试或即时测试两种模式进行检测,自动测试:将测试卡插入干式荧光免疫分析仪的承载器上,按测试键,仪器将自动对测试卡进行扫描分析检测,即时测试:测试卡室温放置10min后,插入干式荧光免疫分析仪的承载器上,点击即时测试。
本发明提供一种利用稀土羧基乳胶微球标记的荧光免疫层析技术制备的孕酮测定试剂盒,同时适合血清、血浆和全血样本,并适合临床上单人份检测,相对于孕酮定性胶体金试剂,能定量检测样本中的孕酮含量,具有更明确的临床指导意义,具有操作简便、反应快速、灵敏度高、特异性强、适合现场检测和经济实用等优点。
附图说明:
附图1是本发明中试纸卡的结构示意图。
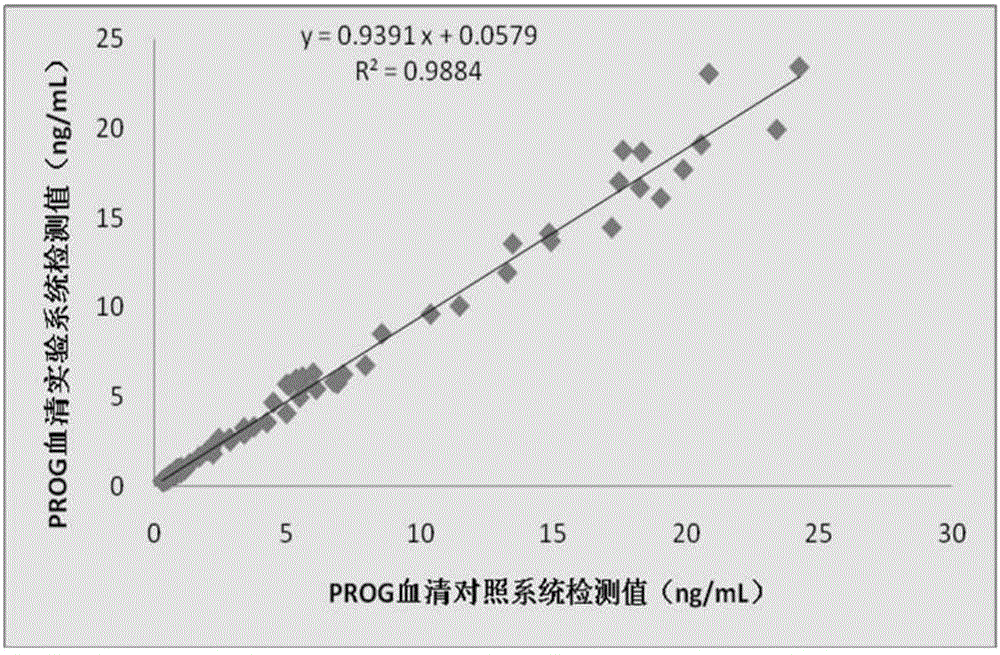
附图2是本发明中实施例2的准确度分析结果示意图。
附图3是本发明中实施例2的准确度分析结果示意图。
附图4是本发明中实施例2的准确度分析结果示意图。
附图标记:PVC板1、样品垫2、结合垫3、硝酸纤维素膜4、吸水垫5。
具体实施方式:
下面结合附图和实施例对本发明作进一步的说明:
如附图1所示,本发明首先提出了一种孕酮测定试剂盒,盒内设有试纸卡,所述试纸卡由下至上依次设有:PVC板1、样品垫2、结合垫3、硝酸纤维素膜4和吸水垫5,其中结合垫上吸附有稀土Eu3+荧光微球标记的抗孕酮单克隆抗体-微球偶联复合物,所述稀土荧光微球的直径为150nm,稀土荧光微球含稀土镧系元素Eu3+,在基态下稳定,在337nm的激发光源作用下发射出波长615nm的荧光;所述单克隆抗体为纯化后混合的单克隆抗体,来源于针对2-6个不同的孕酮抗原表位的单克隆抗体细胞株。
所述结合垫3的稀土荧光微球的直径优选是150nm;所述稀土荧光微球优选含有稀土镧系元素铕(Eu3+);结合垫上稀土荧光微球标记的抗体优选来源于针对2个不同抗原表位的单克隆细胞细胞株。
实施例1:
孕酮测定试剂盒中试纸卡的各组成部分可以通过以下措施制得:
1、样品垫2的制备:
将玻璃纤维膜浸泡于含有1.0%Triton X-100,2.5%BSA,0.15M Tris缓冲液,pH7.5的处理液中,于4℃浸泡4个小时,然后置于烘箱中,37℃烘干2小时。2、吸附荧光微球标记抗体的结合垫3的制备:
将玻璃纤维膜浸泡于150mM Tris-HCL处理液中(含1.0%Triton X-100,2.5%BSA,pH7.4),4℃浸泡2小时,然后取出37℃烘箱烘干4小时,备用,将玻璃纤维膜放在Bio-DotXYZ3050三维喷点平台上,用Bio-Jet Quanti300非接触式微定量喷头将稀土Eu3+荧光微球标记的抗孕酮单克隆抗体偶联复合物喷到玻璃纤维膜,37℃烘干1小时后制得。
稀土荧光纳米微球的醛基化:取5mg稀土荧光纳米微球,用20mM,pH9.5的碳酸盐缓冲液,采用离心法洗涤3遍,离心速度为12000rpm,时间为5分钟,最后重悬于100μl的上述碳酸盐缓冲液中,加入500μl醛基化的葡聚糖,混匀,室温下暗反应4小时,采用同样的离心法洗涤和重悬到100μl的上述碳酸盐缓冲液中,置于4℃备用;
稀土Eu3+荧光微球标记的抗孕酮单克隆抗体的制备:选取来自2个不同抗原表位的单克隆细胞细胞株的单克隆抗体,按照质量比1:1将2mg抗孕酮单克隆抗体用上述碳酸盐缓冲液于4℃透析过夜,然后与上述醛基化的稀土荧光微球混合,4℃反应过夜;然后,加入硼氢化钠至终浓度5mM,4℃反应4小时;再加入等体积的封闭液(50mM Tris-HCL,pH7.4,含2%BSA,5%蔗糖),4℃封闭过夜;然后用50mM Tris-HCL,pH7.4的缓冲液采用离心法洗涤3遍,重悬于100μl的50mM Tris-HCL缓冲液中(含1.2%NaCL,0.5%BSA,0.1%Tween 20),4℃避光保存备用。
3、包被有检测线和质控线的硝酸纤维素膜4的制备:
采用与结合垫上所用抗孕酮单克隆抗体细胞株不同的细胞株,采用标准的腹水生产工艺制备并纯化抗孕酮单克隆抗体,保存于-20℃备用;
分别用包被稀释液将上述鼠源抗孕酮单克隆抗体和羊抗小鼠IgG抗体调整浓度到1mg/ml,膜液量为1μl/cm,将它们分别作为检测线和质控线平行喷洒于硝酸纤维素膜上进行包被,检测线和质控线间隔为4mm,然后置于烘箱中,37℃烘干2小时。
试纸卡的组装:在PVC板1上依次粘贴经过处理的样品垫2、吸附有稀土荧光标记的抗体的结合垫3、包被有检测线和质控线的硝酸纤维素膜4和吸水垫5,组装后得到试纸大板,按照要求切割成4mm宽,将试纸装入塑料卡内形成试纸卡。
上述各步骤中选用的设备及原料优选以下原料:
孕酮特异性配对抗体;孕酮质控品:英国朗道实验诊断有限公司;稀土荧光微球:上海甄准生物科技有限公司;硝酸纤维素(NC)膜:Millipore公司产品;牛血清白蛋白(BSA),聚乙二醇PEG20000,水解酪蛋白:Sigma产品,其它常用试剂均为分析纯试剂。
实施例2:准确度试验
选用上述试纸卡以及荧光免疫层析分析仪(型号:NEO-007),
荧光免疫分析仪参数的设定:在荧光免疫分析仪上设定好试纸卡工艺参数后,取上述组装好的试纸卡,分别用0.3、3、6、10、20、40、50ng/mL的孕酮校准品,用试纸卡进行测定,得到各校准品的荧光强度值,将结果输入到分析仪的参数中,完成分析仪的参数的设定。
主要检测材料:临床样本由相关医院获得,共300份胶乳增强免疫比浊法定值样本,其中血清样本100份,血浆样本100份,全血样本100份,孕酮含量分布区间为0.3-50ng/mL之间。
检测方法:
步骤1:将检测试剂及样本平衡至室温,取出试纸卡,平放;
步骤2:读卡:将IC卡放置在干式荧光免疫分析仪标注位置,读取相关信息;
步骤3:加样:血清/血浆:取100μL血清/血浆样本垂直滴加至测试卡加样处,全血:取150μL全血样本垂直滴加至测试卡加样处,取样时注意不要吸入气泡;
步骤4:检测,可采用自动测试或即时测试两种模式进行检测,自动测试:将测试卡插入干式荧光免疫分析仪的承载器上,按测试键,仪器将自动对测试卡进行扫描分析检测,即时测试:测试卡室温放置10min后,插入干式荧光免疫分析仪的承载器上,点击即时测试。
试验结果分析:
临床样本检测试剂制备完成后,按检测方法对所有临床样本进行检测,并分析检测结果。
试验结果:
如附图2所示,以实验系统的检测值为Y轴,以对照系统的测验值为X轴,绘制散点图,并进行相关性分析。临床样本检测对300份临床定值样本检测,样本平均偏差值小于10%,最大偏差小于20%,R2>0.98,一致性系数>0.90。检测结果表明制备的检测试剂盒性能良好,适合用于临床检测,满足不同客户不同检测场合的差异化需要。
本发明提供一种利用稀土荧光免疫层析技术制备的孕酮快速定量免疫层析检测试剂盒,同时适合血清/血浆和全血样本,并适合临床上单人份检测,相对于孕酮定性胶体金试剂,能定量检测样本中的孕酮含量,具有更明确的临床指导意义,具有操作简便、反应快速、灵敏度高、特异性强、适合现场检测和经济实用等优点。
- 还没有人留言评论。精彩留言会获得点赞!