一种纤维蛋白原含量检测试剂盒的制作方法
本发明涉及生物
技术领域:
,特别涉及一种用Clauss法测定纤维蛋白原含量检测试剂盒。
背景技术:
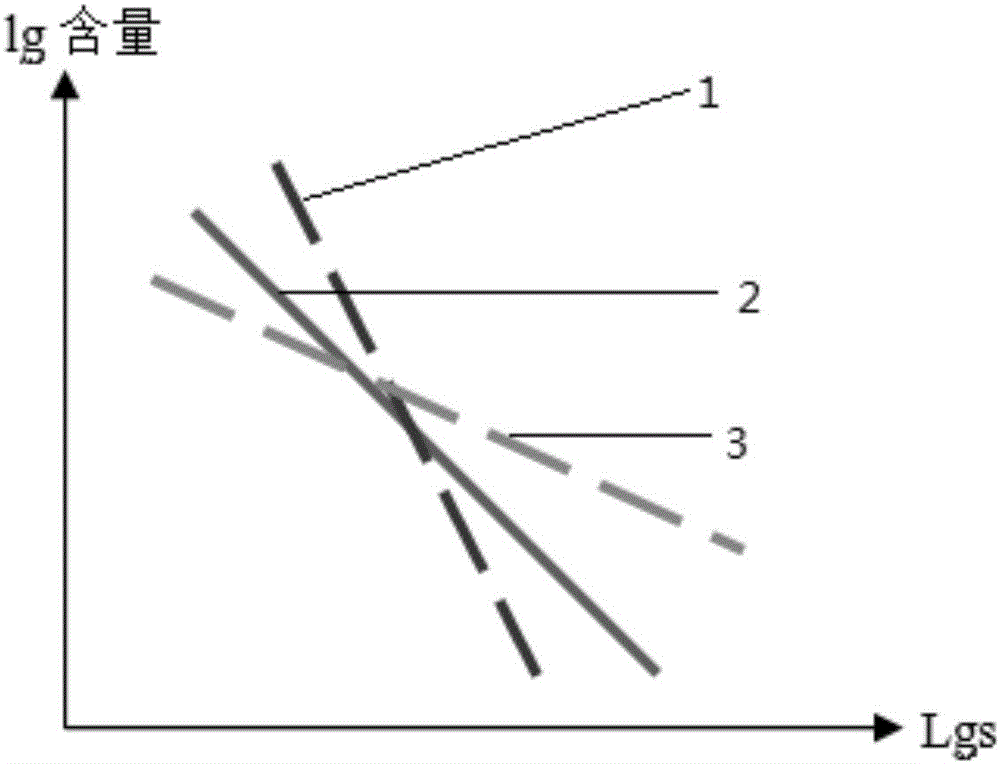
:纤维蛋白原是一种由肝脏合成的具有凝血功能的糖蛋白,是纤维蛋白的前体。纤维蛋白原水平增高多见于糖尿病、炎症应激反应,肥胖症;纤维蛋白原水平降低多见于DIC、纤维蛋白溶解。肝功能严重障碍或先天性缺乏,均可使血浆纤维蛋白原浓度下降,严重时可有出血倾向。此外,纤维蛋白原也被用于心血管意外的致病性研究。纤维蛋白原在肝脏(1.7~5g/天)和巨核细胞内合成,血浆中参考值2~4g/l。纤维蛋白原由2Aα、2Bβ、2γ这6条链组成,在凝血酶(因子IIa)作用下,可将纤维蛋白原分子裂解成两个纤维蛋白肽A片段FPA(从Aα链)和两个纤维蛋白肽B片段FPB(从Bβ链),α链与β链分别释放出A肽与B肽,生成纤维蛋白单体。在此过程中,由于释放了酸性多肽,负电性降低,单体易于聚合成纤维蛋白多聚体。但此时单体之间借氢键与疏水键相连,尚可溶于稀酸和尿素溶液中。内源凝血途径中的FXa与因子V(FV)、PF3和钙离子构成凝血酶原复合物,激活凝血酶原生产凝血酶。进一步在Ca2+与活化的XIII因子(XIIIa)作用下,单体之间以共价键相连,则变成稳定的不溶性纤维蛋白凝块,完成凝血过程。在正常的凝血机制中,必须有钙离子的参与,而标本采集过程中,为了防止血液凝集加入抗凝剂,抗凝剂中的枸橼酸根离子抑制了全血钙离子,因此必须在检测试剂中加入钙离子,以还原或补充被抑制的钙离子,进一步模拟体内正常凝血过程。目前市场上鲜有厂家提到了“含钙”的试剂体系,大部分产品均忽略或未提及试剂中Ca2+对血浆中FIB定量检测的重要意义。本发明中的FIB定量试剂盒特将Ca2+加入凝血酶试剂体系中,将在体外更为精确的检测人血浆中纤维蛋白原的含量,为临床提供有利的数据参考。技术实现要素:有鉴于此,本发明提供了一种纤维蛋白原含量检测试剂盒。该纤维蛋白原含量检测试剂盒稳定性佳、重复性好,同时操作安全简便、准确度高、线性范围宽及兼容性强。为了实现上述发明目的,本发明提供以下技术方案:本发明提供了一种纤维蛋白原含量检测试剂盒,包括凝血酶试剂、咪唑缓冲液和定值血浆;凝血酶试剂包括凝血酶、咪唑、氯化钙、甘露醇、蛋白胨、牛血清白蛋白、叠氮钠和水。纤维蛋白原含量的测定原理:在过量凝血酶的存在下,被稀释血浆的凝固时间可直接反映血浆中纤维蛋白原水平。向血浆中加入过量的凝血酶,使纤维蛋白原变为纤维蛋白,从而出现凝固。凝固时间与纤维蛋白原含量呈负相关,通过建立标准曲线而获得受检血浆FIB含量的方法,即Clauss法。据调研得知,若将FIB含量和凝血时间分别取对数来绘制定标相关曲线时,曲线的最为理想的斜率值为-1,当曲线斜率值控制在-1~0时,表现为线性范围小,FIB含量准确性高,当曲线斜率值小于-1时,表现为线性范围大,FIB含量准确性低。目前未见业内厂家提及该试剂体系中FIB含量对数与凝血时间对数相关曲线斜率值对FIB定量准确性的影响,且同类产品的该相关曲线斜率值大都小于-1。本发明通过研发条件优化,特将该相关曲线斜率值控制在-(1±0.05),既保证了FIB的检测范围又保证了FIB定量的准确性。本发明中的试剂盒适用于临床实验室常规检验用的Clauss法来检测纤维蛋白原含量(Fibrinogentest(VonClauss))。不适用于物理化学测定法和免疫法测定纤维蛋白原含量。本发明中的FIB定量试剂盒特将Ca2+加入凝血酶试剂体系中,将在体外更为精确的检测人血浆中纤维蛋白原的含量,为临床提供有利的数据参考。本发明通过特定的试剂配方,可进一步提高FIB含量检测试剂的稳定性和重复性。作为优选,凝血酶试剂中各组分按如下配比配制:作为优选,该凝血酶试剂还包括水,各组分用量为:优选地,凝血酶试剂中各组分用量为:作为优选,凝血酶试剂的pH值为7.35~7.45。作为优选,凝血酶为牛凝血酶。作为优选,咪唑缓冲液包括咪唑、叠氮钠、氯化钠和水。作为优选,咪唑缓冲液中各组分用量为:优选地,咪唑缓冲液中各组分用量为:作为优选,咪唑缓冲液的pH值为7.35~7.45。在本发明中,定值血浆来源于健康人血浆,由标准血浆标定得到。作为优选,本发明将FIB含量和凝血时间分别取对数来绘制定标相关曲线时,标定的纤维蛋白原含量对数与凝血时间对数的相关曲线斜率控制在-(1±0.05)。该试剂盒的定标曲线的线性范围广,且纤维蛋白原含量测试值准确度高。本发明还提供了一种非诊断目的检测纤维蛋白原含量的方法,包括如下步骤:将定值血浆采用咪唑缓冲液进行稀释,得到不同浓度的定值血浆;将定值血浆在37℃条件下预温3分钟,加入凝血酶试剂,得到定值血浆的凝血时间,根据不同浓度的定值血浆的凝血时间制作标准曲线;将枸橼酸钠(109mmol/L)与静脉血按体积比1:9的比例混合,离心,得到待测血浆,将待测血浆在37℃条件下预温3分钟,加入凝血酶试剂,根据待测血浆的凝血时间获得纤维蛋白原的含量。本发明提供了一种纤维蛋白原含量检测试剂盒。该纤维蛋白原含量检测试剂盒,包括凝血酶试剂、咪唑缓冲液和定值血浆;凝血酶试剂包括凝血酶、咪唑、氯化钙、甘露醇、蛋白胨、牛血清白蛋白、叠氮钠和水。本发明具备以下优点:1、本发明通过分析血浆纤维蛋白原含量检测原理,确定了合适的凝血酶试剂、咪唑缓冲液的配制方案,研制出可用于医院临床检测人血浆FIB含量的体外诊断试剂盒。2、本发明中的凝血酶试剂特含有Ca2+,以还原或补充临床血样中被抑制的钙离子,更为理想地模拟了体内正常凝血过程,为临床检测提供更为精确的数据参考。3、本发明试剂盒的定标曲线的线性范围广,即FIB含量对数与凝血时间对数的相关曲线斜率稳定在-(1±0.05),其纤维蛋白原含量测试值准确度高。4、本发明试剂盒基本性能达到行业内标准要求,其准确度高,检测范围宽,稳定性好,可向市场进一步推广使用。5、0~1IU/mL肝素不影响本发明试剂盒凝血时间的检测,其检测到的凝血时间与正常凝血时间不超过1.5s,达到行业标准要求。附图说明图1示实施例6中FIB含量对数和凝血时间对数相关曲线示意图;图2示实施例6中本发明试剂的FIB含量对数和凝血时间对数相关曲线;图3示实施例6中fisher试剂的FIB含量对数和凝血时间对数相关曲线;图4示实施例6中Biomedica试剂的FIB含量对数和凝血时间对数相关曲线。具体实施方式本发明公开了一种纤维蛋白原含量检测试剂盒,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本
发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。本发明提供的纤维蛋白原含量检测试剂盒中所用试剂或仪器均可由市场购得。下面结合实施例,进一步阐述本发明:实施例1本发明试剂盒的制备及使用方法一、试剂盒制备(1)凝血酶试剂(pH值为7.4):(2)咪唑缓冲液(pH值为7.4):(3)定值血浆:3g/L。二、试剂盒的使用方法本发明的试剂盒是在医院临床实验室常规检验用凝固法全自动凝血测试仪上进行,其具体使用方法为:1、样品及试剂的准备:(1)制备待测血浆样品:静脉采血,109mmol/L枸橼酸钠与全血按1:9比例混合均匀。以2500g离心15分钟,用塑料移液管取出血浆,血浆样品必须在4小时内进行测试。(2)FIB凝血酶试剂:每瓶凝血酶按瓶签标称量精确加入蒸馏水,轻轻混匀,放置10分钟平衡至室温后备用。(3)如需配制参考血浆(或正常质控血浆、异常质控血浆),请按各自的相关说明书配制。2、纤维蛋白原参考曲线制定(以FIB定标为例):(1)用咪唑缓冲液制备不同稀释度的定标血浆,例如定标血浆为3g/L,输入FIB浓度值,如下表所示:表1定标血浆的配制血浆占比1:51:101:201:30咪唑缓冲液(μL)2004509501450参考血浆(μL)50505050FIB浓度(g/L)3×233×1/23×1/3(2)定标测定具体步骤如下:3、测病人血样具体步骤如下:实施例2发明试剂盒最适缓冲体系稳定性的验证实验:本实验为了找到试剂体系中主要成分的最佳配比关系,对该试剂盒中凝血酶试剂和咪唑缓冲液组成成分的浓度进行了对比分析,分别检测了A、B、C三种缓冲体系配制的试剂在37℃条件下FIB含量变化,评估了对应试剂体系的稳定性情况。其中,A、B、C试剂配方为表2所示:表2不同浓度试剂体系成分组成:具体实验数据请见下表3所示:表3不同浓度试剂体系稳定性以上实验数据显示,该试剂盒采用B试剂体系的稳定性更好,8天内FIB含量检测值偏差不超过1秒,所以选用B试剂体系作为本发明试剂盒相应的工作液。实施例3发明试剂盒中Ca2+对FIB定量准确性的验证实验:本实验分组为凝血酶试剂中添加Ca2+组和凝血酶试剂中无Ca2+组,添加Ca2+组采用实施例2的B试剂体系进行检测,无Ca2+组采用在实施例2的B试剂体系基础上缺少氯化钙的试剂。每组随机选取10个试剂进行FIB定量检测,对照血浆FIB参考值为2.8g/L,分别计算每组检测值均值、检测值与参考值的偏差,进而评价凝血酶试剂中Ca2+对FIB定量的影响,相关实验数据如下表4所示:表4凝血酶试剂中Ca2+对FIB定量准确性的影响以上数据显示,凝血酶试剂中加入Ca2+组的FIB检测值与参考值更为相符、偏差较小,即凝血酶试剂中加入Ca2+能使FIB定量结果更为准确。说明本发明试剂盒在FIB凝血酶试剂中添加回补Ca2+可以有效地模拟体内正常凝血过程,为临床检测提供更为精确的数据参考。实施例4发明试剂盒与市售同类试剂盒稳定性的比较实验:此实验将本发明试剂盒与市售Fisher同类试剂盒的FIB检测含量进行对比分析,评估本发明试剂与fisher试剂在37℃条件下的稳定性,具体实验数据如下表5所示:表5发明试剂与市售同类试剂稳定性比较以上实验数据显示,本发明试剂8天内检测值偏差不超过1秒,市售同类检测试剂三天后的检测值偏差就超过了1秒,说明本发明试剂盒试剂体系的稳定性更好。实施例5发明试剂与市售同类试剂盒重复性的比较实验:此实验将本发明试剂与市售同类试剂的FIB含量检测进行对比分析,评估本发明试剂与市售fisher试剂的重复性,具体实验数据如下表6所示:表6发明试剂与市售同类试剂重复性比较以上实验数据显示,本发明试剂的FIB含量检测的变异系数(CV)明显小于市售同类试剂的FIB含量检测,即本发明试剂盒重复性好于市售同类产品的重复性。实施例6发明试剂线性范围验证实验:据调研得知,若将FIB含量和凝血时间分别取对数来绘制定标相关曲线,如图1线1所示,当曲线斜率值为-1时,FIB定量最为精确;如图1线3所示,当曲线斜率值控制在-1~0时,表现为线性范围小,FIB含量准确性高;如图1线2所示,当曲线斜率值小于-1时,表现为线性范围大,FIB含量准确性低。本发明为了提高FIB定量的准确性,不断优化实验条件,最终使该试剂盒的线性范围缩小,如图2所示,FIB含量对数与凝血时间对数的定标相关曲线斜率稳定在-(1±0.05),进而保证了检测数据的可靠性和线性范围。在检测本发明试剂盒相关线性范围的基础上,并与fisher试剂和Biomedica试剂进行了对比分析。相关数据请见图3、图4。实施例7发明试剂盒检测范围验证实验:本实验对两批发明试剂的检测范围进行测试,用接近FIB测试范围上限的高浓度样品和咪唑缓冲液稀释成13个稀释浓度的定标品,使标称含量值范围控制在0.6-8g/L,每个稀释浓度测试两次,分别求出测定结果的均值,以稀释浓度为自变量,测定结果均值为因变量求出线性回归方程。在此基础上,通过血凝仪上检测到的凝血时间换算求出样品检测含量,计算检测含量与标称含量值的偏差,进而评价本发明试剂的检测范围情况及检测范围内试剂的准确性情况。实验检测结果如下表7和表8所示:表7两批发明试剂盒试剂检测范围测试情况表8试剂检测范围内的两批发明试剂盒的准确性情况以上检测结果显示,本发明的FIB定量试剂的检测范围宽,即试剂检测范围在0.6-8g/L之间,且该范围内的检测结果准确性较高。实施例8肝素含量对凝血时间的影响验证实验:因为肝素会抑制凝血酶,影响凝血时间的检测,该实验检测分析了0-1IU/mL肝素对本发明试剂的凝血时间影响,每批次重复检测两次,具体检测结果如下表9所示:表9肝素含量对凝血时间的影响情况以上检测结果显示,0~1IU/mL肝素不影响本发明三批试剂盒凝血时间的检测,其检测到的凝血时间与正常凝血时间不超过1.5s,达到行业标准要求。以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1