定量检测SAA、CRP、PCT的免疫荧光层析试剂盒及其制备方法与流程
本发明属于生物医药技术领域,尤其涉及一种快速、定量检测试剂,采用荧光微球、量子点等为标记物,以免疫层析方法,配合使用荧光免疫分析仪,实现同时检测人血清、血浆和全血样本中的saa、pct、crp的含量,具体是定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。
背景技术:
血清淀粉样蛋白a(saa)是一种急性时限反应蛋白,血清淀粉样蛋白a的含量浓度是反映感染性疾病早期炎症的敏感指标,有助于诊断炎症、评估其活性、监控其活动及治疗。
c反应蛋白(crp)是指在机体受到感染或组织损伤时血浆中含量急剧上升的一种急性相蛋白。传统观点认为crp是一种非特异的炎症标志物,但近十年的研究揭示了crp直接参与了炎症与动脉粥样硬化等心血管疾病,并且是心血管疾病最强有力的预示因子。
降钙素原(pct)是诊断和监测细菌炎性疾病感染的一个参数。pct是严重细菌性炎症和真菌感染的特异性指标,而且也是脓毒症和炎症活动有关的多脏器衰竭的可靠指标。
研究表明在诊断炎症、感染及相关疾病中,单一的saa、pct及crp项目的检测并不能有效准确的诊断疾病,诊断过程中如果将saa、crp及pct等项目检测结果与临床资料结合,在感染性疾病的诊断上有重要的意义。
然而,目前已上市产品中,绝大部分是saa、crp及pct等3个项目的单独检测试剂盒,或者pct和crp同时检测试剂盒,还没有saa、crp及pct3个项目同时联检的试剂盒,如果需要同时检测3个项目的结果,需要2-3次的加样及检测操作,如果检测试剂盒要求的标本类型不一样,还需要对患者重复取样,操作上较为繁琐,试剂及耗材的成本上有所浪费,对患者也造成了额外的负担。
通过对现有文献的检索发现,天津中新科炬生物制药有限公司申请了3个相关发明专利:《一种同时定量检测saa/pct/crp的方法》(申请号为201511018503.2)、《一种同时定量检测saa/pct/crp的检测装置的制备方法》(申请号为201511018504.7)、《一种同时定量检测saa/pct/crp的检测装置》(申请号为201511030398.4)。以上3个专利申请为相似技术,利用互相独立的人血清淀粉样蛋白a(saa)、人降钙素原(pct)和c反应蛋白(crp)检测试纸,三联卡壳和附带了相应判定方法和标准曲线的免疫层析判读结果记录仪,同时快速定量检测saa/pct/crp。但其检测方法为三联卡,需要分别加3次样品,加样量和方法也各不一样,并不能减少试剂及耗材的成本,不能实现真正意义上的联检。且其使用的是胶体金免疫层析法,其saa、pct、crp定量的检测范围分别为5-100mg/l,0.5-20mg/l和1-200mg/l,灵敏度较差,难以满足临床需求。
另外,现有技术中还公开了一种定量联合检测pct/crp/saa胶体金试纸条及其应用的检测装置(申请号为201420797771.3),本发明提供的试纸条,其为在底板上依次相互交错地粘贴的样品垫、涂覆有金标抗体的聚酯膜、包被膜及吸水纸,包被膜上设有一条包被兔抗鼠igg抗体的控制线,包被膜上还设有与所述控制线平行的三条检测线,分别包被能与待检抗原pct特异性结合的抗体、与待检抗原crp特异结合的抗体以及与待检抗原saa特异结合的抗体;所述金标抗体有三种,分别为胶体金标记的能与待检抗原pct特异性结合的抗体、与待检抗原crp特异结合的抗体以及与待检抗原saa特异结合的抗体。该技术在一条试纸条上同时设置三条检测线和一条检测线,同步检测三个指标,经配套免疫荧光分析仪判断结果,灵敏度较差,准确度较低,难以达到临床要求的定量检测要求。
技术实现要素:
针对现有技术的不足,本发明提供定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。该试剂盒通过荧光免疫层析法,配合使用荧光免疫分析仪,可以方便、准确且高灵敏度地同时检测saa、crp、pct的含量。
为实现上述目的,在本发明中采取了以下技术方案:一种定量检测saa、crp、pct的免疫荧光层析试剂盒,其特征在于,包括荧光免疫层析试纸条、荧光物质,所述荧光免疫层析试纸条,底衬上设有硝酸纤维素膜,硝酸纤维素膜的一端衔接有样品垫,硝酸纤维素膜的另一端衔接有吸收垫;所述硝酸纤维素膜上平行设有包被了羊抗兔igg多克隆抗体的质控线、包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线和包被了pct单克隆抗体的检测线;所述荧光物质包括偶联了兔igg多克隆抗体的荧光物质、偶联了配对saa单克隆抗体的荧光物质、偶联了配对crp单克隆抗体的荧光物质和偶联了配对pct单克隆抗体的荧光物质。
进一步的,本发明提供一种定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法,其特征在于,包括以下步骤:
1)荧光免疫层析试纸条的制备:在硝酸纤维素膜的靠近吸收垫的一端划上包被了羊抗兔igg多克隆抗体的质控线、包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线和包被了pct单克隆抗体的检测线,在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜一端贴上吸收垫,在另一端贴上样品垫,制备成试纸板,然后用切条机将试纸板纵向切成4mm宽的试纸条;
2)荧光物质应用溶液的制备:分别将兔igg多克隆抗体、配对saa单克隆抗体的荧光物质、配对crp单克隆抗体和配对pct单克隆抗体偶联荧光物质得到抗体修饰的荧光物质,再将上述抗体修饰的荧光物质一起稀释至稳定缓冲液中得到荧光物质应用溶液。
进一步的,本发明提供另一种定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法,其特征在于,包括以下步骤:
1)固相结合荧光物质的样品垫的制备:分别将兔igg多克隆抗体、配对saa单克隆抗体的荧光物质、配对crp单克隆抗体和配对pct单克隆抗体偶联荧光物质得到抗体修饰的荧光物质,再将上述抗体修饰的荧光物质一起固相结合至样品垫中得到荧光物质样品垫。
2)荧光免疫层析试纸条的制备:在硝酸纤维素膜的靠近吸收垫的一端划上包被了羊抗兔igg多克隆抗体的质控线、包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线和包被了pct单克隆抗体的检测线,在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜一端贴上吸收垫,然后组合上固相结合荧光物质的样品垫,制备成试纸板,最后用切条机将试纸板纵向切成4mm宽的试纸条。
与现有技术相比,本发明的有益效果在于:
1、本发明的定量检测saa、crp、pct的免疫荧光层析试剂盒在试纸条上设有saa、crp跟pct的检测线,能够通过一次加样同步检测saa、crp和pct3个指标,操作简单,能减少试剂及耗材的成本。
2、本发明的定量检测saa、crp、pct的免疫荧光层析试剂盒基于荧光免疫层析技术,荧光物质上偶联的抗体与样本中的抗原相结合然后再与试纸条上面的抗体相互作用,然后通过荧光分析仪将荧光物质的不同光信号转化为电信号得到不同的样本检测浓度,结果精准,能明显改善传统胶体金法肉眼判读结果导致的准确性差、重复性差和效率低的问题。
3、本发明的定量检测saa、crp、pct的免疫荧光层析试剂盒采用的荧光免疫法比传统胶体金法灵敏度更高;saa的检测范围达到0.5~200mg/l,crp的检测范围达到0.2~200mg/l,pct的检测范围达到0.1~100ug/l。saa、crp和pct的灵敏度分别达到0.5mg/l、0.2mg/l和0.1ug/l。
附图说明
图1为本发明定量检测saa、crp、pct的免疫荧光层析试剂盒的试纸条结构示意图图;图中,1-吸收垫;2-控制线;3-saa包被线;4-crp包被线;5-pct包被线;6-样品垫。
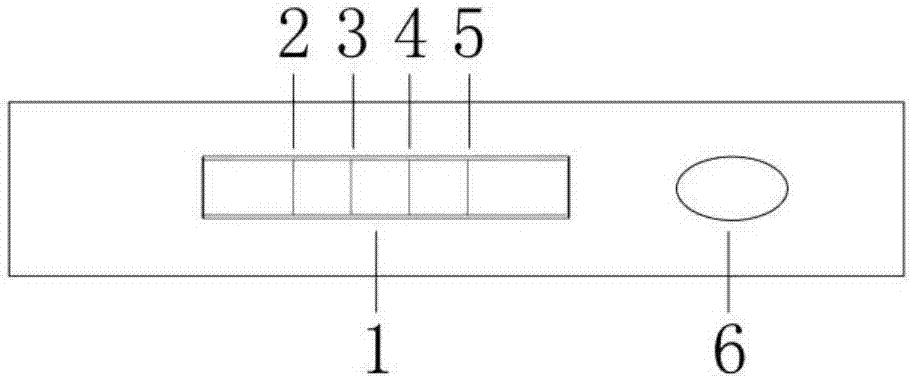
图2为设置有本发明定量检测saa、crp、pct的免疫荧光层析试剂盒的试纸条的试剂卡结构示意图;图中,1-观察槽;2-控制线;3-saa包被线;4-crp包被线;5-pct包被线;6-加样槽。
图3为实施例1所制得的试剂盒测试结果与西门子saa的相关线性图。
图4为实施例1所制得的试剂盒测试结果与西门子crp的相关线性图。
图5为实施例1所制得的试剂盒测试结果与梅里埃pct的相关线性图。
图6为实施例1所制得的试剂盒与实施例2所制得的试剂盒saa测试结果的相关线性图。
图7为实施例1所制得的试剂盒与实施例2所制得的试剂盒crp测试结果的相关线性图。
图8为实施例1所制得的试剂盒与实施例2所制得的试剂盒pct测试结果的相关线性图。
具体实施方式
下面结合具体实施例对本发明进行详细的阐述。
本发明提供一种定量检测saa、crp、pct的免疫荧光层析试剂盒,包括荧光免疫层析试纸条、荧光物质,所述荧光免疫层析试纸条,底衬上设有硝酸纤维素膜,硝酸纤维素膜的一端衔接有样品垫,硝酸纤维素膜的另一端衔接有吸收垫;所述硝酸纤维素膜上平行设有包被了羊抗兔igg多克隆抗体的质控线、包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线和包被了pct单克隆抗体的检测线;所述荧光微球应用溶液包括偶联了兔igg多克隆抗体的荧光物质、偶联了配对saa单克隆抗体的荧光物质、偶联了配对crp单克隆抗体的荧光物质和偶联了配对pct单克隆抗体的荧光物质。
进一步的,上述的定量检测saa、crp、pct的免疫荧光层析试剂盒,是基于侧向流层析及双抗体夹心法检测的免疫反应。
进一步的,上述的定量检测saa、crp、pct的免疫荧光层析试剂盒,所述的荧光物质为普通荧光微球、时间分辨荧光微球、量子点等标记物。
进一步的,上述的定量检测saa、crp、pct的免疫荧光层析试剂盒,所述硝酸纤维素膜的爬速为95s~180s/4cm。
进一步的,上述的定量检测saa、crp、pct的免疫荧光层析试剂盒,所述样品垫为全血过滤膜、聚酯膜、玻璃纤维中的一种。
进一步的,上述的定量检测saa、crp、pct的免疫荧光层析试剂盒,配合使用内置了saa、crp和pct反应曲线的荧光仪来完成saa、crp、pct的定量检测。
进一步的,上述的定量检测saa、crp、pct的免疫荧光层析试剂盒,所述荧光物质为荧光物质应用溶液或者为固相结合到所述样品垫上的荧光物质。
进一步的,本发明还提供一种上述定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法,包括以下步骤:
1)荧光免疫层析试纸条的制备:在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜一端贴上吸收垫,在另一端贴上样品垫,在硝酸纤维素膜的靠近吸收垫的一端依次划上羊抗兔igg多克隆抗体质控线、saa单克隆抗体检测线、crp单克隆抗体检测线和pct单克隆抗体检测线,制备成试纸板,然后用切条机将试纸板纵向切成4mm宽的试纸条;
2)荧光物质应用溶液的制备:分别将兔igg多克隆抗体、配对saa单克隆抗体的荧光物质、配对crp单克隆抗体和配对pct单克隆抗体偶联荧光物质得到抗体修饰的荧光物质,再将上述抗体修饰的荧光物质一起稀释至稳定缓冲液中得到荧光物质应用溶液。
进一步的,本发明提供另一种定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法,其特征在于,包括以下步骤:
1)固相结合荧光物质的样品垫的制备:分别将兔igg多克隆抗体、配对saa单克隆抗体的荧光物质、配对crp单克隆抗体和配对pct单克隆抗体偶联荧光物质得到抗体修饰的荧光物质,再将上述抗体修饰的荧光物质一起固相结合至样品垫中得到荧光物质样品垫。
2)荧光免疫层析试纸条的制备:在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜一端贴上吸收垫,在硝酸纤维素膜的靠近吸收垫的一端依次划上包被了羊抗兔igg多克隆抗体的质控线、包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线和包被了pct单克隆抗体的检测线,制备成试纸半成品板,然后组合上固相结合荧光物质的样品垫,最后用切条机将试纸板纵向切成4mm宽的试纸条。
以下实施例中所使用的原料如无特别说明,均来自于市售。所涉及的%均为重量百分数。
实施例1
本实施例提供定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。
该实施例中,所述荧光物质为激发波长360nm、发射波长为615nm的时间分辨荧光微球,系包裹了稀土铕元素的荧光染料聚苯乙烯微球。
该实施例的定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法包括以下步骤:
(1)时间分辨荧光微球的活化:先取1ml荧光微球加入4ml0.05mol/l、ph6.0mes溶液,用超声波进行超声分散,;称取5mg的n-羟基琥珀酰亚胺(nhs)加入到微球悬浮液中,然后摇匀使之溶解;接着称取5mg的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)加入到微球悬浮液中,混匀后室温搅拌反应1小时;将反应后的悬浮液用超声波超声,将混匀的微球离心处理,离心条件12000r/min,离心20min,倒掉上清液,加入0.8ml0.05mol/l、ph7.4的pb缓冲液,然后用超声波超声分散均匀,接着定容到1ml。
(2)活化的时间分辨荧光微球偶联抗体:取1ml活化后的微球悬浮液,超声分散均匀,然后边搅拌边滴加入兔igg多克隆抗体(购自arista公司),优选的抗体量为0.1~0.3mg,在2-8℃条件下,搅拌反应过夜;加10%的bsa(终浓度在1%)进行封闭,混匀后室温搅拌反应2小时,离心洗涤2次,倒掉上清液,沉淀用0.8ml0.05mol/l、ph7.4的pbst溶解,并用超声波超声分散均匀,接着定容到1ml,4℃保存,备用。
以上述同样方式将活化的时间分辨荧光微球分别偶联至saa单克隆抗体(购自arista公司)、crp单克隆抗体(购自medix公司)和pct单克隆抗体(购自medix公司),4℃保存,备用。
(3)荧光微球应用溶液的配制:将偶联了兔igg多克隆抗体的时间分辨荧光微球、偶联了配对saa单克隆抗体的时间分辨荧光微球、偶联了配对crp单克隆抗体的时间分辨荧光微球、偶联了配对pct单克隆抗体的时间分辨荧光微球稀释至稳定缓冲液(包含3%酪蛋白、5%海藻糖、0.5%吐温-20、3%bsa、0.1%nan3、0.3%pva,余量为0.05mol/l、ph7.4的mes缓冲液)中,4℃保存,备用。
(4)硝酸纤维素膜的制备:用包被缓冲液(包含3%甲醇、2%海藻糖,余量为0.01mol/l、ph7.4的pbs缓冲液)稀释羊抗兔igg多克隆抗体至0.5mg/ml,稀释saa单克隆抗体至1mg/ml,稀释crp单克隆抗体至0.5mg/ml,稀释pct单克隆抗体至0.8mg/ml;然后以划线用量1μl/cm在爬速为95s/4cm的硝酸纤维素膜上依次划上羊抗兔igg多克隆抗体质控线、saa单克隆抗体检测线、crp单克隆抗体检测线和pct单克隆抗体检测线。
包被了羊抗兔igg多克隆抗体的质控线、包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线和包被了pct单克隆抗体的检测线相互间间隔3mm。
将包被好的硝酸纤维素膜放置于37℃真空干燥箱干燥0.5小时以上,密封室温保存,备用。
(5)试纸条的制备:在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜的靠近包被了pct单克隆抗体检测线的一端粘贴样品垫,在硝酸纤维素膜靠近包被了羊抗兔igg多克隆抗体质控线的另一端粘贴吸收垫,制备成试纸板。用切条机将试纸板纵向切成4mm宽的试纸条。
实施例2
本实施例提供定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。
该实施例的试纸条结构与实施例1的结构相同,不同之处在于,实施例2中的荧光物质为激发波长470nm~490mm、发射波长为525~560nm的荧光微球,为包裹了荧光染料的聚苯乙烯微球。
该实施例的定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法包括以下步骤:
(1)荧光微球的活化:先取1ml荧光微球用超声波进行超声分散,超声波100w处理时间30s;加入1ml0.8ml0.1mol/l、ph4.7的mes混匀后离心处理,离心条件12000r/min,离心20min,倒掉上清液,加入1ml0.1mol/l、ph4.7的mes缓冲液。称取3mg的n-羟基琥珀酰亚胺(nhs)加入到微球悬浮液中,然后摇匀使之溶解;接着称取5mg的1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)加入到微球悬浮液中,混匀后室温搅拌反应1小时;将反应后的悬浮液用超声波超声,将混匀的微球离心处理,离心条件12000r/min,离心20min,倒掉上清液,加入0.8ml0.05mol/l、ph7.4的bbs缓冲液,然后用超声波超声分散均匀,接着定容到1ml。
(2)活化的荧光微球偶联抗体:取1ml活化后的微球悬浮液,超声分散均匀,然后边搅拌边滴加入兔igg多克隆抗体(购自arista公司),优选的抗体量为0.1~0.3mg,在2-8℃条件下,搅拌反应过夜;加10%的bsa(终浓度在1%)进行封闭,混匀后室温搅拌反应2小时,离心洗涤2次,倒掉上清液,沉淀用0.8ml0.05mol/l、ph7.4的tris-hcl溶解,并用超声波超声分散均匀,接着定容到1ml,4℃保存,备用。
以上述同样方式将活化的时间分辨荧光微球分别偶联至saa单克隆抗体(购自arista公司)、crp单克隆抗体(购自medix公司)和pct单克隆抗体(购自medix公司),4℃保存,备用。
(3)荧光微球应用溶液的配制:同实施例1。
(4)硝酸纤维素膜的制备:同实施例1。
(5)试纸条的制备:同实施例1。
实施例3
本实施例提供定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。
该实施例的试纸条结构与实施例1的结构相同,不同之处在于,实施例3中的硝酸纤维素膜2为爬速为135s/4cm的为硝酸纤维素膜。
(1)荧光微球的活化:同实施例1。
(2)活化的荧光微球偶联抗体:同实施例1。
(3)荧光微球应用溶液的配制:同实施例1。
(4)硝酸纤维素膜的制备:用包被缓冲液(包含3%甲醇、2%海藻糖,余量为0.01mol/l、ph7.4的pbs缓冲液)稀释羊抗兔igg多克隆抗体至0.3mg/ml,稀释saa单克隆抗体至0.8mg/ml,稀释crp单克隆抗体至0.3mg/ml,稀释pct单克隆抗体至0.6mg/ml;然后以划线用量1μl/cm在爬速为135s/4cm的硝酸纤维素膜上依次划上羊抗兔igg多克隆抗体质控线、saa单克隆抗体检测线、crp单克隆抗体检测线和pct单克隆抗体检测线。
(6)试纸条的制备:同实施例1。
实施例4
本实施例提供定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。
该实施例的试纸条结构与实施例1的结构相同,不同之处在于,实施例3中的硝酸纤维素膜2为爬速为180s/4cm的硝酸纤维素膜。
(1)荧光微球的活化:同实施例1。
(2)活化的荧光微球偶联抗体:同实施例1。
(3)荧光微球应用溶液的配制:同实施例1。
(4)硝酸纤维素膜的制备:用包被缓冲液(包含3%甲醇、2%海藻糖,余量为0.01mol/l、ph7.4的pbs缓冲液)稀释羊抗兔igg多克隆抗体至0.25mg/ml,稀释saa单克隆抗体至0.7mg/ml,稀释crp单克隆抗体至0.25mg/ml,稀释pct单克隆抗体至0.5mg/ml;然后以划线用量1.2μl/cm在爬速为180s/4cm的硝酸纤维素膜上依次划上羊抗兔igg多克隆抗体质控线、saa单克隆抗体检测线、crp单克隆抗体检测线和pct单克隆抗体检测线。
(7)试纸条的制备:同实施例1。
实施例5
本实施例提供定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。
该实施例中,所述荧光物质为激发波长360nm、发射波长为615nm的时间分辨荧光微球,系包裹了稀土铕元素的荧光染料聚苯乙烯微球。
该实施例中,所述荧光物质固相结合到样品垫上形成固相结合荧光物质的样品垫上。
该实施例的定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法包括以下步骤:
(1)时间分辨荧光微球的活化:同实施例1。
(2)活化的时间分辨荧光微球偶联抗体:同实施例1。
(3)固相结合荧光物质的样品垫的制备:将偶联了兔igg多克隆抗体的时间分辨荧光微球、偶联了配对saa单克隆抗体的时间分辨荧光微球、偶联了配对crp单克隆抗体的时间分辨荧光微球、偶联了配对pct单克隆抗体的时间分辨荧光微球稀释至稳定缓冲液(包含3%酪蛋白、5%海藻糖、0.5%吐温-20、3%bsa、0.1%nan3、0.3%pva,余量为0.05mol/l、ph7.4的pbs缓冲液)中,将所配制荧光偶合物液均匀的喷涂在样品垫上(喷液量为50ul/cm2)。将喷好荧光偶合物液的样品垫置于37℃真空干燥箱干燥1小时以上,密封室温保存,备用。
(4)硝酸纤维素膜的制备:同实施例1。
(5)试纸条的制备:在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜的靠近包被了pct单克隆抗体检测线的一端粘贴固相结合荧光物质的样品垫,在硝酸纤维素膜靠近包被了羊抗兔igg多克隆抗体质控线的另一端粘贴吸收垫,制备成试纸板。用切条机将试纸板纵向切成4mm宽的试纸条。
实施例6
本实施例提供定量检测saa、crp、pct的免疫荧光层析试剂盒及其制备方法。
该实施例中,荧光物质为激发波长470nm~490mm、发射波长为525~560nm的荧光微球,为包裹了荧光染料的聚苯乙烯微球。
该实施例中,所述荧光物质固相结合到样品垫上形成固相结合荧光物质的样品垫上,而不是保存在荧光物质应用溶液中。
该实施例的定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法包括以下步骤:
(1)荧光微球的活化:同实施例2。
(2)活化的荧光微球偶联抗体:同实施例2。
(3)荧光偶合物样品垫的制备:将偶联了兔igg多克隆抗体的荧光微球、偶联了配对saa单克隆抗体的荧光微球、偶联了配对crp单克隆抗体的荧光微球、偶联了配对pct单克隆抗体的荧光微球稀释至稳定缓冲液(包含3%酪蛋白、5%海藻糖、0.5%吐温-20、3%bsa、0.1%nan3、0.3%pva,余量为0.05mol/l、ph7.4的pbs缓冲液)中,将所配制荧光偶合物液均匀的喷涂在样品垫上(喷液量为70ul/cm2)。将喷好荧光偶合物液的样品垫置于37℃真空干燥箱干燥1小时以上,密封室温保存,备用。
(4)硝酸纤维素膜的制备:同实施例1。
(5)试纸条的制备:同实施例5。
实施例7
该实施例中,所述荧光物质为激发波长360nm、发射波长为615nm的时间分辨荧光微球,系包裹了稀土铕元素的荧光染料聚苯乙烯微球。
该实施例中,所述样品垫粘贴靠近硝酸纤维素膜上包被了羊抗兔igg多克隆抗体质控线的一端,而吸收垫粘贴靠近硝酸纤维素膜上包被了saa单克隆抗体检测线的另一端。
该实施例的定量检测saa、crp、pct的免疫荧光层析试剂盒的制备方法包括以下步骤:
(1)时间分辨荧光微球的活化:同实施例1。
(2)活化的时间分辨荧光微球偶联抗体:同实施例1。
(3)固相结合荧光物质的样品垫的制备:同实施例1。
(4)硝酸纤维素膜的制备:用包被缓冲液(包含3%甲醇、2%海藻糖,余量为0.01mol/l、ph7.4的pbs缓冲液)稀释saa单克隆抗体至1mg/ml,稀释crp单克隆抗体至0.5mg/ml,稀释pct单克隆抗体至0.8mg/ml,稀释羊抗兔igg多克隆抗体至0.4mg/ml;然后以划线用量1μl/cm在爬速为95s/4cm的硝酸纤维素膜上依次划上saa单克隆抗体检测线、crp单克隆抗体检测线、pct单克隆抗体检测线和羊抗兔igg多克隆抗体质控线。
包被了包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线、包被了pct单克隆抗体的检测线和羊抗兔igg多克隆抗体的质控线相互间间隔3mm。
将包被好的硝酸纤维素膜放置于37℃真空干燥箱干燥0.5小时以上,密封室温保存,备用。
(5)试纸条的制备:在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜的靠近包被了羊抗兔igg多克隆抗体质控线的一端粘贴样品垫,在硝酸纤维素膜靠近包被了saa单克隆抗体检测线的另一端粘贴吸收垫,制备成试纸板。用切条机将试纸板纵向切成4mm宽的试纸条。
实施例8
该实施例中,所述荧光物质为量子点,系发射波长为360nm-1300nm的量子点,或包埋了所述量子点的sio2微球。
(1)量子点标记:
a)取不同波长量子点分别用磷酸缓冲液(pbs)调ph=5-9,加入edc(l-(3-二甲基氨丙基)-3-乙基碳二胺盐酸盐)和nhs(n-羟基硫代琥珀酸亚胺)室温活化15-60分钟。
b)分别对应加入saa/pct/crp的相应抗体,旋涡振荡反应30分钟-2小时。
c)分别对应加入bsa封闭反应30分钟-2小时。
d)离心纯化产物,取沉淀用pbs缓冲液重悬分散,4℃保存备用。
(2)制备试剂条组分:
a)样品垫制备:选用玻璃纤维素膜,将该膜放入含有0.1%-10%bsa和0.01%-10%tween20的pbs中浸泡,取出,干燥备用。
b)结合物垫制备:选用玻璃纤维膜切成一定规格膜块,加入用不同波长量子点对应标记的各抗体的混合物溶液于该膜块上,干燥膜块备用。
c)硝酸纤维素膜制备:用包被缓冲液(包含3%甲醇、2%海藻糖,余量为0.01mol/l、ph7.4的pbs缓冲液)稀释saa单克隆抗体至1mg/ml,稀释crp单克隆抗体至0.5mg/ml,稀释pct单克隆抗体至0.8mg/ml,稀释羊抗兔igg多克隆抗体至0.4mg/ml;然后以划线用量1μl/cm在爬速为95s/4cm的硝酸纤维素膜上依次划上saa单克隆抗体检测线、crp单克隆抗体检测线、pct单克隆抗体检测线和羊抗兔igg多克隆抗体质控线。
包被了包被了saa单克隆抗体的检测线、包被了crp单克隆抗体的检测线、包被了pct单克隆抗体的检测线和羊抗兔igg多克隆抗体的质控线相互间间隔3mm。
将包被好的硝酸纤维素膜放置于37℃真空干燥箱干燥0.5小时以上,密封室温保存,备用。
(3)试剂条的制备:在试纸底衬上粘贴硝酸纤维素膜,在硝酸纤维素膜的靠近包被了羊抗兔igg多克隆抗体质控线的一端粘贴样品垫,在硝酸纤维素膜靠近包被了saa单克隆抗体检测线的另一端粘贴吸收垫,制备成试纸板。用切条机将试纸板纵向切成4mm宽的试纸条。
检测试验例1
将实施例1所制得的定量检测saa、crp、pct的免疫荧光层析试剂盒进行测试效果检测。
试验中设有用来检测实施例1所制得的定量检测saa、crp、pct的免疫荧光层析试剂盒的荧光定量分析仪。
对saa进行检测时,采用德国西门子公司的bnprospec特定蛋白分析仪及配套nlatexsaa试剂盒做检测标准;对crp进行检测时,采用对德国西门子公司的bnⅱ全自动特定蛋白分析仪及配套试剂做检测标准;pct进行检测时,采用梅里埃公司的vidas仪器及配套试剂做检测标准。表1为采用实施例1所制得的试剂盒对部分样品进行定量测定的结果。图3、图4和图5分别为实施例1所制得的试剂盒与西门子saa、西门子crp和梅里埃pct分别检测30份标本的相关线性。
西门子和梅里埃的仪器和配套试剂均是知名试剂盒,其检测精度和结果公认可靠,由表1可看出实施例1所制得的试剂盒能得出与检测标准相当的结果,可以进行定量测定。
进一步的由图3、图4和图5分别得出实施例1所制得的试剂盒与西门子saa线性相关系数为r2=0.98,实施例1所制得的试剂盒与西门子crp线性相关系数为r2=0.99,实施例1所制得的试剂盒与梅里埃pct线性相关系数r2=0.98,相关性良好,可以用于临床诊断。
表1采用实施例1所制得的试剂盒对部分样品进行定量测定结果
检测试验例2
将实施例1及实施例2所制得的定量检测saa、crp、pct的免疫荧光层析试剂盒进行测试比较。
比较激发波长360nm、发射波长为615nm的时间分辨荧光微球和激发波长470nm~490mm、发射波长为525~560nm的普通荧光微球这2种荧光标记微球对结果的影响,图6、图7和图8分别得出实施例1所制得的试剂盒与实施例2所制得的试剂盒saa线性相关系数为r2=0.98,crp线性相关系数为r2=0.98,pct线性相关系数为r2=0.97,相关性良好。
检测试验例3
将实施例1、实施例3、实施例4所制得的定量检测saa、crp、pct的免疫荧光层析试剂盒进行测试比较。
比较爬速为95s/4cm的硝酸纤维素膜、爬速为135s/4cm的硝酸纤维素膜、爬速为180s/4cm的硝酸纤维素膜这3种硝酸纤维素膜对结果的影响,优选的爬速为95s/4cm的硝酸纤维素膜。
本发明试剂盒以荧光物质,如荧光微球、时间分辨荧光微球、量子点等为标记物,以侧向流层析及双抗体夹心法为技术原理,配合使用荧光免疫分析仪,实现快速同时检测saa/pct/crp的含量。标记抗体与样本中的抗原相结合然后再与检测卡上面的抗体相互作用,最后通过荧光分析仪将荧光微球的不同光信号转化为电信号得到不同的样本检测浓度。本发明试剂盒检测范围:crp:0.2~200mg/l,pct:0.1~100ug/l,saa:0.5~200mg/l。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!
- 基于量子点的CA15‑3免疫层析试纸条的制备方法与制造工艺
- 肌红蛋白荧光免疫层析试纸条用活化荧光乳胶微球及应用的制造方法与工艺
- 铁蛋白荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 全程C‑反应蛋白荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 25‑羟基维生素D荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 25‑羟基维生素D3荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 降钙素原荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 一种改变量子点荧光色的方法与制造工艺
- 一种基于荧光免疫层析技术的定量检测计算方法与制造工艺
- 基于量子点的CA15‑3免疫层析试纸条的制备方法与制造工艺
- 肌红蛋白荧光免疫层析试纸条用活化荧光乳胶微球及应用的制造方法与工艺
- 铁蛋白荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 全程C‑反应蛋白荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 25‑羟基维生素D荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 25‑羟基维生素D3荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 降钙素原荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 一种改变量子点荧光色的方法与制造工艺
- 一种基于荧光免疫层析技术的定量检测计算方法与制造工艺