一种改性修饰多壁碳纳米管分散固相萃取/UPLC-MS测定EGCG棕榈酸酯的方法与流程
本发明涉及一种改性修饰多壁碳纳米管分散固相萃取/uplc-ms测定egcg棕榈酸酯的方法,属于茶多酚的egcg分析技术领域。
背景技术:
茶多酚(teapolyphenols,tp)由多种酚类物质组成,具有丰富的酚羟基,因其结构的特殊性而具有多种生物活性。茶多酚除了抗氧化作用外,在抗衰老、抗炎症、抗病毒、预防心血管疾病等方面具有多种保健功能,因而在医疗、食品、保健等方面具有广泛的应用前景。
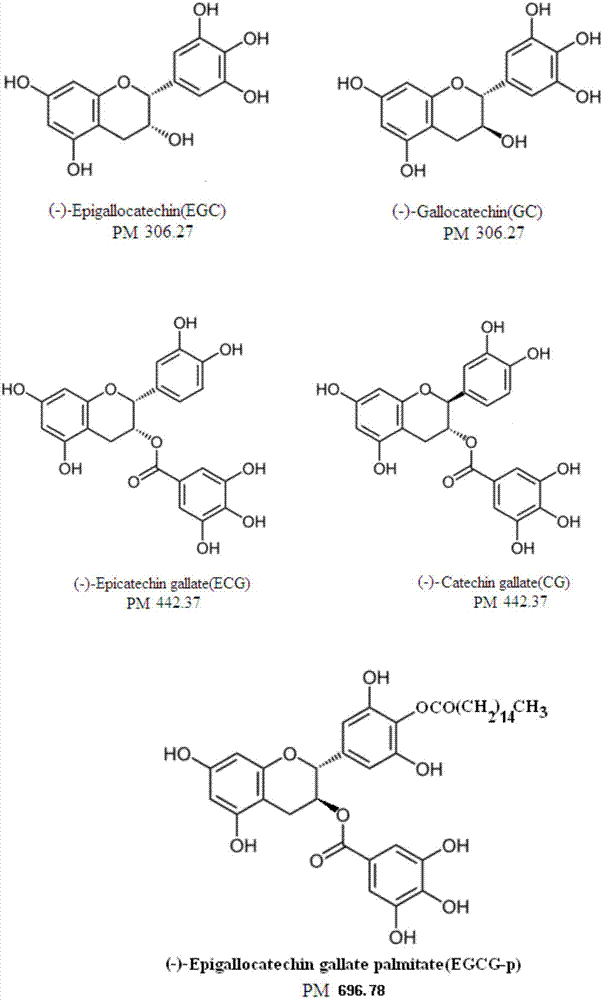
茶多酚组成极为复杂,因分子量及其结构差异而具有不同的生物活性。其中最为核心的成分是儿茶素(黄烷醇类物质),主要包括8种儿茶素类活性成分:儿茶素(catechin,c)、表儿茶素(epicatechin,ec)、没食子儿茶素(gallocatechin,gc)、表没食子儿茶素(epigallocatechin,egc)、儿茶素没食子酸酯(catechingallate,cg)、表儿茶素没食子酸酯(epicatechingallate,ecg)、没食子儿茶素没食子酸酯(gallocatechingallate,gcg)及表没食子儿茶素没食子酸酯(epigallocatechingallate,egcg)。其中egcg含量最高,占儿茶素总量的50%~80%。8种儿茶素类活性成分的分子结构式及egcg-p如图1所示。
由于茶多酚的高水溶性,影响了其在生物体内的利用率。有研究显示取代后的egcg棕榈酸酯(egcg-p)具有更强的抗氧化性。研究人员将茶多酚中的主要成分egcg通过与棕榈酸氯酯化反应制备成脂溶性的egcg-p。
茶多酚含量的检测基本上采用理化分析法、光谱分析法、电化学方法、流动注射化学发光法等,测定的是总酚的含量。对于开发药用级和保健功能的茶多酚,活性成分及异构体的分离检测对茶多酚的功能和应用极为重要。有用hplc分析几种多酚的报道,最近有文献报道了c18核壳粒子填充毛细管柱采用纳米液相色谱法,同时分离分析了几种多酚和甲基黄嘌呤。人们关注的重点是儿茶素类多酚物质的分析分离,而对于茶多酚里是否含有高活性的egcg-p以及egcg-p的提取分析还未有报道。
碳纳米管(cnts)是由碳六元环构成的类石墨平面卷曲而成的纳米级中空管,具有比表面积大、耐酸碱耐热性好等独特的物理化学性质,比c18具有更大的比表面积和更强的吸附能力。然而,cnts表面含有丰富的π电子,存在疏水性较强,易团聚的缺陷。
技术实现要素:
本发明的目的是提供一种改性修饰多壁碳纳米管分散固相萃取/uplc-ms测定egcg棕榈酸酯的方法,用于茶多酚里是否含有高活性的egcg-p以及egcg-p的提取分析。
本发明的技术方案:一种改性修饰多壁碳纳米管分散固相萃取/uplc-ms测定egcg棕榈酸酯的方法,步骤为:
一、磁性碳纳米管制备
(1.1)多壁碳纳米管酸化
取1g外径为10~20nm,纯度97%的多壁碳纳米管mwnts,放入80ml浓硝酸中,60℃回流3.5h;冷却至室温,过滤,用去离子水洗涤至滤液呈中性,于60℃烘干过夜,得到酸化多壁碳纳米管amwnts,干燥器中保存;
(1.2)改性磁性纳米粒子的制备
称取54.0mgfecl3·6h2o,19.8mgfecl2·4h2o,加100ml去离子水,搅拌溶解得溶液a;
(二者摩尔比2/1,fecl3·6h2o分子量270,fecl2·4h2o分子量198二者摩尔比2/1)
称取15.2mg四甲氧基硅烷,22.6mg三甲氧基(2-苯乙基)硅烷,23.4mg辛基三甲氧基硅烷,加100ml含0.01%吐温-100、0.02%十六烷基三甲基溴化铵的10%甲醇水溶液,得溶液b(所述百分浓度均为质量百分浓度,下同);
将溶液a与溶液b混合,加入0.5ml25%nh3水作催化剂,120℃搅拌回流15h;
(1.3)共沉淀法制备改性磁性多壁碳纳米管
在上述(1.2)反应液中加入1g酸化后的amwnts,用5%nh4oh溶液调节ph,使混合液ph>9,氮气保护下,80℃下搅拌反应30min,然后用去离子水反复洗涤直至滤液为中性,60℃过夜烘干,得到fe3o4-sio2-phenylethyl-c8/amwnts磁性多碳纳米管复合物;
二、磁滞回线测定
采用磁强计测量fe3o4-sio2-phenylethyl-c8/amwnts纳米材料的磁学性能,结果见图2,饱和磁化强度为4.85emu/g,具有超顺磁性,能够满足磁分离的要求;
三、富集性能测定
通过计算富集因子ef,比较不同吸附材料对egcg各组分的富集性能,富集因子ef为萃取后的分析物浓度与萃取前分析物浓度的比值;
计算公式为:ef=ca/cb,其中ca为萃取后的分析物浓度,cb为萃取前分析物浓度;图3为fe3o4-sio2-phenylethyl-c8/amwnts复合材料、fe3o4纳米粒子及c18固相萃取柱对9种egcg的富集性能对比。结果显示,fe3o4-sio2-phenylethyl-c8/amwnts对9种egcg的富集因子为fe3o4的2~3.6倍。这是因为碳纳米管具有较大的比表面积,可以为目标物提供更多的吸附位点;并且表面具有丰富的π电子,可与egcg通过π-π键作用。同时修饰后的多壁碳纳米管因含有phenylethyl-c8,与c18相比,对疏水性能不同的化合物具有更高的选择性。通过富集因子评价发现fe3o4-sio2-phenylethyl-c8/amwnts对egcg类似物具有较好的吸附性能;
四、萃取条件优化
(4.1)萃取时间的影响
考察不同萃取时间对萃取性能的影响(见图4),可以看出fe3o4-sio2-phenylethyl-c8/amwnts对9种egcg的吸附在10min内达到平衡,进一步延长萃取时间,峰面积无明显变化;
(4.2)解吸时间的影响
为实现被吸附的目标化合物最大程度地解吸,考察了不同解吸时间对积分面积的影响。结果如图5所示,在10~25min时,9种egcg的峰面积变化不大,故选择解吸时间为10min;通过对萃取及解吸条件优化,确定最佳富集条件为:涡旋震荡速度3000r/min,萃取时间10min,解吸时间10min,制备的改性磁性纳米对9种egcg富集较好;
五、样品制备
将0.5g茶多酚样本用10ml去离子水溶解,取5ml样品溶液放入含10mgfe3o4-sio2-phenylethyl-c8/amwnts纳米材料的离心试管中,置于涡旋震荡器中以3000r/min速度振荡10min,充分萃取后,将磁铁置于离心管管壁收集磁性吸附剂,弃去液体;然后将磁性吸附剂加入100μl85%乙醇超声解吸15min,磁分离后取10μl解吸液进行uplc-ms分析;
六、uplc-ms条件
柱子behc181.7µm2.1×100mm,检测器sqdetctor,梯度洗脱0~10min80/20水/甲醇~40/60水/甲醇;负扫描,0-2000m/z,毛细管电压3kv,锥孔电压30v,脱溶剂气体温度400℃,源气体流速500l/h,锥孔气体流速50l/h,源温度100℃;
七、样品测定
线性范围、检出限及精密度的考察
配制一系列质量浓度μg/l的目标物:c:0.1~10、ec:0.5~50、gc:0.2~50、egc:0.2~20、ecg:0.5~25、cg:5~50、egcg:0.1~25、gcg:2~100、egcg-p:0.5~50的egcg类混合标准溶液,考察fe3o4-sio2-phenylethyl-c8/amwnts与uplc-ms联用分析方法测定9种egcg类的线性范围、相关系数和检出限。
本发明的有益效果:本发明采用低毒、廉价易得的fe3o4作为磁性来源,键合sio2并进行苯乙基-c8修饰多壁碳纳米管(amwnts),制备得到磁性多壁碳纳米管复合材料fe3o4-sio2-phenylethyl-c8/amwnts,具有比表面积大,单分散性好,扩散距离短,只需使用少量的吸附剂和较短的平衡时间就能实现萃取分离。修饰后的多壁碳纳米管对疏水性能不同的化合物具有高度的选择性,分散固相萃取后同时分离了8种茶多酚主要活性成分和egcg-p,并采用uplc-ms进行了鉴别和测定。发现了多酚粗提液中含有具有重要活性的egcg-p,而通常采用离子交换柱制备egcg的过程中忽略并去除了egcg-p。本发明对茶多酚的药理研究和产品开发具有重要的意义,同时具有重要的经济价值。
在磁固相萃取分离过程中,制备对靶物质具有高吸附能力的萃取介质,对目标产物具有高效富集作用至关重要。本发明制备的改性纳米粒子修饰多壁碳纳米管分散固相萃取材料具有很好的磁响应度和分散性,将其用于富集茶多酚提取液中儿茶素类活性物质及egcg-p。与常用的固相萃取方法相比,不必进行固相萃取小柱的清洗活化和平衡,不必进行样品浓缩等步骤,具有操作更简便,萃取效率更高,溶剂消耗量小,分离时间短等优点。
附图说明
图18种儿茶素类活性成分及egcg-p的分子结构式。
图2fe3o4-sio2-phenylethyl-c8/amwnts磁滞回线图。
图3三种吸附材料对9种egcg的富集性能对比,1、fe3o4-sio2-phenylethyl-c8/amwnts复合材料,2、fe3o4纳米粒子,3、c18固相萃取柱。
图4萃取时间对fe3o4-sio2-phenylethyl-c8/amwnts萃取效果的影响
图5解吸时间对fe3o4-sio2-phenylethyl-c8/amwnts萃取效果的影响。
图6混合标准样品色谱图。
图7.195%egcg水溶性色谱图。
图7.295%脂溶性色谱图。
图7.395%tp色谱图。
图7.440%tp色谱图。
图7.520%tp色谱图。
图8.1表儿茶素(epicatechin,ec)质谱图。
图8.2儿茶素(catechin,c)质谱图。
图8.3表儿茶素没食子酸酯(epicatechingallate,ecg)质谱图。
图8.4儿茶素没食子酸酯(catechingallate,cg)质谱图。
图8.5表没食子儿茶素没食子酸酯(epigallocatechingallate,egcg)质谱图。
图8.6没食子儿茶素(gallocatechin,gc)质谱图。
图8.7表没食子儿茶素(epigallocatechin,egc)质谱图。
图8.8没食子儿茶素没食子酸酯(gallocatechingallate,gcg)质谱图。
图8.9egcg棕榈酸酯(egcg-p)质谱图。
具体实施方式
实施例1制备改性磁性多壁碳纳米管
(1.1)多壁碳纳米管酸化
取1g外径为10~20nm,纯度97%的多壁碳纳米管mwnts,放入80ml浓硝酸中,60℃回流3.5h;冷却至室温,过滤,用去离子水洗涤至滤液呈中性,于60℃烘干过夜,得到酸化多壁碳纳米管amwnts,干燥器中保存;
(1.2)改性磁性纳米粒子的制备
称取54.0mgfecl3·6h2o,19.8mgfecl2·4h2o,加100ml去离子水,搅拌溶解得溶液a;
称取15.2mg四甲氧基硅烷,22.6mg三甲氧基(2-苯乙基)硅烷,23.4mg辛基三甲氧基硅烷,加100ml含0.01%吐温-100、0.02%十六烷基三甲基溴化铵的10%甲醇水溶液,得溶液b;
将溶液a与溶液b混合,加入0.5ml25%nh3作催化剂,120℃搅拌回流15h;
(1.3)共沉淀法制备改性磁性多碳纳米管
在上述反应液中加入1g酸化后的amwnts,用5%nh4oh调节ph,使混合液ph>9,氮气保护下,80℃下搅拌反应30min,然后用去离子水反复洗涤直至滤液为中性,60℃过夜烘干,得到fe3o4-sio2-phenylethyl-c8/amwnts磁性多碳纳米管复合物;
实施例2磁滞回线测定
采用磁强计测量fe3o4-sio2-phenylethyl-c8/amwnts纳米材料的磁学性能,结果见图2,饱和磁化强度为4.85emu/g,具有超顺磁性,能够满足磁分离的要求。
实施例3富集性能测定
通过计算富集因子ef,比较不同吸附材料对egcg各组分的富集性能,富集因子ef为萃取后的分析物浓度与萃取前分析物浓度的比值;
计算公式为:ef=ca/cb,其中ca为萃取后的分析物浓度,cb为萃取前分析物浓度;图3为fe3o4-sio2-phenylethyl-c8/amwnts复合材料、fe3o4纳米粒子及c18固相萃取柱对9种egcg的富集性能对比。结果显示,fe3o4-sio2-phenylethyl-c8/amwnts对9种egcg的富集因子为fe3o4的2~3.6倍。这是因为碳纳米管具有较大的比表面积,可以为目标物提供更多的吸附位点;并且表面具有丰富的π电子,可与egcg通过π-π键作用。同时修饰后的多壁碳纳米管因含有phenylethyl-c8,与c18相比,对疏水性能不同的化合物具有更高的选择性。通过富集因子评价发现fe3o4-sio2-phenylethyl-c8/amwnts对egcg类似物具有较好的吸附性能。
实施例4样品测定
(7.1)线性范围、检出限及精密度的考察
配制一系列质量浓度0.1~10(c)、0.5~50(ec)、0.2~50(gc)、0.2~20(egc)、0.5~25(ecg)、5~50(cg)、0.1~25(egcg)、2~100(gcg)、0.5~50(egcg-p)μg/l的egcg类混合标准溶液,考察fe3o4-sio2-phenylethyl-c8/amwnts与uplc-ms联用分析方法测定9种egcg类的线性范围、相关系数和检出限,结果列于表1。混合标准样品色谱图见图6。
表1fe3o4-sio2-phenylethyl-c8/amwnts分散固相萃取-uplc-ms法测定9种egcg的线性关系、检出限及精密度(y为峰面积,x为质量浓度μg/l)
(7.2)样品测定
经提取后的各种茶多酚样品,按上述样品制备方法制备后,进行uplc-ms分析,各产品测定结果见表2,色谱图见图7(1-5)。对应的质谱图见图8(1-9)。在各种级别的茶多酚产品中除20%tp外,均含有egcg-p组分。
表2各种样品含量测定
- 还没有人留言评论。精彩留言会获得点赞!