一种保健品中壳寡糖含量的检测方法与流程
本发明涉及保健品中壳寡糖(聚合度dp=2~7)的定量检测,尤其是保健品中壳寡糖(聚合度dp=2~7)的高效液相色谱串联质谱的快速检测方法。
背景技术:
壳寡糖(chitooligosaccharide)又名低聚葡萄糖胺,是几丁质(chitin,又名甲壳素)脱乙酰得到的产物壳聚糖进一步降解获得的由2~10个氨基葡萄糖以β-1,4键连接而成的低聚糖。研究表明,壳寡糖水溶性良好,易于被人体吸收,具有抗癌、降血糖、降血酯、促进钙的吸收、调节免疫等作用。因此壳寡糖被广泛地应用在医疗保健领域。
当今,市场上保健品的质量良莠不齐,建立保健品中功能性有效成分可行、高效、准确和灵敏的分析方法是保健品市场质量监督管理的需要。目前,壳寡糖含量的检测方法主要分为间接检测法和直接检测法。间接检测法又可分为两种类型,一是将样品中的壳寡糖完全水解成氨基葡萄糖单糖的形式,再进行检测,如分光光度计法和乙酰丙酮法,此类方法既无法检测出每个聚合度的壳寡糖的含量,水解效率又难以保证,准确率不高。二是将样品中各个聚合度的壳寡糖进行衍生化反应后再进行检测,如高效液相色谱串联质谱法,此类方法虽然灵敏度高,但是分析时间长,操作繁琐,不适用于大批量样品的检测。直接检测法是指直接检测不同聚合度的壳寡糖的含量,如高效液相色谱法、离子色谱法等方法,此类方法操作简单快速,但是检测的灵敏度和选择性次于高效液相串联质谱法,在中国海洋大学学报(自然科学版)2002年出版的32卷第4期641-644页中孟显丽等也建立了薄层色谱法来直接分析壳寡糖,但无法准确测定目标物的含量。目前,用高效液相串联质谱法直接检测不同聚合度壳寡糖含量的方法少之又少;经检索未发现利用高效液相串联质谱技术直接检测保健品中不同聚合度壳寡糖含量的检测方法。
技术实现要素:
本发明的目的是提供一种壳寡糖的高效液相色谱串联质谱检测方法,无需衍生反应即可直接检测,其克服现有技术的不足,更直接方便,使检测结果更准确、灵敏。
本发明的目的可通过如下技术方案来实现:
一种保健品中壳聚糖含量的检测方法,包括以下步骤:
(1)制备标准溶液并进行高效液相色谱串联质谱检测
称取壳寡糖标准物并将其配成标准储备液,再将标准储备液用体积比为v乙腈:v水=6:4的乙腈水逐级稀释,配制一系列的标准溶液进行高效液相色谱串联质谱检测并得到标准谱图,标准谱图中保留时间确定壳寡糖品种,色谱面积与对应的壳寡糖浓度成函数关系;
(2)将步骤(1)所得的标准谱图按壳寡糖品种分别制作浓度与色谱峰面积关系曲线图;
(3)保健品样品的预处理及高效液相色谱串联质谱检测
称取样品,加入水,涡旋震荡后超声波提取,离心,取上清液,用乙腈定容,混匀后取上清液过滤膜,取滤液进行高效液相色谱串联质谱检测,得样品谱图;
(4)样品中的壳寡糖的含量的确定;
将步骤(3)中获得的样品谱图的保留时间确定壳寡糖的品种并将其色谱峰面积与步骤(2)对应的壳寡糖品种的标准曲线进行比对,用外标法确定样品中的各种壳寡糖含量;
优化方案是:步骤(1)中不同浓度的标准溶液浓度为壳二糖、壳三糖和壳四糖配制浓度从0.5mg/l至20mg/l分6个等级;壳五糖配制浓度从1.0mg/l至40mg/l分6个等级;壳六糖和壳七糖配制浓度从0mg/l至160mg/l分6个等级;
其中,在步骤(1)和(3)中高效液相色谱串联质谱的实验条件如下:
色谱条件:
(a)色谱柱:acquityuplcbehhilic(1.7μm,2.1×100mm);
进样量:10μl;
(c)柱温:30℃;
(d)流速:0.3ml/min;
(e)流动相和洗脱时间:
流动相a:超纯水(用甲酸调节ph=3),流动相b:200mmol/l乙酸铵水溶液,流动相c:乙腈(用甲酸调节ph=3);
洗脱时间0-3.5min,流动相a保持12%,流动相b保持20%,流动相c保持68%;
洗脱时间3.5-3.6min,流动相a从12%到22%,流动相b保持20%,流动相c从68%到58%;
洗脱时间3.6-6.0min,流动相a保持22%,流动相b保持20%,流动相c保持58%;
洗脱时间6.0-6.1min,流动相a从22%到32%,流动相b保持20%,流动相c从58%到48%;
洗脱时间6.1-9.0min,流动相a保持32%,流动相b保持20%,流动相c保持48%;
洗脱时间9.0-9.1min,流动相a从32%到40%,流动相b保持20%,流动相c从48%到40%;
洗脱时间9.1-11.0min,流动相a保持40%,流动相b保持20%,流动相c保持40%;
洗脱时间11.0-11.1min,流动相a从40%到12%,流动相b保持20%,流动相c从40%到68%;
洗脱时间11.1-15.0min,流动相保持12%,流动相b保持20%,流动相c保持68%;
质谱条件:
(a)电离模式:esi+;
(b)仪器参数:气帘气压力25.0psi,碰撞气压力中档,离子喷雾电压5500v,离子源温度350℃,雾化气压力50.0psi,辅助加热气压力50.0psi,接口加热器为开;
采集模式:多反应监测mrm。
与现有技术对比,本发明具有如下突出的实质性特点和显著进步:
本发明选择特定色谱柱与流动相结合,成功分离六种不同聚合度的壳寡糖,从而实现直接定量检测保健品基质中不同聚合度壳寡糖的基础。
本发明针对保健品中壳寡糖的特点,通过前处理方式和仪器分析的条件的综合优化,开发非衍生前处理的高效液相色谱串联质谱法快速检测壳寡糖含量的方法。该方法前处理简单、快速,分析时间短,灵敏度、准确度和精密度高,满足保健品中壳寡糖的检测要求。
附图说明
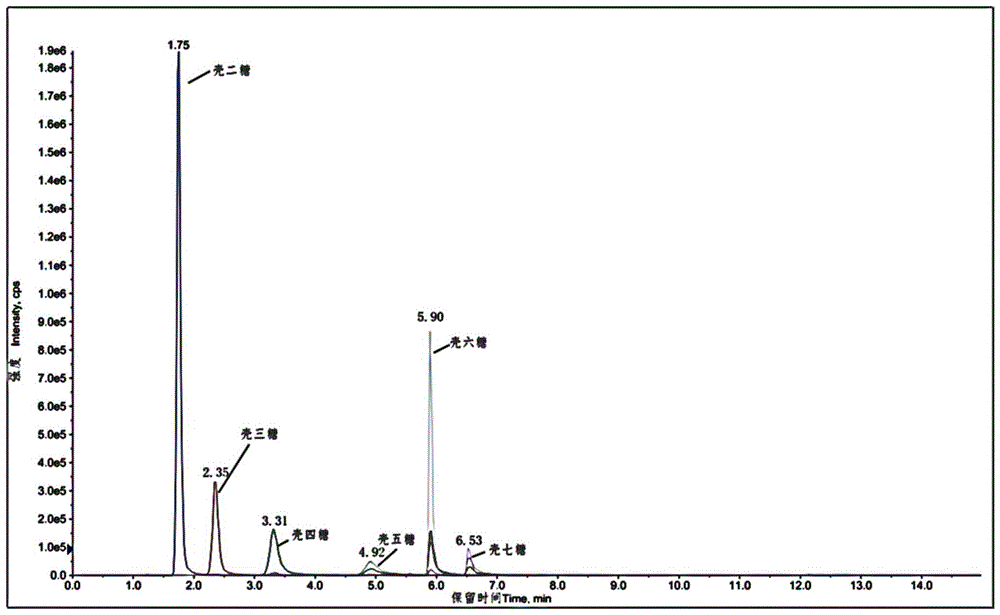
图1为6种壳寡糖标准溶液混标的mrm谱图(壳二糖、壳三糖和壳四糖8mg/l;壳五糖16mg/l;壳六糖和壳七糖160mg/l。
具体实施方案
下面通过实例对本发明做进一步的描述,这些描述并不是对本发明内容进一步的限定。本领域的技术人员应理解,对本发明内容所做的等同替换或相应的改进,仍属于本发明的保护范围之内。
一种保健品中壳聚糖含量的高效液相色谱串联质谱检测方法,其具体实施步骤如下:
1.制备标准溶液并进行高效液相色谱串联质谱检测
分别准确称取6种壳寡糖标准品10.00mg,用超纯水溶解并定容在10ml容量瓶中,配制成1000mg/l的壳寡糖标准储备液,标准储备液置于4℃冰箱中保存。
取上述的标准储备液,用体积比为v乙腈:v水=6:4的乙腈水逐级稀释,壳二糖、壳三糖和壳四糖配制浓度为0.5mg/l、1.0mg/l、2.0mg/l、5.0mg/l、8.0mg/l、20mg/l的标准系列溶液;壳五糖配制浓度为1.0mg/l、2.0mg/l、4.0mg/l、10mg/l、16mg/l、40mg/l的标准系列溶液;壳六糖和壳七糖配制浓度为0mg/l、10mg/l、20mg/l、40mg/l、100mg/l、160mg/l的标准系列溶液。
将不同浓度的标准溶液进行高效液相色谱串联质谱检测并得到标准图谱,即得到壳二糖、壳三糖和壳四糖浓度为0.5mg/l、1.0mg/l、2.0mg/l、5.0mg/l、8.0mg/l、20mg/l;壳五糖浓度为1.0mg/l、2.0mg/l、4.0mg/l、10mg/l、16mg/l、40mg/l;壳六糖和壳七糖浓度为0mg/l、10mg/l、20mg/l、40mg/l、100mg/l、160mg/l的标准溶液的保留时间与响应值之间对应的标准曲线图,保留时间确定壳寡糖种类,由响应值确定的色谱峰面积与对应的壳寡糖浓度成函数关系。
2.将步骤1所得的标准谱图按壳寡糖品种分别制作浓度与色谱峰面积关系曲线图;
壳寡糖(dp=2~7)的方法检出限、定量限、线性范围、线性方程和相关系数如表1所示
表1壳寡糖(dp=2~7)的方法检出限、定量限、线性范围、线性方程和相关系数
3.保健品样品进行预处理及高效液相色谱串联质谱检测
准确称取粉碎后的保健品样品1.00g于50ml离心管中,加入10ml水涡旋震荡超声提取,8000r/min转速下离心5min,精密移取4ml上清液于10ml容量瓶中,用乙腈定容至10ml。涡旋混匀后,过0.22μm滤膜至进样瓶中,进行高效液相色谱串联质谱检测。
4.检测结果
本发明对市面上随机购买的两个标示添加了壳寡糖的保健品进行检测,结果显示片剂保健品1,壳六糖和壳七糖未检出,检出壳二糖、壳三糖、壳四糖、壳五糖,含量分别为682.5mg/kg、3350mg/kg、710mg/kg、173.4mg/kg;胶囊保健品2,六种壳寡糖均有检出,壳二糖、壳三糖、壳四糖、壳五糖、壳六糖和壳七糖的含量分别为3025mg/kg、12137.5mg/kg、7450mg/kg、4662.5mg/kg、3256.2mg/kg、210.5mg/kg。
本发明片剂保健品样品中对壳寡糖按上述实验步骤进行加标回收实验,每个目标物设计三个添加水平,每个水平分别做6次重复实验。其中壳二糖、壳三糖和壳四糖的添加水平为25mg/kg、50mg/kg、100mg/kg;壳五糖的添加水平为50mg/kg、100mg/kg、200mg/kg;壳六糖与壳七糖的添加水平为400mg/kg、800mg/kg、1000mg/kg,结果如表2所示:
表2片剂保健品中壳寡糖平均回收率和精密度数据表(n=6)
步骤1和2中,高效液相色谱串联质谱的实验条件如下:
色谱条件:
(a)色谱柱:acquityuplcbehhilic(1.7μm,2.1×100mm);
进样量:10μl;
(c)柱温:30℃;
(d)流速:0.3ml/min;
(e)流动相和洗脱时间:
流动相a:超纯水(用甲酸调节ph=3),流动相b:200mmol/l乙酸铵水溶液,流动相c:乙腈(用甲酸调节ph=3);
洗脱时间0-3.5min,流动相a保持12%,流动相b保持20%,流动相c保持68%;
洗脱时间3.5-3.6min,流动相a从12%到22%,流动相b保持20%,流动相c从68%到58%;
洗脱时间3.6-6.0min,流动相a保持22%,流动相b保持20%,流动相c保持58%;
洗脱时间6.0-6.1min,流动相a从22%到32%,流动相b保持20%,流动相c从58%到48%;
洗脱时间6.1-9.0min,流动相a保持32%,流动相b保持20%,流动相c保持48%;
洗脱时间9.0-9.1min,流动相a从32%到40%,流动相b保持20%,流动相c从48%到40%;
洗脱时间9.1-11.0min,流动相a保持40%,流动相b保持20%,流动相c保持40%;
洗脱时间11.0-11.1min,流动相a从40%到12%,流动相b保持20%,流动相c从40%到68%;
洗脱时间11.1-15.0min,流动相保持12%,流动相b保持20%,流动相c保持68%;
质谱条件:
(a)电离模式:esi+;
(b)仪器参数:气帘气压力25.0psi,碰撞气压力中档,离子喷雾电压5500v,离子源温度350℃,雾化气压力50.0psi,辅助加热气压力50.0psi,接口加热器为开;
(c)采集模式:多反应监测mrm。
表3六种壳寡糖的保留时间与定量离子对、定性离子对、去簇电压、碰撞电压
- 还没有人留言评论。精彩留言会获得点赞!