一种检测没食子酸丙酯及甲醛的方法
本发明涉及化学分析检测技术领域,具体为一种同时检测没食子酸丙酯及甲醛的方法。
背景技术:
没食子酸丙酯(pg)亦称掊酸丙酯,是食品工业中常用的抗氧化剂,我国gb2760-2014《食品安全国家标准食品添加剂使用标准》规定:pg用于含油脂食品中最大使用量为0.1g/kg(以油脂中的含量计)。研究表明,过量使用pg会对人体健康造成危害,如导致肾脏受损或引起接触性皮炎等。pg常见的检测方法有比色法、液相色谱法、气相色谱法、液质联用法等,比色法由于操作简单、快速、不需要大型仪器设备,而被常采用,但由于特性差、检测干扰严重,成为检测中需要解决的难题。
纳米酶是一类既有纳米材料的独特性能,又有催化功能的模拟酶。单原子催化剂(sacs)是指孤立金属原子稳定在合适载体上的催化剂,sacs中单原子与载体界面结合产生的强金属-支撑相互作用能够有效阻止单原子迁移和聚集,并促进低配位环境和电荷转移效应,同时充分暴露的活性原子中心使其具有更高的催化活性。单原子纳米酶(san-atomnanozymes,sans)是在此基础上发展起来的一种新型纳米酶,其优异的酶活是因为sacs在催化反应中具有最大的原子利用效率(~100%),同时支撑底物的良好配位结构可为机理研究提供明确的实验模型。现有报道金纳米粒子荧光增强测定食用油中pg,由于同类合成酚类抗氧化剂,如bha、bht、tbhq对pg有一定干扰,检测方法的选择性至关重要。由于单原子纳米酶优异的催化活性,本发明合成了锌基单原子纳米酶,以pg为酶反应底物,进行pg比色检测,具有特异性,而利用甲醛对酶催化反应的抑制,同时建立检测甲醛新方法,相关研究未见报道。
技术实现要素:
本发明公开了一种检测没食子酸丙酯及甲醛的方法,该方法通过盐模板法合成了锌基单原子纳米酶(zn-n-c),基于zn-n-c的与天然金属酶的活性中心具有相似的电子和几何结构,表现出的强模拟过氧化酶活性,能够快速氧化底物没食子酸丙酯(pg)为黄色氧化型醌类物质,而甲醛会抑制该催化氧化反应,从而建立了pg及甲醛的快速检测方法,定量检出限分别为1.25mg/kg及5mg/kg;将本方法应用于食品中pg及甲醛的检测分析,结果与gb5009.32-2016食品安全国家标准食品中9种抗氧化剂测定及gb/t5009.49食品中甲醛的测定的方法相符;本发明方法只能选择性快速氧化pg,而其他抗氧化剂反应速度较慢,方法具有灵敏度高、特异性强、操作简单、快速等特点。
本发明快速检测食品中没食子酸丙酯及甲醛的方法如下:
(1)没食子酸丙酯工作曲线制作
在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶100µl、50mmol/lh2o2100µl及浓度在1.25~200mg/kg范围内的没食子酸丙酯标准溶液,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置5~10min,在316nm波长处,测定吸光度a,以没食子酸丙酯浓度为横坐标,吸光度a为纵坐标,绘制标准曲线,得到回归方程;
(2)甲醛工作曲线制作
在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶100µl、50mmol/lh2o2100µl、0.1mmol/l没食子酸丙酯500µl及浓度在5~250mg/kg范围内的甲醛标准溶液,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置5~10min,在316nm波长处,测定吸光度a,以甲醛浓度为横坐标,吸光度a为纵坐标,绘制标准曲线,得到回归方程;
(3)没食子酸丙酯测定的样品处理
(4)甲醛测定的样品处理:称取5~10g固体试样或吸取25ml液体试样,置于500ml水蒸气蒸馏瓶中,加入10.0ml去离子水和10.0ml体积浓度8~12%的磷酸溶液,在水蒸气蒸馏装置中蒸馏,收集馏出液于200ml容量瓶中,加去离子水定容至刻度,得待测样品液;
(5)没食子酸丙酯样品测定:在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶100µl、50mmol/lh2o2100µl、步骤(3)的待测样品液,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置5~10min,在316nm波长处,测定吸光度a,代入步骤(1)回归方程,计算样品中没食子酸丙酯的含量;
(6)甲醛样品测定:在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶100µl、50mmol/lh2o2100µl、0.1mmol/l没食子酸丙酯500µl、步骤(4)的待测样品液,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置5~10min,在316nm波长处,测定吸光度a,代入步骤(2)回归方程,计算样品中甲醛的含量。
锌基单原子纳米酶的制备方法如下:将0.7~1.0g醋酸锌、20ml甲醇与50g氯化钾搅拌混匀后,放置在80℃下真空干燥24~48h,将干燥后固体与0.3~0.5g2-甲基咪唑、15~25ml甲醇混匀后,放置在80℃下真空干燥24~48h除去甲醇,得到的固体颗粒置于管式炉中,在氮气保护下700~800℃煅烧2~3h,得到的固体用纯水洗涤,得到不溶于水的黑色小颗粒,即为锌基单原子纳米酶zn-n-c。
本发明的优点在于:
1、本发明锌基单原子纳米酶,由于其优越的强模拟过氧化酶活性,选择性催化氧化没食子酸丙酯(pg)为黄色氧化型醌类物质,甲醛会抑制该氧化反应,基于pg浓度与黄色氧化pg的线性关系,及甲醛对催化氧化的抑制线性关系,建立快速、选择性强pg及甲醛检测新方法;
2、本发明建立的催化氧化体系对pg有催化氧化速度快,在5min以内完成氧化反应,而其他类似结构及性质的合成酚类抗氧化剂要么无此氧化反应,要么反应速度慢,至少50min以上,该反应体系具有反应快速、灵敏、稳定的特点;
3、本发明建立的方法用于食品中pg及甲醛检测,具有检测可靠、简便、快速的特点,与相关国标方法比较,具有检测结果一致性。
附图说明
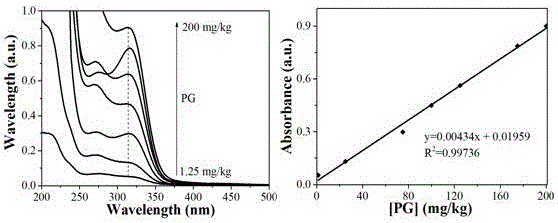
图1为实施例1中zn-n-c氧化pg线性紫外-可见吸收光谱(左图)及回归方程(右图);
图2为实施例1中甲醛抑制zn-n-c氧化pg线性紫外-可见吸收光谱(右图)及回归方程(左图);
图3为共存共存离子对pg的影响结果,图中pg代表单独使用,mixture是pg与所有离子的混合物,其它为与pg共存的离子;
图4为共存抗氧化剂对pg的影响结果,图中pg代表单独使用,mixture是pg与所有抗氧化剂的混合物,其它为与pg共存的抗氧化剂。
具体实施方式
下面将结合具体的实施例对本发明的技术方案作进一步详细地描述说明,但本发明的保护范围并不仅限于此。
实施例1:大豆油样品中pg及干银耳中甲醛的测定
1、锌基单原子纳米酶zn-n-c的制备:将0.7g醋酸锌、20ml甲醇与50g氯化钾搅拌混匀后,放置真空干燥箱,80℃下干燥24h,将干燥后固体与0.4g2-甲基咪唑、20ml甲醇混匀后,放置真空干燥箱,80℃干燥48h除去甲醇,得到的固体颗粒置于管式炉中,在氮气保护下750℃煅烧2h,得到的固体用纯水洗涤,得到不溶于水的黑色小颗粒,即为zn-n-c;
2、没食子酸丙酯工作曲线制作:在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶(zn-n-c)100µl、50mmol/lh2o2100µl及浓度在1.25~200mg/kg范围内的没食子酸丙酯标准溶液,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置8min,在316nm波长处,测定吸光度a,以没食子酸丙酯浓度为横坐标,吸光度a为纵坐标,绘制标准曲线,得到回归方程,见图1;回归方程、相关系数、相对标准偏差、线性范围等见表1;
3、甲醛工作曲线制作:在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶(zn-n-c)100µl、50mmol/lh2o2100µl、0.1mmol/l没食子酸丙酯500µl及浓度在5~250mg/kg范围内的甲醛标准溶液,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置8min,在316nm波长处,测定吸光度a,以甲醛浓度为横坐标,吸光度a为纵坐标,绘制标准曲线,得到回归方程,见图2;回归方程、相关系数、相对标准偏差、线性范围等见表1;
表1线性方程、相关系数、相对标准偏差、线性范围
4、方法特异性考察:将pg和其他抗氧化剂、离子混合作为混合抗氧化剂,检测共存抗氧化剂和共存离子在上述检测体系中对pg的影响,pg浓度为10mg/kg,图3为共存离子(na+、k+、mg2+、cu2+、zn2+、fe2+、cl-、so42-、no3-等)对pg的影响结果,以上干扰物质浓度为50mg/kg,图4是共存抗氧化剂(特丁基对苯二酚tbhq)、2,4,5-三羟基苯丁酮(thbp)、去甲二氢愈创木酸(ndga)、叔丁基对羟基茴香醚(bha)、2,6-二叔丁基-4-羟甲基苯酚(ionox-100)、没食子酸辛酯(og)、2,6-二叔丁基对甲基苯酚(bht)、没食子酸十二酯(dg))及葡萄糖、麦芽糖、蔗糖、淀粉和抗坏血酸对pg的影响结果,从图中可以看出,zn-n-c体系氧化pg有较好的选择特异性,仅有pg有明显的氧化反应,其它物质几乎没有,方法具有好的选择特异性。
5、大豆调和油样品中pg的测定
(1)样品处理:准确称取大豆调和油2g于25ml比色管中,加入6ml体积浓度95%的乙醇溶液,涡旋1min充分混匀,静置片刻,于90℃水浴中加热10s促使其分层;将上层清液用吸管转移到浓缩瓶中,再用6ml95%乙醇溶液重复提取2次,合并提取液并定容到25ml,得待测样品液;
(2)样品测定:在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶(zn-n-c)100µl、50mmol/lh2o2100µl、步骤5(1)的待测样品液4ml,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置8min,在316nm波长处,测定吸光度a,代入步骤2回归方程,计算样品pg含量为4.35mg/kg;
(3)回收率与精密度实验:在大豆调和油样品中分别添加2个不同浓度的pg标准溶液;每个浓度平行测定3次,计算加标回收率,并计算出相对标准偏差rsd,结果见表2,测得pg的加标回收率在97.3%~102.6%,rsd在1.4%~2.1%,本方法有好的准确性和精密度。
表2样品加标回收率及rsd(n=3)
6、干银耳中甲醛测定
(1)样品处理:称取10g粉碎后干银耳试样,置于500ml水蒸气蒸馏瓶中,加入10.0ml去离子水和10.0ml10%的磷酸溶液,接水蒸气蒸馏装置蒸馏,收集馏出液于200ml容量瓶中,加去离子水定容至刻度,得样品液;
(2)样品测定:在10ml具塞比色管中加入0.1mg/ml锌基单原子纳米酶(zn-n-c)100µl、50mmol/lh2o2100µl、0.1mmol/l没食子酸丙酯500µl、步骤6(1)的待测样品液4ml,用ph7.4的柠檬酸-磷酸氢二钠缓冲溶液稀释至刻度,摇匀,静置8min,在316nm波长处,测定吸光度a,代入步骤3回归方程,计算样品中甲醛的含量为15.23mg/kg。
实施例2:调和油样品中pg及凤爪中甲醛的测定
1、zn-n-c制备:同实施例1;
2、没食子酸丙酯工作曲线制作:同实施例1;
3、甲醛工作曲线制作:同实施例1;
4、调和油样品中pg的测定
(1)样品处理:准确称取调和油2g于25ml比色管中,加入7ml体积浓度95%的乙醇溶液,涡旋1min充分混匀,静置片刻,于85℃水浴中加热15s促使其分层;将上层清液用吸管转移到浓缩瓶中,再用7ml95%乙醇溶液重复提取2次,合并提取液并定容到25ml,得待测样品液;
(2)样品测定:同实施例1,调和油样品中pg的含量为11.21mg/kg。
5、凤爪中甲醛的测定
(1)样品处理:称取9g粉碎后凤爪试样,置于500ml水蒸气蒸馏瓶中,加入10.0ml去离子水和10.0ml11%的磷酸溶液,接水蒸气蒸馏装置蒸馏,收集馏出液于200ml容量瓶中,加去离子水定容至刻度,得样品液
(2)样品测定:凤爪中甲醛的58.90mg/kg。
实施例3:曲奇饼干中pg及手撕面包中甲醛的测定
1、zn-n-c制备:将1g醋酸锌、20ml甲醇与50g氯化钾搅拌混匀后,放置在80℃下真空干燥30h,将干燥后固体与0.3g2-甲基咪唑、23ml甲醇混匀后,放置在80℃下真空干燥30h除去甲醇,得到的固体颗粒置于管式炉中,在氮气保护下800℃煅烧2h,得到的固体用纯水洗涤,得到不溶于水的黑色小颗粒,即为锌基单原子纳米酶zn-n-c;
2、没食子酸丙酯工作曲线制作:同实施例1。
3、甲醛工作曲线制作:同实施例1;
4、曲奇饼干中pg的测定
(1)样品处理:称取5.00g粉粹均匀的饼干样品于100ml锥形瓶中,加入8ml无水乙醇,旋涡混合1min后超声提取15min,静置分层,吸取上清液于50ml离心管中,残余物每次用8ml无水乙醇提取2次;合并上清液于50ml离心管中加入1g中性氧化铝,漩涡震荡1min,3000r/min离心8min,移取上清液于25ml容量瓶中,用无水乙醇定容,摇匀,得待测样品液;
(2)样品测定:同实施例1,调和油样品中pg的含量为5.01mg/kg。
5、手撕面包中甲醛的测定
(1)样品处理:同实施例1;
(2)样品测定:手撕面包中甲醛未检出。
实施例4:方便面中pg及啤酒中甲醛的测定
1、zn-n-c制备:同实施例1;
2、没食子酸丙酯工作曲线制作:同实施例1;
3、甲醛工作曲线制作:同实施例1;
4、方便面中pg的测定:
(1)样品处理:称取5.00g粉粹均匀的方便面样品于100ml锥形瓶中,加入9ml无水乙醇,旋涡混合1.5min后超声提取20min,静置分层,吸取上清液于50ml离心管中,残余物每次用9ml无水乙醇提取2次;合并上清液于50ml离心管中加入1g中性氧化铝,漩涡震荡2min,3000r/min离心10min,移取上清液于25ml容量瓶中,用无水乙醇定容,摇匀,得待测样品液;
(2)样品测定:同实施例1,方便面中pg的含量为2.20mg/kg。
5、啤酒中甲醛的测定
(1)样品处理:吸取25ml啤酒样品,置于500ml水蒸气蒸馏瓶中,加入10.0ml去离子水和10.0ml10%的磷酸溶液,接水蒸气蒸馏装置蒸馏,收集馏出液于200ml容量瓶中,加去离子水定容至刻度;
(2)样品测定:啤酒中甲醛未检出。
将实施例1-4用本发明方法与国家标准gb5009.32-2016食品安全国家标准食品中9种抗氧化剂的测定方法及gb/t5009.49食品中甲醛的测定的方法进行比对,结果见表3;从结果可以看出,两种方法结果一致;
表3上述方法比对结果pg/hcho值(mg/kg)
本发明建立的pg及hcho测定法具有处理步骤少,快速、简便,不需要gb5009.32-2016样品净化处理,所用时间短,处理成本低,操作简便,不需要大型仪器设备,在实际检测中具有较强优势。
- 还没有人留言评论。精彩留言会获得点赞!