对解剖结构的基于模型的分割的制作方法
本发明涉及一种用于在医学图像中执行对解剖结构的基于模型的分割的系统和方法。本发明还涉及包括所述系统的工作站和成像装置,并且涉及包括用于令处理器系统执行所述方法的指令的计算机程序产品。
背景技术:
对医学图像中的各种解剖结构的鲁棒自动分割是在改进临床工作流程中的关键使能器。此处,术语分割是指通过例如对解剖结构的边界的描绘、通过对由边界包围的体素进行标记等而对医学图像中的解剖结构的识别。一旦已经执行这样的分割,就能够提取临床参数,诸如,在例如心脏结构的情况下,心室质量、射血分数以及壁厚度。当交叠在医学图像上面或者以其他方式应用到医学图像时,分割还可以提供医学图像中的解剖结构的标注。
已知手动地分割医学图像中的解剖结构。例如,用户可以使用图形用户接口来勾画医学图像中的解剖结构的边界。不利地,这样的人工分割是耗时的,并且因此繁琐的活动,并且最终倾于错误。
还已知使用模型来自动地分割医学图像中的解剖结构。这种类型的分割也被称为基于模型的分割。可以由模型数据来定义模型。模型数据可以定义解剖结构的几何结构,例如以三角网格或(密集采样的)点云的形式。可以通过将仿射变换分配到网格的每个部分来对患者间和疾病阶段间形状变化进行建模。仿射变换覆盖平移、旋转、沿不同坐标轴的缩放以及剪切。可以通过对在模型的不同部分之间的过渡处的仿射变换的内插来维持网格规律性。这样的仿射变换通常用作所谓的“可变形”模型中的分量。
模型到医学图像的图像数据的拟合可以涉及适应技术,在基于网格的模型的情况下也被称为“网格适应”。这样的应用因此也被称为“适应”。适应技术可以优化基于外部能量项和内部能量项的能量函数,所述外部能量项使模型适应于图像数据,所述内部能量项维持模型的刚度。
上述类型以及其他类似的模型本身是已知的,将这样的模型应用于医学图像的各种适应技术同样也是已知的。
例如,o.ecabert等人的题为“automaticmodel-basedsegmentationoftheheartinctimages”(ieeetransactionsonmedicalimaging2008,27(9),第1189-1201页)的出版物描述了一种用于从三维(3d)计算机断层摄影(ct)图像对心脏的自动分割的基于模型的方式。
技术实现要素:
自动分割算法有时会产生错误的分割结果。具体地,如果不同的模型可用于分割解剖结构,则自动算法可能会在模型的选择中出错。这样一来,分割结果可能是次优的,并且因此在各种应用中具有有限的价值或没有价值,包括但不限于临床参数的提取,用作图像标注,在基于训练模型的分割中用作金标准数据等
具有解决上述缺陷中的一个或多个的用于对解剖结构进行分割的系统或方法将是有利的。
本发明的以下方面涉及用户在医学图像的视图中交互地指定解剖结构的边界点的限制的集合。边界点的集合本身可以被认为是医学图像中的解剖结构的不充分的分割,而是用于从多个不同的分割模型中选择分割模型。选择基于边界点和分割模型中的每个之间的拟合优度量度。例如,可以选择最佳拟合模型并将其用于解剖结构的分割。
本发明的第一方面提供了一种用于对解剖结构进行分割的系统,包括:
-图像数据接口,其用于访问表示医学图像的图像数据,所述医学图像包括要分割的解剖结构;
-模型数据接口,其用于访问定义用于分割解剖结构的多个模型的模型数据,其中,所述多个模型中的每个至少部分地可表示为坐标系中的坐标的集合;以及
-用户交互子系统,其包括:
i)显示输出部,其用于在显示器上显示医学图像的视图,以及
ii)用户设备输入部,其用于从用户可操作的用户设备接收输入命令,
其中,所述用户交互子系统被配置用于使得所述用户能够在所述视图中指示所述解剖结构的边界点的集合,从而获得与视图相关联的坐标系中的坐标的集合;
-处理器,其用于通过以下操作选择用于分割医学图像中的解剖结构的多个模型中的一个或多个:
j)基于相应坐标的比较来确定边界点的集合与多个模型中的每个之间的拟合优度,从而获得多个拟合优度量度,并且
jj)基于所述多个拟合优度量度来选择所述多个模型中的一个或多个,从而获得一个或多个选定的模型。
本发明的另一方面提供了一种包括所述系统的工作站或成像装置。
本发明的另一方面提供了一种用于对解剖结构进行分割的方法,包括:
-访问表示医学图像的图像数据,所述医学图像包括要分割的解剖结构;
-访问定义用于分割解剖结构的多个模型的模型数据,其中,所述多个模型中的每个至少部分地可表示为坐标系中的坐标的集合;并且
-使用用户交互子系统,使得用户能够在医学图像的视图中指示解剖结构的边界点的集合,从而获得与视图相关联的坐标系中的坐标的集合;
-通过以下操作来选择用于分割医学图像中的解剖结构的多个模型中的一个或多个:
j)基于相应坐标的比较来确定所述边界点的集合与所述多个模型中的每个之间的拟合优度,从而获得多个拟合优度量度,并且
jj)基于所述多个拟合优度量度来选择所述多个模型中的一个或多个,从而获得一个或多个选定的模型。
本发明的另一方面提供一种包括用于令处理器系统执行所述方法的指令的计算机程序产品。
以上措施涉及获得医学图像。医学图像可以从各种成像模态获得,包括但不限于超声、计算机断层摄影(ct)、磁共振(mr)成像等。此外,提供了定义用于分割解剖结构的多个模型的模型数据。模型可以定义与医学图像中所示的相同类型的解剖结构。解剖结构可以是例如器官、器官系统、器官的特定部分等。这样一来,模型可以被布置用于分割心脏室、脑室等。然而,也可以存在用于不同的解剖结构的模型。模型可以采取各种形式,包括但不限于网格模型、点云模型等。
使得用户能够在视图中交互地指定解剖结构的边界点的集合。这样的集合可以是限制的集合,因为其可能不能在视图中提供解剖结构的完整描绘。此外,该视图可以仅示出解剖结构的整个边界的部分。这样一来,边界点的集合本身可以被认为是医学图像中的解剖结构的不充分的分割。然而,边界点的集合用于选择用于分割解剖结构的至少一个模型。选择基于以下:在用户指示的边界点和模型中的每个之间计算拟合优度量度,并且基于拟合优度的比较来选择至少一个模型。例如,可以选择提供最佳拟合优度的一个或多个模型。拟合优度量度基于相应坐标的比较,涉及特定模型的坐标与边界点的集合的坐标的比较。这样的比较可以指示特定模型多么好地几何拟合该边界点的集合,然后可以将其表达为拟合优度量度。
上述措施的效果是,通过在医学图像的视图中指示解剖结构的边界点的限制的集合,用户可以使得模型被选择用于分割整个解剖结构。因此,用户不需要描绘整个解剖结构,这将是耗时的并且最终是容易出错的,也不需要分割算法自主地选择可能产生错误选择的分割模型。有效地,用户的参与是限制的,其中,他/她仅需要提供不能用于分割本身而是用于选择用于解剖结构的分割模型的边界点的限制的集合。通过仅需要这样限制的努力,避免了用户经历分割耗时。具体地,用户仅在医学图像的有限视图中(例如在一个或多个切片中)指示边界点就足够了,从而仅产生边界点的2d或有限的3d集合。发明人已经认识到,通过合适的拟合优度量度,边界点的这样的有限的集合仍然可以有效地匹配到例如3d模型。
任选地,处理器被配置用于将一个或多个选定的模型拟合到医学图像中的解剖结构,从而获得一个或多个拟合的模型。因此,一个或多个选定的模型被拟合到医学图像中的解剖结构,从而提供解剖结构的分割或标注。注意,拟合可以基于用户指示的边界点,例如通过使用边界点作为模型和医学图像之间的配准中的目标点。
任选地,处理器被配置用于当选择和拟合多个模型时,识别多个拟合的模型之间的几何变化的区域,并且用户交互子系统被配置用于向用户提供关于几何变化的区域的位置的视觉反馈。所要求保护的本发明的该方面涉及以下内容。用户初始指示的边界点的集合可以产生多个模型的选择。例如,若干模型的拟合优度的绝对水平和/或相对差异可能不足以仅选择一个模型。因此,多个模型可以被选择并拟合到医学图像。在拟合之后,可以存在模型一致的区域,例如通过几何重合。然而,也能够存在模型不一致的区域,其中,多个拟合的模型之间可能存在几何变化。这样的几何变化可以指示模型中的一个或多个可能错拟合。通过向用户提供关于几何变化区域的位置的视觉反馈,用户可以考虑该信息。
任选地,用户交互子系统被配置用于使得用户能够基于视觉反馈来调节边界点的集合,从边界点的集合删除边界点和/或向边界点的集合添加边界点,从而获得经调节的边界点的集合,并且处理器被配置用于基于经调节的边界点的集合来重新选择多个模型中的一个或多个。用户可以基于关于几何变化的区域的位置的视觉反馈来修改初始的边界点的集合,例如通过添加、删除或更准确地将边界点放置在几何变化的区域中。这可以使得能够重新选择更好地匹配特定区域的一个或多个模型,从而在多个模型的选择和拟合的情况下,产生较少的几何变化。
任选地,用户交互子系统被配置为当向用户提供关于几何变化的区域的位置的视觉反馈时,显示表示医学图像中几何变化的区域的位置的医学图像的另一视图。在医学图像的初始视图中,几何变化的区域可能不可见或仅次优地可见。通过显示更好地示出该区域的医学图像的另外的视图,向用户提供改进的视觉反馈。有利地,当修改边界点的集合时,用户不限于初始视图,而是可以将边界点添加到另外的视图中,或者将边界点移向另外的视图。
任选地,处理器被配置用于基于超过拟合优度阈值的相应拟合优度量度来选择多个模型中的一个或多个。因此,选择是基于拟合优度量度的阈值化的。
任选地,处理器被配置用于当确定拟合优度时,确定边界点的集合与多个模型中的每个之间的刚性变换。通过确定边界点的集合和多个模型中的每个之间的刚性变换,可以将模型中的每个与用户指示的边界点对准,从而与医学图像中的解剖结构对准。由于边界点被认为是可靠的,由用户指定并且仅在限制的数量中,它们可以用作与医学图像的配准中的可靠的目标点。确定刚性变换可以涉及最小化该边界点的集合与多个模型中的每个之间的距离量度。然后,拟合优度量度可以被定义为表示在刚性变换之后边界点和每个模型之间保持的距离的距离量度。
任选地,处理器被配置为基于相应刚性变换将一个或多个选定的模型应用于医学图像中的解剖结构。刚性变换可以用于将模型应用于解剖结构医学图像,因为其使模型与边界点对齐。
任选地,医学图像是3d医学图像,视图是3d医学图像的2d表示,并且多个模型是3d模型。因此,使得用户能够在一个或多个2d视图中指定边界点,而不必在3d中指定边界点。这使得指定边界点较不耗时。
任选地,多个模型中的每个至少部分地由表面网格表示。
任选地,处理器被配置为基于所述边界点的集合与多中的个模型每个的相应表面网格的点对面匹配来确定拟合优度。在计算机视觉和计算机图形学领域本身已知点对面匹配,也称为点到面配准,并且其可以有利地用于确定每个模型的拟合优度。
任选地,用户交互子系统被配置为使得用户能够使用一个或多个拟合的模型来标注医学图像。
本领域技术人员将认识到,可以用任何认为有用的方式来组合本发明的上述实施例、实施方式和/或各方面中的两个或更多个。
对成像装置、工作站、方法和/或计算机程序产品的修改和变型(其对应于系统的所描述的修改和变型)能够由本领域技术人员基于本说明书来执行。
本领域技术人员将认识到,所述方法可以被应用于多维图像数据,例如应用于二维(2d)、三维(3d)或四维(4d)图像,所述图像是通过各种采集模态采集的,诸如,但不限于,标准x射线成像、计算机断层摄影(ct)、磁共振成像(mri)、超声(us)、正电子发射断层摄影(pet)、单光子发射计算机断层摄影(spect)和核医学(nm)。
附图说明
参考下文描述的实施例,本发明的这些和其他方面将显而易见并得到阐述。在附图中:
图1示出了用于基于用户指示的边界点的限制的集合对解剖结构进行分割的方法;
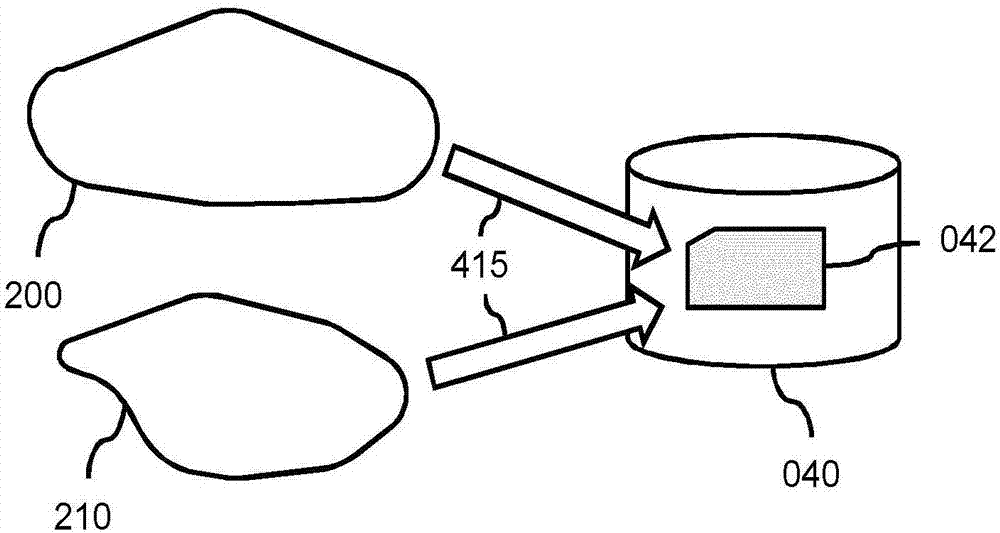
图2图示了被存储为数据库中的模型数据的多个模型;
图3图示了用户使用用户交互系统来指示医学图像的视图中的解剖结构的边界点的集合;
图4图示了在由用户指示的边界点的集合与来自数据库的第一模型之间确定的拟合优度;
图5图示了在由用户指示的边界点的集合与来自数据库的第二模型之间确定的拟合优度;
图6示出了基于用户指示的边界点的限制的集合对解剖结构进行分割的方法;
图7示出了包括用于令处理器系统执行方法的指令的计算机可读介质。
应当注意,在不同图中具有相同附图标记的项目具有相同结构特征和相同功能,或是相同信号。在这样的项目的功能和/或结构已经被解释的情况下,在详细描述中没有对其重复解释的必要。
附图标记列表
为了便于解释附图而提供以下附图标记清单,不应被解释为限制权利要求。
020图像存储库
022医学图像的图像数据
024医学图像的视图
030解剖结构
040模型数据库
042模型数据
060显示器
062显示数据
080用户设备
082输入命令
100用于解剖结构的分割的系统
120图像数据接口
140模型数据接口
160处理器
162去往/来自用户交互子系统的通信
180用户交互子系统
182显示输出部
184用户设备输入部
200第一模型
210第二模型
300用户指示的边界点
302、304被标记为关键点的边界点
400用于结构的分割的方法
410访问图像数据
415数据库中的模型的存储
420访问模型数据
430获得用户指示的边界点
440确定模型的拟合优度
450基于拟合优度选择模型
460计算机可读介质
470被存储为非暂态数据的指令
具体实施方式
图1示出了用于基于用户指示的边界点的限制的集合来对医学图像中的解剖结构进行分割的系统100。这样的系统可以用在各种医学应用中,包括但不限于图像标注。系统100实质上涉及用户在医学图像的视图中交互地指定解剖结构的边界点的限制的集合。边界点的集合本身可以被认为是医学图像中的解剖结构的不充分的分割,而是用于从多个不同的分割模型中选择分割模型。选择基于边界点和分割模型中的每个之间的拟合优度量度。例如,可以选择最佳拟合模型并将其用于解剖结构的分割。
系统100包括用于访问医学图像的图像数据022的图像数据接口120。医学图像包括要分割的解剖结构。在图1的范例中,图像数据接口120被示出为被连接到外部图像存储库020。例如,图像存储库020可以由系统100可以连接或包括在其中的医院信息系统(his)的影像归档和通信系统(pacs)构成或是其部分。因此,系统100可以获得对医学图像的图像数据022的访问。通常,图像数据接口120可以采取各种形式,例如到局域网或广域网的网络接口,例如因特网、到内部或外部数据存储设备的存储接口等。
注意,贯穿本文,并且在适当的情况下,对医学图像的参考要被理解为对医学图像的图像数据的参考。
系统100还包括用于访问定义用于分割解剖结构的多个模型的模型数据042的模型数据接口140。模型数据142可以以任何合适的方式定义每个模型,例如三角网格、点云等。这样一来,每个模型可以至少部分地可表示为坐标系中的坐标的集合。在图1的范例中,模型数据接口120被示出为连接到外部数据库040。然而,数据库040也可以是内部数据库。通常,数据库040可以由例如基于盘的数据存储设备(例如硬盘)、基于半导体的数据存储设备(诸如rom或ram存储器)、插入到存储介质读取器中的可移除存储介质等构成。模型数据接口140可以是与数据库040的相对应的类型。
系统100还包括用户交互子系统180,其包括显示输出部182和用户设备输入部184。显示输出部182被配置为在显示器060上显示系统100的视觉输出,这至少包括显示医学图像的视图。此处,术语“视图”是指医学图像的部分或全部的可视化。例如,医学图像可以是体积3d图像,并且视图可以是体积3d图像的多平面绘制或其他体积可视化。另一范例是医学图像可以由切片的堆叠构成,并且视图可以对应于切片中的一个。另一范例是视图仅仅是2d医学图像的可视化。医学图像的各种其他可视化同样可以想到。为了在显示器060上显示视图,显示输出部182被示出为向显示器提供显示数据062。
用户设备输入部184被配置为从用户可操作的用户设备080接收输入命令082。用户设备080可以采取各种形式,包括但不限于计算机鼠标、触摸屏、键盘等。用户设备输入部184可以是与用户设备080的类型相对应的类型。同时,显示输出部182和用户设备输入部184可以形成用户交互子系统180,用户交互子系统180使用户能够在视图中指示解剖结构的边界点的集合,例如通过适当地操作用户设备080来控制屏幕上光标和“点击”解剖结构的边界,从而指定边界点的集合。然后边界点可以可用于系统,例如作为坐标的集合。
系统100还包括用于基于用户指示的边界点的集合来选择多个模型中的一个或多个的处理器160。(一个或多个)选定的模型然后可以用于分割医学图像中的解剖结构,例如用作解剖结构的标注,用于进一步的自动化分析等。为了选择(一个或多个)模型,处理器160被配置为基于相应坐标的比较来确定该边界点的集合和多个模型中的每个之间的拟合优度,从而获得多个拟合优度量度,并且基于多个拟合优度量度来选择多个模型中的一个或多个,从而获得一个或多个选定的模型。例如,处理器160可以选择其拟合优度量度超过阈值的(一个或多个)模型。已经选择了(一个或多个)模型,然后可以将这些模型拟合到医学图像中的解剖结构,从而提供解剖结构的一个或多个分割。
应当注意,将参考图3-5更详细地说明系统100的各种操作,包括其各种任选方面。
系统100可以被实现为单个设备或装置(例如工作站或成像装置),或者实现在其中。该设备或装置可以包括运行适当软件的一个或多个微处理器。软件可能已经被下载和/或存储在对应的存储器中,例如诸如ram的易失性存储器或诸如闪存的非易失性存储器。备选地,系统的功能单元可以以诸如作为现场可编程门阵列(fpga)的可编程逻辑的形式在设备或装置中实施。通常,系统的每个功能单元可以以电路的形式实施。注意,系统100还可以以分布式方式实施,例如涉及不同的设备或装置。例如,分布可以根据客户端-服务器模型。
图2图示了存储作为数据库中的模型数据的多个模型,其中,示出了被存储415为数据库040中的模型数据042的第一模型200和第二模型210。模型可以采取任何适合于分割解剖对象的形式,如医学图像分割领域本身已知的。例如,模型可以是网格模型、点云模型,可以是2d模型或3d模型等。
图3-5提供了图1的系统的操作的范例,其中,图3示出了用户使用用户交互系统在医学图像的视图中指示解剖结构的边界点的集合。即,如参考子图(i)所示,用户可以在显示器上被提供医学图像的视图024,该视图示出解剖结构030的至少部分,包括解剖结构的边界的至少部分。如参考子图(ii)所示,用户可以在解剖结构的边界上指示边界点300的集合,例如,b在相应屏幕上位置上用屏幕上光标064进行点击,或者经由另一图形用户交互。如参考子图(iii)所示,在具体实施例中,用户还可以将边界点300中的一个或多个标记为关键点,在子图(iii)中指示为黑点302、304。这些关键点302、304可以表示被认为是准确的边界点,例如由用户特别注意其放置,边界在所述点处被特别清楚地限定等。作为关键点的备选,用户还可以为特定边界点指定“拟合确定性”值。然而,用户也可以不指示这样的确定性,而是简单地指示多个边界点而不提供“确定性”输入。
如图3所示,用户可以指定沿着解剖结构的边界相对均匀分布的点。如将参考图4和图5图示的,这可以有助于确定该边界点的集合与模型之间的拟合优度。然而,用户不需要指定均匀分布的点。
图4示出了在由用户指示的边界点的集合300和来自数据库的第一模型200之间确定的拟合优度。注意,解剖结构的轮廓被示为边界点300下面的虚线。然而,轮廓仅仅示出以便于图4以及图5的解释。即,在该阶段只有边界点的限制的集合可能可用于处理器,而不是解剖结构的完整描绘。
子图(i)、(ii)、(iii)和(iv)图示了边界点300可以以各种方式映射到第一模型200。简而言之,处理器可以迭代地确定边界点的集合和模型之间的各种几何变换,选择最佳的一个,并在随后选择或不选择特定模型时考虑该最佳几何变换的拟合优度。这样的几何变换可以是例如刚性变换、约束弹性变换等。确定变换本身是从各种领域中已知的,例如图像配准、模型到图像配准、网格配准等。这样一来,在确定边界点的集合与模型之间的变换中,技术人员可以采用这些领域的配准技术。一种简单的方法可能是穷尽的方法,因为可以评价所有可能的变换。这种方法可能受到额外的要求的限制,其中,可能需要将关键点(标记为黑色)映射到第一模型200的表面上。随后,可以基于应用于剩余的非关键边界点的距离量度来计算拟合优度。从子图(i)-(iv)中可以看出,各种几何变换通常产生较差的拟合优度。子图(iii)中图示的几何变换仍然可以被认为是最佳拟合,因此在随后选择或不选择第一模型200中可以考虑其拟合优度。
图5图示了在如图4所示的相同的边界点300的集合之间确定的拟合优度,但现在相对于来自数据库的第二模型210。如从图5可以看出的,并且特别是在子图(iv)中,第二模型210通常更好地匹配边界点300的集合。子图(iv)中图示的几何变换可以被认为是最佳拟合,因此在随后选择或不选择第二模型210中可以考虑其拟合优度。
已经确定了第一模型200和第二模型210以及可能的其它模型的拟合优度,可以基于它们的相应拟合优度量度来选择模型中的一个或多个。例如,处理器可以基于其拟合优度量度超过第一模型200的而来选择第二模型210。处理器还可以基于它们相应拟合优度量度都超过拟合优度阈值而选择第一模型200和第二模型210两者。
通常,已经基于其拟合优度选择多个模型后,系统可以以以下方式迭代地改进选择。即,选定的模型可以拟合到医学图像,例如使用如先前确定的刚性变换。随后,可以识别多个拟合的模型之间的几何变化的区域。例如,这可以涉及对于最佳匹配模型的每个点确定与其他选定的模型中的每个最接近的点,并且然后计算所述点之间的平均距离。然后,用户交互子系统可以向用户提供关于几何变化的区域的位置的视觉反馈。这种视觉反馈可以包括显示最佳地显示几何变化的区域的医学图像的另一视图,并且例如借助于彩色球体或其他可视化模块在视觉上突出显示所述区域。可以使用户能够基于视觉反馈来调节边界点的集合,例如通过调节边界点的集合,从边界点的集合中删除一个或多个边界点和/或向边界点的集合添加一个或多个边界点。随后,处理器可以基于经调节的边界点的集合重新选择多个模型中的一个或多个。因此,系统可以借助于用户迭代地改进模型选择,例如通过迭代地“缩小”到最佳拟合模型的选择。
注意,确定边界点的集合和模型之间的变换可以涉及点对面匹配,例如使用迭代最近点算法。此处,对于每个用户指示的边界点,可以例如经由全搜索、几何散列或距离变换来确定模型的最近点。然后,可以确定刚性变换的参数,其最小化所有用户指定的边界点和对应的最接近的模型点之间的距离。然后,拟合优度量度可以是剩余的,即“最终”的点面误差。
应当认识到,如权利要求的发明可以有利地用于基于用户指定3d医学图像的2d视图中的边界点来选择3d模型。然而,这不是限制,其中,也可以基于用户指定3d视图中或多个2d视图中的边界点来选择3d模型,或者可以基于用户指定2d视图中的边界点来选择2d模型,等等。
还应注意,除了用户指定的边界点之外,还可以在确定与多个模型中的每个模型的拟合优度中使用一个或多个计算机生成的边界点。计算机生成的边界点可以从或基于用户指定的边界点算法地生成,并且可以有效地用于增强用户指定的边界点,从而获得要用于确定多个模型中的每个中的拟合优度的增强的边界点的集合。例如,可以使用称为“通电电线(livewire)”的算法来生成,以向用户指定的边界点的集合增加更多的点,如在falcao,a.x,等人的题为“anultra-fastuser-steeredimagesegmentationparadigm:livewireonthefly”(ieeetransactionsonmedicalimaging,第19卷、第1期、第55-62页)的文章中所描述的。作为对所述通电电线算法的输入,以及通常,用户指定的边界点可以以线段或其他几何图元的形式来指定。
范例使用可以如下。此处,为了在医学图像中的解剖结构的标注的目的选择模型。用户可以在2d视图中以指定坐标的形式提供初始信息。这些坐标可以有效地表示解剖结构的用户指定的2d模型。这些坐标可用于查询预定义3d模型的数据库。与手动输入的坐标具有最接近相似度的3d模型可以被导入到标注软件中,并根据与手动输入的坐标的最佳拟合而与医学图像对齐。在评估3d模型与医学图像的拟合度时,如果拟合度低于阈值,则可以要求用户将坐标添加到2d模型,使得备选的3d模型被拟合到医学图像。如果3d模型的拟合度高于阈值,则然后可以使用选定的3d模型标注医学图像。
图6示出了用于基于用户指示的边界点的限制的集合来分割解剖结构的方法400。方法400包括,在题为“访问图像数据”的操作中,访问410表示医学图像的图像数据,医学图像包括要分割的解剖结构。方法400还包括,在题为“访问模型数据”的操作中,访问420定义用于分割解剖结构的多个模型的模型数据,其中,多个模型中的每个至少部分地可表示为坐标系中的坐标的集合。方法400还包括,在题为“获取用户指示的边界点”的操作中,使用用户交互子系统使得用户能够在医学图像的视图中指示解剖结构的边界点的集合,从而获得430与视图相关联的坐标系中的坐标的集合。方法400还包括通过以下来选择用于分割医学图像中的解剖结构的多个模型中的一个或多个:在题为“确定模型的拟合优度”的操作中基于相应坐标的比较确定440边界点的集合和多个模型中的每个之间的拟合优度,从而获得多个拟合优度量度;并且在题为“基于拟合优度来选择模型”的操作中,基于多个拟合优度量度选择450多个模型中的一个或多个,从而获得一个或多个选定的模型。
将认识到,以上操作可以例如通过输入/输出关系以任何适当的顺序执行,例如,连续地、同时地、或其组合,在适用的情况下,经受所需的特定顺序。
方法400可以作为计算机实施的方法、作为专用硬件或两者的组合在计算机上实施。还如图7图示的,计算机的指令(例如可执行代码)可以存储在计算机可读介质460上,例如以机器可读物理标记的系列470的形式和/或作为具有不同的电气,例如磁性或光学特性或值的元件的系列。可执行代码可以以暂态或非暂态方式存储。计算机可读介质的范例包括存储器设备、光学存储设备、集成电路、服务器、在线软件等。图7示出了光盘460。
将认识到,本发明也应用于计算机程序,特别是在载体上或在载体中的计算机程序,所述计算机程序适于将本发明付诸实践。程序可以是源代码、目标代码、源代码和目标代码中间的代码的形式,例如部分编译的形式,或者适于用在实施根据本发明的方法中的任何其他形式。还将认识到,这样的程序可以具有许多不同的架构设计。例如,实施根据本发明的方法或系统的功能的程序代码可以被细分为一个或多个子例程。在这些子例程之间分布功能的许多不同方式对本领域技术人员而言将是显而易见的。子例程可以被一起存储在一个可执行文件中,以形成自包含程序。这样的可执行文件可以包括计算机可执行指令,例如,处理器指令和/或解读器指令(例如,java解读器指令)。备选地,一个或多个或所有子例程可以被存储在至少一个外部库文件中,并且静态地或动态地(例如在运行时间处)与主程序链接。主程序包含对子例程中的至少一个的至少一个调用。子例程还可以包括对彼此的函数调用。涉及计算机程序产品的实施例包括计算机可执行指令,其对应于本文中阐述的方法中的至少一个的每个处理阶段。这些指令可以被细分为子例程和/或存储在可以被静态地或动态地链接的一个或多个文件中。涉及计算机程序产品的另一实施例包括计算机可执行指令,其对应于本文中阐述的系统和/或产品中的至少一个的每个模块。这些指令可以被细分为子例程和/或存储在可以被静态地或动态地链接的一个或多个文件中。
计算机程序的载体可以是能够承载程序的任何实体或设备。例如,载体可以包括数据存储设备,例如rom(例如,cdrom或半导体rom),或者磁记录介质(例如,硬盘)。此外,载体可以是诸如电学或光学信号的可传送载体,其可以经由电缆或光缆或通过无线电或其他手段来传达。当程序实现在这种信号中时,载体可以由这种线缆或其他设备或模块构成。备选地,载体可以是程序被实现在其中的集成电路,集成电路适于执行相关方法,或者用于相关方法的执行中。
应当注意,上述实施例说明而非限制本发明,并且本领域技术人员能够在不脱离权利要求的范围的情况下设计许多备选实施例。在权利要求中,置于括号中的任何附图标记不应被解释为对权利要求的限制。动词“包括”及其词性变化的使用不排除存在不同于权利要求中所述的其他元件或步骤。在元件之前的词“一”或“一个”不排除存在多个这样的元件。本发明可以借助于包括若干个不同元件的硬件来实施,并且可以借助于适当编程的计算机来实施。在列举了若干模块的设备权利要求中,这些模块中的若干可以由一个相同的硬件实现。尽管在互不相同的从属权利要求中记载了特定措施,但是这并不表示不能有利地使用这些措施的组合。
- 还没有人留言评论。精彩留言会获得点赞!