电极材料及电池的制作方法
本公开涉及电池用的电极材料及电池。
背景技术:
专利文献1中公开了一种锂二次电池,其在负极集电体中使用了最小细孔径在的范围且比表面积在960m2/g~2000m2/g的范围的活性炭。
现有技术文献
专利文献
专利文献1:(日本)特开2001-85005号公报
技术实现要素:
发明所要解决的课题
现有技术中,期望实现具有高充放电效率的电池。
用于解决课题的手段
本公开的一个实施方式的电极材料,含有碳材料,所述碳材料的比表面积为2m2/g以上且250m2/g以下,通过氦比重瓶求得的所述碳材料的密度为0.2g/cc以上且1.5g/cc以下。
发明效果
根据本公开,能够实现具有高充放电效率的电池。
附图说明
图1是示出作为实施方式2的电池的一例的电池10的概略构成的截面图。
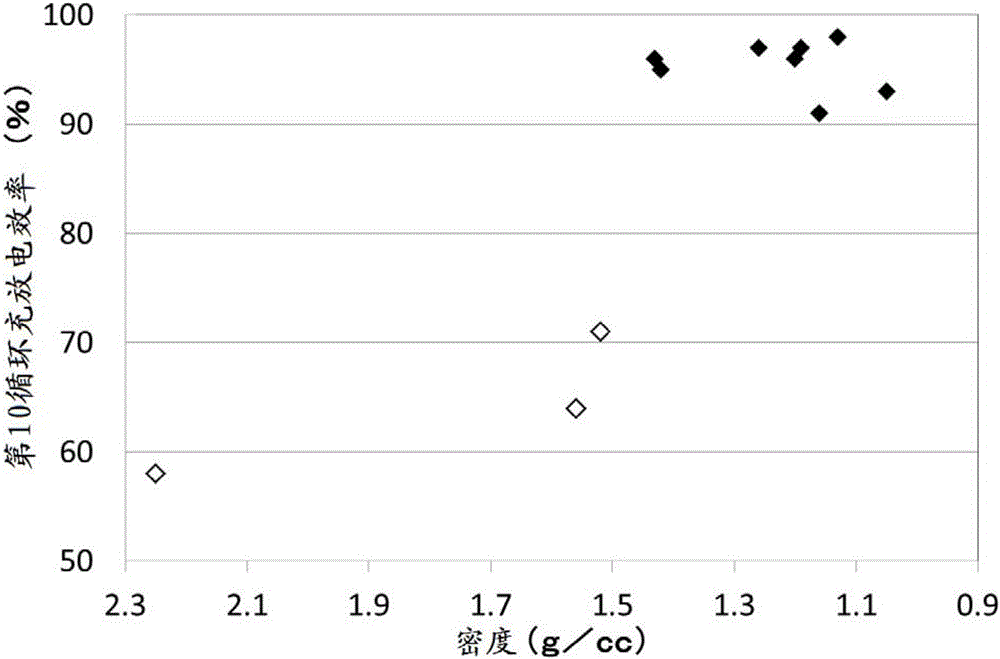
图2是示出实施例1~8及比较例1、比较例3和比较例4的评价用电池的第10循环的充放电效率、与碳材料密度之间的关系的图。
附图标记说明
11 负极
12 正极集电体
13 正极合剂层
14 正极
15 隔膜
16 外壳
具体实施方式
以下,对本公开的实施方式进行说明。
首先,以下说明本发明者的着眼点。
电解液中的碱金属离子以通过构成电解液的溶剂进行了溶剂化的溶剂化离子的状态存在。它们在从电解液中脱溶剂化的同时,还原析出。因此,通过析出的碱金属与电解液接触,发生副反应。
例如,如专利文献1,在使用比表面积大的活性炭的情况下,负极集电体的细孔部以外的表面部等与电解液的接触部位增多。因此,使锂仅在细孔内析出在本质上变得困难。因此,在细孔部以外析出的锂与电解液发生副反应。其结果,在专利文献1那样的电池中,特别是初次(第一循环)的充放电中的充放电效率成为低的值(例如20%以下)。
基于以上的着眼点,本发明者作出了本公开的构成。
(实施方式1)
实施方式1的电极材料含有碳材料。
此时,该碳材料的比表面积为2m2/g以上且250m2/g以下。
并且,通过氦比重瓶求出的该碳材料的密度为0.2g/cc以上且1.5g/cc以下。
根据以上的构成,可以实现具有大的充放电容量密度且具有高充放电效率的电池。
实施方式1的碳材料的特征在于多孔体结构方面。实施方式1的碳材料中,溶剂化了的碱金属离子在浸入多孔体的孔中之前发生脱溶剂化。脱溶剂化了的碱金属离子仅在孔的内部空间电化学地析出。由此,析出的活性碱金属与电解液的接触被抑制。其结果,电解液引起的碱金属的一部分的氧化和惰性化(失活)这样的因碱金属与电解液接触而发生的副反应被抑制。
在此,作为存在于电极内部的孔,可举出存在于集电体内部的孔、或存在于构成电极的粒子的内部的孔、或者存在于粒子间的孔等。其中,特别是作为碱金属离子进入时能够发生脱溶剂的孔,例如可举出存在于粒子内部的孔,即溶剂不能进入的孔即闭塞孔(封闭孔)等。在这样的孔的内部析出的(被充电的)碱金属不与电解液接触。因此,上述的副反应被抑制。
对于通过氦比重瓶进行的密度测定,测定气体使用原子半径约为0.3nm的氦原子,通过超比重计可以求出密度。在此,锂的原子半径约为0.2nm。另外,碳酸亚丙酯溶剂化的Li离子的直径为0.6nm左右(通过Stokes法的计算结果)。如果考虑这些,则通过氦比重瓶求出的密度为碳材料的质量(g)除以碳材料与电解液不能侵入的闭塞孔相加所得的体积(cc)所得的密度(g/cc)。因此,碳材料的通过氦比重瓶求出的密度小意味着存在多个闭塞孔。
通过使利用氦比重瓶求出的碳材料的密度为1.5g/cc以下,可以形成能够将碱金属充分保持在内部的闭塞孔。
根据以上的构成,可以使溶剂化了的碱金属离子在进入多孔体的孔中之前脱溶剂化,使碱金属在电解液不能进入的闭塞孔内析出。
因此,对于实施方式1的碳材料,即使在初次、及循环数增加的情况下,也能够抑制碱金属向电极(例如负极)的表面的析出。由此,能够抑制充放电容量密度的劣化、及充放电效率的劣化。
在此,在通过氦比重瓶求出的密度小于0.2g/cc的情况下,可能难以制作在物理上能够保持的电极。
另外,当碳材料的比表面积小于2m2/g时,反应面积过低。因此,当碳材料的比表面积小于2m2/g时,可能不能进行良好的充放电反应。
另外,当比表面积大于250m2/g时,碱金属也在电极表面析出,从而有副反应增大的可能性。
碳材料的比表面积例如可使用全自动气体吸附量测定装置进行使用氮气的多孔性碳材料的气体吸附测定并通过BET多点法求出。
另外,实施方式1的电极材料中,碳材料的比表面积也可以为2m2/g以上且221m2/g以下。
另外,实施方式1的电极材料中,通过氦比重瓶求出的碳材料的密度也可以为0.2g/cc以上且1.43g/cc以下。
根据以上的构成,可以实现具有大的充放电容量密度且具有高充放电效率的电池。
另外,实施方式1的电极材料中,碳材料的比表面积也可以为2m2/g以上且100m2/g以下。
根据以上的构成,由于比表面积为100m2/g以下,从而可以进一步抑制副反应。
另外,实施方式1的电极材料中,碳材料的比表面积也可以为2m2/g以上且51m2/g以下。
根据以上的构成,由于比表面积为51m2/g以下,从而可以进一步抑制副反应。
另外,实施方式1的电极材料中,碳材料的总细孔容积可以为0.01cc/g以上且0.1cc/g以下。
在总细孔容积比0.1cc/g以上大的情况下,在闭塞孔以外的孔内析出的碱金属的比例可能增大。因此,在闭塞孔以外的孔内析出的碱金属与电解液可能发生副反应。
在此,总细孔容积可使用氮气作为吸附气体种,通过全自动气体吸附量测定装置根据相对压力0.99下的吸附气体量求出。全自动气体吸附量测定装置被用作测定总细孔容积(cc/g)的装置。氮的原子半径约为0.4nm。即,在该测定中,闭塞孔不能吸附气体。因此,该测定中,测定被称作开孔(开放孔)的、闭塞孔以外的细孔的容积。
另外,实施方式1的电极材料中,碳材料的总细孔容积也可以为0.02cc/g以上且0.09cc/g以下。
根据以上的构成,能够实现具有大的充放电容量密度且具有高充放电效率的电池。
<碳材料的制作方法>
实施方式1的电极材料中所含的碳材料例如可通过将作为碳源的有机材料或多孔性碳材料在惰性气氛下进行烧成来制作。
作为成为碳源的有机材料,可以是纤维素系树脂。纤维素系树脂的形状可以为片状、纤维状、粒子状等。如果考虑烧成后的加工,则优选为数μm~数十μm大小的粒子状或短纤维状的纤维素系树脂。作为廉价的纤维素系材料,可举出木炭、锯屑、纸等。热处理温度优选为1500℃~2100℃、烧成气氛适合使用氮气、氩气、氦气、氖气等之类的惰性气体。通过进行热处理,使碳以外的元素从作为碳源使用的原料中蒸发掉,实现原料的碳化。并且,通过将开孔闭塞,可以变换为闭塞孔。
作为多孔性碳材料,可以为活性碳材料或导电性炭黑。活性碳材料或导电性炭黑的形状可以是片状、纤维状、粒子状等。如果考虑烧成后的加工,则优选为数μm~数十μm大小的粒子状或短纤维状的活性碳材料或导电性炭黑。作为廉价的活性碳材料,可举出水蒸汽活化炭等。热处理温度优选为2100℃~2400℃。烧成气氛适合使用氮气、氩气、氦气、氖气等 之类的惰性气体。通常,活性碳材料或导电性炭黑具有大量开孔,几乎没有闭孔。通过进行上述的烧成,将开孔闭塞化,由此可变换为闭塞孔。
此外,在为对碳材料进行造粒而需要进行粉碎的情况下,优选在进行热处理之前,将有机材料或多孔性碳材料进行粉碎。在对通过热处理获得的多孔性碳材料进行粉碎的情况下,多孔性碳材料的结构发生变化,闭塞孔可能变换成溶剂可进入的开孔等。
如上,实施方式1的一个方式的碳材料的制造方法包含:准备作为碳源的有机材料或多孔质碳材料的工序、和将有机材料或多孔质碳材料在惰性气氛下进行热处理的工序。
另外,实施方式1的一个方式的碳材料的制造方法中,有机材料为纤维素系树脂。此时,热处理的温度为1500℃以上且2100℃以下。
另外,实施方式1的一个方式的碳材料的制造方法中,多孔质碳材料为活性碳材料或导电性炭黑。此时,热处理的温度为2100℃以上且2400℃以下。
(实施方式2)
以下,对实施方式2进行说明。此外,与上述的实施方式1重复的说明适宜省略。
实施方式2的电池具备负极、正极和电解质。
在此,负极包含上述实施方式1的电极材料。
根据以上的构成,可以实现具有大的充放电容量密度且具有高充放电效率的电池。
另外,实施方式2的电池中,负极可以含有上述实施方式1的碳材料作为主成分。即,负极可以以例如相对于负极整体的重量比例计为50%以上的比例含有上述的实施方式1的碳材料。
根据以上的构成,能够实现具有更大的充放电容量密度且具有更高的充放电效率的电池。
另外,实施方式2的电池中,正极可以是能够吸藏及释放碱金属离子的电极。
另外,实施方式2的电池中,电解质也可以是含有碱金属离子的电解质。
另外,实施方式2的电池可构成为锂二次电池。
即,实施方式2的电池中,碱金属离子可以是锂离子。
另外,实施方式2的电池中,在充电状态,负极相对于碱金属参比电极的电位可以为0V以下。
根据以上的构成,在负极相对于碱金属参比电极的电位为0V以下时,碱金属存在于孔内。
在使用石墨作为负极的情况下,如果将负极相对于参比电极的电位设为0V以下使用,则会发生碱金属在负极表面析出引起的电池内部短路、或与电解液发生副反应。
与之相对,实施方式2的电池中,在将负极相对于参比电极的电位设为0V以下的情况下,碱金属优先在孔内析出。由此,可以抑制电池内部短路。另外,可以抑制析出的碱金属与电解液发生副反应。由此,可以抑制充放电效率的劣化。
此外,在孔内析出的碱金属在放电时再次溶解于电解质中。之后,以碱金属离子的形式扩散到电解质中,且被再次吸藏于正极活性物质内部。该现象是可逆的,即使将充电和放电重复多次,也能够重复碱金属向孔内的析出和向电解质的溶解。
这样,碱金属离子在孔内析出并再次在电解液内以碱金属离子的形式溶解,由此,可以增加电池的容量。即,在使用具有层状结构的碳材料的情况下,容量起因于层间的碱金属离子的吸藏及释放。与之相对,如果为实施方式2的电池,则不仅利用层间的碱金属离子的吸藏及释放,还利用碱金属向孔内的析出。由此,如果是实施方式2的电池,则能够实现更高容量的二次电池。
另外,实施方式2的电池中,在充电状态下,充电终止电压与碱金属参比电极的电位相比,可以为低电位。
根据以上的构成,能够抑制循环特性的劣化,并且实现容量高的电池。
此外,也可以使用实施方式2的电池来构成蓄电系统。
图1是示出作为实施方式2的电池的一例的电池10的概略结构的截面图。
如图1所示,电池10具备负极11、正极14、隔膜15和外壳16。
正极14由正极集电体12、和与正极集电体12相接形成的正极合剂层13构成。
负极11和正极14被配置为隔着隔膜15彼此对置。
将它们用外壳16覆盖,形成电池10。
负极11包含上述实施方式1的电极材料。例如,负极11可以含有上述的实施方式1的电极材料作为负极活性物质。
此外,负极11也可以具备其它负极活性物质、负极集电体等。
另外,根据需要,负极11也可以含有导电助剂、离子传导体、粘合剂等。
正极合剂层13含有能够吸藏释放碱金属离子的正极活性物质。
此外,根据需要,正极合剂层13也可以含有导电助剂、离子传导体、粘接剂等。
作为正极活性物质,可使用吸藏及释放碱金属离子的材料。作为正极活性物质,例如可举出含碱金属的过渡金属氧化物、过渡金属氟化物、聚阴离子材料、氟化聚阴离子材料、过渡金属硫化物等。其中,从制造成本低且平均放电电压高的观点出发,优选使用含碱金属的过渡金属氧化物。
作为正极集电体12,可使用由铝、不锈钢、钛、及它们的合金等金属材料制作的多孔质或无孔的片材或膜。从廉价且容易薄膜化的观点出发,优选铝及其合金。作为片材或膜,可使用金属箔、网等。为了实现电阻值的降低、催化剂效果的赋予、使正极合剂层13与正极集电体12化学或物理结合时强化正极合剂层13与正极集电体12之间的结合,也可以在正极集电体12的表面涂布碳等碳材料。
导电助剂及离子传导体为降低电极电阻而使用。
作为导电助剂,可举出天然石墨或人造石墨的石墨类、乙炔黑、科琴黑等炭黑类、碳纤维或金属纤维等导电性纤维类、氟化碳、铝等金属粉末类、氧化锌或钛酸钾等导电性晶须类、氧化钛等导电性金属氧化物、聚苯胺、聚吡咯、聚噻吩等导电性高分子化合物等。其中,从实现低成本化的观点出发,优选为碳导电助剂。
作为离子传导体,可举出聚甲基丙烯酸甲酯、聚甲基丙烯酸甲基酯等凝胶电解质、聚氧乙烯等有机固体电解质、Li7La3Zr2O12等无机固体电解质等。
粘合剂为提高构成电极的材料的粘结性而使用。作为粘合剂,可举出聚偏二氟乙烯、聚四氟乙烯、聚乙烯、聚丙烯、芳香族聚酰胺树脂、聚酰胺、聚酰亚胺、聚酰胺酰亚胺、聚丙烯腈、聚丙烯酸、聚丙烯酸甲酯、聚丙烯酸乙酯、聚丙烯酸己酯、聚甲基丙烯酸、聚甲基丙烯酸甲酯、聚甲基丙烯酸乙酯、聚甲基丙烯酸己酯、聚醋酸乙烯酯、聚乙烯基吡咯烷酮、聚醚、聚醚砜、六氟聚丙烯、丁苯橡胶、羧甲基纤维素等。另外,可使用选自四氟乙烯、六氟乙烯、六氟丙烯、全氟烷基乙烯基醚、偏二氟乙烯、氯三氟乙烯、乙烯、丙烯、五氟丙烯、氟甲基乙烯基醚、丙烯酸、己二烯中的2种以上的材料的共聚物。另外,也可以混合使用选自这些粘合剂中的2种以上。
作为隔膜15,可使用由聚乙烯、聚丙烯、玻璃、纤维素、陶瓷等制成的多孔质膜。可以在隔膜15的细孔内部含浸电解质而使用。
作为电解质,可使用含有碱金属盐和非水溶剂的电解液、凝胶电解质、固体电解质等。
作为碱金属盐,可使用锂盐、钠盐等。
作为锂盐,可使用六氟磷酸锂(LiPF6)、四氟硼酸锂(LiBF4)、高氯酸锂(LiClO4)、双三氟甲基磺酰亚胺锂(LiN(SO2CF3)2)、双全氟乙磺酰亚胺锂(LiN(SO2C2F5)2)、双氟甲磺酰亚胺锂(LiN(SO2F)2)、LiAsF6、LiCF3SO3、二氟(草酸)硼酸锂等。其中,从电池的安全性、热稳定性及离子传导性的 观点出发,优选使用LiPF6。此外,可以使用电解质盐中的1种,或者也可以组合2种以上使用。
作为钠盐,可使用六氟磷酸钠(NaPF6)、四氟硼酸钠(NaBF4)、高氯酸钠(NaClO4)、双三氟甲基磺酰亚胺钠(NaN(SO2CF3)2)、双全氟乙磺酰亚胺钠(NaN(SO2C2F5)2)、双氟甲磺酰亚胺钠(NaN(SO2F)2)、NaAsF6、NaCF3SO3、二氟(草酸)硼酸钠等。其中,从电池的安全性、热稳定性及离子传导性的观点出发,优选使用NaPF6。此外,可以使用上述电解质盐中的1种,或者也可以组合2种以上使用。
作为非水溶剂,可使用环状碳酸酯、链状碳酸酯、酯类、环状醚类、链状醚类、腈类、酰胺类等。这些溶剂可以单独使用1种,也可以组合2种以上使用。
作为环状碳酸酯类,可举出碳酸亚乙酯、碳酸亚丙酯、碳酸亚丁酯等。也可以使用它们的氢基的一部分或全部被氟取代了的物质。例如,可举出三氟碳酸亚丙酯、氟代碳酸亚乙酯等。
作为链状碳酸酯类,可举出碳酸二甲酯、碳酸甲乙酯、碳酸二乙酯、碳酸甲丙酯、碳酸乙丙酯、碳酸甲基异丙酯等。可以使用它们的氢基的一部分或全部被氟取代了的物质。
作为酯类,可举出乙酸甲酯、乙酸乙酯、乙酸丙酯、丙酸甲酯、丙酸乙酯、γ-丁内酯等。
作为环状醚类,可举出1,3-二氧戊环、4-甲基-1,3-二氧戊环、四氢呋喃、2-甲基四氢呋喃、环氧丙烷、1,2-环氧丁烷、1,4-二烷、1,3,5-三烷、呋喃、2-甲基呋喃、1,8-桉树脑、冠醚等。
作为链状醚类,可举出1,2-二甲氧基乙烷、二乙基醚、二丙基醚、二异丙基醚、二丁基醚、二己基醚、乙基乙烯基醚、丁基乙烯基醚、甲基苯基醚、乙基苯基醚、丁基苯基醚、戊基苯基醚、甲氧基甲苯、苄基乙基醚、二苯基醚、二苄基醚、邻二甲氧基苯、1,2-二乙氧基乙烷、1,2-二丁氧基乙烷、二乙二醇二甲基醚、二乙二醇二乙基醚、二乙二醇二丁基醚、1,1-二 甲氧基甲烷、1,1-二乙氧基乙烷、三乙二醇二甲基醚、四乙二醇二甲基醚等。
作为腈类,可举出乙腈等。
作为酰胺类,可举出二甲基甲酰胺等。
实施例
以下说明的实施例为一例,本公开不仅限于以下的实施例。
(实施例1)
[碳材料的制作]
通过以下的炭化工序、分级工序、热处理工序这3阶段的步骤制作碳材料。
首先,对炭化工序进行说明。作为碳源,使用α-纤维素(Whatman社制定量滤纸(No.40))。将其用Ar气氛下的环状炉(Ar气体流量1L/min)从室温以每分钟10℃的比例升温,加热至达到1000℃,并在1000℃下保持1小时。之后,停止加热,自然冷却后从管状炉中取出炭化物。
接着,对分级工序进行说明。将上述炭化工序中获得的炭化物用玛瑙乳钵粉碎。将其使用网眼40μm的SUS制标准筛进行分级。由此,获得碳粉末。
最后,对热处理工序进行说明。使用上述的碳粉末,用Ar气氛下的管环状炉(Ar气体流量1L/min)从室温以每分钟10℃的比例升温,加热至达到1500℃,并在1500℃下保持1小时。即,实施例1的热处理工序的温度(热处理温度)为1500℃。之后,停止加热,自然冷却后从管状炉取出碳材料。
通过如上操作,获得碳材料。
[试验电极的制作]
以重量比9:1称量获得的碳材料和粘接剂聚偏二氟乙烯。
将其分散于NMP溶剂中,制作浆料。
使用涂布机,将制作的浆料涂布于Cu集电体上。
将涂布好的极板用压延机压延,冲压成直径20mm的正方形。
将其加工成电极状态,获得试验电极。
[评价用电池的制作]
使用上述试验电极,制作了以锂为对电极及参比电极的锂二次电池(评价用电池)。
电解液的调制及评价用电池的制作在露点-60度以下、氧值1ppm以下的Ar气氛的手套箱内进行。
作为电解液,使用在将碳酸亚乙酯和碳酸二乙酯以体积比为1:1的方式混合而成的溶剂中溶解有1摩尔浓度的六氟磷酸锂(LiPF6)的电解液。
另外,在边长为20mm的正方形的镍网上压接锂。将其作为对电极使用。
使上述试验电极和对电极隔着含浸有电解液的聚乙烯微多孔膜的隔膜而对置。在该状态下收纳于外壳内,并将外壳封口。
通过如上操作,获得评价用电池。
(实施例2)
将热处理工序的温度(热处理温度)设为2100℃。
除此之外,以与上述的实施例1相同的方法制作了碳材料。
另外,以与上述的实施例1相同的方法制作了试验电极及评价用电池。
(实施例3)
作为碳材料的碳源,使用活性碳材料(比表面积1900m2/g、平均粒径20μm)。
另外,将热处理工序的温度(热处理温度)设为2100℃。
除此之外,以与上述实施例1相同的方法制作了碳材料。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(实施例4)
作为碳材料的碳源,使用活性碳材料(比表面积2500m2/g、平均粒径9μm)。
另外,将热处理工序的温度(热处理温度)设为2400℃。
除此之外,以与上述实施例1相同的方法制作了碳材料。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(实施例5)
作为碳材料的碳源,使用活性碳材料(比表面积2000m2/g、平均粒径8μm)。
另外,将热处理工序的温度(热处理温度)设为2400℃。
除此之外,以与上述实施例1相同的方法制作了碳材料。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(实施例6)
作为碳材料的碳源,使用活性碳材料(比表面积1600m2/g、平均粒径6μm)。
另外,将热处理工序的温度(热处理温度)设为2400℃。
除此之外,以与上述实施例1相同的方法制作了碳材料。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(实施例7)
作为碳材料的碳源,使用科琴黑(ライオン社制、EC600)。
另外,将热处理工序的温度(热处理温度)设为2100℃。
除此之外,以与上述实施例1相同的方法制作了碳材料。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(实施例8)
将热处理工序的温度(热处理温度)设为2400℃。
除此之外,以与上述实施例7相同的方法制作了碳材料。
另外,以与上述实施例7相同的方法制作了试验电极及评价用电池。
(比较例1)
作为碳材料,使用石墨系碳材料(NG12)。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(比较例2)
将热处理工序的温度(热处理温度)设为1000℃。
除此之外,以与上述实施例1相同的方法制作了碳材料。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(比较例3)
将热处理工序的温度(热处理温度)设为1800℃。
除此之外,以与上述实施例4相同的方法制作了碳材料。
另外,以与上述实施例4相同的方法制作了试验电极及评价用电池。
(比较例4)
作为碳材料的碳源,使用活性碳材料(比表面积2000m2/g、平均粒径2μm)。
另外,将热处理工序的温度(热处理温度)设为2600℃。
除此之外,以与上述实施例1相同的方法制作了碳材料。
另外,以与上述实施例1相同的方法制作了试验电极及评价用电池。
(比较例5)
将热处理工序的温度(热处理温度)设为1500℃。
除此之外,以与上述实施例3相同的方法制作了碳材料。
另外,以与上述实施例3相同的方法制作了试验电极及评价用电池。
(比较例6)
将热处理工序的温度(热处理温度)设为1800℃。
除此之外,以与上述实施例3相同的方法制作了碳材料。
另外,以与上述实施例3相同的方法制作了试验电极及评价用电池。
(比较例7)
将热处理工序的温度(热处理温度)设为1800℃。
除此之外,以与上述实施例7相同的方法制作了碳材料。
另外,以与上述实施例7相同的方法制作了试验电极及评价用电池。
[密度、比表面积及总细孔容积的测定]
对于实施例1~8及比较例1~7,测定了碳材料的密度、比表面积和总细孔容积。
使用超比重计(Quantachrome社制Ultrapic1200e),测定气体使用氦气,求出碳材料的密度。
使用全自动气体吸附量测定装置(Quantachrome社制AS1-MP-9),进行使用了氮气的多孔性碳材料的气体吸附测定,且通过BET多点法求出碳材料的比表面积。
另外,根据相对压力0.99下的吸附气体量求出碳材料的总细孔容积。
[充放电试验]
对于实施例1~8及比较例1~7,进行评价用电池的充放电试验,评价充放电特性。
对其方法及结果进行说明。
评价用电池的充放电试验在25℃的恒温槽内进行。
在充放电试验中进行如下实验,即、进行试验电极的充电,在停止20分钟后进行放电。
充放电对单位重量碳材料以15mA的恒流充电至与参比电极的电位差达到0V。
之后,以15mA的恒流进行20小时充电,使单位重量碳材料析出300mAh的量的锂。
析出锂时的试验电极(作用极)的电位以参比电极的锂基准计为0V以下。
之后,通过放电至与参比电极的电位差达到2V,来调查充放电特性。
计算出第1循环的放电容量除以第1循环的充电容量所得的值,将其作为第1循环充放电效率(%)。
计算出第10循环的放电容量除以第10循环的充电容量所得的值,将其作为第10循环充放电效率(%)算出。
对于实施例1~8及比较例1~7,将评价用电池的充放电试验的结果与碳材料的密度和比表面积以及总细孔容积汇总示于表1。
【表1】
[考察]
根据表1所示的结果可知,根据碳材料的结构不同,其充放电特性有很大不同。
实施例7中,碳材料的密度小至1.16g/cc。
因此,实施例7的碳材料含有大量可在内部保持锂的闭塞孔。
因此,实施例7中,第1循环充放电效率为80%,且第10循环充放电效率为91%,显示高的值。
另一方面,比较例7中,碳材料的密度为1.18g/cc。因此,比较例7的碳材料含有与实施例7同等的闭塞孔。
尽管如此,在比较例7中,第1循环充放电效率为61%,且第10循环充放电效率为84%,为低的值。
比较例7中,碳材料的比表面积高达269m2/g。
因此,闭塞孔以外的表面部和电解液的接触部位增多。因此,认为难以使锂仅在闭塞孔内析出。其结果,不能充分抑制在闭塞孔以外析出的锂与电解液的副反应。因此,认为虽然含有大量闭塞孔,但显示低的充放电效率。
根据以上的结果可知,为获得高的第1循环充放电效率及第10循环充放电效率,碳材料的比表面积需要为250m2/g以下。
在此,实施例1~8及比较例1、比较例3和比较例4中,碳材料的比表面积为250m2/g以下。
图2是表示实施例1~8及比较例1、比较例3和比较例4的评价用电池的第10循环充放电效率与碳材料的密度的关系的图。
实施例1~8中,碳材料的比表面积均为250m2/g以下,且通过氦比重瓶求得的密度为1.5g/cc以下。
另外,实施例1~8中,第10充放电效率均显示90%以上。
在此,关于比较例1、比较例3以及比较例4,碳材料的比表面积小至250m2/g以下。因此,表面部与电解液的接触部位少,能够抑制副反应。因此,第1循环充放电效率为78%以上,显示较高的值。
但是,在比较例1、比较例3以及比较例4中,通过氦比重瓶求得的密度大于1.5g/cc。
因此,可在内部保持锂的闭塞孔的量不充分。因此,不能仅在闭塞孔内保持的锂在表面部析出。由此,锂与电解液发生副反应,该副反应通过充放电循环而累积。其结果,认为在比较例1、比较例3以及比较例4中,第10循环充放电效率均小至71%以下。
根据以上的结果可知,如果碳材料的比表面积为250m2/g以下,且通过氦比重瓶求得的密度为1.5g/cc以下,则与现有的将锂用作负极的锂电池 相比,可实现高的充放电效率。即,确认到,可以使第1循环充放电效率为80%以上且第10循环充放电效率为91%以上。
另外,比较例2中,碳材料的比表面积高达250m2/g以上。因此,比较例2中,与电解液的接触部位增多。
另外,比较例2中,通过氦比重瓶求得的密度高达1.5g/cc以上。因此,比较例2中,可在内部保持锂的闭塞孔的量不充分。
根据以上的结果,比较例2中,第1循环充放电效率为54%,且第10循环充放电效率为72%,为低的值。
另外,比较例5中碳材料的比表面积为1258m2/g。
另外,比较例6中,碳材料的比表面积为484m2/g。
这样,在碳材料的比表面积极大的情况下,表面部与电解液的接触部位过多。因此,副反应非常显著。
根据以上的结果,比较例5的第1循环充放电效率为13%,比较例6的第1循环充放电效率为14%,均为显著小的值。
另外,实施例1~6及实施例8中,碳材料的比表面积为100m2/g以下。
因此,实施例1~6及实施例8中,第1循环充放电效率为82%以上,且第10循环充放电效率为93%以上,均为高的值。
另外,实施例1~6中,碳材料的总细孔容积为0.1cc/g以下。因此,在闭塞孔以外的孔内析出的锂的比例减小。
其结果,实施例1~6中,第10循环充放电效率为95%以上,均为非常高的值。
此外,实施方式中,碳材料的密度也可以尽可能地小。例如,碳材料的密度也可以为小于1.05g/cc。
例如,通过适宜选择形成闭塞孔的热处理条件,能够进一步减小碳材料的密度。
另外,实施方式中,示出了使用碳粒子作为碳材料而形成试验电极的例子。在此,实施方式中,也可以使用具有同样的碳结构的片状的碳材料 作为试验电极或负极集电体的一部分。即使在该情况下,也能够实现同样的充放电特性。
产业上的可利用性
本公开的电极材料可作为二次电池等电池的电极材料适宜地利用。
- 还没有人留言评论。精彩留言会获得点赞!