一种固体氧化物燃料电池阳极材料及其制备方法和应用
本发明涉及能源技术领域,尤其涉及一种固体氧化物燃料电池阳极材料及其制备方法和应用。
背景技术:
固体氧化物燃料电池(sofc)是发电效率高且环境友好的能量转换装置,因而被应用于各种移动和固定的发展装置中。sofc是一种可以将储存于燃料内部的化学能转化为电能的装置,不需要经过燃烧过程,不受卡诺循环的限制,具有高能量转化率、污染小、噪声小等优点。固体氧化物燃料电池阳极端的供给气体一般为氢气或者一氧化碳等还原性气体。阳极端甲烷与二氧化碳重整制氢是一种较为经济与方便的制氢技术。然而甲烷与二氧化碳重整制氢的最大问题便是在传统的阳极材料(如ni-ysz)上存在严重的积碳现象以及ni粒粗化现象,会造成阳极孔隙率降低以及催化效率降低,从而导致电池性能急剧下降,因此对催化剂表面材料的改进至关重要。
上述电池阳极积碳现象以及ni粒粗化现象是困扰现有sofc发展的两个主要问题,现阶段,固体氧化物燃料电池的研究主要集中在阳极材料上。在阳极的研究过程中,ni-ysz阳极是sofc中非常经典和最常用的固体氧化物燃料电池阳极材料,但是ni-ysz作为阳极的电池要在1000℃情况下操作,高温环境下运行会导致ch4在阳极的表面发生裂解,容易发生碳沉积会导致阳极材料失去其活性和结构遭破坏问题,从而导致电池性能的衰减。
lscm(laxsr1-xcrymn1-yo3-δ)是一种兼有离子导电与电子导电的新型复合型钙钛矿材料,它主要用于固体氧化物燃料电池阳极端。而现有技术中通过固相法合成lscm的制备方案流程复杂且不易操作;且通过甘氨酸-硝酸盐法制备lscm的过程中粉末会剧烈膨胀导致收集困难且会浪费原材料。
技术实现要素:
为了解决上述现有阳极材料的不足,本发明提供一种固体氧化物燃料电池阳极材料及其制备方法和应用,本发明的电池阳极材料能提高甲烷重整反应的催化活性、降低sofc阳极的积碳现象,且其制备流程简单,安全易操作。
本发明是通过以下技术方案实现的:
本发明的第一个目的是提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:
将铜源、镍源及lscm粉末均匀分散于水溶剂中,再加入碱直至反应无蓝色絮状沉淀生成后,即确保铜源中的铜离子沉淀完全,获得中间产物,随后将中间产物于600~700℃烧结0.5~3h,获得前驱体,命名为cuo-nio-lscm;
在氢气氛围下,将前驱体于600~700℃保温0.5~3h,即得所述固体氧化物燃料电池阳极材料,命名为cu-ni-lscm;
所述lscm的通式为laxsr1-xcrymn1-yo3-δ,其中,x=0.2~0.8,y=0.4~0.6。
进一步地,所述铜源和所述镍源的总质量与lscm粉末的质量比为1:1~2。
进一步地,所述铜源为硝酸铜;所述镍源为硝酸镍;所述碱为氢氧化钠或氢氧化钾。
进一步地,所述硝酸铜和所述硝酸镍的总量与lscm粉末的质量比为1:1.5。
进一步地,所述氢气的流速为45~55ml/min。
进一步地,将铜源、镍源及lscm粉末在70~90℃的温度下,搅拌均匀分散于水溶剂中。
进一步地,所述lscm粉末是按照以下步骤制得:
按照锶:镧:铬:锰为1:1~4:1~3:1~3的元素摩尔比,称取硝酸锶、硝酸镧、硝酸铬及硝酸锰,加水搅拌溶解至溶液呈均相;加入柠檬酸,搅拌均匀,并将其加热沸腾至发生自燃烧,得到燃烧产物;
收集燃烧产物并将其进行煅烧处理,得到lscm粉末。
进一步地,所述镧、锶、铬及锰的总元素摩尔量与所述柠檬酸的摩尔比为:1:1~3。
进一步地,所述煅烧处理是在1000~1500℃的温度下煅烧2~6h。
本发明的第二个目的是提供一种根据上述制备方法制成的固体氧化物燃料电池阳极材料。
进一步地,所述阳极材料具有较高的比表面积、抗高温烧结能力以及抗积碳能力。
本发明的第三个目的是提供一种上述固体氧化物燃料电池阳极材料lscm在催化甲烷与二氧化碳干重整制氢中的应用。
本发明与现有技术相比,具有以下有益效果:
本发明通过使cu、ni形成合金,ni能增强导电性能又具有催化能力,且cu对石墨层具有较好的亲和力可以抑制石墨层在cu颗粒表面的富集,从而增强本发明阳极材料的催化性能,且本发明的阳极材料cu-ni-lscm是通过考虑催化剂对化学反应(与ni相比)的优越性,对碳沉积的抗性(cu,lscm)和增强电导率而开发的。
本发明的制备过程简单,制备周期短,原料价格低廉、安全,所需设备简单,适合大规模生产。
本发明与运用固相法合成lscm相比,制备流程更加简单,更容易操作,且制成的lscm的比表面积比固相法制成的lscm大。
本发明通过柠檬酸-硝酸盐法制备lscm,采用低温燃烧合成技术,制备方法稳定且节约原材料,避免了甘氨酸-硝酸盐法制备lscm的过程中粉末会剧烈膨胀导致前驱体收集困难以及浪费原材料等问题的发生。
附图说明
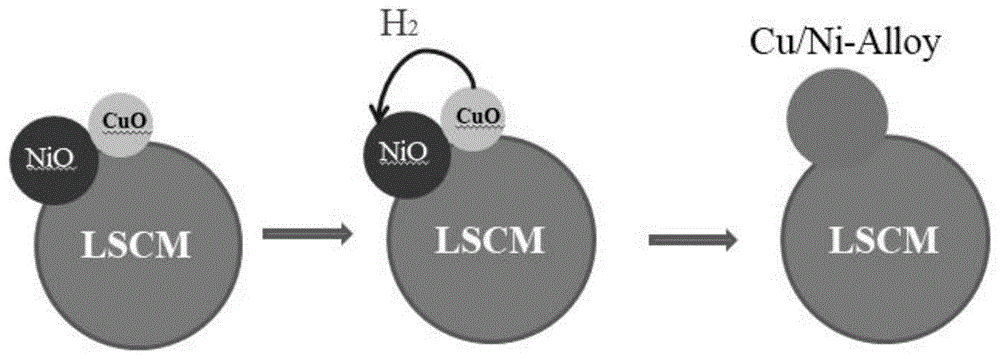
图1为实施例1-3的前驱体还原得到阳极材料的原理示意图;
图2为本发明的阳极材料在催化甲烷制氢反应中,甲烷及二氧化碳转化率的柱状图;其中,case1为对比例1的阳极材料催化剂在甲烷制氢反应中,甲烷及二氧化碳转化率的柱状图;case2为实施例1的阳极材料催化剂在甲烷制氢反应中,甲烷及二氧化碳转化率的柱状图;case3为实施例2的阳极材料催化剂在甲烷制氢反应中,甲烷及二氧化碳转化率的柱状图;case4为实施例3的阳极材料催化剂在甲烷制氢反应中,甲烷及二氧化碳转化率的柱状图;case2为实施例4的阳极材料催化剂在甲烷制氢反应中,甲烷及二氧化碳转化率的柱状图。
图3为对比例1及实施例2的阳极材料经催化甲烷制氢反应后所得材料的xrd图谱;
图4为对比例1及实施例2的阳极材料经催化甲烷制氢反应后所得材料经过德拜-谢乐公式计算出的镍(111)晶面尺寸图;
图5为本发明的阳极材料经催化甲烷制氢反应后所得材料中活性颗粒的fe-sem图;其中图5a为对比例1的阳极材料经催化甲烷制氢反应后所得材料中活性颗粒的fe-sem图;其中图5b为实施例1的阳极材料经催化甲烷制氢反应后所得材料中活性颗粒的fe-sem图;其中图5c为实施例2的阳极材料经催化甲烷制氢反应后所得材料中活性颗粒的fe-sem图;其中图5d为实施例3的阳极材料经催化甲烷制氢反应后所得材料中活性颗粒的fe-sem图;
图6为本发明的阳极材料经催化甲烷制氢反应后所得材料的透射电镜图(200nm尺寸);其中,图6a为对比例1的阳极材料经催化甲烷制氢反应后所得材料的透射电镜图;图6b为本发明实施例2的阳极材料经催化甲烷制氢反应后所得材料的透射电镜图;
图7为本发明的阳极材料经催化甲烷制氢反应后所得材料的透射电镜图(3μm尺寸);其中,图7a为对比例1的阳极材料经催化甲烷制氢反应后所得材料的透射电镜图;图7b为本发明实施例2的阳极材料经催化甲烷制氢反应后所得材料的透射电镜图;图7c为图7b画框处的局部放大图;
图8为本发明对比例1和实施例2的阳极材料经催化甲烷制氢反应后所得材料的热重图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述。
实施例1
本实施例提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:
按照锶:镧:铬:锰=3:7:5:5的摩尔比,称取sr(no3)2·6h2o、la(no3)3·6h2o、cr(no3)2·6h2o以及mn(no3)2,置于烧杯中,加入去离子水搅拌溶解至溶液呈混合均相;再按照镧、锶、铬及锰总元素摩尔量的1.5倍称取相应质量的柠檬酸,然后在磁力搅拌器中搅拌2小时搅拌均匀,然后将烧杯置于电炉上加热沸腾直至发生自燃现象,收集反应后的产物并将其置于管式炉中,在1350℃的空气氛围中煅烧4小时,得到lscm粉末laxsr1-xcrymn1-yo3-δ中x=0.7,y=0.5,即本实施例的lscm粉末的结构式为la0.7sr0.3cr0.5mn0.5o3-δ。
称取6g煅烧后的产物lscm粉末于烧杯中,并加入3.43g硝酸镍和0.57g硝酸铜,加去离子水使其分散均匀,并将盛有混合溶液的烧杯置于大功率磁力搅拌器中,在80℃下搅拌2小时;随后向其加入过量的0.1g/ml氢氧化钠溶液直到不再产生蓝色絮状沉淀,沉淀完全,然后将伴有沉淀的溶液放入超声清洗器中进行超声30min,然后再进行抽滤,将滤渣用去离子水洗涤5次,完全除去样品中的硝酸盐,再次抽滤得到水洗后的产物并将其置于鼓风干燥箱中干燥12小时,然后将干燥后的产物置于管式电阻加热炉中650℃空气氛围下烧结30min得到前驱体。
将本实施例所得前驱体在高纯氮气(>99.9%)的保护下,从室温升至650℃,然后在氩气为保护气的条件下通入氢气,即以50ml/min的流量通入10%h2+10%ar,并保持1小时进行还原,即得到最终产物。
实施例2
本实施例提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:
按照锶:镧:铬:锰=3:7:5:5的摩尔比,称取sr(no3)2·6h2o、la(no3)3·6h2o、cr(no3)2·6h2o以及mn(no3)2,置于烧杯中,加入去离子水搅拌溶解至溶液呈混合均相;再按照镧、锶、铬及锰的总元素摩尔量的1.5倍量,称取相应质量的柠檬酸,然后在磁力搅拌器中搅拌2小时搅拌均匀,然后将烧杯置于电炉上加热沸腾直至发生自燃现象,收集反应后的产物并将其置于管式炉中,在1350℃的空气氛围中煅烧4小时,得到结构式为la0.7sr0.3cr0.5mn0.5o3-δ的lscm粉末。
称取6g煅烧后的产物lscm粉末于烧杯中,并加入3g硝酸镍和1g硝酸铜以及去离子水,将盛有混合溶液的烧杯置于大功率磁力搅拌器中,在80℃下搅拌2小时;随后向其加入过量的0.1g/ml氢氧化钠溶液直到沉淀完全,然后将伴有沉淀的溶液放入超声清洗器中进行超声30min,然后再进行抽滤,将滤渣用去离子水洗涤5次,完全除去样品中的硝酸盐,再次抽滤得到水洗后的产物并将其置于鼓风干燥箱中干燥12小时,然后将干燥后的产物置于管式电阻加热炉中650℃空气氛围下烧结30min得到前驱体。
将本实施例所得前驱体在高纯氮气(>99.9%)的保护下,从室温升至650℃,然后在氩气为保护气的条件下通入氢气,即以50ml/min的流量通入10%h2+10%ar,并保持1小时进行还原,即得到最终产物。
实施例3
本实施例提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:
按照锶:镧:铬:锰=3:7:5:5的摩尔比,称取sr(no3)2·6h2o、la(no3)3·6h2o、cr(no3)2·6h2o以及mn(no3)2,置于烧杯中,加入去离子水搅拌溶解至溶液呈混合均相;再按照镧、锶、铬及锰的总元素摩尔量的1.5倍量,称取相应质量的柠檬酸,然后在磁力搅拌器中搅拌2小时搅拌均匀,然后将烧杯置于电炉上加热沸腾直至发生自燃现象,收集反应后的产物并将其置于管式炉中,在1350℃的空气氛围中煅烧4小时,得到lscm粉末。
称取6g煅烧后的产物lscm粉末于烧杯中,并加入2g硝酸镍和2g硝酸铜以及去离子水,将盛有混合溶液的烧杯置于大功率磁力搅拌器中,在80℃下搅拌2小时;随后向其加入过量的0.1g/ml氢氧化钠溶液直到沉淀完全,然后将伴有沉淀的溶液放入超声清洗器中进行超声30min,然后再进行抽滤,将滤渣用去离子水洗涤5次,完全除去样品中的硝酸盐,再次抽滤得到水洗后的产物并将其置于鼓风干燥箱中干燥12小时,然后将干燥后的产物置于管式电阻加热炉中650℃空气氛围下烧结30min得到前驱体。
将本实施例所得前驱体在高纯氮气(>99.9%)的保护下,从室温升至650℃,然后在氩气为保护气的条件下通入氢气,即以50ml/min的流量通入10%h2+10%ar,并保持1小时进行还原,即得到最终产物。
实施例4
本实施例提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:按照锶:镧:铬:锰=3:7:5:5的摩尔比,称取sr(no3)2·6h2o、la(no3)3·6h2o、cr(no3)2·6h2o以及mn(no3)2,置于烧杯中,加入去离子水搅拌溶解至溶液呈混合均相;再按照镧、锶、铬及锰的总元素摩尔量的1.5倍量,称取相应质量的柠檬酸,然后在磁力搅拌器中搅拌2小时搅拌均匀,然后将烧杯置于电炉上加热沸腾直至发生自燃现象,收集反应后的产物并将其置于管式炉中,在1350℃的空气氛围中煅烧4小时,得到得到结构式为la0.7sr0.3cr0.5mn0.5o3-δ的lscm粉末。
称取6g煅烧后的产物lscm粉末于烧杯中,并加入4g硝酸铜以及去离子水,将盛有混合溶液的烧杯置于大功率磁力搅拌器中,在80℃下搅拌2小时;随后向其加入过量的0.1g/ml氢氧化钠溶液直到沉淀完全,然后将伴有沉淀的溶液放入超声清洗器中进行超声30min,然后再进行抽滤,将滤渣用去离子水洗涤5次,完全除去样品中的硝酸盐,再次抽滤得到水洗后的产物并将其置于鼓风干燥箱中干燥12小时,然后将干燥后的产物置于管式电阻加热炉中650℃空气氛围下烧结30min得到前驱体。
将本实施例所得前驱体在高纯氮气(>99.9%)的保护下,从室温升至650℃,然后在氩气为保护气的条件下通入氢气,即以50ml/min的流量通入10%h2+10%ar,并保持1小时进行还原,即得到最终产物。
实施例5
本实施例提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:
按照锶:镧:铬:锰=1:1:1:1的摩尔比,称取sr(no3)2·6h2o以及相应质量的la(no3)3·6h2o、cr(no3)2·6h2o及mn(no3)2,置于烧杯中,加入去离子水搅拌溶解至溶液呈混合均相;再按照镧、锶、铬及锰的总元素摩尔量的1倍量,称取相应质量的柠檬酸,然后在磁力搅拌器中搅拌2小时搅拌均匀,然后将烧杯置于电炉上加热沸腾直至发生自燃现象,收集反应后的产物并将其置于管式炉中,在1250℃的空气氛围中煅烧5小时,得到结构式为la0.5sr0.5cr0.5mn0.5o3-δ的lscm粉末。
称取6g煅烧后的产物lscm粉末于烧杯中,并加入3g硝酸镍和1g硝酸铜以及去离子水后,将盛有混合溶液的烧杯置于大功率磁力搅拌器中,在90℃下搅拌1小时;随后向其加入过量的0.1g/ml氢氧化钠溶液直到沉淀完全,然后将伴有沉淀的溶液放入超声清洗器中进行超声30min,然后再进行抽滤,将滤渣用去离子水洗涤5次,完全除去样品中的硝酸盐,再次抽滤得到水洗后的产物并将其置于鼓风干燥箱中干燥12小时,然后将干燥后的产物置于管式电阻加热炉中650℃空气氛围下烧结2h得到前驱体;
将所得前驱体在高纯氮气(>99.9%)的保护下,从室温升至650℃,然后在氩气为保护气的条件下通入氢气,即以50ml/min的流量通入10%h2+10%ar,并保持2小时进行还原,即得到最终产物。
实施例6
本实施例提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:
按照锶:镧:铬:锰=1:1.5:1:1.5的摩尔比,称取sr(no3)2·6h2o以及相应质量的la(no3)3·6h2o、cr(no3)2·6h2o及mn(no3)2,置于烧杯中,加入去离子水搅拌溶解至溶液呈混合均相;再按照镧、锶、铬及锰的总元素摩尔量的2倍量,称取相应质量的柠檬酸,然后在磁力搅拌器中搅拌2小时搅拌均匀,然后将烧杯置于电炉上加热沸腾直至发生自燃现象,收集反应后的产物并将其置于管式炉中,在1000℃的空气氛围中煅烧6小时,得到结构式为la0.6sr0.4cr0.4mn0.6o3-δ的lscm粉末。
称取6g煅烧后的产物lscm粉末于烧杯中,并加入2.5g硝酸镍和0.5g硝酸铜以及去离子水后,将盛有混合溶液的烧杯置于大功率磁力搅拌器中,在70℃下搅拌3小时;随后向其加入过量的0.1g/ml氢氧化钠溶液直到沉淀完全,然后将伴有沉淀的溶液放入超声清洗器中进行超声30min,然后再进行抽滤,将滤渣用去离子水洗涤5次,完全除去样品中的硝酸盐,再次抽滤得到水洗后的产物并将其置于鼓风干燥箱中干燥12小时,然后将干燥后的产物置于管式电阻加热炉中600℃空气氛围下烧结3h得到前驱体;
将所得前驱体在高纯氮气(>99.9%)的保护下,从室温升至600℃,然后在氩气为保护气的条件下通入氢气,即以45ml/min的流量通入10%h2+10%ar,并保持1小时进行还原,即得到最终产物。
实施例7
本实施例提供一种固体氧化物燃料电池阳极材料的制备方法,包括以下步骤:
按照锶:镧:铬:锰=1:3:3:2的摩尔比,称取sr(no3)2·6h2o以及相应质量的la(no3)3·6h2o、cr(no3)2·6h2o及mn(no3)2,置于烧杯中,加入去离子水搅拌溶解至溶液呈混合均相;再按照镧、锶、铬及锰的总元素摩尔量的3倍量,称取相应质量的柠檬酸,然后在磁力搅拌器中搅拌2小时搅拌均匀,然后将烧杯置于电炉上加热沸腾直至发生自燃现象,收集反应后的产物并将其置于管式炉中,在1500℃的空气氛围中煅烧2小时,得到结构式为la0.75sr0.25cr0.6mn0.4o3-δ的lscm粉末。
称取6g煅烧后的产物lscm粉末于烧杯中,并加入4g硝酸镍和2g硝酸铜以及去离子水后,将盛有混合溶液的烧杯置于大功率磁力搅拌器中,在90℃下搅拌1小时;随后向其加入过量的0.1g/ml氢氧化钾溶液直到沉淀完全,然后将伴有沉淀的溶液放入超声清洗器中进行超声30min,然后再进行抽滤,将滤渣用去离子水洗涤5次,完全除去样品中的硝酸盐,再次抽滤得到水洗后的产物并将其置于鼓风干燥箱中干燥12小时,然后将干燥后的产物置于管式电阻加热炉中700℃空气氛围下烧结1h得到前驱体;
将所得前驱体在高纯氮气(>99.9%)的保护下,从室温升至700℃,然后在氩气为保护气的条件下通入氢气,即以55ml/min的流量通入10%h2+10%ar,并保持0.5小时进行还原,即得到最终产物。
实施例8
本实施例提供一种上述固体氧化物燃料电池阳极材料在催化甲烷与二氧化碳干重整制氢中的应用。
对比例1
与实施例1相同,不同之处在于,原料中未添加铜源,获得一种阳极材料(ni-lscm)。
为了说明按照本发明的制备方法制得的阳极材料的催化性能,本发明进行了催化试验,并对经过催化反应后得到的材料进行了测试,具体测试情况如下:
测试部分
(一)催化试验:
分别称取600mg对比例1及实施例1-实施例4中的前驱体粉末置于内径为11mm的催化反应管内,在高纯氮气(>99.9%)的保护下从室温升至650℃,然后在氩气为保护气的条件下通入氢气,即以50ml/min的流量通入10%h2+10%ar,保持1小时进行还原,即分别得到对比例1及实施例1-实施例4相应的最终产物。
还原后,再次通入高纯氮气吹扫管内残余氢气,分别以上述步骤得到的对比例1及实施例1-实施例4的最终产物为催化剂,以50ml/min的流量通入甲烷与二氧化碳的混合气体(10%ch4+10%co2+80%ar)完成催化反应过程,其中催化反应持续13小时。
(二)催化试验下的燃料转化率:
通过烟气分析仪对上述出口处气体进行收集检测。相关反应方程式如下:
ch4→c+2h2
图2为上述催化试验中,甲烷及二氧化碳转化率的柱状图,且从图中2可以看到,在650℃下,对比例1及实施例1-实施例4阳极材料催化的甲烷的最大转化率分别为37.5%、45.8%、44.62%、34.01%以及1.85%。且最大燃料转化率出现在实施例1,而实施例4中燃料转化率最低。
(三)催化后材料的积碳量:
表1为上述催化试验反应后,对比例1及实施例1-4所得的催化后材料积碳后的质量,以及用h2除去积碳后的催化后材料的质量,可以看到,经过甲烷干重整后的积碳量随着cu的引入积碳速率明显下降。
表1650℃下经过甲烷干重整后的积碳量
其中,a1表示经过催化反应后的催化后材料(积碳后)质量;表示用h2除去积碳后的催化后材料质量。
(四)催化后材料的xrd测试:
本发明为了探究cu的加入对产物催化性能的影响,对对比例1(ni-lscm)和实施例2(cu-ni-lscm)所得的催化后材料进行了xrd测试,结果如图3所示。由图4可以看出ni-lscm与cu-ni-lscm的镍(111)晶面晶粒尺寸分别为36.95nm以及31.10nm,也就是说,cu-ni-lscm相较于ni-lscm有着更好的抗烧结能力。此外,经过650℃还原后的cu-ni-lscm以及ni-lscm的比表面积分别为14.60m2/g以及3.56m2/g。
(五)催化后材料的fe-sem测试:
为了研究引入cu之后对cu-ni-lscm活性颗粒形貌大小的影响,本发明使用fe-sem对对比例1及实施例1-实施例4阳极材料的形貌进行检测。如图5所示,对比例1及实施例1-实施例4的阳极材料经催化甲烷制氢反应后所得材料中活性颗粒的fe-sem图。从图5中可以看到:随着cu的引入,活性颗粒的颗粒大小明显减小,分散性能得以提升,尤其是在实施例1和实施例2中。
(六)催化后材料的透射电镜测试:
图6为对比例1及实施例2的阳极材料经催化甲烷制氢反应后所得材料在200nm尺寸下的透射电镜图,对比两图可以看到,两图均出现了丝状碳(碳纳米管)。且对比例1中无论是活性颗粒大小还是碳纳米管的直径都大于实施例2。除此之外,对比例1中出现了较为强烈的团聚现象。对比两图可以看到,随着cu的引入会有更多小碎片状的催化剂以及积碳的产生(如图5b所示)。一定量的铜的引入在一定程度上增加了燃料的转换率,因为随着cu的引入,小碎片更多产生致使分散性地提高,这将大大增加气体分子与活性颗粒ni的接触几率。然而过多cu的引入,虽然小碎片增多,但是却降低了气体分子与活性颗粒ni的接触几率最终导致转化率下降。
图7a和图7b分别为对比例1及实施例2的阳极材料经催化甲烷制氢反应后所得材料在3微米尺寸下的透射电镜图,可以看出:为对比例1与实施例2均出现的碳纳米管,且无论是活性颗粒尺寸还是碳纳米管的直径,对比1均高于实施例2。在对比例1中,由甲烷干重整过程产生的碳纳米管的直径介于104.6nm到196nm之间。且大多数活性颗粒的直径都大于168nm。然而在实施例2中,碳纳米管的直径介于27.21nm到38.29nm之间。且实施例2中的大多数活性颗粒的直径都小于121nm,介于40nm到70nm之间。而对比例1中大直径颗粒之间的相互作用会降低气体分子与颗粒之间的接触几率从而降低催化剂的催化性能。在引入铜之后,实施例2有着非常好的催化性能。且对于新鲜催化剂(fe-sem),实施例2中的直径大小变化并不强烈。这显示了实施例2较好的抗碳沉积,抗金属烧结以及较好的催化性能。
(七)催化后材料的热重测试:
图8为对比例1及实施例2的阳极材料经催化甲烷制氢反应后所得材料在3微米尺寸下的热重图,可以看出:ni-lscm与cu-ni-lscm的质量损失量/(沉积碳量)分别为36.76%与28.94%。即铜的引入降低了沉积碳量。
综上,本发明通过使cu、ni形成合金,ni能增强导电性能又具有催化能力,且cu对石墨层具有较好的亲和力可以抑制石墨层在cu颗粒表面的富集,从而增强本发明阳极材料的催化性能,且本发明的阳极材料cu-ni-lscm是通过考虑催化剂对化学反应(与ni相比)的优越性,对碳沉积的抗性(cu,lscm)和增强电导率而开发的。且本发明的制备过程简单,制备周期短,原料价格低廉、安全,所需设备简单,适合大规模生产。
本发明与运用固相法合成lscm相比,制备流程更加简单,更容易操作,且制成的lscm的比表面积比固相法制成的lscm大。
本发明通过柠檬酸-硝酸盐法制备lscm,采用低温燃烧合成技术,制备方法稳定且节约原材料,避免了甘氨酸-硝酸盐法制备lscm的过程中粉末会剧烈膨胀导致前驱体收集困难以及浪费原材料等问题的发生。
显然,上述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!