防粘连材料的制作方法
本发明涉及一种防粘连材料。特别涉及由水溶性高分子及脂肪族酯构成的固态或半固态基体、与作为该基体所含抗氧化物质的由抗坏血酸或其衍生物构成的防粘连材料。
背景技术:
:本专利申请人以提供防粘连材料为目的,在专利文献1(日本专利第5686297号)公开了新颖的防粘连材料的发明,其中,于活体内,(a)贴附于活体组织时的分解性及(b)防粘连性能均优异,且较已知(c)湿润时的处置性及(d)贴附于活体组织时的密接性均更优异。专利文献1中记载的防粘连材料的主旨为,于基体层中使用水溶性高分子,且在该基体层的至少一面或双面上配置由含活体分解性聚脂肪族酯的极薄膜(使用分光式椭圆偏光仪依波长380nm~900nm测定时,上述被覆层的光学厚度为27nm以上且小于160nm)构成的被覆层。另一方面,专利文献2中公开有:以海藻糖为有效成分,且含有作为抗氧化物质的抗坏血酸衍生物的防组织粘连液的发明。[
背景技术:
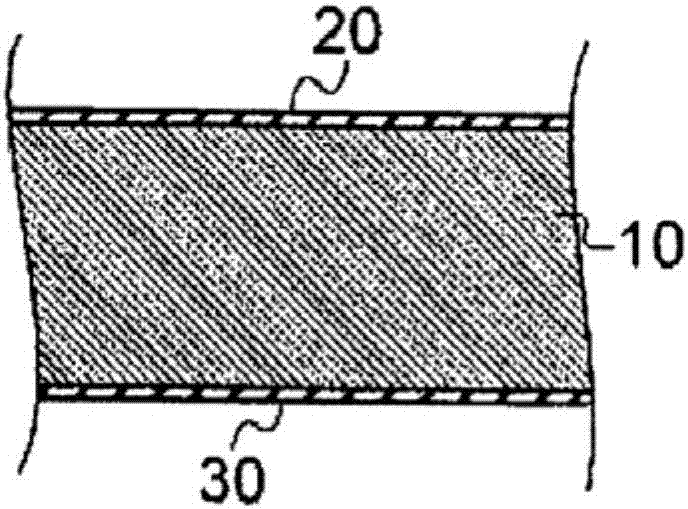
文献][专利文献]专利文献1:日本专利第5686297号(权利要求书、图1至图4)专利文献2:日本专利第4447640号(权利要求书、权利要求1至3)技术实现要素:(发明所要解决的问题)专利文献1中记载的发明,虽为在活体内(a)贴附活体组织时的分解性、(c)湿润时的处置性及(d)贴附于活体组织时的密接性等数方面而言提供具优异特性的防粘连材料的发明,但经本发明者等更进一步研究后,发现就确保更充分(b)防粘连性能方面、或以提供更优异防粘连材料为目的方面而言,尚残留有数个待获改善的课题。专利文献2中记载的组织防粘连液属于喷雾方式,就剂形而言,不同于专利文献1中记载的薄膜或薄片状防粘连材料,结果防粘连功能的表现机制便有所不同。(解决问题的技术手段)于是,本发明者为解决上述课题,经深入钻研,结果达成下述发明。[1]根据本发明所提供的防粘连材料,在由水溶性高分子及聚脂肪族酯构成的固态或半固态基体中,含有抗坏血酸或抗坏血酸衍生物作为抗氧化物质。[2]再者,根据本发明所提供的防粘连材料,在[1]记载的防粘连材料中,上述固态基体为从薄膜状、薄片状及筛网状的任一者中选择的形态;上述薄膜状、上述薄片状及筛网状的形态为,实质由该基体形成的单层构造、或具有在该基体的基体层上更进一步设置由聚脂肪族酯构成的被覆层的层积构造;或上述筛网状的形态具有复合体所构成的纤维状构造,且其基重为0.8g/m2~830g/m2,该复合体为,将固态的水溶性高分子及聚脂肪族酯构成的基体形成为棒状而得到。[3]再者,根据本发明所提供的防粘连材料,在[1]记载的防粘连材料中,半固态基体为包含胶质状的凝胶状形态,具有单层构造或层积构造,37℃的粘度为100pa·s至1,000,000pa·s。[4]再者,根据本发明所提供的防粘连材料,在[2]记载的防粘连材料中,在该基体的基体层上具有被覆层的层积构造以3层形成,该3层为,在该基体层的双面上分别具有被覆层的双面被覆层及基体层。[5]再者,根据本发明所提供的防粘连材料,在[4]记载的防粘连材料中,当对上述被覆层的厚度使用分光式椭圆偏光仪以波长380nm~900nm测定时,上述被覆层的光学厚度为50nm以上且小于7000nm。[6]再者,根据本发明所提供的防粘连材料,在[1]记载的防粘连材料中,相对于构成基体或基体层的基材料重量(质量),含有0.5(w/w)%以上~10(w/w)%以下的抗坏血酸及其衍生物。[7]再者,根据本发明所提供的防粘连材料,将[1]至[6]中任一项记载的防粘连材料浸渍于牛血浆时,其24小时后的ph为7.5~6.0。[8]再者,根据本发明所提供的防粘连材料,在[2]至[7]中任一项记载的防粘连材料中,上述被覆层具备有:在上述基体层的一侧面上所配置的第1被覆层、及在上述基体层的另一侧面上所配置的第2被覆层,上述第1被覆层与第2被覆层为由同一材料料所构成。[9]再者,根据本发明所提供的防粘连材料,在[2]至[7]中任一项记载的防粘连材料中,上述被覆层具备有:在上述基体层的一侧面上所配置的第1被覆层、及在上述基体层的另一侧面上所配置的第2被覆层,上述第1被覆层与上述第2被覆层由不同材料所构成。[10]再者,根据本发明所提供的防粘连材料,在[1]至[9]中任一项记载的防粘连材料中,上述水溶性高分子为多糖类、蛋白质或合成高分子。[11]再者,根据本发明所提供的防粘连材料,在[1]至[10]中任一项记载的防粘连材料中,构成上述基体的水溶性高分子(a)与聚脂肪族酯(b)的重量比例ω(=a/b)为1~99/99~1。[12]再者,根据本发明所提供的防粘连材料,在实质由水溶性高分子构成的固态或半固态基体中,含有抗坏血酸或抗坏血酸衍生物作为抗氧化物质,或者更进一步在该基体的基体层双面上分别具有由聚脂肪族酯构成的被覆层。[13]再者,根据本发明所提供的防粘连材料,在[2]至[12]中任一项记载的防粘连材料中,上述[1]的抗氧化物质含有属于植物的脂溶性色素的类胡萝卜素类或含多酚类的源自植物的抗氧化物质。(发明的效果)本发明的防粘连材料的特征在于,具有下述构成:基本上在由水溶性高分子及聚脂肪族酯构成的固态或半固态基体中,含有抗坏血酸或抗坏血酸衍生物作为抗氧化物质。本发明防粘连材料通过具有该构成,而达成下述事项:<1>由聚脂肪族酯及水溶性高分子构成的基体发挥作为创伤面与创伤面的物理性屏障(physicalbarrier)的功能,且利用连续地缓释于创伤面的抗坏血酸或其衍生物促进创伤面治愈,由此,高效地表现出具有叠加效应的防粘连功能。<2>再者,基体形状为具有固态(薄膜状、薄片状、筛网状)或半固态(包含胶质状的凝胶状形态),且使此种形状的基体或基体层中含有抗坏血酸或抗坏血酸衍生物,因而可确保上述物理性屏障功能,且能可靠地在该创伤面上表现出促进创伤面治愈效果。基体或基体层中所含有的抗坏血酸等会与形成具粘性溶液的水溶性高分子一起逐渐溶出,并滞留于基体表面(创伤面附近),而对促进治愈效果产生贡献。<3>再者,在固相或半固态基体中调配抗坏血酸或抗坏血酸衍生物而使用的优点,为抗坏血酸可对该创伤面持续地缓释。一般而言,创伤治愈通常至少24~48小时,依情况也会需要1~2周,在该所需期间内,抗坏血酸或抗坏血酸衍生物能连续地缓释于创伤面而呈持续存在的状态。另外,专利文献1中记载的防粘连材料,过度在意加速基体层的分解吸收性,并未考虑这些抗坏血酸或抗坏血酸衍生物的缓释,即便添加作为防粘连材料成分(创伤治愈促进成分)的抗坏血酸或抗坏血酸衍生物的情况,虽经足够期间,但该抗坏血酸或抗坏血酸衍生物仍无法缓释,会有无法获得充分防粘连效果的可能性。即,专利文献1中记载的防粘连材料中,基体层为由水溶性高分子构成,由于该基体层在水中较快速溶解并被分解吸收,因而没有从该基体层缓释抗坏血酸的考虑余地。再者,如专利文献2中记载的组织防粘连液那样,为呈液体状,同样地无法考虑药剂缓释、药剂持续地缓释于创伤面,不同于本发明所产生的防粘连功能的表现机制。关于此点,经本发明者等深入钻研,结果确认到依后述代表例所表示的适当形状的情况,能确保最佳的缓释性。附图说明图1为用于说明本发明代表实施形态的防粘连材料1的图,图1(a)为防粘连材料1的立体图,图1(b)为其一部分的放大剖视图。图2为在防粘连材料1的基体层所添加的抗坏血酸的缓释的随时间变化评价图。具体实施方式(定义)为了明确地说明本发明的防粘连材料,针对本发明的“基体”、“基体层”、“被覆层”设置以下定义。所谓“基体”为构成防粘连材料主要的基质部件,由水溶性高分子(a)及聚脂肪族酯(b)构成,于其中添加并含有抗坏血酸或抗坏血酸衍生物(以下有时称为“抗坏血酸等”),由此构成防粘连材料。该防粘连材料置于活体内时,该基体在一定期间内保持形状的状态下缓释抗坏血酸等。具体而言,该基体为了在活体内贴附于脏器,通常形成单层构造或层积构造的层构造,尤其将形成单层构造时的基体称为“基体层”,又,在层积构造中具备有以被覆该“基体层”表面(双面或单面)的方式所形成的外层(称为“被覆层”)。通常,基体层为相对较厚的层,相较于基体层,被覆层构成为较薄的层。“被覆层”为如后述那样的层,主要为控制来自基体层的抗坏血酸等的缓释,又,当强度上保持基体层使防粘连材料置于活体中时,具有保持形状的功能。根据上述,所谓“基体”属于添加抗坏血酸等的基质部件,且为由此缓释该抗氧化剂的物质,因而不仅“基体层”,就连“被覆层”也对应于“基体”(参照后记实施例5-6)。又,本发明的防粘连材料的基质部件,根据定义由水溶性高分子(a)及聚脂肪族酯(b)构成,但当为单层构造的情况,该层由水溶性高分子(a)及聚脂肪族酯(b)的双成分组成物(a/b)所构成,另一方面,当为层积构造的情况,可设为例如典型地由“基体层”与“被覆层”所构成,则“基体层”实质上仅由水溶性高分子(a)构成,“被覆层”实质上仅由聚脂肪族酯(b)构成(参照后记实施例1-4)。以下,针对本发明的防粘连材料,根据图1所示代表实施形态进行说明。但是,本发明的实施形态并不局限于图1所示实施形态,在具备本发明特征的核心发明特定事项的前提下,可为各种实施形态。首先,针对本发明概要进行说明,本发明的防粘连材料在使由水溶性高分子及聚脂肪族酯构成的所谓固态基体中,含有抗坏血酸或抗坏血酸衍生物(以下有时称为“抗坏血酸等”)。防粘连材料的形态,具体而言,固态基体为从薄膜状、薄片状及筛网状中选择的任一者,半固态基体为包含胶质状的凝胶状形态。当固态基体为薄膜状、薄片状的情况,其构造基本上为由单层构造所构成的基体层,但视所需也可如下述,设为在基体层上更进一步具备被覆层的层积构造。即,此种层积构造的情况,基体最典型地由:由水溶性高分子构成的基体层、及形成于其上面且由聚脂肪族酯构成的被覆层所构成。另外,一般而言,薄膜状与薄片状二者并没有明确区分,本发明中将厚度小于200μm的情况设为薄膜状,而薄片状为设定为厚度达200μm以上的情况。筛网状的情况为复合体所构成的纤维状构造体,且其基重设定为0.8g/m2~830g/m2范围内,该复合体为,将固态的由水溶性高分子与聚脂肪族酯构成的基体形成为棒状而得到。当固态基体为半固态的情况,便为包含胶质状的凝胶状形态,具有单层构造或层积构造,且其在37℃下的粘度为100pa·s至1,000,000pa·s,该范围的物性能表现出有效的物理性屏障功能。任一形态的基体均为由水溶性高分子及脂肪族酯构成的所谓固态或半固态基体,含有抗坏血酸等,这些的基础在于,成为创伤面与创伤面的物理性屏障,以及有效率地可靠发挥缓释于该创伤面的抗坏血酸等促进创伤面治愈所产生的叠加防粘连功能。[代表实施形态说明]图1所示为用于说明本发明代表实施形态的防粘连材料1的图。本发明并不局限于下述代表实施形态。虽未图示,也可设为仅在如专利文献1的图2所示基体层单面上形成被覆层的情况,或者由在如图4所示基体层的双面上形成被覆层,再将其形成为棒状复合体所构成的纤维状(筛网状)构造形态。图1(a)为防粘连材料1的立体图,图1(b)为防粘连材料1的一部分的放大剖视图。另外,图1(a)及图1(b)中,为求轻易理解发明,基体层10的层厚、以及第1被覆层20与第2被覆层30相对于基体层10的层厚,有某程度夸张的表示。代表实施形态的防粘连材料1为如图1所示,具备有:由薄膜状构成的基体层10、视需要设置在基体层10的一侧面上所配置的第1被覆层20、以及在基体层10的另一侧面上所配置的第2被覆层30。(基体的基本构成)本发明防粘连材料的特征在于:当基体为单层构造的情况,便由水溶性高分子(a)与活体分解性聚脂肪族酯(b)构成的二成分树脂组合物(树脂的均匀混合物)所构成;当层积构造的情况,便具备有:由水溶性高分子(a)构成的基体层、与由活体分解性聚脂肪族酯(b)构成的固态或半固态的被覆层。针对此点而言,彻底不同于基底为仅由水溶性高分子(单一成分)构成的基体层的专利文献1所公开的已知产品。由于本发明的基体为由水溶性高分子与活体分解性聚脂肪族酯构成的二成分组合物的单层构造,或由上述层积构造构成,因而当其设置于活体中时,聚脂肪族酯部分(不同于水溶性高分子部分)不会迅速分解,能在相当长期间保持层状(薄膜状或薄片状)形态(薄膜形状保持部分)。另一方面,因为水溶性高分子部分会与属于形状保持部分的活体分解性聚脂肪族酯相互混合、或者相互接触存在(不会如单一成分层的情况那样比较迅速溶解),而从该基体表面接触到活体液的部分逐渐溶出。如此从基体逐渐溶出(缓释性)的水溶性高分子成分,可达对创伤面促进治愈的作用。(抗氧化物质/抗坏血酸等)本发明防粘连材料的特征在于:在如此所构成的二成分组合物构成的单层构造基体、或由上述层积构造构成的基体中,含有抗坏血酸或抗坏血酸衍生物作为抗氧化物质。根据本发明者等的研究,当在基体中调配抗坏血酸等,企图从该基体缓释时,如专利文献1所记载,仅由聚三葡萄糖等水溶性高分子构成的基体层的情况,如上述,基体层自体在较短时间便会溶解,无法达成作为基质层(形态保持层)的功能,因而无法实现充分的缓释性。另一方面,本发明中由水溶性高分子与聚脂肪族酯构成的二成分组合物所构成的单层构造基体、或层积构造基体的情况,活体分解性聚脂肪族酯可达基质(骨架形成)的功能,所以基体能长时间保持其形态。另一方面,本发明在基体中所调配的抗坏血酸等,会从基体表面溶出,由该二成分组合物构成的单层构造基体、或由层积构造构成的基体,如上述,例如水溶性高分子部分会与属于形状保持部分的活体分解性聚脂肪族酯相互混合,或者相互接触存在,并从该基体表面逐渐溶出。该溶出的水溶性高分子部分,被认为会与(该部分所含有)抗坏血酸等一起溶出。如此,从基体溶出的水性高分子成分,便一起与抗坏血酸等逐渐溶出,并经常存在于创伤面,所以可认为达较高的治愈促进作用。(缓释性的控制)本发明在基体中所含有抗坏血酸等的缓释机制可认为如上述,因而抗坏血酸等的缓释速度也可广范围控制。即,由水溶性高分子(a)与活体分解性聚脂肪族酯(b)构成的二成分组合物所构成的单层构造基体、或层积构造中,水溶性高分子(a)的比例越大,则该水溶性高分子的溶出量(溶出速度)越大(但是,若水溶性高分子的比例过大,则由于活体分解性聚脂肪族酯(b)减少,因而薄膜状的形态保持力会降低)。另一方面,若增加聚脂肪族酯(b)的比例,则薄膜状等基体的形态可长时间稳定地保持,相反,水溶性高分子(a)、以及抗坏血酸等的溶出速度会降低。若考虑以上事项,可配合其目的实现最佳的缓释性。由此项观点,本发明中,构成上述基体的水溶性高分子(a)与聚脂肪族酯(b)的重量比例ω(=a/b)较理想为1~99/99~1、更优选ω(=a/b)为20~80/80~20、特别优选ω(=a/b)为30~70/70~30。若水溶性高分子(a)的比例过少,则其溶出速度变小,且所调配的抗坏血酸等的缓释速度极小。另一方面,若聚脂肪族酯(b)的量过大,则虽形状保持性获提升,但水溶性高分子(a)与抗坏血酸等的缓释性变为过低。本发明的防粘连材料为当单层构造的情况,最有代表性的为,基体由水溶性高分子与活体分解性聚脂肪族酯所构成,当层积构造的情况,基体层10为如上述,由水溶性高分子所构成,而被覆层为由聚脂肪族酯所构成。首先,针对水溶性高分子进行说明。(水溶性高分子)水溶性高分子较优选为可使用多糖类、蛋白质或合成高分子。多糖类可适当使用例如:淀粉、直链淀粉、支链淀粉、糖原、聚葡甘露糖、糊精、葡聚糖、果聚糖等动植物储存多糖类;纤维素、果胶、几丁质等动植物构造多糖类;鹿角菜胶、琼脂糖等源自海藻的多糖类;聚三葡萄糖等微生物多糖类;刺槐豆胶、瓜尔豆胶等植物胶多糖类;肝素、玻尿酸、硫酸软骨胶、硫酸乙酰肝素、硫酸皮肤素、硫酸角质素等糖胺聚糖;以及这些多糖类的衍生物。蛋白质可适当使用例如:明胶、酪蛋白、胶原等。合成高分子可适当使用例如:聚乙烯醇、聚乙烯醇衍生物、聚丙烯酸类水溶性聚合物、聚丙烯酰胺、聚丙烯酰胺衍生物、聚环氧乙烷、聚环氧乙烷衍生物、聚乙烯吡咯啶酮、聚乙烯吡咯啶酮衍生物、聚酰胺类聚合物、聚环氧烷类聚合物、聚醚二醇类聚合物、顺丁烯二酸酐共聚物类聚合物等。从提高防粘连材料全体柔顺度的观点而言,就所例示的水溶性高分子中,特别适合使用聚三葡萄糖。(聚脂肪族酯)接着,针对聚脂肪族酯进行说明。聚脂肪族酯可适当使用例如:聚(交酯)类;聚(乙交酯)类;聚(交酯-ε-乙交酯)类;聚(乳酸)类;聚(甘醇酸)类;聚(乳酸-ε-甘醇酸)类;聚己内酯类;聚酯酰胺类;聚酸酐类;聚原酸酯类;聚氰基丙烯酸酯类;聚醚酯类;聚(二氧杂环己酮)类;聚(亚烷基烷基化物)类;聚乙二醇与聚原酸酯的共聚物、以及其它这些的共聚物;高分子掺合物等。特别为从活体内适合性与活体分解性优异的观点,较优选为使用聚(乳酸)类、聚(甘醇酸)类、聚己内酯类、及这些的共聚物中的至少一种。特别优选为乳酸/甘醇酸/ε-己内酯的三元共聚物(la/ga/ε-clt),分子量20,00~300,000左右者较适合。(基体层的厚度)基体或基体层10(以下有时简称为基体层10)的层厚,设定为例如1μm~5000μm。薄膜状防粘连材料的情况,基体层10的层厚为小于200μm、较优选为1μm~150μm、更优选为10μm至100μm、特别优选为30μm~80μm。薄片状防粘连材料的情况,基体层10的层厚形成为200μm以上。较优选为200μm至5000μm、更优选为300μm~3000μm、特别优选为500~2000μm、最优选为800~1000μm。基体层10的厚度为利用卡尺、微量测仪等直接接触进行测定,此外,也可采用红外线膜厚计、静电容式厚度计、激光位移传感器等适当仪器进行测定。(抗坏血酸、抗坏血酸衍生物)本发明中抗氧化成分的使用是为了更好地使抗坏血酸或其衍生物从防粘连材料缓释,而使其含于基体或基体层(或视情况也可进一步含于被覆层)中。抗坏血酸(ascorbicacid)为以营养素维生素c的形式作用,具内酯构造有机化合物的一种,化学式为如下所示。在(iupac命名法)中视同呋喃的衍生物,表示为(r)-3,4-二羟基-5-((s)-1,2-二羟乙基)呋喃-2(5h)-酮。分子量为176.13g/mol、熔点为190℃、沸点为553℃的光学活性化合物。本发明可适当使用已知作为维生素c的l体、即l-抗坏血酸。[化1]本发明中,其它可使用的抗坏血酸衍生物,为包括有:抗坏血酸钙、抗坏血酸钠、磷酸-l-抗坏血酸钠、磷酸-l-抗坏血酸镁、抗坏血酸葡萄糖苷、抗坏血酸乙酯等。抗坏血酸或抗坏血酸衍生物,相对于防粘连材料全体重量(质量),较理想至少添加0.1(w/w)%以上~20(w/w)%以下、通常添加为0.5(w/w)%以上~10(w/w)%以下、较优选为1.0(w/w)%以上~9.0(w/w)%以下、更优选为1.5(w/w)%以上~8.0(w/w)%以下。将抗坏血酸或抗坏血酸衍生物依上述比例添加于基体或基体层,而使含有的本发明防粘连材料浸渍于100×100mm/30ml牛血浆时,经24小时后其ph成为7.5~6.0。其为用于促进创伤面治愈的最佳ph。此现象意味着当将本发明防粘连材料配置于活体内时,在该基体或基体层中所含有抗坏血酸等持续缓释的前提下,防粘连材料配置部分附近的ph并不会偏离初期值,而是仍可维持治愈的最佳7.5~6.0值。如此,本发明防粘连材料的缓释性为可配合目的而广范围变化,且可使创伤面附近长期间维持一定所需的ph。若针对此点更进一步演绎,则本发明中,若水溶性高分子部分从基体表面逐渐溶出,则抗坏血酸等也会一起溶出。值得一提的是,所溶出属于水溶性高分子的聚三葡萄糖等会形成具粘性的溶液,因而推定该溶液会在溶解抗坏血酸等的状态下,依覆盖基体表面的方式滞留于该位置处。而且,具粘性的水溶性高分子溶液中的抗坏血酸等的浓度,理应大致等于基体中的浓度cm*(基体中调配cm*=8%时,合理认为溶出水溶性高分子溶液中的浓度也大致成为8%)。如此,含有抗坏血酸等的聚三葡萄糖等粘性溶液,会稳定地覆盖创伤部,因而认为该创伤部为利用抗坏血酸与聚三葡萄糖等的叠加效应被保护,由此促进防粘连效果。本发明基体的形成为可将既定的抗坏血酸等树脂组合物利用薄膜挤出法、片材料挤出法(sheetextrusion)形成,又也可从该树脂组合物的溶液利用浇铸法等形成。(其它抗氧化物质)本发明中,虽抗坏血酸等最具效果,但视所需也可取代抗坏血酸等,改为使用例如以下的抗氧化剂。即,可使用:维生素e;α-胡萝卜素、β-胡萝卜素、γ-胡萝卜素、茄红素、叶黄素等属于植物脂溶性色素的类胡萝卜素类;类黄酮素、儿茶素、单宁、花青苷、异黄酮、槲黄素等植物的花或叶、树皮、茎等所含的源自含多酚类植物的抗氧化物质(sod用物质)等。(被覆层)本发明基本上为如上述那样由水溶性高分子(a)与聚脂肪族酯(b)的组合物所构成的基体实质上形成的单层构造,即便未设置被覆层仍可达抗坏血酸等的缓释性。其中,视所需,也可设为具有在该基体所构成的基体层上更进一步具有由聚脂肪族酯构成的被覆层的层积构造。此种层积构造的情况如前所述,最典型的情况为基体实质上由以水溶性高分子所构成的基体层、以及在其上所形成且由聚脂肪族酯构成的被覆层所构成。此情况下由聚脂肪酸酯所构成的被覆层的功能,基本上为控制添加于由水溶性高分子所构成的基体层的抗坏血酸的缓释性。当被覆层不存在的情况,短时间内与水溶性高分子一起,抗坏血酸也会在短时间内溶出,而较难在充分的时间内确保其缓释性。即,层积构造的情况,如图1所示,可在基体层10的一面上形成被覆层20(第1被覆层),并在另一面上形成被覆层30(第2被覆层)。(被覆层的构成成分)作为被覆层的第1被覆层20及第2被覆层30,较优选为均由活体分解性聚脂肪族酯所构成。即,可使用与属于基体构成成分的聚脂肪族酯相同的成分。为求谨慎,不厌其烦地再度进行例示。杂脂肪族酯可适当使用例如:聚(交酯)类、聚(乙交酯)类;聚(交酯-ε-乙交酯)类;聚(乳酸)类;聚(甘醇酸)类;聚(乳酸-共-甘醇酸)类;聚己内酯类;聚酯酰胺类;聚酸酐类;聚原酸酯类;聚氰基丙烯酸酯类;聚醚酯类;聚(二氧杂环己酮)类;聚(亚烷基烷基化物)类;聚乙二醇与聚原酸酯的共聚物、以及其它这些的共聚物;高分子掺合物等。特别为与构成基体层的情况同样地,从活体内适合性与活体分解性优异的观点,较优选为使用聚(乳酸)类、聚(甘醇酸)类、聚己内酯类、及这些的共聚物中的至少一种。更优选为上述特佳的乳酸/甘醇酸/ε-己内酯的三元共聚物(la/ga/ε-clt)。另外,代表实施形态中,第1被覆层20与第2被覆层30较优选为由这些例示材料中利用相同的材料所构成。(被覆层也含有抗坏血酸的情况)另外,基本上,被覆层由这些聚脂肪族酯所构成,但如后记当以该被覆层的强度保持为目的的情况,形成相对较厚的被覆层。于该情况,视所需也可使该被覆层含有抗坏血酸等。通过使其含于被覆层,特别为当将防粘连材料设置于创伤部时,在初期阶段可可靠地执行缓释。但由于被覆层的厚度ld如前述远薄于基体层的厚度ld,因而该被覆层中所含抗坏血酸等的总量并无法如此增加,较难持续过长时间(长期间)缓释,而最重要的为基体层中所含的抗坏血酸等便可达辅助性效果,故优选。单层构造仅于基体层添加抗坏血酸所形成,但该情况,由于抗坏血酸被包含于水溶性多醣类,因而其缓释相对较快地进行。又,通过形成较薄的被覆层,如后记实施例3-4所记载的那样,该抗坏血酸的溶出速度可实现适当地控制所需的缓释率。另一方面,层积构造的情况如后记的实施例5-6,当形成较通常厚的被覆层的情况下,优选为于基体层与被覆层两者添加抗坏血酸。当被覆层含有抗坏血酸的情况,可考虑依以下的方式进行被覆层部分的缓释率(溶出速度)即,当将对被覆层的抗坏血酸的添加量(浓度cm*)设为一定,且改变被覆层的厚度(ld)的场合,在被覆层厚度ld越薄的初期阶段中缓释得越快,但在较短的时间内被覆层内的抗坏血酸匮乏。另一方面,被覆层厚度ld越厚缓释越缓慢,但认为因被覆层内的抗坏血酸总量较多,而可持续长时间缓释。又,若针对被覆层的厚度ld为一定,且改变对被覆层的抗坏血酸的添加量(浓度)cm*的情况进行考察,则在浓度cm*越高的初期阶段中缓释越快,浓度cm*越低则缓释越缓慢。如上述那样,通过适当调整被覆层的厚度ld、抗坏血酸的添加量(浓度)cm*,由于可任意地变更缓释速度、缓释持续时间等,因而可大幅地扩展治疗方法的选项。对于被覆层添加的抗坏血酸的含有量(浓度)cm*,添加量为0.01(w/w)%以上~1.0(w/w)%以下、优选为0.02(w/w)%以上~0.8(w/w)%以下、更优选为0.1(w/w)%以上~0.5(w/w)%以下。(被覆层的厚度)被覆层的功能基本上如已记述那样控制缓释性(溶解速度)。例如后述实施例所示,通过设置由属于生物分解性的聚脂肪族酯构成的被覆层,将其厚度控制于光学厚度为50nm以上且800nm以下,较优选为75nm以上且小于600nm左右的范围内,便可使(来自基体的)抗坏血酸的缓释性变化。换言之,本发明为如前述,基本上通过改变构成基体层的水溶性高分子(a)与聚脂肪族酯(b)的重量比例ω(=a/b),便可控制水溶性高分子(a)的溶出速度(及抗坏血酸等的溶出速度),更进一步通过形成被覆层,使其厚度(ld)在上述范围内变化,便可更巧妙地进行缓释性控制。被覆层(第1被覆层20与第2被覆层30)为使用分光式椭圆偏光仪,依波长380nm~900nm测定时的光学厚度,在基体层10中添加抗坏血酸或抗坏血酸衍生物的情况,为形成为50nm以上且800nm以下,较优选为75nm以上且小于600nm。较优选形成为75nm以上且500nm以下。即便被覆层(第1被覆层20与第2被覆层30)的光学厚度较薄(50~75nm左右),因为本发明在基体层10中有添加抗坏血酸等,故能发挥充分的防粘连性能。另外,若被覆层过厚(超过800nm),则活体中的被覆层分解性能会降低。又,由于来自基体层的抗坏血酸向活体中溶出(扩散)受到阻碍,因而从维持缓释性的观点而言并不优选。但,另一方面,从基体层(进而防粘连材料)的强度维持(形态保持)的观点而言,要求被覆层本身具有不容易破裂程度的强度而具有某程度的厚度,例如后记实施例5-6所示,基本上设为800~7000nm、较优选为900~5000nm、更优选为1000~3000nm左右。如此,被覆层的厚度必需从强度维持的观点考虑。即,如猴子或人类那样的双足步行动物,因腹腔内压的上升或者胃或肠等脏器的移动,而有构成防粘连材料的基体(或被覆层)的薄膜状或薄片状的膜破裂的可能性。本发明通过后述的实施例5-6将猴子使用于动物实验而重复研讨,其结果可确认,上述程度的被覆层越厚越好。再者,如上述那样,被覆层若过厚则有分解性能降低(抗坏血酸缓释性降低)的危险,但当应用于如猴子或人类那样的双足步行动物,优先确保被覆层的机械强度的场合,基本上优选具有上述程度的厚度。此情况下,通过将调配于被覆层的抗坏血酸等的浓度cm*充分提高,可实质上抑制其缓释性的降低。又,通过于相对较厚的被覆层中含有水溶性高分子,可某程度地抑制抗坏血酸缓释性降低。基于上述,概括而言,被覆层的厚度ld形成为50nm以上且7000nm以下、优选为100nm以上且5000nm以下、更优选为1000nm以上且3000nm以下。而且,在此厚度范围内,较优选为通过考虑防粘连材料所设置的腹腔内压与力的环境、对象脏器的种类、所需缓释期间等诸多条件,优先进行缓释性、或优选进行形态保持性(但在任何情况下都必需考虑两者),决定被覆层的厚度(及调配于被覆层中之抗坏血酸浓度cm*)。[实施例(a)]在如上述图1所示的代表实施形态的防粘连材料1的构成基础下,于基体层的材料中添加既定量l-抗坏血酸(和光纯药公司制),成形为薄膜状的基体层双面上,配置由相同材料构成的第1被覆层与第2被覆层(以下也有简称为“被覆层”的情况),如上所述,将ph调整为既定范围的方式设为实施例试料(又,将未添加l-抗坏血酸的情况设为比较例试料)。(基体层的形成)具体而言,首先,基体层的材料为使用属于水溶性高分子的聚三葡萄糖,在其中添加既定量抗坏血酸,利用浇铸法对100mm×120mm×厚50μm的由聚三葡萄糖构成的膜进行成膜,而形成含抗坏血酸的基体层(基体层中的抗坏血酸浓度:cm)。(被覆层的形成)其次,依照常法的浸涂法施行被覆层的形成。即,制作经调整为既定浓度的属于聚脂肪族酯的聚乳酸-聚甘醇酸-聚ε-己内酯的甲苯溶液(以下称为涂布液),在该涂布液中浸渍上述调制的基体层,而在该基体层两表面上形成由聚乳酸-聚甘醇酸-聚ε-己内酯三元共聚物构成的被覆层。经浸涂后在室温中干燥30分钟~1小时左右,将其设为实施例的试料(试验片)。[比较例]除在上述实施例的基体层中未添加(未含有)抗坏血酸外,其余均与上述实施例同样地制作防粘连材料,设为比较例的试料(试验片)。(被覆层的光学厚度的测定方法)由于本发明的被覆层属于极薄膜,因而优选以光学厚度(ld)表示。在基体层上所层积的被覆层的光学厚度(ld)的测定,为使用分光式椭圆偏光仪(j.a.woollamjapan公司制“alpha-se(美国注册商标)”)。另外,测定波长设为380nm~900nm。(实施例1~3)(抗坏血酸添加浓度cm*的研究)将上述由聚乳酸-聚甘醇酸-聚ε-己内酯构成被覆层的厚度(ld)固定为300nm,改变对基体层的抗坏血酸的添加浓度cm(w/w)%,浸渍于牛血浆后,测定24小时后的ph(24)。结果示于表1。即,实施例1的抗坏血酸添加浓度cm=2.0(w/w)%、ph(24)=7.0、实施例2为cm=4.0(w/w)%、ph(24)=7.0,实施例3为cm=8.0(w/w)%、ph(24)=6.0。(比较例1)(无添加抗坏血酸的情况)比较例1为除了基体层中未添加抗坏血酸(cm=0%)外,其余均施行与实施例1~3同样的试验(被覆层的厚度(ld)=300nm)。浸渍于牛血浆后24小时后的ph(24)=7.3。结果示于表1。(实施例4)(被覆层的厚度(ld)的研究)除将被覆层的厚度(ld)设为75nm外,其余均施行与实施例3同样的试验。结果如表2所示,cm=8.0%的情况,与ld=300nm时的ph(24)=6.0之间差异并未被确认。(比较例2~3)(被覆层的厚度(ld)的研究)除将被覆层的厚度(ld)设为75nm(比较例2)或600nm(比较例3)外,其余均施行与比较例1同样的试验。结果与比较例1(ld=300nm)一并示于表2。在基体层中未添加抗坏血酸(cm=0%)的比较例的情况,即便使被覆层的厚度(ld)以75nm→300nm→600nm变化,仍为ph(24)=7.3(一定)。(抗坏血酸添加量与ph)[表1]比较例1实施例1实施例2实施例3被覆层的光学厚度ld(nm)300nm300nm300nm300nm抗坏血酸浓度cm(w/w)(%)0%2.0%4.0%8.0%浸渍牛血浆时的ph(24hr)7.37.07.06.0(被覆层的光学厚度与抗坏血酸添加量)[表2]比较例2比较例1比较例3实施例4被覆层的光学厚度ld(nm)75nm300nm600nm75nm抗坏血酸浓度cm(w/w)(%)0%0%0%8.0%浸渍牛血浆时的ph(24hr)7.37.37.36.0[试验例i](防粘连性能评价)本试验例1为用于评价防粘连材料的防粘连性能的试验(另外,本试验例1为对应于本案申请人所提出的专利文献1的试验例2)。在评价防粘连性能时,由实施例与比较例的试料制作试验片,将试验片贴附于猪的腹腔内,观察粘连程度并评级,以评价防粘连性能。(1)试验片的准备裁剪上述实施例1~4与比较例1~3的试料,而制作100mm×120mm长方形状的试验片。(2)试验方法(粘连模型的制作)首先,将猪在全身麻醉下在腹部正中央切开15cm而剖开腹部,使小肠露出于创口外。其次,针对所露出的小肠的一定面积(1×5cm左右),使用锉刀摩擦直到出现点状出血。在出现点状出血后,正确地暴露于空气中10分钟。然后,将小肠塞回腹腔内,于切开部分的正下方贴附上述试验片的防粘连材料。腹壁使用吸收性缝合线(2-0)依双层连续缝合而封闭,以制作粘连模型。另外,实施例、比较例均设为各组5例左右的例数。(3)试验方法(粘连程度的观察、粘连评级的计算)从粘连模型制作起14天后,使猪在全身麻醉下放血而牺牲死亡,肉眼观察剖腹正中央创口正下方的粘连,求取粘连的发生机率。另外,本件为属于下腹部的评价,故忽视上腹部的肝脏粘连。试验结果示于以下的表3、表4。表3与表4的读法,为例如表3的“实施例1”(被覆层的厚度(ld)300nm、抗坏血酸添加浓度cm=2.0%)的栏,对应于表4的“粘连发生率σ:20%(1/5)”(被覆层的厚度(ld)300nm、抗坏血酸添加浓度cm=2.0(w/w)%的栏);而表3的“比较例2”(被覆层的厚度(ld)75nm、抗坏血酸添加浓度cm=0%)的栏,对应于表4的“粘连发生率σ:75%(3/4)”(被覆层的厚度(ld)75nm、抗坏血酸添加浓度cm=0%的栏)。[表3][表4](考察1)(1)(抗坏血酸添加浓度cm的研究(i))由表4可确认到当被覆层的厚度(ld)设为300nm的情况,改变对基体层的抗坏血酸既定添加浓度cm(2.0(w/w)%至8.0(w/w)%)的实施例1(粘连发生率σ为20%)及实施例2~3(粘连发生率σ为0%)的结果,对比于被覆层的厚度(ld)同为300nm而未添加抗坏血酸的比较例1(粘连发生率σ为66%),实施例的情况明显降低粘连发生率。又,若将实施例1与实施例2~3进行比较,可确认到抗坏血酸的添加浓度cm从2.0(w/w)%增加至4.0~8.0(w/w)%,粘连发生率σ呈现20%→0%的更加降低状态。(2)(抗坏血酸添加浓度cm的研究(ii))将被覆层的光学厚度(ld)固定为75nm,并对基体层高浓度(cm=8.0(w/w)%)添加抗坏血酸的实施例4(粘连发生率σ=50%),相较于未添加抗坏血酸的比较例2(粘连发生率σ=75%),可确认到粘连发生率σ降低。[试验例ii]本试验例ii为用于评价表现防粘连性能的抗坏血酸缓释性的试验。即,将对基体层的抗坏血酸添加浓度cm=8.0w/w%(一定),与仅被覆层的厚度ld不同的情况([实施例3](ld=75nm)及[实施例4](ld=300nm))进行比较,确认是否达成最佳的缓释。试验片的准备裁剪上述实施例及比较例的试料,制作50mm×50mm正方形状的试验片。试验方法在磷酸缓冲液(ph7.4)100ml中,浸渍1片前述实施例3(ld=75nm)及实施例4(ld=300nm)的防粘连材料,测定磷酸缓冲液中的抗坏血酸浓度随时间变化直到24小时为止。抗坏血酸的定量为采用使用维生素c定量套件(cosmobio公司制)的比色定量法实施。再者,将防粘连材料中所含抗坏血酸量全量溶出于磷酸缓冲液时的浓度设为100%,求取各测定点的缓释率再者,试验所使用的材料为24小时观察形状。(试验结果)试验结果示于图2。另外,超过24小时的数据,因为抗坏血酸已分解故不采用。直到24小时为止的数据中,实施例3的缓释率为60~70%,实施例4的缓释率为20~30%左右。若比较二者,被覆层的厚度ld较薄的实施例4(ld=75nm),相较于被覆层的厚度较大的实施例4(ld=300nm),缓释速度更大,在经过时间t=10hr时溶出70%以上。相对于此,得知具有更厚被覆层的实施例4(ld=300nm),缓释更缓慢(即便t=24hr仍为左右)。然而,关于t=14天后的粘连发生率σ,实施例3的粘连发生率σ为0%,达远较实施例4的50%更优越的防粘连效果。此现象推定为实施例3中经过t=14天仍维持最佳缓释速度的缘故。反之,可认为实施例4的情况,为因为缓释速度过大,导致在短时间内该基体层中的抗坏血酸耗尽的缘故。再者,试验所使用的材料(试验片)虽经24小时后几乎凝胶化而维持形状,但可谓呈半固态。(考察2)依照使用固态或半固态的材料,得知缓释率会有差异。更具体而言,设置由属于生物分解性的聚脂肪族酯构成的被覆层,且将其厚度控制于光学厚度75nm以上且小于600nm的范围,便可长时间维持(添加于基体的)抗坏血酸的缓释性。此现象表示可依照适用的损伤部位或损伤深度,调整材料特性。又,不会有如液性物(例如专利文献2)般在刚贴附后便(全量短暂)缓释,若根据本发明具有基体层形态的防粘连材料,可随时间变化(长期间,例如实施例所示14天)仍维持缓释、即长期间进行缓释。[实施例(b)]与实施例(a)同样地在如图1所示实施形态的防粘连材料1构成基础上,于基体层的材料中添加既定量l-抗坏血酸(和光纯药公司制),在成形为薄膜状的基体层双面上,同样地配置添加l-抗坏血酸的第1被覆层及第2被覆层(以下也有同样地简称为「被覆层」的情况),并将其设为实施例试料。(又,将于基体层、被覆层均未添加l-抗坏血酸的情况设为比较例试料。)(实施例5-6)(添加抗坏血酸后的较厚的被覆层的形成)(基体层的形成)与实施例(a)同样,基体层的材料使用作为水溶性高分子的三葡萄糖,在其中(以成为cm=4(w/w)%的方式)添加既定量的抗坏血酸,利用浇铸法对100mm×120mm×厚(ld)50μm的由聚三葡萄糖构成的膜进行成膜,以形成含抗坏血酸的基体层。(被覆层的形成)其次,依照浸涂法进行被覆层的形成。即,制作调整为既定浓度的作为聚脂肪族酯的聚乳酸-聚甘醇酸-聚ε-己内酯的甲苯溶液(以下称为涂布液),在该涂布液中以成为既定量(cm*=0.4(w/w)%)的方式添加抗坏血酸。于该含抗坏血酸涂布液中浸渍上述调制的基体层,而在该基体层两表面上形成由聚乳酸-聚甘醇酸-聚ε-己内酯三元共聚合体构成的被覆层。经浸涂后在室温中干燥30分钟~1小时左右,通过重复施行此涂布步骤(浸涂)、干燥步骤,而形成较实施例1-4更厚膜厚(ld)的被覆层(基体层双面的第1外层、第2外层)(其中,cm*=0.4(w/w)%)。于此,形成被覆层的厚度ld=1000nm(实施例5)、ld=3000nm(实施例6)的试料(试验片)。(比较例4)(无添加抗坏血酸的情况)再者,比较例与实施例5-6同样,于基体层(ld=50μm)两侧形成被覆层(ld=1000nm),但于任一层中均完全未添加抗坏血酸(cm=0、cm*=0),将其设为比较例4的试料(试验片)。[试验例iii](防粘连性能评价)本试验例iii用于评价与试验例i同样防粘连材料的防粘连性能的试验,但将对象动物种类变更为更接近人类。该情况假设防粘连材料的应用环境(腹腔内压或脏器移动的发生)为更严酷的条件,以确认是否适合此环境。在评价防粘连性能时,从上述实施例(b)及比较例的试料制作试验片,将试验片贴附于猴子(macacafascicularis)的腹腔内并观察粘连的程度,且通过测定粘连长度,评价防粘连性能。(1)试验片的准备裁剪上述实施例5-6及比较例4的试料,制作100mm×120mm长方形状的试验片。(2)试验方法(粘连模型的制作)首先,将猴子在全身麻醉下在腹部正中央切开8cm而剖开腹部,使大肠露出于创口外。其次,针对所露出之大肠的一定面积(3×4cm左右),使用锉刀摩擦直到出现点状出血。在出现点状出血后,正确地暴露于空气中10分钟。然后,将大肠塞回腹腔内,于切开部分的正下方贴附上述试验片的防粘连材料。腹膜、腹壁及肌肉层使用尼龙缝合线(3-0)连续缝合,皮下组织及皮肤利用尼龙缝合线(4-0)简单结扎并封闭,以便制作封闭的粘连模型。另外,实施例5-6、比较例4均设为各组3例左右的例数。试验方法(粘连程度的观察、粘连长度比例的测定)从粘连模型制作起14天后,在猴子全身麻醉下开腹,肉眼观察正中央创口正下方的粘连,求出粘连的发生机率、粘连长度比例。(考察3)从为了提高防粘连材料的强度且确实地施行形态维持的观点来看,相对由与实施例1-4相同厚度的聚三葡萄糖构成的基体层(ld=50μm)(于其双面)形成更厚的聚脂肪酸酯的被覆层的情况,通过形成该较厚的被覆层,认为可阻碍来自基体层的抗坏血酸的缓释。然而,即便在该情况下(ld=1000nm(实施例5)、ld=3000nm(实施例6)),因该被覆层也含有抗坏血酸,故如表5所示,表示可使粘连发生率显着降低。(再者,确认到所贴附的防粘连材料的形状于14天后也几乎保持当初的形态,且确认到通过具备实施例中所使用程度的厚度的被覆层,从形态维持的观点而言,防粘连材料可达到初期之目的。)即,于实施例5中,当将被覆层的厚度(ld)设为1000nm的情况,相对于基体层的抗坏血酸浓度cm(4.0(w/w)%),通过将被覆层的抗坏血酸浓度cm设为0.4(w/w)%,可使粘连发生率σ降低为67%(2/3)、粘连长度比例β(=l*/l)降低为15.50%。这一情况的原因认为是,当将比较例4的相同被覆层的厚度(ld)设为1000nm的情况,相较于在基体层及被覆层中未添加抗坏血酸时的(浓度cm=0%、cm*=0%)粘连发生率σ为100%(3/3)、粘连长度比例β(=l*/l)为82.60%,认为可显著提升抗粘连性能的评价。又,于实施例6中,虽将被覆层的厚度(ld)设为更厚的3000nm,但于此情况下也与实施例5同样地通过将基体层的抗坏血酸浓度cm设为4.0(w/w)%、被覆层的抗坏血酸浓度cm*设为0.4(w/w)%,相较于比较例4,表示可使粘连发生率σ显着地降低为33%(1/3)、粘连长度比例β(=l*/l)显着地降低为33.30%。再者,进一步进行研讨,若与表3的实施例2(基体(ld=50μm)的抗坏血酸浓度cm=4.0(w/w)%、被覆层(厚度ld=300nm,但抗坏血酸浓度cm*=0%)进行比较,粘连发生率σ在表4(cm=4.0%的情况)中为0%(无粘连),相对于此,于实施例5-6中粘连发生率σ并非完全没有,可确认其差异。基本上,此差异的最大原因可认为,因供于试验的动物种类(猪与猴子)不同,而使基线粘连的发生频率不同,且为了将被覆层的厚度(ld=1000或3000nm)保持作为防粘连材料的强度,因而基于一直较厚地形成等理由而产生,并非源自防粘连材料的性能的本质差异。在此项观点中,认为通过使添加于该被覆层的抗坏血酸浓度cm*进一步增加为0.4%→0.6%→0.8%→1.0%等,可充分减低粘连发生率σ。又,认为虽目前被覆层ld为仅由活体分解性的聚脂肪酸酯(b)构成,但通过于被覆层ld中含有少量的例如与抗坏血酸相同程度的聚三葡萄糖等的水溶性高分子(a),可采用更加速抗坏血酸缓释等的手段,进一步减低粘连发生率。[表5]另外,关于专利文献1中记载的下述试验例1、试验例3、试验例4,也是为求谨慎而施行对应的试验,但如下所述,得知实用上并没有功能性问题,因而此处不记载详细内容。即,(i)(试验例1)(防粘连材料贴附于活体组织时的分解性评价):贴附于活体直到表现强度为止的时间虽稍长,但不致影响功能。(ii)(试验例3)(防粘连材料湿润时的处置性评价):试验例2中,虽施行猪以及猴子腹腔内的贴附,但能毫无问题地贴附。(iii)(试验例4)(防粘连材料贴附于活体组织时的密接性评价):试验例2中,虽施行猪以及猴子腹腔内的贴附,但能毫无问题地贴附。(产业上的可利用性)本发明的防粘连材料为基本上使由水溶性高分子(a)与活体分解性聚脂肪族酯(b)构成的固态或半固态基体中,含有作为抗氧化物质的抗坏血酸或抗坏血酸衍生物的构成,因而由水溶性高分子与聚脂肪族酯构成的基体,发挥作为创伤面与创伤面的物理性屏障的功能,且通过缓释的抗坏血酸或其衍生物促进创伤面的治愈,能效率极佳地表现出叠加效应的防粘连功能,故在医疗领域中产业上的可利用性极大。符号说明1防粘连材料10基体层20第1被覆层30第2被覆层cm基体层的抗坏血酸等的浓度cm*被覆层(外层)的抗坏血酸等的浓度ld基体层的厚度ld被覆层的厚度(光学厚度)l切开创口长度l*切开创口的粘连长度抗坏血酸的缓释率(溶出速度)。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1