一种神经酰胺在制备抗肿瘤药物中的应用的制作方法
1.本发明属于医药技术领域,具体涉及一种神经酰胺(正辛基神经酰胺-1-磷酸(铵盐))在制备抗肿瘤药物中的应用。
背景技术:
2.宫颈癌是第四大最常见的女性恶性肿瘤,每年导致全球超过30万人死亡,近99.7%的女性宫颈癌可归因于人乳头瘤病毒感染。高危型人乳头瘤病毒(hr-hpv)的持续感染被认为是宫颈癌最重要的流行病学危险因素,其中,hpv16和18型占宫颈癌的70%以上,hr-hpv可以导致基底上皮细胞功能障碍和宫颈癌的发生。
3.目前宫颈癌的治疗主要采用以手术和放疗为主、化疗为辅的综合治疗方案。其中,手术主要用于早期宫颈癌患者,包括:全子宫切除术;次广泛全子宫切除术及盆腔淋巴结清扫术;广泛全子宫切除术及盆腔淋巴结清扫术;腹主动脉旁淋巴切除或取样。放射治疗适用于:
①
中晚期患者;
②
全身情况不适宜手术的早期患者;
③
宫颈大块病灶的术前放疗;
④
手术治疗后病理检查发现有高危因素的辅助治疗。化疗主要用于晚期或复发转移的患者,近年也采用手术联合术前新辅助化疗(静脉或动脉灌注化疗)来缩小肿瘤病灶及控制亚临床转移,也用于放疗增敏,常用化疗药物有顺铂、卡铂、紫杉醇、博来霉素、异环磷酰胺、氟尿嘧啶等。但手术及放化疗的副作用一直困扰着宫颈癌的患者。
4.肿瘤细胞会重新编程它的代谢以支持自身细胞的生长增殖和迁移,从而促使癌症的进一步发展。先前的研究认为代谢物是各种生物过程的最终产物,也可能是反映上游生物事件(如环境影响和基因突变)的生物标志物。代谢组学变异被认为是筛查和诊断癌症理想的生物标志物,并且越来越多的研究强调了代谢物在生理学和疾病中的功能作用。hpv的感染会引起代谢修饰,从而使之代谢物可能作为预测宫颈癌风险的潜在标志物,而活性代谢物的作用和潜在机制在宫颈癌领域相关的研究非常有限。中国专利cn201610850050.8公开了apigenin在制备治疗宫颈癌药物中的应用,发现其对人宫颈癌细胞株hela、hela229、hce1和caski的生长具有显著的抑制作用。中国专利cn201880023127.1则公开了非类固醇选择性糖皮质激素受体调节剂(sgrm)在治疗宫颈癌中的应用,所述的sgrm为稠合的氮杂萘烷。
5.因此,随着对代谢物作用的认知不断深入,找寻安全有效的代谢物及治疗方法,在保证治疗效果的同时提高治疗的安全性及宫颈癌患者的生活质量,逐渐成为了该研究领域的热点。
技术实现要素:
6.发明目的:为了克服现有技术中存在的不足,本发明提供了正辛基神经酰胺-1-磷酸(铵盐)在制备抗肿瘤药物中的应用。本发明发现正辛基神经酰胺-1-磷酸(铵盐)具有良好的抑制宫颈癌细胞的增殖、emt(上皮间质转化)和癌细胞迁移的作用,为宫颈癌的治疗提供了一种新的思路。
7.技术方案:为实现上述目的,本发明的技术方案如下:
8.一方面,本发明提供了正辛基神经酰胺-1-磷酸(铵盐)在制备抗肿瘤药物中的应用,所述的正辛基神经酰胺-1-磷酸(铵盐)的分子式为c
26h55
n2o6p,cas为474943-70-9,分子量为522.7,结构式如下式1所示:
[0009][0010]
具体地,所述的正辛基神经酰胺-1-磷酸(铵盐)通过抑制肿瘤细胞的增殖、迁移和上皮间质转化抑制肿瘤。
[0011]
具体地,所述的正辛基神经酰胺-1-磷酸(铵盐)的浓度为5-50μm,优选为10-30μm,进一步优选为30μm。
[0012]
具体地,所述的肿瘤为宫颈癌。
[0013]
又一方面,本发明提供了一种抗肿瘤药物,所述的药物包含上述正辛基神经酰胺-1-磷酸(铵盐)。
[0014]
具体地,所述的药物还包括药学上可接受的载体,所述的载体为缓释剂、赋形剂、填充剂、粘合剂、润湿剂、崩解剂、吸收促进剂、吸附载体、表面活性剂或润滑剂中的任意一种或多种。
[0015]
具体地,所述的药物为外用制剂、口服制剂或注射制剂中的任意一种。
[0016]
进一步具体地,所述的外用制剂为喷雾剂或气雾剂。
[0017]
进一步具体地,所述的口服制剂为颗粒剂、胶囊剂、片剂或囊泡剂中的任意一种。
[0018]
进一步具体地,所述的注射制剂采用皮内、皮下、肌内、局部或静脉内注射作为给药方式。
[0019]
有益效果:与现有技术相比,本发明的积极和有益效果在于:
[0020]
本发明所述的正辛基神经酰胺-1-磷酸(铵盐)能够明显抑制宫颈癌细胞(hela和gh354细胞)的增殖、emt(上皮间质转化)和癌细胞的迁移,为宫颈癌的治疗提供了一种新的思路。
附图说明
[0021]
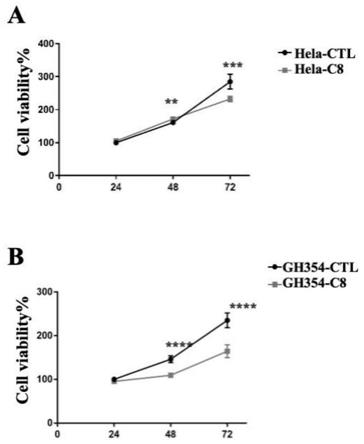
附图1为细胞增殖检测结果图,其中,a为hela细胞,b为gh354细胞。
[0022]
附图2为细胞迁移检测结果图,其中,a为hela细胞,b为gh354细胞。
[0023]
附图3为emt相关基因rt-qpcr检测结果图,其中,a为hela细胞,b为gh354细胞。
[0024]
附图4为emt相关蛋白表达检测结果图,其中,a为hela细胞,b为gh354细胞。
具体实施方式
[0025]
下面结合具体实施例,对本发明作进一步详细的阐述,下述实施例不用于限制本发明,仅用于说明本发明。以下实施例中所使用的实验方法如无特殊说明,实施例中未注明
具体条件的实验方法,通常按照常规条件,下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0026]
实施例中未注明具体技术或条件者,均按照本领域内的文献所描述的技术或条件(如参考j.萨姆布鲁克等著,黄培堂等译的《分子克隆实验指南》,第三版,科学出版社)或者按照产品说明书进行。
[0027]
本发明采取独立重复实验,均重复3次。实验数据采用spss18.0统计分析软件分析,计量资料以均数
±
标准差表示,两样本均数之间的比较,经正态性检验和方差齐性检验后,采用t或t'检验,p《0.05提示差异有统计学意义。
[0028]
实施例1.细胞培养
[0029]
hela(atcc ccl-2)和gh354(atcc crl-13003)在dmem(dulbecco改良eagle培养基)中培养,该培养基含有10%胎牛血清(gibco,新西兰)和500μl青霉素-链霉素(gibco,美国),并保存在5%co2和37℃的培养箱中。每三天更换一次培养基。当细胞融合到80%时,用0.05%胰蛋白酶(sciencell,美国)消化细胞进行接种和传代。
[0030]
实验例1.细胞增殖检测
[0031]
通过cck8(targetmol,china)检测正辛基神经酰胺-1-磷酸(铵盐)(简称c8,购于avanti,产品编号860532p)对宫颈癌细胞增殖的影响。将培养的hela和gh354细胞悬浮在100μl含有10%fbs的培养基中,并与30μm的c8一起接种到96孔板(3000个细胞/孔)中分别孵育24小时、48小时和72小时,在使用酶标仪测量450nm波长处的吸光度值前加入10μl cck8溶液加入每个孔中并孵箱中孵育1小时。结果如图1所示,在48小时-72小时30μm c8干预的hela和gh354细胞增殖率有明显的下降。
[0032]
实验例2.细胞迁移检测
[0033]
用细胞划痕实验观察宫颈癌细胞(hela和gh354)向无细胞的划痕区域迁移的情况,来判断用c8干预后的宫颈癌细胞相比对照组迁移能力的差别。将培养的细胞悬浮在含有16%fbs的2ml培养基中,并与浓度为30μm的c8一起接种在6孔板(100000个细胞/孔)中,对照添加了相同的dmso。分别在0小时、24小时、36小时和72小时检测迁移效率。结果如图2所示,c8组迁移指数明显降低。
[0034]
实验例3.rna的提取和实时定量基因扩增荧光检测系统(rt-qpcr)
[0035]
在宫颈癌细胞(hela和gh354)中加入浓度是30μm的c8干预48小时后,用trizol(invitrogen,carlsbad,ca,usa)分别提取实验组和对照组的rna,再用逆转录试剂盒ⅱqrt super mix(vazyme,nanjing,china)进行逆转录,最后用sybr green pcr master mix(vazyme,nanjing,china)进行rt-qpcr,检测两组之间emt相关基因表达量的差异,引物的序列见表1。rt-qpcr的程序如下:95℃5s,95℃10s,60℃30s,40个循环。量化的mrna被标准化为β-肌动蛋白作为对照,2-δδct
法测定mrna相对表达量。
[0036]
表1.用于rt-qpcr的引物序列
[0037][0038][0039]
检测结果如图3所示。在c8干预hela和gh354后e-钙粘蛋白(e-cadherin)的mrna表达量上调,n-钙粘蛋白(n-cadherin)与波形蛋白(vimentin)的mrna表达量下调,表明c8有抑制宫颈癌细胞上皮间质转化(emt)的作用。
[0040]
实验例4.蛋白质提取和蛋白质印迹分析
[0041]
在蛋白酶抑制剂(thermo fisher scientific,waltham,ma,usa)存在下通过匀浆制备细胞,并离心去除细胞沉淀。样品在95℃下用5
×
sds-page上样缓冲液加热变性5分钟,然后在10%sds-page凝胶(bio-rad,hercules,ca,usa)上分级。gapdh(hrp-60004,proteintech,manchester,uk)用作标准对照蛋白质。电泳后,将蛋白质转移到硝酸纤维素膜上并用5%脱脂奶粉封闭。一抗使用抗e-钙粘蛋白、抗n-钙粘蛋白、抗mmp9和抗波形蛋白抗体(1:2000,proteintech,manchester,uk)。
[0042]
检测结果如图4所示。在蛋白质水平上c8干预hela后,e-钙粘蛋白(e-cadherin)显著上调和n-钙粘蛋白(n-cadherin)下调,再一次在蛋白水平验证了c8有抑制宫颈癌细胞上皮间质转化(emt)的作用。
[0043]
以上所述仅是本发明的优选实施方式,应当指出:对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1