一种肿瘤诊疗多模态纳米粒及其制备方法
本发明涉及医学领域,特别涉及一种肿瘤诊疗多模态纳米粒及其制备方法。
背景技术:
1、恶性肿瘤已对人类生命健康构成严重威胁,开发针对肿瘤的高选择性及高效率治疗方法意义重大。
2、n6-甲基腺嘌呤核苷酸(m6a)是rna甲基化修饰中最常见的修饰。ythdf1是参加m6a甲基化reader蛋白中的一种,可以识别有m6a修饰的mrna,并促进其翻译。ythdf1可识别dc细胞中溶酶体蛋白酶m6a标记的转录本,并促进抗原的降解,进而抑制抗原的交叉呈递和特异性cd8+t细胞的产生,从而导致免疫逃逸和肿瘤的不完全消除。敲低ythdf1之后可以促进淋巴细胞在肿瘤组织中的浸润,并发现在ythdf1缺乏的患者中联合pd-l1抑制剂,其免疫治疗效果更佳。
3、rnai(rnainterfering,rna干扰)是一种高效的序列特异性基因沉默技术,sirna(small interfering rna,小干扰rna)能够特异性降解同源序列的mrna,抑制相关基因表达,是目前新药创制研究的热点领域之一。由于sirna自身的聚阴离子中心和强亲水性基团,加之sirna在细胞质内容易被核酸酶降解,因此外源性的sirna不能直接进入细胞质内发挥其功效。因此需要纳米材料作为安全高效的基因递送载体。纳米载体具有许多优点:①具备良好的生物相容性;②材料的粒径小,容易穿过细胞膜进入细胞;③制备较为简单且结构可控,可以进行多功能修饰;④负载基因的能力强,并保护基因免受核酸酶降解。主要包括脂质体、高分子聚合物、量子点、碳、硅纳米颗粒、金属纳米颗粒等。
4、光热治疗因其无创、成本低、副作用小、时空可控等优点成为抗肿瘤领域的研究热点,利用光热药剂吸收特定波长的光能并将其转化为热能,通过调节外部激光照射的剂量和范围来选择性地消除各种类型的肿瘤,并最大限度地减少其对周围正常组织的损害。同时,光热治疗也可以诱导免疫原性细胞死亡(icd)和淋巴细胞浸润,增强肿瘤免疫疗法在“冷”肿瘤中的疗效。吲哚菁绿(icg)是fda批准用于临床的近红外(nir)染料,可以用于荧光成像和光声成像,同时icg能将近红外光转化为热能,可作为良好的光热药剂。
5、综上,结合rnai治疗和光热治疗开发具有靶向效果的肿瘤诊疗多模态纳米粒具有重要意义。
技术实现思路
1、为解决上述技术问题,本发明将吲哚菁绿(icg)与ythdf1 sirna包载于纳米材料中,开发了具有靶向效果的肿瘤诊疗多模态纳米粒。具体地,
2、本发明第一方面提供了一种肿瘤诊疗多模态纳米粒,所述纳米粒包载肿瘤治疗性sirna和光热治疗剂。
3、在某些实施方式中,所述sirna靶向ythdf1。
4、在某些实施方式中,所述sirna序列为5’-ggacauugguacuugggautt-3’。
5、在某些实施方式中,所述光热治疗剂选自有机染料、有机纳米粒子、金纳米粒子、碳纳米管、氧化石墨烯、金属氧化纳米粒子、量子点;优选地,所述光热治疗剂为有机染料吲哚菁绿(icg)。
6、在某些实施方式中,所述光热治疗剂为有机染料吲哚菁绿(icg)。
7、在某些实施方式中,所述纳米粒为缩醛化环糊精和聚乙烯亚胺。
8、本发明第二方面提供了一种肿瘤诊疗多模态纳米粒的制备方法,包括如下步骤:1)缩醛化α-环糊精的制备;2)肿瘤治疗性sirna和光热治疗剂的包覆。
9、在某些实施方式中,所述sirna靶向ythdf1。
10、在某些实施方式中,sirna序列为5’-ggacauugguacuugggautt-3’。
11、在某些实施方式中,所述光热治疗剂优选为吲哚菁绿(icg)。
12、在某些实施方式中,所述步骤1)中将2-甲氧基丙烯(2-mp)加入到含有α-cd的无水dmso中,再加入4-甲基苯磺酸吡啶(pts),室温搅拌进行缩醛化反应,在混合物中加入三乙胺以终止反应;将缩醛产物从水中沉淀出来,通过过滤收集,用水彻底洗涤后使用冻干成白色的缩醛化α-cd(ac-acd)粉末。
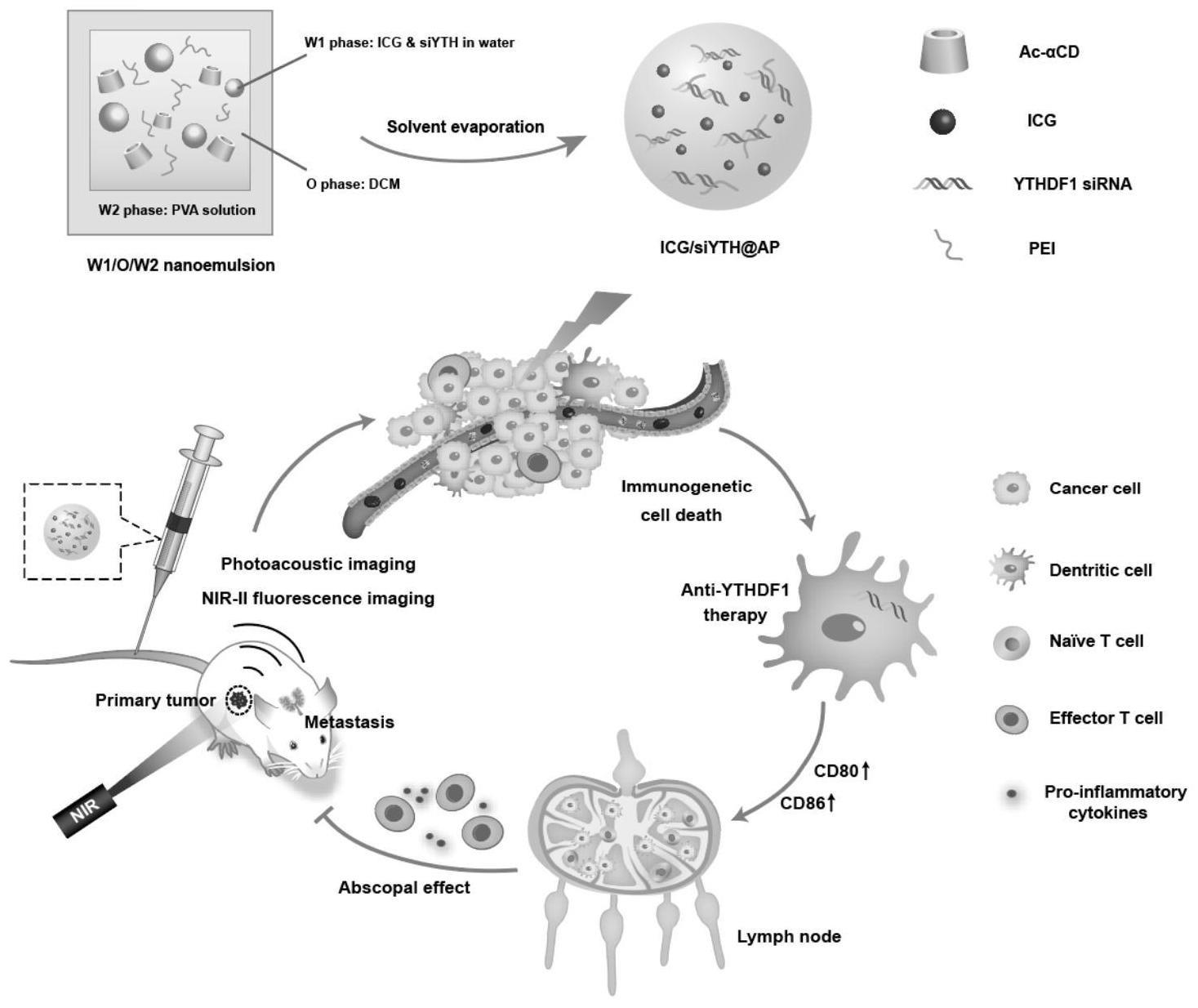
13、在某些实施方式中,所述步骤2)中将含有sirna和icg的溶液加入含有ac-acd和聚乙烯亚胺(pei1800)的二氯甲烷(dcm)中,超声乳化得到油包水纳米乳;将得到的油包水(w1/o)纳米乳在聚乙烯醇(pva)水溶液中乳化得到w1/o/w2双纳米乳;将上述双纳米乳倒入pva溶液中,室温下磁力搅拌,通过离心收集固化的纳米颗粒,冲洗,得到icg/siyth@ap纳米粒。
14、本发明第三方面提供了本发明第一方面所述的纳米粒或根据本发明第二方面所述的制备方法获得的纳米粒在制备肿瘤诊疗药物中的应用。
15、与现有技术相比,本发明的有益效果在于:
16、本发明制备了一种包载ythdf1小干扰rna和吲哚菁绿(icg)的肿瘤酸性微环境响应的纳米粒,利用ythdf1对肿瘤抗原呈递、肿瘤微环境的调节与icg光热治疗诱导免疫原性细胞死亡联合增敏肿瘤免疫治疗,同时利用icg的成像性能进行光声成像与近红外荧光成像,开发了具有靶向效果的肿瘤诊疗多模态纳米粒,实现了光热和免疫治疗协同增敏,实现诊疗一体化。
17、本发明诊疗多模态纳米粒的制备工艺简单,反应条件温和,成本较低,无需复杂设备。制备所得的纳米粒可以靶向肿瘤组织并释放ythdf1 sirna和icg,在808nm近红外激光的照射下,实现肿瘤的光热治疗,同时与免疫微环境的调控联合增敏肿瘤治疗。
技术特征:
1.一种肿瘤诊疗多模态纳米粒,其特征在于,所述纳米粒包载肿瘤治疗性sirna和光热治疗剂。
2.根据权利要求1所述的纳米粒,其特征在于,所述sirna靶向ythdf1。
3.根据权利要求2所述的纳米粒,其特征在于,所述sirna序列为5’-
4.根据权利要求1所述的纳米粒,其特征在于,所述光热治疗剂选自有机染料、有机纳米粒子、金纳米粒子、碳纳米管、氧化石墨烯、金属氧化纳米粒子、量子点;优选地,所述光热治疗剂为有机染料吲哚菁绿(icg)。
5.根据权利要求1所述的纳米粒,其特征在于,所述纳米粒为缩醛化环糊精和聚乙烯亚胺。
6.一种肿瘤诊疗多模态纳米粒的制备方法,其特征在于,包括如下步骤:1)缩醛化α-环糊精的制备;2)肿瘤治疗性sirna和光热治疗剂的包覆。
7.根据权利要求6所述的制备方法,其特征在于,所述sirna靶向ythdf1;
8.根据权利要求6所述的制备方法,其特征在于,所述光热治疗剂优选为吲哚菁绿(icg)。
9.根据权利要求6所述的制备方法,其特征在于,所述步骤1)中将2-甲氧基丙烯(2-mp)加入到含有α-cd的无水dmso中,再加入4-甲基苯磺酸吡啶(pts),室温搅拌进行缩醛化反应,在混合物中加入三乙胺以终止反应;将缩醛产物从水中沉淀出来,通过过滤收集,用水彻底洗涤后使用冻干成白色的缩醛化α-cd(ac-acd)粉末。
10.根据权利要求6所述的制备方法,其特征在于,所述步骤2)中将含有sirna和icg的溶液加入含有ac-acd和聚乙烯亚胺(pei1800)的二氯甲烷(dcm)中,超声乳化得到油包水纳米乳;将得到的油包水(w1/o)纳米乳在聚乙烯醇(pva)水溶液中乳化得到w1/o/w2双纳米乳;将上述双纳米乳倒入pva溶液中,室温下磁力搅拌,通过离心收集固化的纳米颗粒,冲洗,得到ythdf1sirna/icg@ap(“icg/siyth@ap”)纳米粒。
11.根据权利要求1-5任一项所述的纳米粒或根据权利要求6-10任一项所述的制备方法获得的纳米粒在制备肿瘤诊疗药物中的应用。
技术总结
本发明提供了一种包载YTHDF1小干扰RNA和吲哚菁绿(ICG)的肿瘤酸性微环境响应的纳米粒,利用YTHDF1对肿瘤抗原呈递、肿瘤微环境的调节与ICG光热治疗诱导免疫原性细胞死亡联合增敏肿瘤免疫治疗,同时利用ICG的成像性能进行光声成像与近红外荧光成像,开发了具有靶向效果的肿瘤诊疗多模态纳米粒,实现了光热和免疫治疗协同增敏,实现诊疗一体化。
技术研发人员:宋少莉,徐明真,钱余义
受保护的技术使用者:复旦大学附属肿瘤医院
技术研发日:
技术公布日:2024/1/14
- 还没有人留言评论。精彩留言会获得点赞!