一种注射用尼可地尔冻干粉针的制备方法与流程
本发明属于药物制剂领域,具体涉及一种注射用尼可地尔冻干粉针的制备方法。
背景技术:
1、尼可地尔,化学名为n-(2-羟基乙基)烟酰胺硝酸酯,分子式为c8h9n3o4,是首个用于临床的atp敏感的钾离子通道开放剂。临床又称为烟酞胺硝酸酯,其本质是一种尼克酰胺硝酸盐类衍生物,临床研究表明其具有改善心脏供血、抑制心肌细胞凋亡、减轻微循环障碍等功效,是临床治疗冠心病、心绞痛的常用药物。
2、目前尼可地尔主要上市剂型分为片剂和冻干粉针剂,然而对于吞咽困难或者急症患者,注射用制剂明显有着更加良好的适应性。但由于注射用制剂制备工艺不同以及贮藏条件而产生不稳定性。同时尼可地尔对潮湿环境和温度敏感,其冻干制剂在保存过程中尼可地尔含量会经常性的降低,杂质增多,因此需要解决如何在保证稳定性的同时,减少杂质,保证尼可地尔的含量,提升药品质量。
技术实现思路
1、为了解决上述技术问题,本发明提供了一种注射用尼可地尔冻干粉针的制备方法,具体包括如下步骤:
2、将尼可地尔原料药配制成基础溶液步骤,所述基础溶液在配制过程中的ph值范围为7.78~7.98;
3、将基础溶液进行冷冻干燥制得所述注射用尼可地尔冻干粉针步骤;
4、所述冷冻干燥的条件包括:
5、预冻:包括三次预冻,其中,第二次预冻和第三次预冻条件相同,均为先升温至-1℃~-5℃再降温至-40℃;
6、升华干燥:先将温度降至-50℃~-60℃,开始预抽真空,在保持预抽真空条件下进行升华干燥;优选的是:所述升华干燥的条件为升温至-20℃,升温至-15℃,升温至-10℃;
7、极限干燥:开始极限真空,在保持极限真空条件下进行极限干燥;优选的是:所述极限干燥的升温条件为升温至-5℃、0℃、20℃、25℃。
8、优选的,将尼可地尔原料药配制成基础溶液步骤中,包括定容步骤,定容后的ph值范围为7.82~7.98。
9、优选的,配制基础溶液步骤中定容后:ph值为7.98。
10、所述将尼可地尔原料药配制成基础溶液步骤,包括:
11、准备用于配置基础溶液的配液罐,向配液罐内加入如下原料药:
12、注射用水:称取配制总量90%~95%的注射用水加入配液罐中,水温控制在5℃~15℃;
13、甘露醇:称取指令量的甘露醇加入上述配液罐的溶液中,于液面下鼓氮,磁力搅拌溶解;
14、枸橼酸钠:加入原料前停止充氮,称取指令量的枸橼酸钠加入上述配液罐的溶液中,液面下鼓氮,磁力搅拌溶解;
15、尼可地尔:加入原料前停止充氮,再加入处方量的尼可地尔加入上述配液罐的溶液中,液面下鼓氮,磁力搅拌溶解完全,调节ph值范围为7.78~7.98;
16、原料药液降温至5~10℃以下,除菌,过滤,灌装,半压塞。
17、优选的,在制备基础溶液的过程中灌装步骤与半压塞步骤之间还包括中间品检验步骤,其中间品检验过程中控制ph值范围为7.84~7.87。
18、优选的,在基础溶液制备过程中半压塞时控制基础溶液ph值范围为7.78~7.93。
19、优选的,在将基础溶液进行冷冻干燥制得所述注射用尼可地尔冻干粉针步骤中;
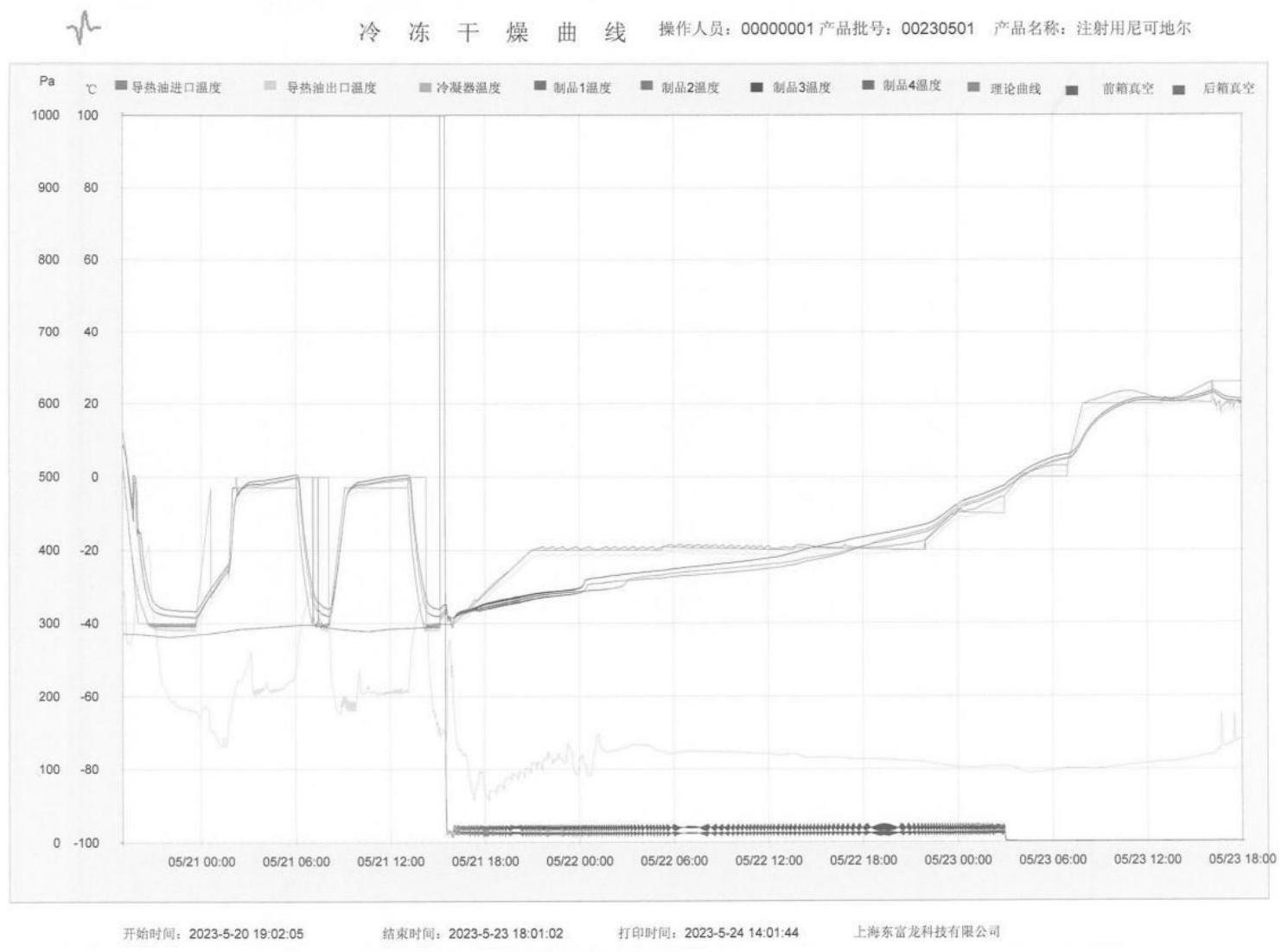
20、预冻:一次降温至-40℃保温≥2h;一次升温至-3℃保温≥3h;二次降温至-40℃保温≥0.5h;二次升温至-3℃保温≥3h;三次降温至-40℃保温≥1h;
21、升华干燥:一次升温至-55℃保温1h~5h,1h将板层二次升温至-20℃,保温≥1h;1h将板层三次升温至-15℃,保温≥1h;1h将板层四次升温至-10℃,保温≥1h;
22、极限干燥:继续对板层升温,1h将板层一次升温至-5℃,保温≥1h;1h将板层二次升温至0℃,保温≥1h;1h将板层三次升温至20℃,保温≥3h;1h将板层四次升温至25℃,保温≥3h。
23、8、优选的,在将基础溶液进行冷冻干燥制得所述注射用尼可地尔冻干粉针步骤中;
24、预冻:一次降温后保温2h~3h;一次升温后保温3h~5h;二次降温后保温1h~3h;二次升温后保温3h~5h;三次降温后保温1h~3h;
25、升华干燥:一次升温后,保温1h~3h,将板层二次升温后,保温1h~5h;将板层三次升温后,保温1h~5h;将板层四次升温后,保温1h~5h;
26、极限干燥:将板层一次升温后,保温1h~5h;将板层二次升温后,保温1h~5h;将板层三次升温后,保温3h~6h;将板层四次升温后,保温3h~6h。
27、优选的,在冷冻干燥的升华干燥步骤中,抽真空条件为:真空度达到0.2mbar。
28、优选的,在冷冻干燥的极限干燥步骤后包括升压力步骤,压力达到100kpa,抽真空至≤10pa,充入氮气,压力达到100kpa时压塞。
29、本发明的有益效果在于:利用本发明的方法制备的注射用尼可地尔具有良好的稳定性的同时,在尼可地尔含量标准中靠近高标准线,水分含量符合标准,有效减少杂质的生成,使药品预期有效期得到提高。
技术特征:
1.一种注射用尼可地尔冻干粉针的制备方法,其特征在于,包括如下步骤:
2.根据权利要求1的制备方法,其特征在于:将尼可地尔原料药配制成基础溶液步骤中,包括定容步骤,定容后的ph值范围为7.82~7.98。
3.根据权利要求2的制备方法,其特征在于:配制基础溶液步骤中定容后:ph值为7.98。
4.根据权利要求1的制备方法,其特征在于,所述将尼可地尔原料药配制成基础溶液步骤,包括:
5.根据权利要求4的制备方法,其特征在于:在制备基础溶液的过程中灌装步骤与半压塞步骤之间还包括中间品检验步骤,其中间品检验过程中控制ph值范围为7.84~7.87。
6.根据权利要求4的制备方法,其特征在于:在基础溶液制备过程中半压塞时控制基础溶液ph值范围为7.78~7.93。
7.根据权利要求1的制备方法,其特征在于:在将基础溶液进行冷冻干燥制得所述注射用尼可地尔冻干粉针步骤中;
8.根据权利要求7的制备方法,其特征在于:在将基础溶液进行冷冻干燥制得所述注射用尼可地尔冻干粉针步骤中;
9.根据权利要求8的制备方法,其特征在于:在冷冻干燥的升华干燥步骤中,抽真空条件为:真空度达到0.2mbar。
10.根据权利要求9的制备方法,其特征在于:在冷冻干燥的极限干燥步骤后包括升压力步骤,压力达到100kpa,抽真空至≤10pa,充入氮气,压力达到100kpa时压塞。
技术总结
本发明涉及一种注射用尼可地尔冻干粉针的制备方法,该方法包括步骤1:制备基础溶液,基础溶液调节pH值为7.78~7.98之间;步骤2:冷冻干燥,步骤2中冷冻干燥包括:预冻,抽真空,升华干燥,极限干燥,压力升,充氮,压塞,氮气压平,采用在制备基础溶液阶段调节pH值与本申请制备方法相结合实现了在保证较好的稳定性的同时,减少杂质含量,在质量标准范围内提升尼可地尔的含量,使药品质量提升。
技术研发人员:周文,崔少婷,肖劲
受保护的技术使用者:湖南赛隆药业(长沙)有限公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!