猪繁殖与呼吸综合征病毒经典株、变异株和疫苗株多重RT‑PCR检测试剂盒及其引物组的制作方法
本发明属于RT-PCR检测技术领域,尤其涉及一种猪繁殖与呼吸综合征病毒经典株、变异株和疫苗株多重RT-PCR检测试剂盒及其引物组。
背景技术:
猪繁殖与呼吸综合征(porcine reproductive and respiratory syndrome,PRRS)是一种急性、高度传染的病毒性传染病,其主要特征是怀孕母猪发生流产、早产、产死胎、木乃伊胎等繁殖障碍以及各种年龄猪、特别是仔猪的呼吸系统疾病。该病病原PRRS病毒(PRRSV)可以分为欧洲型(基因I型)毒株(EU-PRRSV)和美洲型(基因II型)毒株(NA-PRRSV)。我国PRRSV流行毒株以NA-PRRSV经典株、高致病性变异株为主,但在部分省份也检测到EU-PRRSV。
技术实现要素:
本发明要解决的技术问题是提供一种特异性强、敏感性高、稳定性好的猪繁殖与呼吸综合征病毒经典株、变异株和疫苗株多重RT-PCR检测试剂盒及其引物组,可同时检测并区分PRRSV野毒株、疫苗株。
为解决上述技术问题,本发明采用以下技术方案:猪繁殖与呼吸综合征病毒经典株、变异株和疫苗株多重RT-PCR检测引物组,包括两对特异性引物,分别是引物1和2、引物3和4,它们分别具有序列表SEQ.ID.No.1至SEQ.ID.No.4的碱基序列。
引物1、引物2、引物3、引物4的摩尔比为1∶1∶1∶1。
猪繁殖与呼吸综合征病毒经典株、变异株和疫苗株多重RT-PCR检测试剂盒,该试剂盒含有以下试剂:反转录RT反应液、PCR反应液、灭菌双蒸水,PCR反应液包括两对特异性引物,分别是引物1和2、引物3和4,它们分别具有序列表SEQ.ID.No.1至SEQ.ID.No.4的碱基序列。
反转录RT反应液每管15μL,包括:5×Prime Scrip II buffer 4.0μL,dNTP1.0μL含各dNTP 10mM,随机引物6聚体50pmol/μL、1.5μL,RNA酶抑制剂40U/μL、0.5μL,RNase H-型反转录酶200U/μL、1.0μL,灭菌双蒸水7μL;PCR反应液每管45μL,包括:2×Taq PCR MasterMix 25μL,引物1至425pmol/μL各1.0μL,灭菌双蒸水16μL。
针对目前猪繁殖与呼吸综合征病毒检测存在的问题,根据NA-PRRSV经典株(C-PRRSV)与变异株(HP-PRRSV)在Nsp2基因的序列差异(变异株在Nsp2基因共缺失90个核苷酸)以及TJM-F92疫苗株(V-PRRSV)在Nsp2基因的序列特点(在缺失90个核苷酸的基础上还另外连续缺失360个核苷酸),由此,发明人设计了猪繁殖与呼吸综合征病毒经典株、变异株和疫苗株多重RT-PCR检测引物组,包括两对特异性引物,分别是引物1和2、引物3和4,它们分别具有序列表SEQ.ID.No.1至SEQ.ID.No.4的碱基序列。其中,引物1和2(B2-F/B2-R)用于区分美洲型经典株、变异株,引物3和4(TJM-F/TJM-R)用于区分野毒株和TJM-F92株,可实现三种不同类型毒株的鉴定在同一个扩增反应中一次性完成。据此,发明人还制备了检测试剂盒,并建立了相应的多重RT-PCR检测方法,该法可以特异检测PRRSV,而与猪的其他重要病原无交叉反应;对重组质粒标准品的检出下限为1.13×103拷贝。临床检测结果表明,本发明具有特异性强、敏感性高、重复性好等特点,可同时检测并区分PRRSV美洲型经典株、变异株及TJM-F92疫苗株,为临床快速鉴别检测及流行病学调查提供了有效的技术平台。
附图说明
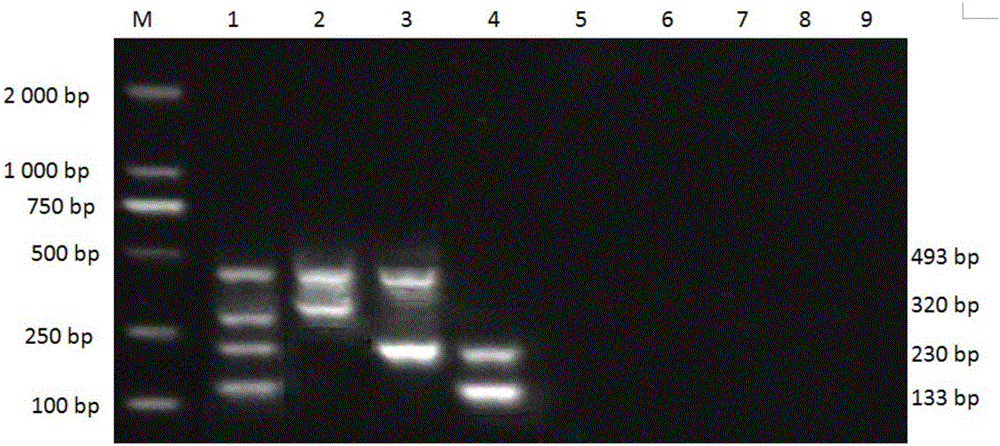
图1是多重PCR特异性试验结果图,图中:M 2000bp DNA分子质量标准,1四种重组质粒混合物,2 CH-1R,3 HuN4-F112,4 TJM-F92,5 PCV2,6 PRV,7 FMDV,8 CSFV,9阴性对照。
图2是多重PCR敏感性试验结果图,图中:M 2000bp DNA分子质量标准,1-9质粒浓度分别为1.13×109-1.13×101拷贝/μL,10阴性对照。
图3是多重PCR重复性试验结果图,图中M 2000bp DNA分子质量标准,1-6相同条件下的6次重复反应。
具体实施方式
以下实施例中,PRRSV美洲型经典毒株(CH-1R株)、美洲型变异毒株(HuN4-F112株)、疫苗毒TJM-F92株、猪瘟病毒(CSFV,疫苗毒C株)、猪口蹄疫病毒(FMDV,疫苗毒O/MYA/BY/2010株)、猪圆环病毒2型(PCV2,疫苗毒LG株)、猪伪狂犬病病毒(PRV,疫苗毒Bartha-K61株)均由广西壮族自治区动物疫病预防控制中心提供。
1、引物的设计
针对PRRSV美洲型经典株、高致病性变异株及疫苗株TJM-F92的Nsp2基因系列特点,利用Primer Express3.0软件设计并合成两对特异性引物。参照GenBank中发表的PRRSV VR-2332株、JXA1株、TJ株基因组序列,设计两对特异性引物,扩增Nsp2基因(表1)。
表1 引物信息
表1中,引物对B2-F/B2-R扩增C-PRRSV 320bp片段、扩增HP-PRRSV和V-PRRSV(TJM-F92株)230bp片段;引物对TJM-F/TJM-R扩增C-PRRSV和HP-PRRSV 493bp片段、扩增V-PRRSV(TJM-F92株)133bp片段。因此,利用引物对B2-F/B2-R和TJM-F/TJM-R扩增出320bp、493bp时为C-PRRSV,扩增出230bp、493bp时为HP-PRRSV,扩增出230bp、133bp时为V-PRRSV(TJM-F92株)。
2、样本制备
取2014-2016年广西各地发病死亡的疑似病猪的脾、肺、淋巴结适量,按比例(1∶4)加入1mol/L PBS(pH7.2)混合研磨后,反复冻融3次,离心取上清提取总RNA。应用所建立的多重RT-PCR,对PRRSV进行检测。
提取病毒总RNA后反转录获得cDNA,以此为模板进行PCR扩增PRRSV Nsp2基因片段,回收产物,连接载体、转化感受态细胞,选取阳性克隆,提取质粒,进行PCR鉴定、酶切鉴定、测序鉴定,证实成功构建了重组质粒标准品。
以CH-1R株、HuN4-F112株的cDNA为模板,由引物B2-F/B2-R扩增产物构建的重组质粒p-CH1R-B和p-HuN4-B;以HuN4-F112株、TJM-F92株的cDNA为模板,由引物TJM-F/TJM-R扩增产物构建的重组质粒p-HuN4-T和p-TJM-T。
3、试剂盒配置
根据研究结果,组装检测试剂盒以方便使用。试剂盒含有以下试剂:反转录RT反应液、PCR反应液、灭菌双蒸水,其中:
反转录RT反应液每管15μL,包括:5×Prime Scrip II buffer 4.0μL,dNTP(各10mM)1.0μL,随机引物6聚体(50pmol/μL)1.5μL,RNA酶抑制剂(40U/μL)0.5μL,RNase H-型反转录酶(200U/μL)1.0μL,灭菌双蒸水7μL;
PCR反应液每管45μL,包括:2×Taq PCR MasterMix 25μL,引物B2-F/B2-R上、下游引物(25pmol/μL)各1μL、引物TJM-F/TJM-R上、下游引物(25pmol/μL)各1μL,
灭菌双蒸水16μL。
4、多重RT-PCR程序及条件
经优化,确定多重RT-PCR的反应条件,包括反转录和PCR扩增两步程序。
20μL反转录体系为:5×Prime Scrip II buffer 4.0μL,dNTP(各10mM)1.0μL,随机引物6聚体(50pmol/μL,购自TaKaRa公司),PrimeScriptTM II 1st Strand cDNA Synthesis Kit试剂盒1.5μL,RNA酶抑制剂(40U/μL)0.5μL,RNase H-型反转录酶(200u/μL)1.0μL,模板总RNA 5.0μL,灭菌双蒸水7.0μL;反转录程序为:30℃10min,48℃45min,95℃5min。
50μL PCR反应体系为:2×Taq PCR MasterMix 25μL,引物B2-F/B2-R上、下游引物(25pmol/μL)各1μL、引物TJM-F/TJM-R上、下游引物(25pmol/μL)各1μL,cDNA 5μL,灭菌双蒸水补至50μL;反应程序为:94℃2min;94℃30s,58.9℃30s,72℃30s,35个循环;72℃10min。
5、本发明实验应用
应用前述配制的试剂盒和确定的最佳反应条件,以PRRSV经典株CH-1R、变异株HuN4-F112、疫苗株TJM-F92、CSFV、FMDV的cDNA以及PCV2、PRV的DNA为模板,进行多重PCR检测其特异性。如图1所示,只有PRRSV的3种毒株呈阳性,而CSFV、FMDV、PCV2、PRV均为阴性,没有交叉反应。结果表明,本发明PRRSV美洲型经典株、变异株和TJM-F92疫苗株多重RT-PCR检测试剂盒及其检测方法具有较强的特异性。
将4种重组质粒p-CH1R-B、p-HuN4-B、p-HuN4-T和p-TJM-T作10倍系列稀释成1.13×109-1.13×101拷贝/μL,将同一浓度梯度的各种质粒等体积混合后作为模板,进行多重PCR检测其敏感性,结果如图2,结果引物对B2-F/B2-R检测质粒p-CH1R-B、p-HuN4-B的检出下限均为1.13×103拷贝/μL,引物对TJM-F/TJM-R检测质粒p-HuN4-T、p-TJM-T的检出下限均为1.13×102拷贝/μL。表明本发明PRRSV美洲型经典株、变异株和TJM-F92疫苗株多重RT-PCR检测试剂盒及其检测方法具有较强的敏感性。
以等体积混合后浓度均为1.13×105拷贝/μL的4种重组质粒为模板,进行多重PCR,重复6次反应,分析其重复性。结果如图3,6次重复试验均能扩增出均匀一致的目的片段,表明本发明PRRSV美洲型经典株、变异株和TJM-F92疫苗株多重RT-PCR检测试剂盒及其检测方法具有较好的重复性。
- 还没有人留言评论。精彩留言会获得点赞!