一种2-氟-3-溴-苄胺的制备方法
一种2
‑
氟
‑3‑
溴
‑
苄胺的制备方法
技术领域
1.本发明属于化学合成技术领域,具体涉及一种2
‑
氟
‑3‑
溴
‑
苄胺的制备方法。
背景技术:
[0002]2‑
氟
‑3‑
溴
‑
苄胺是一种重要的化工中间体,在药物合成等领域具有广阔的应用前景。
[0003]
目前已公开的2
‑
氟
‑3‑
溴
‑
苄胺的合成方法主要有以下几种:
[0004]
(1)美国专利us8067408 b2以3
‑
溴
‑2‑
氟苯为原料,经多步反应先制得苯甲酰氯,又与氨水反应制得3
‑
溴
‑2‑
氟苯甲酰胺,最后采用硼烷二甲硫醚为还原剂,还原反应46%的收率得到2
‑
氟
‑3‑
溴
‑
苄胺。
[0005][0006]
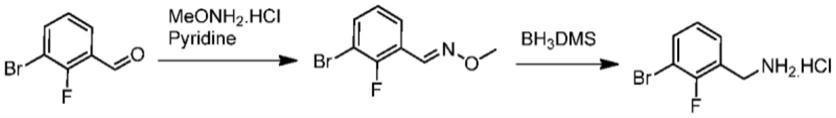
(2)pct专利wo2018/15879以3
‑
溴
‑2‑
氟苯甲醛,制得3
‑
溴
‑2‑
氟苯甲醛
‑
氧
‑
甲基肟,再以10当量硼烷二甲硫醚还原,然后与20%盐酸反应,87%收率制得2
‑
氟
‑3‑
溴
‑
苄胺盐酸盐。
[0007][0008]
(3)pct专利wo2012/93101公开了以3
‑
溴
‑2‑
氟苯甲腈为底物,在4%的氨
‑
乙醇溶液中,raney镍催化进行氢气还原,室温反应6.5h,再与1m盐酸反应制得目标化合物的盐酸盐。
[0009]
上述方法存在以下问题:或者原料成本高;或者反应步骤繁琐,导致反应收率低;或者涉及到危险试剂,不利于批量生产的安全操作。
技术实现要素:
[0010]
本发明针对现有技术合成2
‑
氟
‑3‑
溴
‑
苄胺存在的问题,提供一种新颖的2
‑
氟
‑3‑
溴
‑
苄胺合成方法,该合成方法生产成本低,产品收率高,适合工业化生产。
[0011]
本发明上述目的通过以下技术方案来实现:
[0012]
一种2
‑
氟
‑3‑
溴
‑
苄胺的合成方法,所述合成方法包括以下步骤:
[0013]
将2
‑
氟
‑3‑
溴苯腈溶解在有机溶剂中形成2
‑
氟
‑3‑
溴苯腈溶液,往2
‑
氟
‑3‑
溴苯腈溶液中滴加bh3.me2s(硼烷二甲基硫醚)溶液反应,然后滴加甲醇淬灭反应直至无氢气放出;反应物浓缩后加入甲醇溶解,回流搅拌,优选为回流搅拌2~5小时,去除溶剂后,将浓缩物过层析柱、洗脱得2
‑
氟
‑3‑
溴
‑
苄胺。
[0014]
作为优选,2
‑
氟
‑3‑
溴苯腈溶液中,2
‑
氟
‑3‑
溴苯腈的浓度为0.05~0.5g/ml。
[0015]
进一步优选,2
‑
氟
‑3‑
溴苯腈溶液中,2
‑
氟
‑3‑
溴苯腈的浓度为0.1~0.3g/ml。
[0016]
作为优选,滴加bh3.me2s溶液之前,将2
‑
氟
‑3‑
溴苯腈溶液降低温度至
‑
5~5℃,并充惰性气体保护。惰性气体优选为氮气或氩气。
[0017]
进一步优选,将2
‑
氟
‑3‑
溴苯腈溶液降低温度至
‑
2~2℃。
[0018]
作为优选,bh3.me2s溶液为bh3.me2s溶于有机溶剂中形成,bh3.me2s的浓度为1~5mol/l。
[0019]
作为优选,2
‑
氟
‑3‑
溴苯腈溶解的有机溶剂以及bh3.me2s溶解的有机溶剂为二氯甲烷、四氢呋喃中的一种或两种。
[0020]
进一步优选,2
‑
氟
‑3‑
溴苯腈溶解的有机溶剂以及bh3.me2s溶解的有机溶剂相同。
[0021]
作为优选,2
‑
氟
‑3‑
溴苯腈与bh3.me2s的摩尔比为1:(1.2~2.2)。
[0022]
进一步优选,,2
‑
氟
‑3‑
溴苯腈与bh3.me2s的摩尔比为1:(1.5~2.0)。
[0023]
作为优选,往2
‑
氟
‑3‑
溴苯腈溶液中滴加bh3.me2s溶液后保持温度搅拌20~60min,然后在室温下反应8~15h。
[0024]
本发明的室温定义为18~37℃。
[0025]
进一步优选,在室温下反应9~12h。
[0026]
作为优选,层析柱为氧化铝柱,洗脱剂为乙酸乙酯。
[0027]
作为优选,2
‑
氟
‑3‑
溴
‑
苄胺的收率≥93%,纯度≥99%。
[0028]
本发明相对于现有技术具有如下有益效果:
[0029]
1、本发明以成本低廉的2
‑
氟
‑3‑
溴苯腈作为原料,实现了2
‑
氟
‑3‑
溴
‑
苄胺的低成本制备;
[0030]
2、本发明精选bh3.me2s作为还原剂,相对于其它还原剂可有效提高2
‑
氟
‑3‑
溴
‑
苄胺的收率;
[0031]
3、本发明的反应体系在室温下反应8~15h,相对于高温反应,具有更高的2
‑
氟
‑3‑
溴
‑
苄胺收率;
[0032]
4、本发明的2
‑
氟
‑3‑
溴
‑
苄胺合成方法避免了气体反应物、叠氮化试剂,以及金属催化剂的使用,生产成本低,产品收率、纯度高,操作简易,适合工业化大批量生产。
具体实施方式
[0033]
在下文中,针对本发明的2
‑
氟
‑3‑
溴
‑
苄胺的合成方法,对本发明的技术方案作进一步描述说明,但并不构成对本发明的限制。
[0034]
在本发明的一些实施方式中,2
‑
氟
‑3‑
溴
‑
苄胺的合成路线如下所示:
[0035][0036]2‑
氟
‑3‑
溴
‑
苄胺的合成方法具体包括以下步骤:
[0037]
将2
‑
氟
‑3‑
溴苯腈溶解在有机溶剂中形成2
‑
氟
‑3‑
溴苯腈溶液,每100ml有机溶剂
加入5~50g 2
‑
氟
‑3‑
溴苯腈,其中有机溶剂为二氯甲烷、四氢呋喃中的一种或两种;将2
‑
氟
‑3‑
溴苯腈溶液降低温度至
‑
5~5℃,并充惰性气体保护,然后缓慢滴加bh3.me2s溶液,使得2
‑
氟
‑3‑
溴苯腈与bh3.me2s的摩尔比为1:(1.2~2.2),滴加完毕后,保持
‑
5~5℃搅拌20~60min,然后在室温下反应8~15h,其中bh3.me2s溶液为bh3.me2s溶于有机溶剂中形成,有机溶剂为二氯甲烷、四氢呋喃中的一种或两种,bh3.me2s溶液中bh3.me2s的浓度为1~5mol/l;然后滴加甲醇淬灭反应直至无氢气放出;减压蒸去溶剂,浓缩物加入甲醇溶解,回流搅拌2~5h,再次减压去除溶剂,将浓缩物过氧化铝层析柱、乙酸乙酯洗脱得2
‑
氟
‑3‑
溴
‑
苄胺。
[0038]
本发明2
‑
氟
‑3‑
溴
‑
苄胺的合成方法中,以廉价的2
‑
氟
‑3‑
溴苯腈作为原料,硼烷二甲基硫醚作为还原剂,室温下反应8~15h,然后以甲醇作为猝灭剂,柱层析获得2
‑
氟
‑3‑
溴
‑
苄胺。本发明的2
‑
氟
‑3‑
溴
‑
苄胺合成方法避免了气体反应物、叠氮化试剂,以及金属催化剂的使用,生产成本低,产品收率、纯度高,操作简易,适合工业化生产。
[0039]
下面通过具体实施例,对本发明的技术方案作进一步描述说明,应当理解的是,此处所描述的具体实施例仅用于帮助理解本发明,不用于本发明的具体限制。如果无特殊说明,本发明的实施例中所采用的原料均为本领域常用的原料,实施例中所采用的方法,均为本领域的常规方法。
[0040]
实施例1
[0041]
本实施例的2
‑
氟
‑3‑
溴
‑
苄胺由以下步骤合成:
[0042]
将2.37g 2
‑
氟
‑3‑
溴苯腈溶解在20ml四氢呋喃中形成2
‑
氟
‑3‑
溴苯腈溶液,将2
‑
氟
‑3‑
溴苯腈溶液降低温度至0℃,并充氮气保护,然后缓慢滴加8.9ml 2mol/l的bh3.me2s四氢呋喃溶液,滴加完毕后,保持0℃搅拌30min,然后在室温下继续反应12h;然后缓慢滴加甲醇至反应体系中淬灭反应,直至无氢气放出;减压蒸去溶剂,浓缩物加入20ml甲醇溶解,回流搅拌3h,将硼化物完全淬灭,再次减压去除溶剂,将浓缩物过氧化铝层析柱、乙酸乙酯洗脱得无色油状物2
‑
氟
‑3‑
溴
‑
苄胺2.32g,收率95.7%。
[0043]1h nmr(300mhz,d2o)δ4.10(s,2h),7.01(t,j=7.8hz,1h),7.27(t,j=7.2hz,1h),7.55(t,j=7.5hz,1h);纯度(99.7%,hplc)。
[0044]
收率=(实际获得的无色油状物质量*2
‑
氟
‑3‑
溴
‑
苄胺纯度)/理论获得的2
‑
氟
‑3‑
溴
‑
苄胺质量
[0045]
实施例2
[0046]
将4g 2
‑
氟
‑3‑
溴苯腈溶解在20ml二氯甲烷中形成2
‑
氟
‑3‑
溴苯腈溶液,将2
‑
氟
‑3‑
溴苯腈溶液降低温度至
‑
2℃,并充氮气保护,然后缓慢滴加18ml 2mol/l的bh3.me2s二氯甲烷溶液,滴加完毕后,保持
‑
2℃搅拌40min,然后在室温下继续反应11h;然后缓慢滴加甲醇至反应体系中淬灭反应,直至无氢气放出;减压蒸去溶剂,浓缩物加入40ml甲醇溶解,回流搅拌4h,将硼化物完全淬灭,再次减压去除溶剂,将浓缩物过氧化铝层析柱、乙酸乙酯洗脱得无色油状物2
‑
氟
‑3‑
溴
‑
苄胺3.87g,收率94.5%,纯度(99.6%,hplc)。
[0047]
实施例3
[0048]
将6g 2
‑
氟
‑3‑
溴苯腈溶解在20ml四氢呋喃中形成2
‑
氟
‑3‑
溴苯腈溶液,将2
‑
氟
‑3‑
溴苯腈溶液降低温度至2℃,并充氩气保护,然后缓慢滴加12ml 5mol/l的bh3.me2s四氢呋喃溶液,滴加完毕后,保持2℃搅拌60min,然后在室温下继续反应10h;然后缓慢滴加甲醇至反应体系中淬灭反应,直至无氢气放出;减压蒸去溶剂,浓缩物加入60ml甲醇溶解,回流搅拌
5h,将硼化物完全淬灭,再次减压去除溶剂,将浓缩物过氧化铝层析柱、乙酸乙酯洗脱得无色油状物2
‑
氟
‑3‑
溴
‑
苄胺5.92g,收率96.2%,纯度(99.4%,hplc)。
[0049]
实施例4
[0050]
将2g 2
‑
氟
‑3‑
溴苯腈溶解在20ml四氢呋喃中形成2
‑
氟
‑3‑
溴苯腈溶液,将2
‑
氟
‑3‑
溴苯腈溶液降低温度至1℃,并充氩气保护,然后缓慢滴加13ml 1mol/l的bh3.me2s四氢呋喃溶液,滴加完毕后,保持1℃搅拌50min,然后在室温下继续反应11h;然后缓慢滴加甲醇至反应体系中淬灭反应,直至无氢气放出;减压蒸去溶剂,浓缩物加入30ml甲醇溶解,回流搅拌5h,将硼化物完全淬灭,再次减压去除溶剂,将浓缩物过氧化铝层析柱、乙酸乙酯洗脱得无色油状物2
‑
氟
‑3‑
溴
‑
苄胺1.91g,收率93.2%,纯度(99.5%,hplc)。
[0051]
对比例1
[0052]
对比例1与实施例1的区别在于,采用还原剂bh3.thf四氢呋喃溶液取代bh3.me2s四氢呋喃溶液,其它与实施例1相同。获得的2
‑
氟
‑3‑
溴
‑
苄胺收率为90.9%,纯度(99.3%,hplc)。
[0053]
对比例2
[0054]
对比例2与实施例1的区别在于,滴加bh3.me2s四氢呋喃溶液,保持0℃搅拌30min,然后升温至65℃继续反应1h,其它与实施例1相同。获得的2
‑
氟
‑3‑
溴
‑
苄胺收率为92.8%,纯度(99.2%,hplc)。
[0055]
对比例3
[0056]
对比例3与实施例1的区别在于,滴加bh3.me2s四氢呋喃溶液,保持0℃搅拌30min,然后升温至65℃继续反应2h,其它与实施例1相同。获得的2
‑
氟
‑3‑
溴
‑
苄胺收率为92.2%,纯度(99.4%,hplc)。
[0057]
本发明采用bh3.me2s作为还原剂,相对于还原剂bh3.thf具有更好的收率。对比例2和对比例3采用高温反应,虽然能缩短反应时间,但是2
‑
氟
‑3‑
溴
‑
苄胺的收率相对于实施例1的95.7%下降显著。
[0058]
本文中所述具体实施例仅是对本发明精神作举例说明,并不限定本发明的保护范围。本发明所属技术领域的技术人员可以对所描述的具体实施例做各种各样的修改或补充或采用类似的方式替代,但并不会偏离本发明的精神或者超越所附权利要求书所定义的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1