倍癌霉素衍生物及其应用
1.本发明涉及倍癌霉素衍生物与生物素修饰二聚体的缀合物、以及其应用。
背景技术:
2.抗生物素蛋白与生物素、或链霉亲和素与生物素之间的亲和性非常高(kd=10-15
~10-14
m),并且生物双分子间的相互作用是最强的相互作用之一。目前,抗生物素蛋白/链霉亲和素-生物素相互作用被广泛应用于生物化学、分子生物学或医学领域。已经设计了将抗生物素蛋白/链霉亲和素与生物素的高结合能力和抗体分子组合的药物递送的方法和预靶向法。专利文献1中报道了降低了对天然生物素的亲和性的链霉亲和素突变体、以及对该对天然生物素的低亲和性的链霉亲和素突变体具有高亲和性的生物素修饰二聚体。
3.倍癌霉素是从链霉菌属分离的一组天然产物,并且已经分离、合成了多种类似物。具有二烯酮环丙烷作为共用结构的这些化合物显示dna烷基化作用,显示强力的抗肿瘤活性。二烯酮环丙烷环通常缺乏亲电子性。若倍癌霉素与双链dna的次要组(minor group)结合,则空间构象以扭转的形式固定。此时,二烯酮与氮原子的孤对电子不能共轭,二烯酮部分的亲电子性提高。其结果是,dna的腺嘌呤碱基的烷基化在环丙烷位点进行,显示高抗癌作用。
4.显示强力的抗肿瘤活性的倍癌霉素类作为抗癌剂是有吸引力的,临床应用的研究也在进行。但是,由于使用后的迟发性肝毒性的问题、低分子药剂所引起的脱靶的问题等,没有倍癌霉素类单独被承认作为医药品的实例。
5.另一方面,专利文献2中记载了毒素复合体,其中,通过含有聚亚烷基二醇和二肽的间隔物将来源于对靶细胞具有亲和性的化合物的残基与毒素残基结合。另外,非专利文献1中记载了新的倍癌霉素衍生物du-257的合成和在免疫缀合物中的应用,所述免疫缀合物使用能够肿瘤特异性活化的聚(乙二醇)二肽基接头。
6.现有技术文献专利文献专利文献1:国际公开wo2015/125820;专利文献2:国际公开wo96/35451;非专利文献非专利文献1:bioorganic & medicinal chemistry 8 (2000) 2175-2184。
技术实现要素:
7.发明所要解决的课题本发明要解决的课题在于提供可用于预靶向法的倍癌霉素衍生物与生物素修饰二聚体的缀合物。此外,本发明要解决的课题还在于提供使用上述的倍癌霉素衍生物与生物素修饰二聚体的缀合物、以及链霉亲和素突变体-分子探针缀合物的组合的治疗试剂盒。
8.用于解决课题的手段
本发明人为了解决上述课题而进行了深入研究,结果发现,通过合成新的倍癌霉素衍生物与生物素修饰二聚体的缀合物,并将其与链霉亲和素突变体-分子探针缀合物组合使用,可有效地抑制细胞增殖,从而完成了本发明。
9.即,根据本发明,提供以下发明。
10.《1》 用下述式(1)或式(2)表示的化合物:[化学式1]式中,r1和r2各自独立地表示氢原子、低级烷基或低级烷氧基羰基;r3、r4和r5中的一个表示-o-l
7-(xaa)
m-l
6-n3,剩余的2个各自独立地表示氢原子、低级烷基或低级烷氧基;x表示反应性基团;l6和l7各自独立地表示2价连接基;xaa表示氨基酸残基;m表示2~10的整数;me表示甲基。
[0011]
《2》 根据《1》所述的化合物,其用下述式(3a)或式(3b)表示:[化学式2]
式中的符号的定义与权利要求1同义。
[0012]
《3》 根据《1》或《2》所述的化合物,其中,-(xaa)
m-为-val-ala-。
[0013]
《4》 根据《1》~《3》中任一项所述的化合物,其中,l6为-co-(-o-ch2)
n-,式中,n表示1~10的整数,l7为-(ch2)
p-nh-,式中,p表示1~5的整数。
[0014]
《5》 用下述式(4)表示的化合物:[化学式3]式中,r1和r2各自独立地表示氢原子、低级烷基或低级烷氧基羰基,r
30
、r
40
和r
50
中的一个表示以下基团,[化学式4]剩余的2个各自独立地表示氢原子、低级烷基或低级烷氧基,x1a、x1b、x2a和x2b各自独立地表示o或nh,y1和y2各自独立地表示c或s,z1和z2各自独立地表示o、s或nh,
v1和v2各自独立地表示s或s
+-o-,n1和n2各自独立地表示0或1的整数,l1和l2各自独立地表示2价连接基,l3表示3价连接基,l4、l5、l6和l7各自独立地表示2价连接基,xaa表示氨基酸残基,m表示2~10的整数。
[0015]
《6》 根据《5》所述的化合物,其中,r
30
、r
40
和r
50
中的一个为以下基团:[化学式5]式中的各符号的含义与权利要求5同义。
[0016]
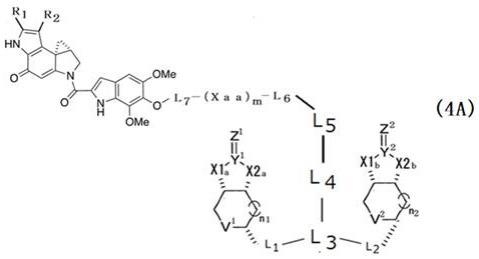
《7》 用下述式(4a)表示的化合物:[化学式6]式中,x1a、x1b、x2a和x2b各自独立地表示o或nh,y1和y2各自独立地表示c或s,z1和z2各自独立地表示o、s或nh,v1和v2各自独立地表示s或s
+-o-,n1和n2各自独立地表示0或1的整数,l1和l2各自独立地表示2价连接基,l3表示3价连接基,
l4、l5、l6和l7各自独立地表示2价连接基,xaa表示氨基酸残基,m表示2~10的整数,me表示甲基,r1和r2各自独立地表示氢原子、低级烷基或低级烷氧基羰基。
[0017]
《8》 根据《5》所述的化合物,其用下述式(5)表示:[化学式7]式中的各符号的含义与权利要求5同义。
[0018]
《9》 根据《5》~《8》中任一项所述的化合物,其中,x1a、x1b、x2a和x2b表示nh,y1和y2表示c,z1和z2表示nh,v1和v2表示s。
[0019]
《10》 根据《5》~《9》中任一项所述的化合物,其中,l1和l2各自独立地为包含选自-conh-、-nhco-、-coo-、-oco-、-co-、-o-和碳原子数为1~10的亚烷基的基团的组合的2价连接基。
[0020]
《11》 根据《5》~《10》中任一项所述的化合物,其中,l4为包含选自-conh-、-nhco-、-coo-、-oco-、-co-、-o-、-nh-和碳原子数为1~10的亚烷基的基团的组合的基团。
[0021]
《12》 根据《5》~《11》中任一项所述的化合物,其中,l5为包含三唑基、-s-、-conh-、-nhco-、-coo-、-oco-、-co-、-o-、-nh-、碳原子数为1~10的亚烷基或它们的组合的基团。
[0022]
《13》 以下的化合物或其盐:[化学式8]
。
[0023]
《14》 治疗试剂盒,其中,包含:(a) 《5》~《13》中任一项所述的化合物;和(b) 链霉亲和素突变体与分子探针的缀合物,其包含seq id no: 1中记载的氨基酸序列,其中,c末端的组氨酸标签的一部分或全部可缺失。
[0024]
《15》 根据《14》所述的治疗试剂盒,其中,分子探针为抗ereg抗体、抗cea抗体或抗her2抗体。
[0025]
发明效果通过使用本发明的缀合物,可有效地抑制癌细胞的增殖。
附图说明
[0026]
[图1] 图1表示结构域结构的概略。
[0027]
[图2] 图2表示cea-v2122的sds-page电泳cbb 染色图像。
[0028]
[图3] 图3表示cea-v2122与抗原(ceacam5)的结合性能评价。
[0029]
[图4] 图4表示cea-v2122与生物素修饰体的结合性能评价。
[0030]
[图5] 图5表示fitc标记cea-v2122的细胞染色图像。
[0031]
[图6] 图6表示fitc标记cea-v2122的细胞染色图像mkn45 细胞时序数据。
[0032]
[图7] 图7表示化合物5的结构。
[0033]
[图8] 图8表示使用cea-v2122 和抗癌剂标记生物素修饰体的细胞毒性试验的测定结果。
[0034]
[图9] 图9表示化合物x (倍癌霉素sa)的结构。
[0035]
[图10] 图10表示化合物y (倍癌霉素sa-缬氨酸)的结构。
[0036]
[图11] 图11表示化合物x (倍癌霉素sa)和化合物y (倍癌霉素sa-缬氨酸)的细胞毒性试验的测定结果。
具体实施方式
[0037]
以下,对本发明进行更详细的说明。
[0038]
(1) 倍癌霉素衍生物本发明的倍癌霉素衍生物是在倍癌霉素类上结合有接头(linker)的化合物,具体而言,是用下述式(1)、式(2) (例如式(2a)或式(2b))表示的化合物。
[0039]
[化学式9]
[化学式10][化学式11]本发明的化合物更优选为用下述式(3a)或下述式(3b)表示的化合物。
[0040]
[化学式12]
[化学式13]在式(1)中,x表示反应性基团。作为反应性基团,可列举出:-n3、碳化二亚胺(例如edc)、nhs酯、酰亚胺酯、马来酰亚胺、卤乙酸(溴乙酸或碘乙酸)、吡啶基二硫醚、硫代砜、乙烯基砜、酰肼、烷氧基胺、芳基叠氮化物、异氰酸酯、炔烃、烯烃、四嗪等,但没有特别限定。
[0041]
在式(2)中,r3、r4和r5中的一个表示-o-l
7-(xaa)
m-l
6-n3,剩余的2个各自独立地表示氢原子、低级烷基(例如碳原子数为1~6的烷基,优选为碳原子数为1~4的烷基)或低级烷氧基(例如碳原子数为1~6的烷氧基,优选为碳原子数为1~4的烷氧基)。
[0042]
在式(1)~式(3)中,l6和l7各自独立地表示2价连接基。作为2价连接基,可列举出:组合-co-、-o-、-ch
2-、-nh-而成的基团。作为2价连接基,更具体地说,可列举出:组合-co-、(-o-ch2)n‑ꢀ
(式中,n表示1~10的整数)、-(ch2)
p (式中,p表示1~5的整数)、-nh-而成的基团。作为l6的一个实例,为-co-(-o-ch2)n‑ꢀ
(式中,n表示1~10的整数)。作为l7的一个实例,为-(ch2)
p-nh
‑ꢀ
(式中,p表示1~5的整数)。
[0043]
在式(1)~式(3)中,xaa表示氨基酸残基,m表示2~10的整数,优选表示2~7的整数,更优选表示2~5的整数,进一步优选为2、3或4。
[0044]
作为氨基酸残基,可以是丙氨酸残基、半胱氨酸残基、天冬氨酸残基、谷氨酸残基、苯丙氨酸残基、甘氨酸残基、组氨酸残基、异亮氨酸残基、赖氨酸残基、亮氨酸残基、蛋氨酸残基、天冬酰胺残基、脯氨酸残基、谷氨酰胺残基、精氨酸残基、丝氨酸残基、苏氨酸残基、缬氨酸残基、色氨酸残基、酪氨酸残基、瓜氨酸残基(cit)中的任一种。氨基酸残基优选为缬氨酸残基和丙氨酸残基。作为-(xaa)
m-的具体例,可列举出:-val-ala-、-phe-lys-和-val-cit-,但没有特别限定。
[0045]
在式(1)~式(3)中,me表示甲基。
[0046]
在式(2)中,r1和r2各自独立地表示氢原子、低级烷基(例如碳原子数为1~6的烷基,优选为碳原子数为1~4的烷基)或低级烷氧基羰基(优选为碳原子数为2~7的烷氧基羰基,优选为碳原子数为2~5的烷氧基羰基)。
[0047]
本发明的倍癌霉素衍生物可依据实施例中记载的方法合成。
[0048]
(2) 缀合物本发明涉及倍癌霉素衍生物与生物素修饰二聚体的缀合物,是用下述式(4)表示的化合物或其盐。本发明的缀合物优选为用下述式(4a)表示的化合物或其盐,或用下述式(5)表示的化合物或其盐。
[0049]
[化学式14]式中,r1和r2各自独立地表示氢原子、低级烷基或低级烷氧基羰基,r
30
、r
40
和r
50
中的一个表示以下基团,[化学式15]剩余的2个各自独立地表示氢原子、低级烷基或低级烷氧基,x1a、x1b、x2a和x2b各自独立地表示o或nh,y1和y2各自独立地表示c或s,z1和z2各自独立地表示o、s或nh,v1和v2各自独立地表示s或s
+-o-,n1和n2各自独立地表示0或1的整数,l1和l2各自独立地表示2价连接基,l3表示3价连接基,l4、l5、l6和l7各自独立地表示2价连接基,xaa表示氨基酸残基,m表示2~10的整数。
[0050]
[化学式16]
[化学式17]在上述中,r
30
、r
40
和r
50
中的一个优选为以下基团,[化学式18]。
[0051]
生物素修饰二聚体部分是用下述式(11)表示的化合物或其盐,优选为用下述式
(12)表示的化合物或其盐。生物素修饰二聚体可使用国际公开wo2015/125820号中记载的化合物。
[0052]
[化学式19][化学式20]式中,x1a、x1b、x2a和x2b各自独立地表示o或nh,y1和y2各自独立地表示c或s,z1和z2各自独立地表示o、s或nh,v1和v2各自独立地表示s或s
+-o-,n1和n2各自独立地表示0或1的整数,l1和l2各自独立地表示2价连接基,l3表示3价连接基,l4表示2价连接基。
[0053]
在上述式中,用下述结构:[化学式21]表示的部分优选为以下基团中的任一种,[化学式22]
但不限定于这些。
[0054]
x1a、x1b、x2a和x2b优选表示nh,y1和y2优选表示c,z1和z2优选表示nh,v1和v2优选表示s。
[0055]
l1和l2各自独立地优选为包含选自-conh-、-nhco-、-coo-、-oco-、-co-、-o-和碳原子数为1~10的亚烷基的基团的组合的2价连接基。
[0056]
l1和l2各自独立地优选为包含选自-conh-、-nhco-、-o-和碳原子数为1~10的亚烷基的基团的组合的2价连接基。
[0057]
l1和l2各自独立地优选为包含选自-conh-、-nhco-和碳原子数为1~10的亚烷基的基团的组合的2价连接基。
[0058]
l3表示3价连接基,优选为[化学式23]或[化学式24](来源于苯的3价连接基或氮原子)。
[0059]
l4优选为包含选自-conh-、-nhco-、-coo-、-oco-、-co-、-o-、-nh-和碳原子数为1~10的亚烷基的基团的组合的基团。
[0060]
l5优选为包含三唑基、-s-、-conh-、-nhco-、-coo-、-oco-、-co-、-o-、-nh-、碳原子数为1~10的亚烷基或它们的组合的基团。
[0061]
本发明的缀合物可依据后述的实施例中的使化合物3 (在末端具有反应性基团的生物素修饰二聚体)与化合物4 (倍癌霉素衍生物)反应来合成化合物5的方法合成。
[0062]
(3) 使用倍癌霉素衍生物与生物素修饰二聚体的缀合物的治疗试剂盒
根据本发明,提供组合倍癌霉素衍生物与生物素修饰二聚体的缀合物、和链霉亲和素突变体-分子探针缀合物而成的治疗试剂盒。
[0063]
作为链霉亲和素突变体,可使用国际公开wo2014/129446和国际公开wo2015/125820中记载的链霉亲和素突变体。特别优选可使用国际公开wo2015/125820的实施例3 (国际公开wo2015/125820的seq id no: 4) (本技术说明书的seq id no: 1)中记载的链霉亲和素突变体lisa314-v2122。
[0064]
作为分子探针,例如可列举出:抗体、肽、核酸、适配体等,具体而言,可使用以在癌症中特异性表达的以下抗原为靶的抗体、肽、核酸、适配体等。
[0065]
表皮调节素(ereg),robo1、2、3、4,1-40-β-淀粉状蛋白,4-1bb,5ac,5t4,acvr2b,腺癌抗原,α-胎蛋白,血管生成素2,炭疽毒素,aoc3 (vap-1),b-淋巴瘤细胞,b7-h3,baff,β淀粉状蛋白,c242抗原,c5,ca-125,碳酸酐酶9 (ca-ix),心脏肌球蛋白,ccl11 (嗜酸性粒细胞趋化因子-1),ccr4,ccr5,cd11,cd18, cd125,cd140a,cd147 (basigin),cd147 (basigin),cd15,cd152,cd154 (cd40l),cd154,cd19,cd2,cd20,cd200,cd22,cd221,cd23 (ige受体),cd25 (il-2受体的α链),cd28,cd3,cd30 (tnfrsf8),cd33,cd37,cd38 (cadp核糖水解酶),cd4,cd40,cd41 (整合素α-iib),cd44 v6,cd5,cd51,cd52,cd56,cd6,cd70,cd74,cd79b,cd80,cea,cfd,ch4d5,cldn18.2,艰难梭状芽孢杆菌(clostridium difficile),凝聚因子a,csf2,ctla-4,巨细胞病毒,巨细胞病毒糖蛋白b,dll4,dr5,大肠杆菌志贺毒素1型,大肠杆菌志贺毒素2型,egfl7,egfr,内毒素,epcam,episialin,erbb3,大肠杆菌(escherichia coli),呼吸道合胞体病毒(respiratory syncytial virus)的f蛋白,fap,纤维蛋白iiβ链,纤维连接蛋白额外结构域-b,叶酸受体1,frizzled 受体,gd2,gd3神经节苷脂,gmcsf受体α链,gpnmb,乙型肝炎表面抗原,乙型肝炎病毒,her1,her2/neu,her3,hgf,hiv-1,hla-drβ,hngf,hsp90,人β淀粉状蛋白,人分散因子(scatter factor)受体激酶,人tnf,icam-1 (cd54),ifn-α,ifn-γ,ige,ige fc区,igf-1受体,igf-i,igg4,ighe,il-1β,il-12,il-13,il-17,il-17a,il-22,il-23,il-4,il-5,il-6,il-6受体,il-9,ilgf2,甲型流感血凝素,胰岛素样生长因子i受体,整合素α4,整合素α4β7,整合素α5β1,整合素α7β7,整合素αiibβ3,整合素αvβ3,整合素γ诱导蛋白,干扰素受体,干扰素α/β受体,itga2,itgb2 (cd18),kir2d,l-选择蛋白(cd62l),lewis-y抗原,lfa-1 (cd11a),脂磷壁酸,loxl2,lta,mcp-1,间皮素,ms4a1,muc1,粘蛋白canag,肌抑素,n-羟乙酰神经氨酸,narp-1,nca-90 (粒细胞抗原),ngf,nogo-a,nrp1,穴兔(oryctolagus cuniculus),ox-40,oxldl,pcsk9,pd-1,pdcd1,pdgf-rα,磷酯酰丝氨酸,前列腺癌细胞,绿脓杆菌(pseudomonas aeruginosa),狂犬病病毒糖蛋白,rankl,呼吸道合胞体病毒,rhd,rh (猕猴)因子,ron,rtn4,硬化蛋白(sclerostin),sdc1,选择蛋白p,slamf7,sost,鞘氨醇-1-磷酸酯,tag-72,tem1,肌腱蛋白c,tfpi,tgfβ1,tgfβ2,tgf-β,tnf-α,trail-r1,trail-r2,肿瘤抗原ctaa16.88,muc1的肿瘤特异性糖基化,tweak受体,tyrp1 (糖蛋白75),vegf-a,vegfr-1,vegfr2,波形蛋白,vwf。
[0066]
在上述中,优选表皮调节素(ereg)、cea和her2。
[0067]
调制癌抗原特异性抗体分子等的分子探针与链霉亲和素突变体的融合体,并对患者进行给药,由此可使链霉亲和素突变体特异性地聚集在癌细胞中。接着,通过将对上述链霉亲和素突变体具有亲和性的生物素修饰二聚体与倍癌霉素衍生物的缀合物,对患者进行
给药,可使酞菁染料可靠地向癌细胞聚集。
[0068]
或者,在本发明中,也可调制使癌抗原特异性抗体分子等的分子探针与链霉亲和素突变体的缀合物、和生物素修饰二聚体与倍癌霉素衍生物的缀合物结合而成的复合体,并将该复合体对患者进行给药。
[0069]
与链霉亲和素突变体结合的抗体可使用各种分子。多克隆抗体、单克隆抗体均可使用。对抗体的亚类没有特别限制,优选使用igg、特别适合使用igg1。另外,“抗体”包括所有的修饰抗体和抗体片段。可列举出:人源化抗体、人型抗体、人抗体,小鼠、兔、大鼠、豚鼠、猴等各种动物来源抗体,人抗体与各种动物来源抗体的嵌合抗体,双抗体(diabody)、scfv、fd、fab、fab’、f(ab)
’2,但不限于这些。
[0070]
链霉亲和素突变体与抗体的结合物可使用本领域技术人员公知的方法得到。例如,既可通过化学结合方法(us5,608,060)得到,也可通过将编码链霉亲和素突变体的dna和编码抗体的dna连接,使用表达载体等使其在宿主细胞中表达,由此作为融合蛋白得到。编码链霉亲和素突变体的dna和编码抗体的dna的连接可介助被称为接头的编码合适肽的dna。链霉亲和素突变体-抗体结合物希望保留抗体与靶分子的特异性结合力而制作。
[0071]
通过以下的实施例来更具体地说明本发明,但本发明不受实施例的限定。
实施例
[0072]
实施例1:缀合物的合成6-(2-((叔丁氧基羰基)氨基)乙氧基)-5,7-二甲氧基-1h-吲哚-2-甲酸甲酯[化学式25]在化合物1 (suzawa, t.; nagamura, s.; saito, h.; ohta, s.; hanai, n.; yamasaki, m. j. control. release 2000, 69, 27) (70.8mg,0.241mmol)的四氢呋喃(4.8ml)溶液中加入二碳酸二叔丁酯(106mg,0.486mmol),在氩气氛下、在室温下搅拌4小时。减压馏去溶剂,用硅胶柱色谱法(己烷/乙酸乙酯=5:1
→
1:1)纯化所得到的粗产物,得到化合物2 (92.2mg,收率97%,无色无定形状)。
[0073]
hrms (esi): m/z 417.1627 [m
+
+na]1h nmr (400mhz, cdcl3) δ:1.38 (s, 9h), 3.31-3.39 (m, 2h), 3.82 (s, 3h), 3.85 (s, 3h), 3.97 (s, 3h), 4.06 (t, 2h, j=5.0 hz), 5.57 (br s, 1h), 6.76 (s, 1h), 7.02 (d, 1h, j=2.4hz), 8.79 (br s, 1h)。
[0074]
6-(2-((叔丁氧基羰基)氨基)乙氧基)-5,7-二甲氧基-1h-吲哚-2-甲酸[化学式26]
在化合物2 (233mg,0.591mmol) 的四氢呋喃(6.0ml)溶液中加入1当量的氢氧化钠水溶液 (6.0ml),在氩气氛下、在50 ℃下搅拌8.5小时。在室温下加入1当量的盐酸,用二氯甲烷进行提取后,用饱和食盐水洗涤有机层。用硫酸钠干燥后,馏去溶剂,得到化合物3 (198mg,收率88%,无色无定形状)。
[0075]
hrms (esi): m/z 381.1642 [m
+
+h]1h nmr (400mhz, cd3od) δ:1.42 (s, 9h), 3.37 (t, 2h, j=5.4hz), 3.86 (s, 3h), 4.01 (s, 3h), 4.06 (t, 2h, j=5.4hz), 5.57 (br s, 1h), 6.91 (s, 1h), 7.07 (s, 1h)。
[0076]
(2-((2-(氯羰基)-5,7-二甲氧基-1h-吲哚-6-基)氧基)乙基)氨基甲酸叔丁酯[化学式27]在化合物3 (120mg,0.315mmol) 的二氯甲烷(3.2ml)溶液中加入草酰氯(41
µ
l,0.47mmol)和n,n-二甲基甲酰胺(1
µ
l),在氩气氛下、在室温下搅拌30分钟。馏去溶剂,得到化合物4的粗产物。
[0077]
(4-硝基苯基)甲酸2-(2-(2-叠氮基乙氧基)乙氧基)乙酯[化学式28]在0℃下在醇5 (dijken, d. j.; chen, j.; stuart, m. c. a.; hou, j.; feringa, b. l. j. am. chem. soc. 2016, 138, 660) (186mg,1.06mmol)和三乙胺(520
µ
l,3.72mmol)的二氯甲烷(5.3ml)溶液中加入氯甲酸4-硝基苯酯(257mg,1.28mmol),在氩气氛下、在0℃下搅拌1.5小时。加入二氯甲烷,用饱和碳酸氢钠水溶液和水洗涤有机层,用硫酸钠干燥。馏去溶剂,通过硅胶柱色谱法(二氯甲烷/乙酸乙酯=100:0
→
4:1)纯化所得到的粗产物,得到化合物6 (325mg,收率97%,淡黄色油状)。
[0078]
hrms (esi): m/z 363.0909 [m
+
+na]1h nmr (400mhz, cdcl3) δ:3.37 (t, 2h, j=5.2hz), 3.65-3.73 (m, 6h), 3.80-3.85 (m, 2h), 4.41-4,46 (m, 2h), 7.38 (d, 2h, j=9.2hz), 8.26 (d, 2h, j=9.2hz)。
[0079]
((2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)羰基)-l-丙氨酸甲酯[化学式29]在0℃下在碳酸酯6 (47.9mg,0.151mmol)、l-丙氨酸甲酯盐酸盐(32.2mg,0.231mmol)的n,n-二甲基甲酰胺(760
µ
l)溶液中加入n,n-二异丙基乙胺(65
µ
l,0.38mmol)。在氩气氛下、在室温下搅拌6小时后,减压馏去溶剂。用硅胶柱色谱法(己烷/乙酸乙酯=1:1
→
1:3)纯化所得到的粗纯化物,得到化合物 7 (39.8mg,收率87%,淡黄色油状)。
[0080]
hrms (esi): m/z 327.1283 [m
+
+na]1h nmr (600mhz, cdcl3) δ:1.41 (d, 3h, j=6.6hz), 3.40 (t, 2h, j=4.8hz), 3.65-3.71 (m, 8h), 3.75 (s, 3h), 4.20-4.27 (m, 2h), 4.36 (quint, 1h, j=7.2hz), 5.50 (d, 1h, j=6.0hz)。
[0081]
((2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)羰基)-l-丙氨酸[化学式30]在室温下在化合物7 (12.5mg,41.1
µ
mol)的四氢呋喃(1.0ml)溶液中加入1当量的氢氧化钠水溶液(1.0ml)。在氩气氛下、在室温下搅拌2.5小时后,加入1当量的盐酸,用二氯甲烷提取。用饱和食盐水洗涤有机层,用硫酸钠干燥后,馏去溶剂,得到化合物8 (11.0mg,收率92%,白色无定形状)。
[0082]
hrms (esi): m/z 313.1121 [m
+
+na]1h nmr (600mhz, cd3od) δ:1.38 (d, 3h, j=7.2hz), 3.35-3.40 (m, 2h), 3.63-3.71 (m, 8h), 4.13-4.22 (m, 3h, overlapped)。
[0083] ((2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)羰基)-l-丙氨酸2,5-二氧代吡咯烷-1-基酯[化学式31]在0℃下在羧酸8 (11.0mg,37.9
µ
mol)的四氢呋喃(500
µ
l)溶液中加入n-羟基琥珀酰亚胺(4.8mg,42
µ
mol)和n,n
’‑
二环己基碳化二亚胺(8.6mg,42
µ
mol)。在氩气氛下、在室温下搅拌12小时,过滤所生成的白色悬浮液。馏去溶剂,用硅胶柱色谱法(己烷/乙酸乙酯=1:1
→
1:3)纯化所得到的粗产物,得到化合物9 (6.6mg,42%,无色油状)。
[0084]
hrms (esi): m/z 410.1276 [m
+
+na]1h nmr (600mhz, cdcl3) δ:1.60 (d, 3h, j=7.8hz), 2.85 (s, 4h), 3.39 (t, 2h, j=4.8hz), 3.65-3.73 (m, 8h), 4.23-4.32 (m, 2h), 4.70-4.80 (m, 1h), 5.35 (d, 1h, j=6.6hz)。
[0085]
(s)-4-(苄氧基)-6-(6-(2-((叔丁氧基羰基)氨基)乙氧基)-5,7-二甲氧基-1h-吲哚-2-羰基)-8-((叔丁基二甲基甲硅烷基)氧基)-6,7,8,9-四氢-3h-吡咯并[3,2-f]喹啉-2,3-二甲酸3-苄基-2-甲酯[化学式32]在0℃下在化合物10 (yamada, k.; kurokawa, t.; tokuyama, h.; fukuyama, t. j. am. chem. soc. 2003, 125, 6630;和okano, k.; tokuyama, h.; fukuyama, t. chem. asian. j. 2008, 3, 296.) (150mg,0.250mmol)的二氯甲烷(2.5ml)溶液中加入吡啶(45
µ
l,0.56mmol)和化合物4 (130mg,0.313mmol)的二氯甲烷(4.0ml)溶液,在氩气氛下、在0℃下搅拌5分钟。加入1当量的盐酸,用二氯甲烷提取,用饱和碳酸氢钠水溶液、水、饱和食盐水洗涤有机层。用硫酸钠干燥后,馏去溶剂,用硅胶柱色谱法(己烷/乙酸乙酯=1:1)纯化所得到的粗产物,得到化合物11 (229mg,收率95%,黄色无定形状)。
[0086]
hrms (esi): m/z 985.3979 [m
+
+na]1h nmr (600mhz, cdcl3) δ:0.04 (s, 3h), 0.09 (s, 3h), 0.81 (s, 9h), 1.47 (s, 9h), 2.91 (dd, 1h, j=4.8, 16.2hz), 3.24 (dd, 1h, j=6.0, 16.8hz), 3.37-3.45 (m, 2h), 3.867 (s, 3h), 3.874 (s, 3h), 4.00 (s, 3h), 4.04-4.15 (m, 3h), 4.33-4.39 (m, 1h), 4.79 (s, 2h), 5.06 (s, 2h), 5.82 (br s, 1h), 6.28 (br s, 1h), 6.71 (s, 1h), 6.76 (br s, 1h), 7.20-7.29 (m, 11h), 9.08 (br s, 1h)。
[0087]
(s)-4-(苄氧基)-6-(6-(2-((叔丁氧基羰基)氨基)乙氧基)-5,7-二甲氧基-1h-吲哚-2-羰基)-8-((甲基磺酰基)氧基)-6,7,8,9-四氢-3h-吡咯并[3,2-f]喹啉-2,3-二甲酸3-苄基-2-甲酯[化学式33]在室温下在化合物11 (88.7mg,92.1
µ
mol)的四氢呋喃(1.0ml)溶液中加入四正丁基氟化铵(1.0m四氢呋喃溶液,100
µ
l,100
µ
mol)。在氩气氛下、在室温下搅拌30分钟后,减压馏去四氢呋喃。在0℃下在所得到的粗产物的二氯甲烷(1.0ml)溶液中加入吡啶(150
µ
l,1.86mmol)和甲磺酰氯(75
µ
l,0.97mmol),在氩气氛下、在室温下搅拌2.5小时。加入乙酸乙酯,用1当量的盐酸、饱和碳酸氢钠水溶液、饱和食盐水洗涤有机层。用硫酸钠干燥后,馏去
(s, 1h), 7.07 (br s, 1h), 7.20-7.36 (m, 17h), 9.26 (br s, 1h)。
[0092]
(7br,8as)-2-(6-(2-((s)-2-氨基-3-甲基丁酰氨基)乙氧基)-5,7-二甲氧基-1h-吲哚-2-羰基)-4-氧代-1,2,4,5,8,8a-六氢环丙烷并[c]吡咯并[3,2-e]吲哚-6-甲酸甲酯[化学式35]在氢气氛下(1大气压)、在室温下将化合物15 (10.0mg,9.43
µ
mol)与10%钯碳(25.0mg,23.5
µ
mol)的乙酸乙酯(500
µ
l)和叔丁醇(500
µ
l)的混合溶液搅拌3.5小时。通过硅藻土过滤除去钯碳,用二氯甲烷/甲醇(10:1)混合液洗涤后,减压馏去溶剂,得到化合物16的粗产物(5.2mg,无色膜状)。
[0093]
将化合物16的粗产物(5.2mg)和钯碳(30.0mg,92.1
µ
mol)的甲苯溶液减压馏去后,加入乙腈(1.0ml),在氩气氛下、在室温下搅拌30分钟。在所生成的黄色悬浮液中加入乙酸乙酯,通过过滤除去固体,用二氯甲烷洗涤。减压馏去溶剂,用制备薄层色谱法(二氯甲烷/甲醇=10:1)纯化所得到的粗产物,得到化合物17 (3.1mg,两阶段收率54%,黄色膜状)。
[0094]
hrms (esi): m/z 606.2529 [m
+
+h]1h nmr (600mhz, cdcl3) δ:0.84 (d, 3h, j=6.6hz), 1.00 (d, 3h, j=6.6hz), 1.57 (t, 1h, j=4.8hz), 1.76 (dd, 1h, j=4.8, 6.6hz), 2.22-2.31 (m, 1h), 2.76-2.82 (m, 1h), 3.26 (d, 1h, j=3.6hz), 3.56-3.62 (m, 2h), 3.90 (s, 3h), 3.91 (s, 3h), 4.06 (s, 3h), 4.14-4.22 (m, 2h), 4.39 (d, 1h, j=10.2hz), 4.47 (dd, 1h, j=4.8, 9.6hz), 6.61 (s, 1h), 6.81 (s, 1h), 6.96 (s, 1h), 7.03 (s, 1h), 7.96 (br s, 1h), 9.36 (br s, 1h)。
[0095]
(7br,8as)-2-(6-(((5s,8s)-19-叠氮基-5-异丙基-8-甲基-4,7,10-三氧代-11,14,17-三氧杂-3,6,9-三氮杂十九烷基)氧基)-5,7-二甲氧基-1h-吲哚-2-羰基)-4-氧代-1,2,4,5,8,8a-六氢环丙烷并[c]吡咯并[3,2-e]吲哚-6-甲酸甲酯[化学式36]
将化合物17 (4.4mg,7.3
µ
mol)和化合物9 (3.4mg,8.8
µ
mol)的二氯甲烷溶液减压馏去后,加入吡啶(0.50ml),在氩气氛下、在0℃下搅拌1小时。加入二氯甲烷和甲苯,减压馏去溶剂,用制备薄层色谱法(二氯甲烷/甲醇=10:1)纯化所得到的粗产物,得到化合物18 (4.6mg,72%,黄色膜状)。
[0096]
hrms (esi): m/z 878.3647 [m
+
+h]1h nmr (600mhz, cdcl3) δ:0.88 (d, 3h, j=7.2hz), 0.93 (d, 3h, j=6.6hz), 1.37 (d, 3h, j=6.6hz), 1.57 (t, 1h, j=4.8hz), 1.75 (dd, 1h, j=4.8, 7.2hz), 2.08-2.18 (m, 1h), 2.76-2.81 (m, 1h), 3.38 (t, 2h, j=5.1hz), 3.50-3.62 (m, 2h), 3.64-3.71 (m, 8h), 3.908 (s, 3h), 3.914 (s, 3h), 4.04 (s, 3h), 4.19 (t, 2h, j=4.8hz), 4.18-4.31 (m, 3h, overlapped), 4.32-4.37 (m, 1h), 4.38 (d, 1h, j=10.2hz), 4.47 (dd, 1h, j=5.4, 10.8hz), 5.42 (br s, 1h), 6.60 (s, 1h), 6.71 (d, 1h, j=8.4hz), 6.83 (s, 1h), 6.96 (d, 1h, j=1.8hz), 7.03 (s, 1h), 7.15 (br s, 1h), 9.61 (br s, 1h), 10.03 (br s, 1h)。
[0097]
2-((4-(5-((3as,4s,6ar)-2-亚氨基六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰氨基)丁基)氨基)-n-(2-((4-(5-((3as,4s,6ar)-2-亚氨基六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰氨基)丁基)氨基)-2-氧代乙基)-2-氧代-n-(2-(2-(2-(戊-4-炔酰氨基)乙氧基)乙氧基)乙基)乙烷-1-铵2,2,2-三氟乙酸盐[化学式37]在双亚氨基生物素化合物1 (wo/2020/032165) (5.3mg,4.04μmol)和戊-4-炔酸
2,5-二氧代吡咯烷-1-基酯2 (funder, e. d.; jensen, a. b.; t
ø
rring, t.; kodal, a. l. b.; azcargorta, a. r.; gothelf, k. v. j. org. chem. 2012, 77, 3134-3142) (0.95mg,4.85μmol)的dmf (200μl)溶液中加入三乙胺(8.4μl,60.6μmol)。在氩气氛下、在室温下搅拌18小时,减压除去溶剂。用反相hplc (梯度:0% 5分钟、0-100% 90分钟 ch3cn的0.1% cf3cooh水溶液,ymc-triart c18,流速=3.5ml/分钟)纯化所得到的粗产物,得到化合物3 (2.8mg,收率54 %)。
[0098]
lrms (esi): m/z 312.65 [m+3h]
3+1
h nmr (500mhz, cd3od) δ:1.40-1.82 (m, 20h), 2.20 (t, j=7.4 hz, 4h), 2.28 (t, j=2.9hz, 1h), 2.38-2.50 (m, 4h), 2.82 (d, j=13.4hz, 2h), 3.00 (dd, j=4.6hz, 13.2hz, 2h), 3.12-3.30 (m, 12h), 3.38 (t, j=5.2hz, 2h), 3.55 (t, j=5.7hz, 2h), 3,62 (s, 4h), 3.66-3.90 (m, 6h), 4.53 (dd, j=4.6hz, 8.0hz, 2h), 4.73 (dd, j=4.6hz, 8.0hz)。
[0099]
n-(2-(2-(2-(3-(1-((5s,8s)-1-((5,7-二甲氧基-2-((7br,8as)-6-(甲氧基羰基)-4-氧代-1,2,4,5,8,8a-六氢环丙烷并[c]吡咯并[3,2-e]吲哚-2-羰基)-1h-吲哚-6-基)氧基)-5-异丙基-8-甲基-4,7,10-三氧代-11,14,17-三氧杂-3,6,9-三氮杂十九烷-19-基)-1h-1,2,3-三唑-4-基)丙酰氨基)乙氧基)乙氧基)乙基)-2-((4-(5-((3as,4s,6ar)-2-亚氨基六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰氨基)丁基)氨基)-n-(2-((4-(5-((3as,4s,6ar)-2-亚氨基六氢-1h-噻吩并[3,4-d]咪唑-4-基)戊酰氨基)丁基)氨基)-2-氧代乙基)-2-氧代乙烷-1-铵甲酸盐[化学式38]在室温下在化合物3 (2.8mg,2.19μmol)和化合物4 (1.9mg,2.19μmol)的水(150μl)、乙腈(100μl)和
t
buoh (150μl)的混合溶液中加入硫酸铜(ii)五水合物(1.1mg,4.38μmol)、三[(1-苄基-1h-1,2,3-三唑-4-基)甲基]胺(tbta,4.6mg,8.76μmol)和抗坏血酸钠
(2.6mg,13.1μmol)。在氩气氛下、在室温下搅拌3小时。用反相hplc (梯度:0% 5分钟、0-100% 90分钟 ch3cn的0.1% hcooh水溶液,保留时间:40.4分钟,ymc-triart c18,流速=3.5ml/分钟)纯化所得到的反应溶液,得到化合物5 (0.4mg,收率10%)。lrms (esi): m/z 605.15 [m+3h]
3+
。
[0100]
(2-((2-(氯羰基)-1h-吲哚-5-基)氧基)乙基)氨基甲酸叔丁酯[化学式39]在化合物19 (20mg,0.0624mmol)的二氯甲烷(0.6ml)溶液中加入草酰氯(8.2
µ
l,0.0936mmol)和n,n-二甲基甲酰胺(0.2
µ
l),在氩气氛下、在室温下搅拌30分钟。馏去溶剂,得到化合物20的粗产物。
[0101]
(s)-4-(苄氧基)-6-(5-(2-((s)-2-(((苄氧基)羰基)氨基)-3-甲基丁酰氨基)乙氧基)-1h-吲哚-2-羰基)-8-((甲基磺酰基)氧基)-6,7,8,9-四氢-3h-吡咯并[3,2-f]喹啉-2,3-二甲酸3-苄基-2-甲酯[化学式40]在0℃下在化合物10 (31.2mg,0.0520mmol)的二氯甲烷(0.6ml)溶液中加入吡啶(10
µ
l,0.124mmol)和化合物20的粗产物,在氩气氛下、在0℃下搅拌10分钟。加入1当量的盐酸,用二氯甲烷提取,用饱和碳酸氢钠水溶液、水、饱和食盐水洗涤有机层。用硫酸钠干燥后,馏去溶剂,用硅胶柱色谱法(己烷/乙酸乙酯=3:1)纯化所得到的粗产物,得到含有结构确定的杂质的化合物21 (36.2mg)。
[0102]
在室温下在化合物21 (36.2mg)的四氢呋喃(1.0ml)溶液中加入四正丁基氟化铵(1.0m四氢呋喃溶液,44
µ
l,44
µ
mol)。在氩气氛下、在室温下搅拌30分钟后,减压馏去四氢呋
(ddd, 1h, j=5.2, 5.2, 14.0hz), 3.88 (s, 3h), 4.08 (m, 2h), 4.48 (d, 1h, j=10.8hz), 4.53 (dd, 1h, j=5.2, 10.8hz), 6.73 (s, 1h), 6.81 (s, 1h), 6.97 (dd, 1h, j=2.0, 8.8hz),7.07 (s, 1h), 7.12 (d, 1h, j=2.0hz), 7.35 (d, 1h, j=8.8hz)。
[0109]
(7br,8as)-2-(5-(((6s,9s)-1-叠氮基-9-异丙基-6-甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十三烷-13-基)氧基)-1h-吲哚-2-羰基)-4-氧代-1,2,4,5,8,8a-六氢环丙烷并[c]吡咯并[3,2-e]吲哚-6-甲酸甲酯[化学式42]将化合物26 (3.0mg,5.5
µ
mol)和化合物9 (2.6mg,6.72
µ
mol)的二氯甲烷溶液减压馏去后,加入吡啶(0.50ml),在氩气氛下、在0℃下搅拌30分钟。加入二氯甲烷和甲苯,减压馏去溶剂,用制备薄层色谱法(二氯甲烷/甲醇=9:1)纯化所得到的粗产物,得到化合物27 (4.0mg,89%,无色粉状)。
[0110]
hrms (esi): m/z 818.3444 [m
+
+h]1h nmr (400mhz, cd3cl3) δ:0.92 (d, 3h, j=6.8hz), 0.94 (d, 3h, j=6.8hz), 1.33 (d, 3h, j=7.2hz), 1.54 (t, 1h, j=4.4hz), 1.72-1.75 (m, 1h), 2.16-2.21 (m, 1h), 2.77-2.81 (m, 1h), 3.38 (t, 2h, j=5.8hz), 3.65-3.68 (m, 10h), 3.91 (s, 3h), 4.03-4.05 (m, 2h), 4.19-4.26 (m, 3h), 4.3 (dd, 1h, j=6.4, 8.8hz), 4.39-4.49 (m, 2h), 5.41 (d, 1h, j=6.8hz), 6.59 (s, 1h), 6.68 (br, 1h), 6.76 (dd, 1h, j=8.4hz), 6.93-6.99 (m, 3h), 7.08 (s, 1h), 7.32 (d, 1h, j=9.2hz), 79.57 (s, 1h), 10.0 (br s, 1h)。
[0111]
实施例2:cea-v2122蛋白的表达与纯化v2122是国际公开wo2015/125820的实施例3 (国际公开wo2015/125820的seq id no: 4)中记载的链霉亲和素突变体。v2122的氨基酸序列(在c末端具有6
×
his标签的序列)记载于序列表的seq id no: 1中。
[0112]
scfv-v2122是将针对ceacam5的单链抗体(scfv)与上述的v2122结合而成的。该scfv型的抗ceacam5抗体是专利文献us7626011b2中记载的scfv序列。将scfv型的抗ceacam5抗体的氨基酸序列记载于序列表的seq id no: 2中。另外,将用氨基酸接头(ggggsgggg) (seq id no: 7)将scfv型的抗ceacam5抗体和v2122结合而成的cea-v2122的氨基酸序列记载于序列表的seq id no: 3中。
[0113]
为了表达cea-v2122融合蛋白,使在n末端整合有用于在大肠杆菌中分泌表达的pelb信号、而且在c末端整合有6
×
his-tag序列的cea-v2122基因序列的dna密码子在大肠杆菌中优化,以进行人工基因合成。将该氨基酸序列记载于序列表的seq id no: 4中,将dna序列记载于序列表的seq id no: 5中。另外,将结构域结构的概略示出于图1中。
[0114]
具体的蛋白表达载体使用在petduet1载体的mcs2中整合了伴侣蛋白skp基因的载体。skp基因以序列表的seq id no: 6中记载的氨基酸序列为基础,进行使密码子在大肠杆菌中优化的dna的人工基因合成。所合成的skp基因使用引物(aaggagatatacatatggataaaattgccattgttaatat (seq id no: 8)、ttgagatctgccatatgttatttcacttgtttcagaacg (seq id no: 9)),通过pcr进行扩增,使用in-fusion hd cloning kit克隆到用限制酶ndei直链化的petdue1载体的mcs2中,称为petduet_skp。接着,在petduet_skp 的mcs1中整合cea-v2122基因。具体而言,使用引物(agaaggagatataccatgaaatatctgctgccgac (seq id no: 10)、cgccgagctcgaattttaatgatggtgatgatgatg (seq id no: 11))通过pcr将人工合成的cea-v2122基因扩增。另外,使用引物(ggtatatctccttcttaaagttaaac (seq id no: 12)、aattcgagctcggcgcgcctgcag (seq id no: 13))通过pcr将petduet_skp直链化。使用in-fusion hd cloning kit对通过pcr扩增的 cea-v2122和直链化的petduet_skp进行克隆。所克隆的载体通过测序进行所整合的基因序列的确认,称为petduet_cea-v2122_skp。
[0115]
为了表达蛋白,将petduet_cea-v2122_skp转化到bl21(de3) (nippon gene公司),用2
×
yt培养基(sigma-adlrich公司)在37℃下预培养过夜。将进行了预培养的培养基以100倍稀释的方式添加到新的培养基中,在37℃下进行培养直至od(600nm)=0.5~2.0。接着,添加最终浓度为0.5mm的iptg,在37℃下培养4小时,回收培养上清液后,在4℃下保存。
[0116]
cea-v2122蛋白利用附加在c末端的6
×
his-tag,通过分批法进行粗纯化。具体而言,向在4℃下保存的培养上清液中添加用缓冲液a (50mm trishcl、0.2m nacl、1mm edta、5mm咪唑,ph8.0)平衡的complete his-tag purification resin,在4℃下搅拌2小时至过夜,以进行与树脂的蛋白结合处理。接着,将树脂回收到柱中,用缓冲液a进行20个柱容量的洗涤操作。然后,用缓冲液b (50mm trishcl、0.2m nacl、1mm edta、400mm咪唑,ph8.0)洗脱,进行cea-v2122的粗纯化物的回收。
[0117]
接着,利用蛋白l柱对粗纯化物进行纯化。具体而言,将1ml的capto l (ge healthcare life sciences)填充到pd-10柱中,用10个柱容积的pbs进行平衡后,应用上述的粗纯化物,用10个柱容积的pbs洗涤后,用10mm甘氨酸盐酸ph2.0洗脱,利用vivaspin turbo 15 (mwco 100,000)进行离心浓缩。进而使用pd-10 (ge healthcare life sciences公司)将缓冲液置换为pbs,进而利用vivaspin turbo 4 (mwco 100,000)进行离心浓缩,作为最终纯化物。sds-page电泳后,通过cbb染色进行四聚体cea-v2122的纯度检测,将结果示出于图2中。sds-page凝胶使用mini-protean tgx 4-15% (bio-rad公司),cbb染色液使用bullet cbb stain one (ready to use) (nacalai tesque公司)。
[0118]
由图2确认到,所纯化的cea-v2122是以约150kda的四聚体为主的成分。
[0119]
实施例3:利用spr的cea-v2122性能评价cea-v2122与抗原ceacam5的亲和性使用表面等离子体共振(spr)测定装置:biacore t200 (ge healthcare life sciences公司)来实施。具体而言,使用胺偶联试剂盒(ge healthcare life sciences公司)将重组人ceacam-5/cd66e蛋白cf (r&d systems
公司)在sensor chip cm5 (ge healthcare life sciences公司)上进行固定操作,配体的最终固定量为279ru。另外,所纯化的cea-v2122调整1e-08m~6.25e-10m的2倍稀释系列作为分析物。相互作用分析通过单循环动力学分析进行数据的获取。用biacore t200 evaluation software、version 2.0对所得到的数据实施二价体分析模式下的曲线拟合,得到ka1=3.208e+5、kd1=3.461e-7的值。另外,由于在二价体分析中可用kd=kd1/ka1进行评价,所以得到kd=kd1/ka1=3.461e-7/3.208e+5=1.078e-12的评价值。将这些结果示出于图3中。
[0120]
由图3所示的传感图、kd值确认到,cea-v2122与ceacam5强烈地结合。
[0121]
另外,cea-v2122与生物素修饰体的相互作用分析也使用biacore t200来实施。具体的生物素修饰体为国际公开wo2018/07239的实施例1中记载的标题化合物14。另外,具体的分析方法如下所述。使用胺偶联试剂盒,以目标值达到5000ru的方式对sensor chip cm5进行设定,进行所纯化的cea-v2122的固定。使用分析物的浓度为1e-08m~6.25e-10m的5种2倍稀释系列。相互作用分析通过单循环动力学分析进行数据的获取。用biacore t200 evaluation software、version 2.0对所得到的数据实施二价体分析模式下的曲线拟合,得到ka1=3.792e+4、kd1=4.424e-6的值。另外,由于在二价体分析中可用kd=kd1/ka1进行评价,所以得到kd=kd1/ka1=3.792e+4/4.424e-6=1.167e-10的评价值。将这些结果示出于图4中。
[0122]
由图4所示的传感图、kd值确认到,cea-v2122与生物素修饰体强烈地结合。
[0123]
实施例4:使用fitc标记cea-v2122的ceacam5表达细胞株的细胞染色为了对ceacam5表达阳性的癌细胞株进行染色,使用100μg的经纯化的cea-v2122蛋白进行fitc标记。具体而言,使用fluorescein labeling kit-nh
2 (同仁化学研究所),按照操作流程的用法用量实施标记,将所得到的产物称为cea-v2122-fitc。具体的ceacam5表达阳性的癌细胞株的染色如下所述。在cellstar、
µ
clear、96孔板(greiner公司)中以2.0
×
104细胞/孔的方式接种ceacam5阳性的来源于人胃癌的mkn-45细胞和ceacam5阴性的来源于人结肠癌的dld1细胞,培养过夜。接着,以100
µ
l/孔的方式添加含有20nm cea-v2122-fitc和1
µ
m hoechist的培养液,在4 ℃下反应30分钟后,利用in cell analyzer 6000 (ge healthcare life sciences公司)进行图像的获取。将其结果示出于图5和图6中。
[0124]
由图5所示的结果确认到,cea-v2122-fitc特异性地识别细胞膜表面的ceacam5。另外,由图6所示的结果确认到,ceacam5在结合cea-v2122-fitc后滞留在细胞膜表面。
[0125]
实施例5:使用cea-v2122和抗癌剂标记生物素修饰体的体外细胞毒性试验使用抗癌剂标记生物素修饰体来实施细胞毒性试验。抗癌剂标记生物素修饰体是化合物5中记载的化合物。将化合物5示出于图7中。在测定中,首先将ceacam5阳性mkn45细胞和ceacam5阴性dld1细胞以细胞数为 5
×
103细胞/孔、培养液为 50
µ
l/孔的方式接种到细胞培养用96孔板中,培养过夜。cea-v2122和光活化化合物标记生物素修饰体的复合体溶液以cea-v2122与化合物5的摩尔比为1:2的方式混合,在室温下培养10分钟,然后,用培养液进行浓度调制,使化合物5的最终浓度达到1200nm。稀释系列是由包含浓度为600nm的cea-v2122和浓度为1200nm的化合物5的混合溶液,将3倍稀释系列调制11个系列(2.0e-11、6.1e-11、1.8e-10、5.5e-10、1.6e-09、4.9e-09、1.5e-08、4.4e-07、1.3e-07、4.0e-07、1.2e-06),作为复合体稀释系列溶液。另外,只将不含有复合体的培养基作为空白对照。
[0126]
在培养过夜的细胞中,将复合体稀释系列溶液以达到最终摩尔浓度(1.0e-11、3.0e-11、9.1e-11、2.7e-10、8.2e-10、2.5e-09、7.4e-09、2.2e-08、6.7e-08、2.0e-07、6.0e-07)的方式,分别以50
µ
l/孔添加到各孔中。添加复合体稀释系列溶液后,培养48小时,使用cell counting kit-8 (同仁化学社)进行活细胞数的比较。各条件设为n=5。用法用量按照操作说明书,添加试剂1个半小时后,在37℃下、在co2培养箱中培养后,测定450nm吸光度,计算平均值,进行背景校正后,以对照为100%,计算相对于各条件的对照的细胞增殖的比例。将该实验重复3次,将以图形表示平均值和标准偏差的结果示出于图8中。
[0127]
如图8所示,对于ceacam5阳性细胞mkn45,确认到依赖于复合体浓度地抑制细胞增殖。另一方面,对于ceacam5阴性dld1细胞,未确认到浓度依赖性的细胞增殖抑制效果。
[0128]
实施例6:倍癌霉素sa和倍癌霉素sa-缬氨酸的细胞毒性为了确认图9、图10所示的化合物x (倍癌霉素sa)和化合物y (倍癌霉素sa-缬氨酸)的活性,使用hela s3细胞进行细胞毒性的确认。
[0129]
将细胞以细胞数为5
×
103细胞/孔、培养液为 50μl/孔的方式接种到细胞培养用96孔板中,培养过夜。以化合物x或化合物y的最终浓度达到600nm的方式用培养液进行浓度调制。稀释系列是由化合物x 或化合物y 的600nm溶液,将3倍稀释系列调制11个系列(1.0e-11、3.0e-11、9.1e-11、2.7e-10、8.2e-10、2.5e-09、7.4e-09、2.2e-08、6.7e-08、2.0e-07、6.0e-07),作为药剂稀释溶液。另外,只将不含有化合物的培养基作为空白对照。
[0130]
将培养过夜的细胞的培养基与所调制的药剂稀释溶液进行交换,培养48小时,使用cell counting kit-8 (同仁化学社)进行活细胞数的比较。各条件设为n=3。测定的用法用量按照操作说明书,添加试剂1个半小时后,在37℃下、在co2培养箱中培养后,测定450nm吸光度,计算平均值,进行背景校正后,以对照为100%,计算相对于对照的各条件的细胞增殖的比例。将该实验重复3次,将以图形表示所得的平均值和标准偏差的结果示出于图11中。
[0131]
由图11确认到,倍癌霉素sa-缬氨酸与倍癌霉素sa相比,细胞增殖抑制效果更高。
[0132]
seq id no: 1aeagitgtwsdqlgdtfivtagadgaltgtyenavggaesryvltgrydsapatdgsgtalgwtvawknnsknahsattwsgqyvggadakintqwlltsgttnanawkstlvghdtftkvkpsaashhhhhh。
[0133]
seq id no: 2 (sm3e-scfv序列)qvkleqsgaevvkpgasvklsckasgfnikdsymhwlrqgpgqrlewigwidpengdteyapkfqgkatfttdtsantaylglsslrpedtavyycnegtptgpyyfdywgqgtlvtvssggggsggggsggggsenvltqspssmsvsvgdrvniacsasssvpymhwlqqkpgkspklliyltsnlasgvpsrfsgsgsgtdysltissvqpedaatyycqqrssypltfgggtkleik。
[0134]
seq id no: 3qvkleqsgaevvkpgasvklsckasgfnikdsymhwlrqgpgqrlewigwidpengdteyapkfqgkatfttdtsantaylglsslrpedtavyycnegtptgpyyfdywgqgtlvtvssggggsggggsggggsenvltqspssmsvsvgdrvniacsasssvpymhwlqqkpgkspklliyltsnlasgvpsrfsgsgsgtdysltissvqpedaatyycqqrssypltfgggtkleikggggsggggaeagitgtwsdqlgdtfivtagadgaltgtyenavggaesryvltgrydsapatdgsgtalgwtvawknnsknahsattwsgqyvggadakintqwlltsgttnanawkstlvghdtftkvkpsaashhhhhh。
[0135]
seq id no: 4mkyllptaaagllllaaqpamaqvkleqsgaevvkpgasvklsckasgfnikdsymhwlrqgpgqrlewigwidpengdteyapkfqgkatfttdtsantaylglsslrpedtavyycnegtptgpyyfdywgqgtlvtvssggggsggggsggggsenvltqspssmsvsvgdrvniacsasssvpymhwlqqkpgkspklliyltsnlasgvpsrfsgsgsgtdysltissvqpedaatyycqqrssypltfgggtkleikggggsggggaeagitgtwsdqlgdtfivtagadgaltgtyenavggaesryvltgrydsapatdgsgtalgwtvawknnsknahsattwsgqyvggadakintqwlltsgttnanawkstlvghdtftkvkpsaashhhhhh。
[0136]
seq id no: 5atgaaatatctgctgccgaccgcagcagcgggtctgctgctgctggcagcacagcctgcaatggcacaggttaaactggaacagagcggtgccgaagttgttaaaccgggtgcaagcgttaaactgagctgtaaagcaagcggctttaacatcaaagatagctatatgcattggctgcgtcagggtccgggtcagcgtctggaatggattggttggattgatccggaaaatggtgataccgaatatgcaccgaaatttcagggtaaagcaacctttaccaccgataccagcgcaaataccgcatatctgggtctgagcagcctgcgtccggaagataccgcagtgtattattgtaatgaaggcaccccgaccggtccgtattatttcgattattggggtcagggcaccctggttaccgttagcagcggtggtggtggtagtggtggcggtggttcaggcggtggcggtagcgaaaatgttctgacccagagcccgagcagcatgagcgttagcgttggtgatcgtgttaatattgcatgtagcgcaagcagcagcgttccgtacatgcactggctgcagcagaaaccgggtaaaagcccgaaactgctgatttatctgaccagcaatctggcaagcggtgttccgagccgttttagcggtagcggtagtggcaccgattatagcctgaccattagcagcgtgcagcctgaagatgcagcaacctattattgtcagcagcgtagcagttatccgctgacctttggtggtggcaccaaactggaaattaaagggggtggtggctcaggtggcggaggtgcagaagcaggtattaccggtacatggtcagatcagctgggtgatacctttattgttaccgcaggcgcagatggtgcactgaccggcacctatgaaaatgcagttggtggtgcagaaagccgttatgtgctgaccggtcgttatgatagcgcaccggcaaccgatggtagcggcaccgcactgggttggaccgttgcatggaaaaataacagcaaaaatgcacatagcgcaaccacctggtcaggtcagtatgtgggtggtgccgatgccaaaattaacacccagtggctgctgaccagcggtacaaccaatgcaaatgcctggaaaagtaccctggttggtcatgatacattcaccaaagttaaaccgagcgcagcaagccatcatcatcaccatcattaa。
[0137]
seq id no: 6mdkiaivnmgslfqqvaqktgvsntlenefkgraselqrmetdlqakmkklqsmkagsdrtklekdvmaqrqtfaqkaqafeqdrarrsneergklvtriqtavksvansqdidlvvdanavaynssdvkditadvlkqvk。
[0138]
seq id no: 7ggggsgggg。
[0139]
seq id no: 8aaggagatatacatatggataaaattgccattgttaatat。
[0140]
seq id no: 9ttgagatctgccatatgttatttcacttgtttcagaacg。
[0141]
seq id no: 10agaaggagatataccatgaaatatctgctgccgac。
[0142]
seq id no: 11cgccgagctcgaattttaatgatggtgatgatgatg。
[0143]
seq id no: 12
ggtatatctccttcttaaagttaaac。
[0144]
seq id no: 13aattcgagctcggcgcgcctgcag。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1