HDAC抑制剂固态形式的制作方法
背景技术:
1、本公开涉及组蛋白脱乙酰酶抑制剂化合物的药学上可接受的盐形式和所述盐形式的药物组合物,以及所述化合物在药物组合物和药物中的用途。
技术实现思路
1、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1。
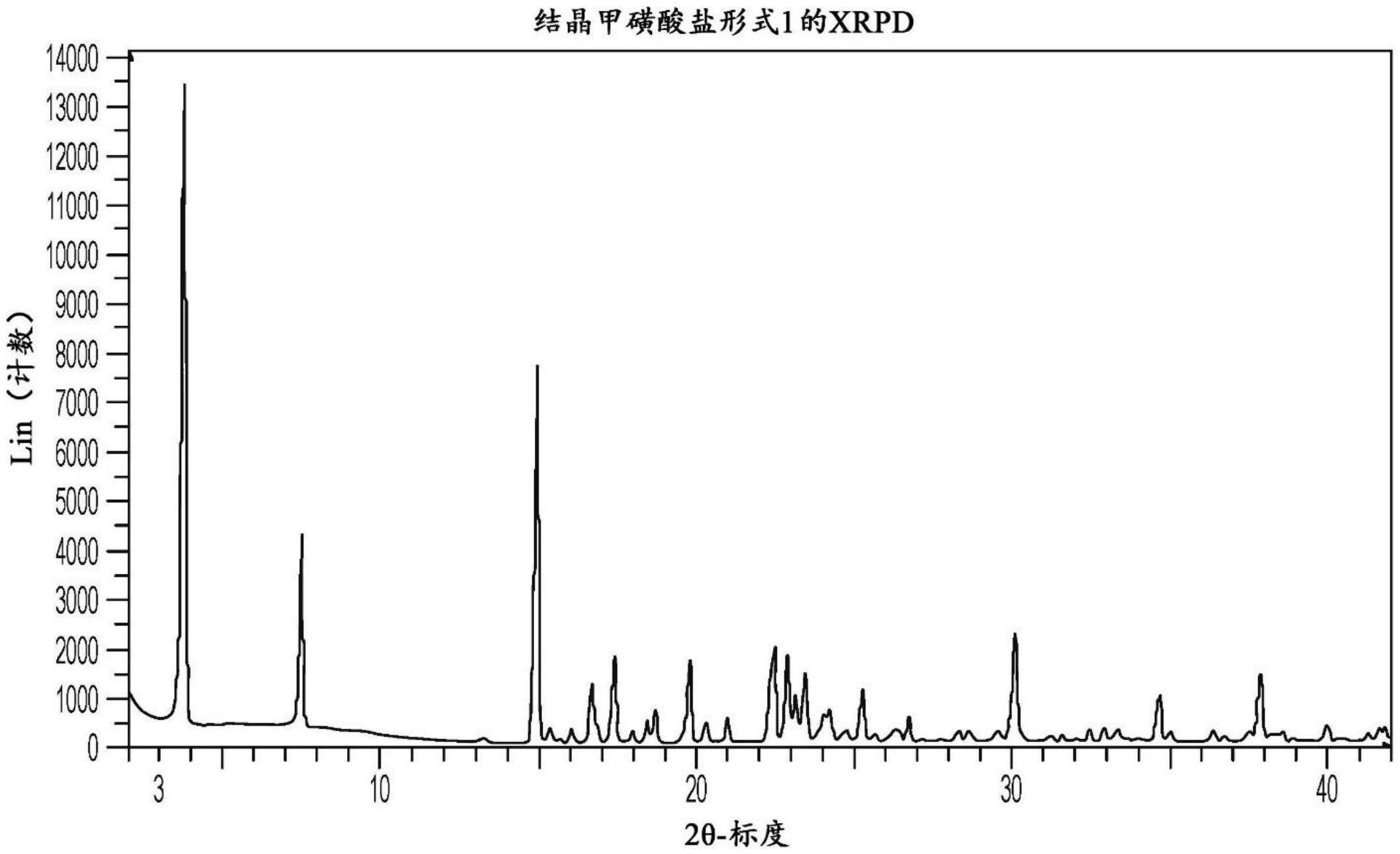
2、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其特征在于在3.7°±0.3的2θ值处的x射线衍射图案反射。一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其特征在于在3.7°±0.3和14.9°±0.3的2θ值处的x射线衍射图案反射。一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其特征在于在3.7°±0.3、7.5°±0.3和14.9°±0.3的2θ值处的x射线衍射图案反射。
3、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中所述结晶甲磺酸盐形式1的特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少一个x射线衍射图案反射。一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中所述结晶甲磺酸盐形式1的特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少两个x射线衍射图案反射。一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中所述结晶甲磺酸盐形式1的特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少三个x射线案反射。一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中所述结晶甲磺酸盐形式1的特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少四个x射线衍射图案反射。一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中所述结晶甲磺酸盐形式1的特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少五个x射线衍射图案反射。
4、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其展现如图1中所示的x射线粉末衍射图案。
5、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其展现如图3中所示的tga图案。
6、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中dsc的特征在于起始温度在约222.1℃±5.0(433j/g)或放热峰在225.8℃±5.0的单一放热事件。
7、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其展现如图3中所示的dsc图案。
8、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的无定形甲磺酸盐。
9、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的固态形式,其中其它结晶或无定形形式的量为5%(w/w)或更少。
10、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的固态形式,其中所述固态形式基本上不含杂质。
11、一个实施方案提供n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的固态形式,其中杂质的量为3%或更少。
12、一个实施方案提供药物组合物,所述药物组合物包含本文所述的组合物中的任一种和一种或多种药学上可接受的赋形剂或载体(carrier)。一个实施方案提供了进一步包含一种或多种附加的活性药物成分(api)的药物组合物。一个实施方案提供了药物组合物,其中所述附加的api是缬更昔洛韦(valganciclovir)。
13、通过引用并入
14、本说明书中提到的所有出版物和专利申请都通过引用并入本文中,其程度如同每个单独的出版物或专利申请被明确和单独地指示通过引用并入本文中。
技术特征:
1.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1。
2.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其特征在于在3.7°±0.3的2θ值处的x射线衍射图反射。
3.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其特征在于在3.7°±0.3和14.9°±0.3的2θ值处的x射线衍射图反射。
4.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其特征在于在3.7°±0.3、7.5°±0.3和14.9°±0.3的2θ值处的x射线衍射图反射。
5.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中所述结晶甲磺酸盐形式1的特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少一个x射线衍射图反射。
6.根据权利要求5所述的结晶形式,进一步特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少两个x射线衍射图反射。
7.根据权利要求5所述的结晶形式,进一步特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少三个x射线衍射图反射。
8.根据权利要求5所述的结晶形式,进一步特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少四个x射线衍射图反射。
9.根据权利要求5所述的结晶形式,进一步特征在于选自3.7°±0.3、7.5°±0.3、14.9°±0.3、17.3°±0.3、19.7°±0.3、22.5°±0.3、22.9°±0.3或30.1°±0.3的2θ值中的至少五个x射线衍射图反射。
10.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其展现如图1中所示的x射线粉末衍射图。
11.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其展现如图3所示的tga图。
12.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其中dsc的特征在于起始温度在约222.1℃±5.0(433j/g)或放热峰在225.8℃±5.0的单一放热事件。
13.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的结晶甲磺酸盐形式1,其展现如图3所示的dsc图。
14.n-羟基2-{6-[(6-氟-喹啉-2-基甲基)-氨基]-3-氮杂-双环[3.1.0]己-3-基}嘧啶-5-甲酰胺的无定形甲磺酸盐。
15.根据权利要求1至14中任一项所述的固态形式,其中其它结晶或无定形形式的量是5%(w/w)或更少。
16.根据权利要求1至15中任一项所述的固态形式,其中所述固态形式基本上不含杂质。
17.根据权利要求16所述的固态形式,其中所述杂质的量为3%或更少。
18.一种药物组合物,包含根据权利要求1-17所述的组合物中的任一种和一种或多种药学上可接受的赋形剂或载体。
19.根据权利要求18所述的药物组合物,进一步包含一种或多种附加的活性药物成分(api)。
20.根据权利要求19所述的药物组合物,其中所述附加的api是缬更昔洛韦。
技术总结
本公开涉及N‑羟基2‑{6‑[(6‑氟‑喹啉‑2‑基甲基)‑氨基]‑3‑氮杂‑双环[3.1.0]己‑3‑基}嘧啶‑5‑甲酰胺的结晶甲磺酸盐形式1及其制备方法。N‑羟基2‑{6‑[(6‑氟‑喹啉‑2‑基甲基)‑氨基]‑3‑氮杂‑双环[3.1.0]己‑3‑基}嘧啶‑5‑甲酰胺的结晶甲磺酸盐形式1可用于制备用于治疗癌症、免疫障碍和炎症的药物组合物和剂型。
技术研发人员:邓晓虎,麦婉萍,罗伯特·C·麦克雷,比利安娜·纳吉松巴蒂
受保护的技术使用者:维拉克塔附属公司
技术研发日:
技术公布日:2024/1/14
- 还没有人留言评论。精彩留言会获得点赞!