妥卡替尼关键中间体及其制备方法与流程
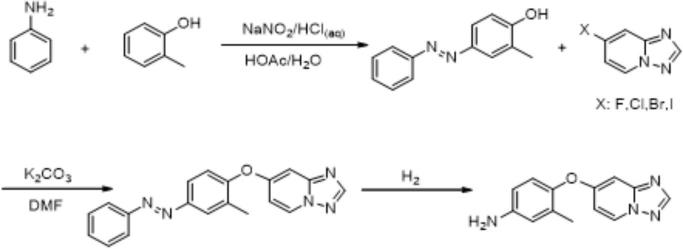
1.本发明涉及有机合成制药技术领域,尤其涉及一种妥卡替尼关键中间体4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺及其制备方法。
背景技术:
[0002]
妥卡替尼(tucatinib)是治疗her2+乳腺癌的口服抑制剂,其化学式为:
[0003][0004]
妥卡替尼(tucatinib)的关键中间体4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺的化学式如下:
[0005][0006]
现有技术采用2-甲基-4-硝基苯酚或2-甲基-4-氨基苯酚作为起始原料合成4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺。
[0007]
然而,发明人在实施本发明的过程中发现,上述技术方案存在以下缺陷:
[0008]
现有技术的起始原料价格昂贵、生产成本高;且其化学性质活泼,在生产过程中产生的反应副产物多,难以纯化。
技术实现要素:
[0009]
本发明所要解决的技术问题是,提供一种妥卡替尼关键中间体4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺及其制备方法,以降低原料成本、缩短合成步骤、提高收率、提升制备的产品性质的稳定性、降低三废的产生、适合工业化放大生产。
[0010]
为解决上述技术问题,第一方面,本发明公开了一种妥卡替尼关键中间体的制备方法,该关键中间体为4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺,包括以下步骤:
[0011]
对苯胺进行重氮化反应,制备重氮盐溶液;
[0012]
将化合物2-甲基苯酚在碱性条件下与所述重氮盐溶液进行偶联反应,制备2-甲基-4-(苯基二氮烯基)苯酚;
[0013]
将所述2-甲基-4-(苯基二氮烯基)苯酚与7-卤代-[1,2,4]三唑并[1,5-a]吡啶进行亲核取代反应,制备7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品;
[0014]
对所述7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品进行氢化还原反应,制得4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺。
[0015]
在一些可能的实施方式中,所述重氮化反应具体包括:
[0016]
在冰盐浴环境中,在1当量苯胺中加入盐酸、去离子水和冰乙酸搅拌,再加入1.0~1.05当量nano2水溶液,反应生成重氮盐溶液。
[0017]
在一些可能的实施方式中,所述偶联反应具体包括:
[0018]
将1当量化合物2-甲基苯酚加入水中,滴加入naoh水溶液使化合物2-甲基苯酚完全溶解后,滴加所述重氮盐溶液,并滴加naoh水溶液使得混合溶液的ph值为碱性,保持15~45℃温度反应完全后,盐析,过滤,洗涤,干燥后得纯品,即化合物2-甲基-4-(苯基二氮烯基)苯酚。
[0019]
在一些可能的实施方式中,所述亲核取代反应具体包括:
[0020]
在氮气保护下,将所述2-甲基-4-(苯基二氮烯基)苯酚溶于有机溶剂1,加入7-卤代-[1,2,4]三唑并[1,5-a]吡啶、无机碱和催化剂1升温到70~160℃反应完全后,水析、过滤,干燥,得到7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品。
[0021]
在一些可能的实施方式中,所述氢化还原反应具体包括:
[0022]
将所述7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品溶于醇溶剂后,加入催化剂2,常压通氢氢化,反应完全后,垫硅藻土过滤,滤液减压浓缩后,加入有机溶剂2搅拌析晶,过滤,真空干燥后,得到4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺。
[0023]
在一些可能的实施方式中,所述有机溶剂1为n,n-二甲基甲酰胺,二甲基亚砜,n-甲基吡咯烷酮中的任意一种;和/或者
[0024]
所述无机碱为碳酸钠、碳酸钾、碳酸铯、叔丁醇钾其中的任意一种;
[0025]
所述催化剂1为四丁基溴化铵、四丁基碘化铵中的任意一种。
[0026]
在一些可能的实施方式中,所述7-卤代-[1,2,4]三唑并[1,5-a]吡啶为7-氯-[1,2,4]三唑并[1,5-a]吡啶、7-氟-[1,2,4]三唑并[1,5-a]吡啶、7-溴-[1,2,4]三唑并[1,5-a]吡啶、7-碘-[1,2,4]三唑并[1,5-a]吡啶中的任意一种;
[0027]
所述醇溶剂为甲醇和/或者乙醇;和/或者
[0028]
所述的催化剂2为pd/c,rey-ni中的任意一种;
[0029]
所述有机溶剂2为石油醚、正己烷、庚烷、甲基叔丁基醚中的任意一种或其混合溶剂。
[0030]
在一些可能的实施方式中,所述冰浴盐的温度控制在-10~5℃。
[0031]
在一些可能的实施方式中,保持所述混合溶液的ph值为8~10。
[0032]
第二方面,本发明实施例公开了一种妥卡替尼关键中间体,所述妥卡替尼关键中间体为采用如上所述的方法制备得到的4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺。
[0033]
本发明的有益效果是:
[0034]
本发明实施例通过使用廉价易得且化学性质相对不活泼的2-甲基苯酚和苯胺替代现有技术中昂贵或化学性质活泼的原料2-甲基-4-硝基苯酚的2-甲基-4-氨基苯酚作为起始原料,从而达到了路线经济价值高,整个合成步骤短,收率高,制备的中间体和产品性质稳定,三废少,适合工业化放大生产的技术效果。
具体实施方式
[0035]
下面详细描述本发明实施例提供的一种妥卡替尼关键中间体的制备方法,该关键中间体为4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺,包括以下步骤:
[0036]
对苯胺进行重氮化反应,制备重氮盐溶液;
[0037]
将化合物2-甲基苯酚在碱性条件下与所述重氮盐溶液进行偶联反应,制备2-甲基-4-(苯基二氮烯基)苯酚;
[0038]
将所述2-甲基-4-(苯基二氮烯基)苯酚与7-卤代-[1,2,4]三唑并[1,5-a]吡啶进行亲核取代反应,制备7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品;
[0039]
对所述7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品进行氢化还原反应,制得4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺。
[0040]
上述各反应过程的化学方程式如下:
[0041][0042]
在一些可能的实施方式中,所述重氮化反应具体包括:
[0043]
在冰盐浴环境中,在1当量苯胺中加入盐酸、去离子水和冰乙酸搅拌,再加入1.0~1.05当量nano2水溶液,反应生成重氮盐溶液。
[0044]
在一些可能的实施方式中,所述偶联反应具体包括:
[0045]
将1当量化合物2-甲基苯酚加入水中,滴加入naoh水溶液使化合物2-甲基苯酚完全溶解后,滴加所述重氮盐溶液,并滴加naoh水溶液使得混合溶液的ph值为碱性,保持15~45℃温度反应完全后,盐析,过滤,洗涤,干燥后得纯品,即化合物2-甲基-4-(苯基二氮烯基)苯酚。
[0046]
在一些可能的实施方式中,所述亲核取代反应具体包括:
[0047]
在氮气保护下,将所述2-甲基-4-(苯基二氮烯基)苯酚溶于有机溶剂1,加入7-卤代-[1,2,4]三唑并[1,5-a]吡啶、无机碱和催化剂1升温到70~160℃反应完全后,水析、过滤,干燥,得到7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品。
[0048]
在一些可能的实施方式中,所述氢化还原反应具体包括:
[0049]
将所述7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品溶于醇溶剂后,加入催化剂2,常压通氢氢化,反应完全后,垫硅藻土过滤,滤液减压浓缩后,加入有机溶剂2搅拌析晶,过滤,真空干燥后,得到4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺。
[0050]
在一些可能的实施方式中,所述有机溶剂1为n,n-二甲基甲酰胺,二甲基亚砜,n-甲基吡咯烷酮中的任意一种;和/或者
[0051]
所述无机碱为碳酸钠、碳酸钾、碳酸铯、叔丁醇钾其中的任意一种;和/或者
[0052]
所述催化剂1为四丁基溴化铵、四丁基碘化铵中的任意一种;和/或者
[0053]
所述7-卤代-[1,2,4]三唑并[1,5-a]吡啶为7-氯-[1,2,4]三唑并[1,5-a]吡啶、7-氟-[1,2,4]三唑并[1,5-a]吡啶、7-溴-[1,2,4]三唑并[1,5-a]吡啶、7-碘-[1,2,4]三唑并[1,5-a]吡啶中的任意一种。
[0054]
在一些可能的实施方式中,所述醇溶剂为甲醇和/或者乙醇;和/或者
[0055]
所述的催化剂2为pd/c,rey-ni中的任意一种;
[0056]
所述有机溶剂2为石油醚、正己烷、庚烷、甲基叔丁基醚中的任意一种或其混合溶剂。
[0057]
在一些可能的实施方式中,所述冰浴盐的温度控制在-10~5℃。
[0058]
在一些可能的实施方式中,保持所述混合溶液的ph值为8~10。
[0059]
与现有技术相比,本发明的优点在于:
[0060]
本发明实施例提供的制备4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺方法使用廉价易得且化学性质相对不活泼的2-甲基苯酚和苯胺作为起始原料,避免使用昂贵或化学性质活泼的原料2-甲基-4-硝基苯酚或2-甲基-4-氨基苯酚,路线经济价值高,整个合成步骤短,收率高,制备的中间体和产品性质稳定,三废少,适合工业化放大生产。
[0061]
为了更进一步阐释本实施例为达成预定发明目的所采取的技术手段和效果,对本实施例制备妥卡替尼关键中间体4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺的具体步骤,通过实例数据详细说明如下。
[0062]
实施例1
[0063]
重氮化偶联反应:
[0064]
在1l三口反应瓶中,加入苯胺(23.3g)、水(225ml)搅拌配制成体系均一的悬浮液,依次滴加盐酸(65ml),乙酸(37.5ml),搅拌15min反应液变为淡棕黄色,冰盐浴降温5℃以下,滴加nano2(19g溶于75ml水),滴加完毕后搅拌1.5h,反应液变为棕绿色并最终变为棕黄色。同时滴加邻甲酚溶液和naoh溶液,逐渐有黄色固体产生,然后慢慢溶解,溶液变为棕色。邻甲酚滴加完毕,继续滴加naoh溶液,ph调至8~10,停止滴加naoh溶液,25℃搅拌反应4h,有土黄色固体析出,过滤固体、烘干称重2-甲基-4-(苯基二氮烯基)苯酚(49.3g),收率93%。
[0065]1h nmr(600mhz,dmso-d6)δ7.80(d,j=8.0hz,2h),7.69(s,1h),7.65(d,j=8.5hz,1h),7.55(t,j=7.5hz,2h),7.48(t,j=7.2hz,1h),6.97(d,j=8.5hz,1h),2.21(s,3h)。
[0066]
亲核取代反应:
[0067]
在500ml三口瓶中,氮气保护下加入2-甲基-4-(苯基二氮烯基)苯酚(22.1g),7-氯-(1,2,4)三唑并(1,5-a)吡啶(12.2g),碳酸铯(27.6g),dmf(100ml),四丁基溴化铵(1.5g)。搅拌加热至回流(130℃~140℃),保温反应48h。中控反应结束后,将反应液缓慢滴入水(300ml),5℃-10℃搅拌1h,有黄棕色固体析出,过滤得到产物,鼓风干燥后得到7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品(23.3g),收率89%,直接用于下一步反应。
[0068]
氢化还原反应:
[0069]
在500ml单口瓶,加入7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶6(20.0g),加入乙醇(150ml),搅拌溶解,加入5%pd/c(1.0g),氢气置换体系,氢气
球保护,升温至50℃反应2h,取样点板,原料反应完全,反应液垫硅藻土过滤,滤液浓缩至干,加入甲基叔丁基醚(100ml),搅拌打浆,减压抽滤,得到灰白色固体,真空干燥,得到4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺(13.3g),收率91.3%。
[0070]1h nmr(600mhz,dmso-d6)δ8.85(d,j=7.5hz,1h),8.33(s,1h),6.94(dd,j=7.5,2.6hz,1h),6.81(d,j=8.5hz,1h),6.61(d,j=2.6hz,1h),6.54(d,j=2.7hz,1h),6.49(dd,j=8.5,2.7hz,1h),5.08(s,2h),1.98(s,3h)。
[0071]
实施例2
[0072]
本实施例在其他步骤与实施例1相同的条件下将实施例1的亲核取代反应替换为:
[0073]
在50ml单口瓶中,氮气保护下加入2-甲基-4-(苯基二氮烯基)苯酚(2.0g),7-碘-(1,2,4)三唑并(1,5-a)吡啶(1.0g),碳酸钾(1.7g),dmf(15ml)。搅拌加热至回流(140℃~150℃),保温反应36h。中控反应结束后,将反应液缓慢滴入水(30ml),5℃~10℃搅拌1h,有黄棕色固体析出,过滤得到产物,鼓风干燥后得到7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品(1.1g),收率81.8%。
[0074]
实施例3
[0075]
本实施例在其他步骤与实施例1相同的条件下将实施例1的亲核取代反应替换为:
[0076]
在50ml单口瓶中,氮气保护下加入2-甲基-4-(苯基二氮烯基)苯酚(2.2g),7-氟-(1,2,4)三唑并(1,5-a)吡啶(1.0g),碳酸钠(1.5g),dmf(15ml),四丁基碘化铵(0.1g)。搅拌加热至回流(100℃~120℃),保温反应30h。中控反应结束后,将反应液缓慢滴入水(30ml),5℃~10℃搅拌1h,有黄棕色固体析出,过滤得到产物,鼓风干燥后得到7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶粗品(1.9g),收率79.1%。
[0077]
实施例4
[0078]
本实施例在其他步骤与实施例1相同的条件下将实施例1的氢化还原反应替换为:
[0079]
在100ml单口瓶中,加入7-(2-甲基-4-(苯基二氮烯基)苯氧基)-[1,2,4]三唑并[1,5-a]吡啶6(5.0g),加入甲醇(35m1),搅拌溶解,加入rey-ni(0.5g),氢气置换体系,氢气球保护,升温至30~40℃反应4h,取样点板,原料反应完全,反应液垫硅藻土过滤,滤液浓缩至干,加入正己烷(20ml),搅拌打浆,减压抽滤,得到灰白色固体,真空干燥,得到4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺(3.5g),收率95.9%。
[0080]
本发明实施例还公开了一种妥卡替尼关键中间体,该妥卡替尼关键中间体为采用前述实施例所述的制备方法得到的4-([1,2,4]三唑并[1,5-a]吡啶-7-基氧基)-3-甲基苯胺,不再赘述。
[0081]
以上内容是结合具体的优选实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以作出若干简单推演或替换,都应当视为属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1