一种提高雨生红球藻生物量和虾青素产量的方法
1.本发明属于生物工程技术领域,尤其涉及一种提高雨生红球藻生物量和虾青素产量的方法。
背景技术:
2.目前,虾青素是一种红色的类胡萝卜素,与番茄红素、玉米黄质等类胡萝卜素同属于叶黄素类。有研究表明,虾青素具有抗氧化、抗炎、抗凋亡、保护神经、保护皮肤、保护肝肾等作用,现已被批准作为一种膳食补充剂。虾青素具有三种立体异构体,天然虾青素的主要存在形式是3s,3’s和3r,3’r,前者来源于藻类,后者来源于酵母细胞。天然虾青素稳定性高,食用安全性已被广泛接受。尽管有文献表明可以从石化资源中通过化学合成的方法获取虾青素,但是过程繁琐价格昂贵。出于毒性考虑,化学合成的虾青素不适合人类食用,且fda已明确规定化学合成的虾青素不得进入保健品市场。
3.微藻是天然虾青素的巨大来源,其中雨生红球藻被认为是虾青素的细胞工厂。虽然已有大量研究工作优化了雨生红球藻虾青素的生产、提取和纯化过程,但仍然存在着虾青素生产成本高、产量低等问题。一般来说,雨生红球藻在诱导阶段的培养中通过氮消耗、改变光照强度、盐浓度、铁离子浓度或提高温度等非生物胁迫干预后开始积累虾青素。但传统的非生物胁迫会抑制藻细胞生长,而减少藻类生物量。目前,非生物胁迫耦合化学诱导剂的培养策略在雨生红球藻产虾青素方面引起了广泛关注,该策略可以在维持雨生红球藻生物量的同时有效地提高虾青素产量。选用高效可行的诱导剂是该策略的关键。
4.有机酸在植物代谢中尤为重要。低浓度的有机酸对作物的生长可产生积极的影响,具有提高根系活力、促进生长发育、增强抗性等功能。在许多植物中,苹果酸是积累最多的有机酸,并且被认为是植物呼吸作用的主要底物。此外,遗传学及分子生物学表明,苹果酸作为叶绿体中氧化还原平衡的调节物,与线粒体的nad
+
共同作用,导致活性氧的产生,影响胞内稳态。前期也表明了雨生红球藻积累虾青素的过程受多种信号调控,其中活性氧发挥了重要作用。因此苹果酸可能在雨生红球藻虾青素的积累过程中发挥作用。更重要的是,苹果酸廉价易得,使用l-苹果酸作为诱导剂具有经济效益。
5.通过上述分析,现有技术存在的问题及缺陷为:
6.(1)现有技术不易于操作而且成本高。在养藻废液上废液利用率低。
7.(2)现有技术中在提高了雨生红球藻的生物量及虾青素产量中,获得的虾青素浓度低,不能满足实际需求。
技术实现要素:
8.针对现有技术存在的问题,本发明提供了一种提高雨生红球藻生物量和虾青素产量的方法。具体涉及一种利用l-苹果酸提高雨生红球藻生物量和虾青素产量的方法。
9.本发明是这样实现的,一种提高雨生红球藻的生物量和虾青素的方法包括:将配制的l-苹果酸母液添加到诱导种子液中,进行培养,诱导雨生红球藻生物量和虾青素的积
累;利用有机溶剂提取虾青素,并测定虾青素浓度以及雨生红球藻生物量。
10.进一步,所述提高雨生红球藻的生物量和虾青素的方法具体包括:步骤一,配制bg-11培养基并灭菌,将培养至对数生长期的雨生红球藻种子液接种到培养基中进行培养;
11.步骤二,配制缺氮bg-11培养基并灭菌,用缺氮bg-11培养基将步骤一中的种子液稀释作为诱导种子液;
12.步骤三,配制l-苹果酸母液,将配制好的母液添加到步骤二已稀释好的诱导种子液中;对该种子液持续通入无菌空气,培养,诱导雨生红球藻生物量和虾青素的积累;
13.步骤四,利用有机溶剂提取虾青素,使用分光光度法测定虾青素浓度;使用干重法测定雨生红球藻生物量。
14.进一步,在步骤一中培养温度为24~26℃,光照强度为1900~2100lux,使藻细胞浓度达到1.0
×
106cells ml-1
。
15.进一步,在步骤二中种子液稀释至3.0
×
105cells ml-1
作为诱导种子液。
16.进一步,在步骤三中用超纯水配制浓度为350mmol l-1
的l-苹果酸母液,诱导种子液中l-苹果酸终浓度达到0.5~2mmol l-1
;所述种子液在温度为27~29℃,光照强度为18000~20000lux条件下培养15天,诱导雨生红球藻生物量和虾青素的积累。
17.进一步,在步骤四中利用有机溶剂提取虾青素包括:在对反应器补液后,取5ml藻液,3500rpm离心5分钟,弃上清,得到藻细胞沉淀;向藻细胞沉淀中加入2ml含有30%(v/v)甲醇和5%(w/w)氢氧化钾的水溶液,65℃水浴15分钟,3500rpm离心5分钟;弃上清,加入纯水洗涤2次,去除碱液残留,加入5ml二甲基亚砜,于45℃水浴超声至藻体泛白。
18.进一步,在步骤四中离心收集上清,利用分光光度计测定od
490nm
;按如下公式计算:虾青素浓度c(mg l-1
)=4.5
×
od
490nm
×v二甲基亚砜
/v
藻液
。
19.进一步,在步骤四中生物量浓度的具体测定方法为:每隔一天用无菌水向鼓泡塔式光生物反应器进行补液,取10ml藻细胞培养液,3500rpm离心5分钟,弃上清,加入纯水洗涤2次,转移至提前称重的1.5ml离心管中,12000rpm离心2分钟,弃上清,冷冻干燥至恒重,称取藻细胞干重;按如下公式计算:生物量(g l-1
)=干重(g)/藻液体积(l)。
20.本发明的另一目的在于提供一种具有抗氧化、抗炎、抗凋亡、保护神经的膳食补充剂,其特征在于,所述膳食补充剂包含所述提高雨生红球藻的生物量和虾青素的方法制备的虾青素。
21.本发明的另一目的在于提供一种具有保护皮肤、保护肝肾的膳食补充剂,其特征在于,所述膳食补充剂包含所述提高雨生红球藻的生物量和虾青素的方法制备的虾青素。
22.结合上述的技术方案和解决的技术问题,请从以下几方面分析本发明所要保护的技术方案所具备的优点及积极效果为:
23.第一、针对上述现有技术存在的技术问题以及解决该问题的难度,紧密结合本发明的所要保护的技术方案以及研发过程中结果和数据等,详细、深刻地分析本发明技术方案如何解决的技术问题,解决问题之后带来的一些具备创造性的技术效果。具体描述如下:
24.微藻是天然虾青素的巨大来源,其中雨生红球藻被认为是虾青素的细胞工厂。虽然已有大量分析工作优化了雨生红球藻虾青素的生产、提取和纯化过程,但仍然存在着虾青素生产成本高、产量低等问题。雨生红球藻积累虾青素会受到各种环境因素和培养方式等影响,氮缺乏在虾青素生产的经济性方面比光照的改变具有更大的优势。然而,如果提供
的氮太少,细胞会因大量的叶绿素降解而受损,从而使得生物量降低。本发明中使用l-苹果酸作为化学诱导剂,在高光缺氮条件下对雨生红球藻进行培养,有效提高了诱导阶段的雨生红球藻生物量浓度。在微藻培养的第13天,l-苹果酸添加浓度为1mmol l-1
时,生物量浓度最高为2.31g l-1
,是对比例空白对照的1.53倍。在微藻培养的第15天,l-苹果酸添加浓度为1mmol l-1
时,虾青素浓度最高为47.53mg l-1
,是对比例空白对照的1.68倍。本方案同时提高了生物量和虾青素产率,为雨生红球藻高密度发酵奠定了基础。
25.第二,把技术方案看做一个整体或者从产品的角度,本发明所要保护的技术方案具备的技术效果和优点,具体描述如下:
26.本发明公开了l-苹果酸的新的应用领域,且易于操作成本低廉。实验所用藻株可按照常规方法培养,养藻废液可以无需额外处理直接应用于农业灌溉,提高了废液利用率。
27.本发明方法提高了雨生红球藻的生物量及虾青素产量。实验证明添加l-苹果酸的诱导组比对照组生物量提高了12%~53%,最高达到了2.31g l-1
;实验证明添加l-苹果酸的诱导组比对照组虾青素浓度提高了5%~68%,最高达到了47.53mg l-1
;l-苹果酸添加量为1mmol l-1
的诱导组效果最佳。
28.第三,作为本发明的权利要求的创造性辅助证据,还体现在以下几个重要方面:
29.本发明的技术方案填补了国内外业内技术空白:使用廉价易得且安全的l-苹果酸作为诱导剂培养雨生红球藻,有效克服了氮缺乏对于雨生红球藻生物量的抑制,同时提高了藻体生物量和虾青素含量。
30.本发明的技术方案解决了人们一直渴望解决、但始终未能获得成功的技术难题:商业化生产虾青素的最大障碍是诱导雨生红球藻中虾青素的生物合成耗时长产量低。本发明同时提高了生物量和虾青素产率,为雨生红球藻高密度发酵奠定了基础。
附图说明
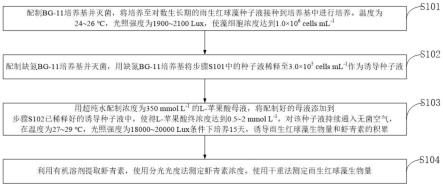
31.图1是本发明实施例提供的提高雨生红球藻生物量和虾青素产量的方法流程图。
32.图2是本发明实施例提供的实施例1、2、3、对比例中雨生红球藻的生物量浓度示意图。
33.图3是本发明实施例提供的实施例1、2、3、对比例中雨生红球藻的虾青素浓度示意图。
具体实施方式
34.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
35.一、解释说明实施例。为了使本领域技术人员充分了解本发明如何具体实现,该部分是对权利要求技术方案进行展开说明的解释说明实施例。
36.如图1所示,本发明提供一种提高雨生红球藻的生物量和虾青素的方法包括以下步骤:
37.s101,配制bg-11培养基并灭菌,将培养至对数生长期的雨生红球藻种子液接种到培养基中进行培养。温度为24~26℃,光照强度为1900~2100lux,使藻细胞浓度达到1.0
×
106cells ml-1
。
38.s102,配制缺氮bg-11培养基并灭菌,用缺氮bg-11培养基将步骤s101中的种子液稀释至3.0
×
105cells ml-1
作为诱导种子液。
39.s103,用超纯水配制浓度为350mmol l-1
的l-苹果酸母液,将配制好的母液添加到步骤s102已稀释好的诱导种子液中,使得l-苹果酸终浓度达到0.5~2mmol l-1
。对该种子液持续通入无菌空气,在温度为27~29℃,光照强度为18000~20000lux条件下培养15天,诱导雨生红球藻生物量和虾青素的积累。
40.s104,利用有机溶剂提取虾青素,使用分光光度法测定虾青素浓度。使用干重法测定雨生红球藻生物量。
41.步骤s101中雨生红球藻为雨生红球藻藻株haematococcuspluvialis lugu;该菌株为现有文献中公开的藻株(yongteng zhao,minmin shang,jun-wei xu,et al.enhanced astaxanthin production from a novel strain ofhaematococcuspluvialis using fulvic acid[j].process biochemistry,2015,50(12):2072-2077)。
[0042]
步骤s101中雨生红球藻种子液接种到培养基中进行培养具体包括:配制bg-11培养基并灭菌,将培养至对数生长期的雨生红球藻种子液接种到培养基中进行培养。在温度为24~26℃、光照强度为1900~2100lux、持续光照条件下培养,使藻细胞浓度达到1.0
×
106cells ml-1
。
[0043]
步骤s103诱导雨生红球藻生物量和虾青素的积累包括:
[0044]
用超纯水配制浓度为350mmol l-1
的l-苹果酸母液,将l-苹果酸母液添加到步骤s102中已经用缺氮bg-11培养基稀释好的用于诱导的种子液中,使l-苹果酸浓度达到0.5~2mmol l-1
。将该种子液接种到鼓泡塔式光生物反应器中,持续鼓入无菌空气,在27~29℃、光照强度为18000~20000lux的持续光照及氮饥饿的复合胁迫条件下对藻细胞进行诱导,实现雨生红球藻生物量和虾青素的积累。
[0045]
步骤s104中利用有机溶剂提取虾青素为:在反应器补液后,取5ml藻液,3500rpm离心5分钟,弃上清,得到藻细胞沉淀;向藻细胞沉淀中加入2ml含有30%(v/v)甲醇和5%(w/w)氢氧化钾的水溶液,65℃水浴15分钟,3500rpm离心5分钟;弃上清,加入纯水洗涤2次,去除碱液残留,加入5ml二甲基亚砜,于45℃水浴超声至藻体泛白。
[0046]
步骤s104中离心收集上清,利用分光光度计测定od
490nm
;按如下公式计算:虾青素浓度c(mg l-1
)=4.5
×
od
490nm
×v二甲基亚砜
/v
藻液
。
[0047]
步骤s104中生物量浓度的具体测定方法为:每隔一天用无菌水向鼓泡塔式光生物反应器进行补液,取10ml藻细胞培养液,3500rpm离心5分钟,弃上清,加入纯水洗涤2次,转移至提前称重的1.5ml离心管中,12000rpm离心2分钟,弃上清,冷冻干燥至恒重,称取藻细胞干重。按如下公式计算:生物量(g l-1
)=干重(g)/藻液体积(l)。
[0048]
下面结合具体实施例以及对比例对本发明的技术方案作进一步描述。
[0049]
实施例1
[0050]
利用l-苹果酸提高雨生红球藻生物量和虾青素产量的方法,具体步骤如下:
[0051]
(1)种子液的制备:配制bg-11培养基并灭菌,将雨生红球藻藻种haematococcuspluvialis lugu接种到培养基中进行培养。在温度为25℃、光照强度为2000lux、持续光照条件下培养至对数生长期后期,使藻细胞浓度达到1
×
106cells ml-1
。配
制缺氮bg-11培养基并灭菌,将细胞浓度稀释到3.0
×
105cells ml-1
作为后续诱导种子液。
[0052]
(2)诱导雨生红球藻积累虾青素:用超纯水配制浓度为350mmol l-1
的l-苹果酸母液,取350ml步骤(1)已经稀释好的诱导藻液,将l-苹果酸母液添加到步骤(1)中的诱导种子液中,使l-苹果酸浓度达到0.5mmol l-1
。将该种子液接种到鼓泡塔式光生物反应器中,持续鼓入无菌空气,在28℃、光照强度为20000lux的持续光照及氮饥饿的复合胁迫条件下对藻细胞进行培养,诱导雨生红球藻生物量和虾青素的积累。
[0053]
按照实施例1的方法,再进行三组平行实验,其他条件与实施例1相同,连续光照及l-苹果酸的诱导,使藻细胞积累虾青素。
[0054]
本实施例培养完的藻液利用干重法测定生物量、分光光度法检测藻细胞的虾青素含量,其具体步骤为:
[0055]
生物量浓度测定:每隔一天向鼓泡塔式光生物反应器用无菌水进行补液,取10ml藻细胞培养液,3500rpm离心5分钟,弃上清,用超纯水洗2次,转移至提前称重的1.5ml离心管中,12000rpm离心2分钟,弃上清,冷冻干燥至恒重,称取藻细胞干重。按如下公式计算:
[0056]
生物量(g l-1
)=干重(g)/藻液体积(l)
[0057]
虾青素提取的方法为:在反应器补液后,取5ml藻液,3500rpm离心5分钟,弃上清,得到藻细胞沉淀;向藻细胞沉淀中加入2ml含有30%(v/v)甲醇和5%(w/w)氢氧化钾的水溶液,65℃水浴15分钟,3500rpm离心5分钟;弃上清,加入纯水洗涤2次,去除碱液残留,加入5ml二甲基亚砜,于45℃水浴超声破碎细胞至藻体泛白。离心收集上清,利用分光光度计测定od
490nm
;按如下公式计算:
[0058]
虾青素浓度c(mg l-1
)=4.5
×
od
490nm
×v二甲基亚砜
/v
藻液
[0059]
检测结果:当l-苹果酸浓度为0.5mmol l-1
时,培养至第13天时,雨生红球藻生物量最高为2.11g l-1
;培养至第15天时,虾青素浓度最高为43.42mg l-1
。且培养完藻的培养基无污染,可以直接排放。
[0060]
实施例2
[0061]
利用l-苹果酸提高雨生红球藻生物量和虾青素产量的方法,具体步骤如下:
[0062]
(1)种子液的制备:配制bg-11培养基并灭菌,将本实验室筛选保藏的雨生红球藻藻种haematococcuspluvialis lugu(ncbi:km115647)接种到培养基中进行培养。在温度为25℃、光照强度为2000lux的持续光照条件下培养至对数生长期后期,使藻细胞浓度达到1
×
106cells ml-1
。配制缺氮bg-11培养基并灭菌,将细胞浓度稀释到3.0
×
105cells ml-1
作为后续诱导种子液。
[0063]
(2)诱导雨生红球藻积累虾青素:用超纯水配制浓度为350mmol l-1
的l-苹果酸母液,取350ml步骤(1)已经稀释好的诱导藻液,将l-苹果酸母液添加到步骤(1)中的诱导种子液中,使l-苹果酸浓度达到1mmol l-1
。将该种子液接种到鼓泡塔式光生物反应器中,持续鼓入无菌空气,在28℃、光照强度为20000lux的持续光照及氮饥饿的复合胁迫条件下对藻细胞进行培养,诱导雨生红球藻生物量和虾青素的积累。
[0064]
按照实施例2的方法,再进行三组平行实验,其他条件与实施例2相同,连续光照及l-苹果酸的诱导,使藻细胞积累虾青素。
[0065]
按照实施例1的检测结果:当l-苹果酸浓度为1mmol l-1
时,培养至第13天时,雨生红球藻生物量最高为2.31g l-1
;培养至第15天时,虾青素浓度最高为47.53mg l-1
。且培养
完藻的培养基无污染,可以直接排放。
[0066]
实施例3
[0067]
利用l-苹果酸提高雨生红球藻生物量和虾青素产量的方法,具体步骤如下:
[0068]
(1)种子液的制备:配制bg-11培养基并灭菌,将雨生红球藻藻种haematococcuspluvialis lugu接种到培养基中进行培养。在温度为25℃、光照强度为2000lux的持续光照条件下培养至对数生长期后期,使藻细胞浓度达到1
×
106cells ml-1
。配制缺氮bg-11培养基并灭菌,将细胞浓度稀释到3.0
×
105cells ml-1
作为后续诱导种子液。
[0069]
(2)诱导雨生红球藻积累虾青素:用超纯水配制浓度为350mmol l-1
的l-苹果酸母液,取350ml步骤(1)已经稀释好的诱导藻液,将l-苹果酸母液添加到步骤(1)中的诱导种子液中,使l-苹果酸浓度达到2mmol l-1
。将该种子液接种到鼓泡塔式光生物反应器中,持续鼓入无菌空气,在28℃、光照强度为20000lux的持续光照及氮饥饿的复合胁迫条件下对藻细胞进行培养,诱导雨生红球藻生物量和虾青素的积累。
[0070]
按照实施例3的方法,再进行三组平行实验,其他条件与实施例2相同,连续光照及l-苹果酸的诱导,使藻细胞积累虾青素。
[0071]
按照实施例1的检测结果:当l-苹果酸浓度为2mmol l-1
时,培养至第13天时,雨生红球藻生物量最高为1.70g l-1
,虾青素浓度最高为29.89mg l-1
。且培养完藻的培养基无污染,可以直接排放。
[0072]
对比例
[0073]
(1)种子液的制备:配制bg-11培养基并灭菌,将雨生红球藻藻种haematococcuspluvialis lugu接种到培养基中进行培养。在温度为25℃、光照强度为2000lux的持续光照条件下培养至对数生长期后期,使藻细胞浓度达到1
×
106cells ml-1
。配制缺氮bg-11培养基并灭菌,将细胞浓度稀释到3.0
×
105cells ml-1
作为后续诱导种子液。
[0074]
(2)诱导雨生红球藻积累虾青素:取350ml步骤(1)已经稀释好的诱导藻液,将该种子液接种到鼓泡塔式光生物反应器中,持续鼓入无菌空气,在28℃、光照强度为20000lux的持续光照及氮饥饿的复合胁迫条件下对藻细胞进行培养,诱导雨生红球藻生物量和虾青素的积累。
[0075]
按照实施对比例的方法,再进行三组平行实验,其他条件与对比例相同,连续光照及l-苹果酸的诱导,使藻细胞积累虾青素。按照实施对比例的检测结果,当l-苹果酸浓度为0mmol l-1
时,第15天时雨生红球藻生物量达到最高,为1.52g l-1
;第15天时虾青素浓度达到最高,为28.26mg l-1
。且培养完藻的培养基无污染,可以直接排放。
[0076]
利用干重法和分光光度法测定对比例和实施例1~3中雨生红球藻生物量浓度和虾青素浓度,每个实施例中的三个平行实验取平均值。结果显示:(1)实施例1、2中雨生红球藻生物量浓度在第13天达到最高值,虾青素浓度在第15天达到最高值;(2)实施例3中雨生红球藻生物量浓度和虾青素浓度均在第13天达到最高值;(3)实施例1、2、3中第13天时雨生红球藻的生物量与虾青素浓度均高于对比例中没有加入l-苹果酸的情况。结果说明:当l-苹果酸浓度为0.5~2mmol l-1
时,l-苹果酸对雨生红球藻生物量与虾青素的积累具有促进作用。在微藻培养的第13天,l-苹果酸浓度为1mmol l-1
时,生物量浓度最高为2.31g l-1
,是
对比例空白对照的1.53倍。在微藻培养的第15天,l-苹果酸浓度为1mmol l-1
时,虾青素浓度最高为47.53mg l-1
,是对比例空白对照的1.68倍。
[0077]
二、应用实施例。为了证明本发明的技术方案的创造性和技术价值,该部分是对权利要求技术方案进行具体产品上或相关技术上的应用实施例。
[0078]
基于目前虾青素的益处,它在人类治疗方面具有前瞻性的应用价值,如抗炎、抗衰老等特性,在食品和饲料养殖领域也具有优势。虾青素是一种天然的强抗氧化类胡萝卜素,具有抗炎活性,虾青素可以通过抑制大鼠冠状动脉微栓塞引起的心室的氧化应激和凋亡来保护心脏,并减少运动对小鼠的骨骼肌和心脏的相关损伤。虾青素是一种调节氧化还原平衡的抗氧化剂,被认为是心血管疾病炎症反应的重要调节因子。虾青素可作为一种营养补充剂,可防止正常人类真皮成纤维细胞中双酚a产生引发的皮肤成纤维细胞自噬性细胞死亡。虾青素也经常被用作食品和饲料行业的膳食补充剂。欧洲食品安全局在2020年得出结论,成年人从食品补充剂中摄入8mg虾青素是安全的。
[0079]
三、实施例相关效果的证据。本发明实施例在研发或者使用过程中取得了一些积极效果,和现有技术相比的确具备很大的优势,下面内容结合试验过程的数据、图表等进行描述。
[0080]
现有使用诱导剂来提高雨生红球藻中虾青素产量的手段多数与营养限制耦合,造成了藻体生物量低下,不适合进行商业生产。多数诱导策略会使得雨生红球藻生物量低于1.5g l-1
,一些条件下会使得藻体生物量低于1.0g l-1
。这些都限制了雨生红球藻高密度培养。本发明中使用l-苹果酸作为化学诱导剂,在高光缺氮条件下对雨生红球藻进行培养,有效提高了诱导阶段的雨生红球藻生物量浓度。在l-苹果酸添加浓度为1mmol l-1
时,生物量浓度最高为2.31g l-1
,是对比例空白对照的1.53倍;虾青素浓度最高为47.53mg l-1
,是对比例空白对照的1.68倍。本发明同时提高了生物量和虾青素产率,为雨生红球藻高密度发酵奠定了基础。
[0081]
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1