一种D-来苏糖的制备方法
本发明涉及功能糖制备,尤其是涉及一种d-来苏糖的制备方法。
背景技术:
1、单糖类化合物在医药医学、食品工业、精细化工等领域占有重要地位。遗憾的是,自然界天然存在的单糖只有区区7种(d-葡萄糖、d-果糖、d-核糖、d-半乳糖、d-木糖、d-甘露糖以及l-阿拉伯糖),故绝大部分单糖都需要人工制备。其中d-来苏糖(ⅰ)是极其重要的一种单糖,比如d-来苏糖(ⅰ)是制备某些抗肿瘤药物以及免疫兴奋剂的关键中间体(biosci.biotechnol.biochem.1996.288–292、j.med.chem.1996.1582–1588)。
2、
3、然而目前已知的制备化合物(ⅰ)的方法却很少,主要以d-木糖作为起始原料。比如有文献报导,可以通过金属催化的方法将d-木糖转化为d-来苏糖(金属sn催化剂:acs.catal.2017.3792–3798;金属ni催化剂:inorg.chem.1988.4085–4094)。然而这类方法仅限于理论研究,首先反应体系形成的是一系列化合物的混合物(d-木糖、d-来苏糖、d-木酮糖等),这些化合物极性极其相近从而导致无法分离。其次所使用的金属催化剂结构复杂,制备成本非常高。这些缺陷意味着较低的放大生产可能性。
4、此外,文献carbohydr.res.1992.281–288介绍了一种改进合成路线,如下式所示:
5、
6、d-木糖首先在酸催化下分别在c-1羟基上引入甲基、c-5羟基上引入三苯甲基,从而形成糖苷a。a在溴甲烷以及二硫化碳作用下,形成二取代物b。b发生自由基消除形成烯烃c(为α/β=1/1的混合物)。c在高锰酸钾氧化下形成顺式二羟基产物,并且羟基与c-1甲氧基互为反式。在α-c被分离出来进行相应的反应形成α-d。α-d在强酸高温下发生水解反应,最终形成d-来苏糖(ⅰ)。
7、虽然该路线相对于其它路线有明显的改进,但依然有不少缺陷,首先该路线需要使用溴甲烷。气体状态的溴甲烷不仅操作不便,更是在2017年10月被世界卫生组织国际癌症研究机构定义为3类致癌物。而二硫化碳,三丁基锡都是高毒性化合物,不适合大规模使用。此外,为了获得单一的α-c,必须对极性非常接近的α/β混合的c进行仔细的分离,才能勉强获得纯α-c,虽然作者未提及收率,但显然所要的α-c的收率不会大于50%。该路线最终的总收率不到20%。
技术实现思路
1、本发明的目的就是为了克服上述现有技术存在涉及到的材料成本高且具有毒性、过程复杂且收率低等的缺陷而提供一种d-来苏糖的制备方法。
2、本发明的目的可以通过以下技术方案来实现:
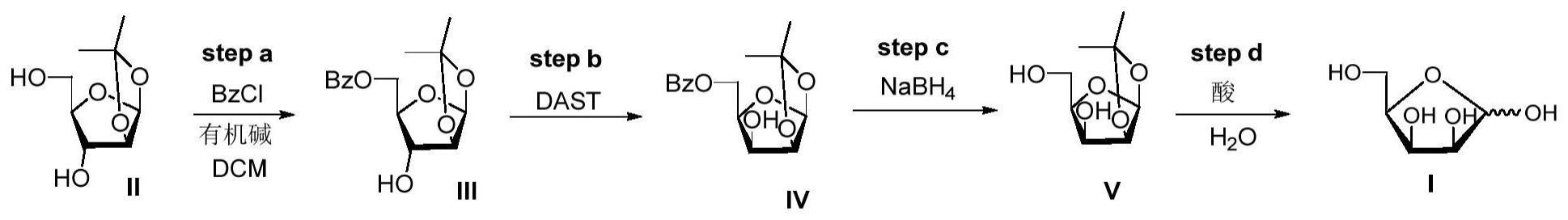
3、本发明的技术方案为提供一种d-来苏糖的制备方法,包括如下步骤:
4、s1、将如式(ⅱ)所示1,2-异丙基-β-d-阿拉伯糖苷、有机碱、二氯甲烷混合并滴加苯甲酰氯进行反应,反应结束后加入水混合分层,取有机相经稀盐酸水溶液洗涤、无水硫酸镁干燥、蒸干、纯化,得到如式(ⅲ)所示中间体:
5、
6、s2、将s1步骤得到如式(ⅲ)所示中间体与有机溶剂混合并滴加dast试剂反应,反应结束后将反应体系滴加到碳酸氢钠水溶液中混合分层,取有机相依次用柠檬酸水溶液和食盐水洗涤、无水硫酸镁干燥、蒸干、纯化,得到如式(ⅳ)所示中间体:
7、
8、s3、将s2步骤得到的如式(ⅳ)所示中间体进行还原反应并纯化得到如式(ⅴ)所示中间体:
9、
10、s4、将s3步骤得到的如式(ⅴ)所示中间体进行酸性水解并纯化得到如式(ⅰ)所示d-来苏糖:
11、
12、如式(ⅰ)所示d-来苏糖中的波浪线表明,这个位置的羟基取代是没有手性的,是α和β构型的混合物。
13、进一步地,s1步骤中,所述有机碱选自吡啶、三乙胺、二异丙基乙基胺或n-甲基吗啉中的任意一种。
14、进一步地,s1步骤中,如式(ⅱ)所示1,2-异丙基-β-d-阿拉伯糖苷:苯甲酰氯:有机碱的摩尔比为1:0.5:1~1:2:5。
15、进一步地,s1步骤中,反应的温度为-25℃~25℃,反应的时间为0.5~12h。
16、进一步地,s2步骤中,所述有机溶剂选自二氯甲烷或四氢呋喃中的任意一种。
17、进一步地,s2步骤中,如式(ⅲ)所示中间体与所述dast试剂的摩尔比为1:1~1:15。
18、进一步地,s2步骤中,反应的温度为-25℃~25℃,反应的时间为1~36h;反应结束后,将反应体系在0℃下滴加到碳酸氢钠水溶液中混合分层。
19、进一步地,s3步骤中,还原反应为:将如式(ⅳ)所示中间体与有机溶剂混合,并分批加入硼氢化钠在25℃~85℃下还原反应1~12h,反应结束后除去溶剂;所述有机溶剂选自甲醇或乙醇;如式(ⅳ)所示中间体与硼氢化钠的摩尔比为1:1~1:5。
20、进一步地,s4步骤中,酸性水解为:将如式(ⅴ)所示中间体、酸催化剂和水在25℃~85℃下反应1~36h,反应结束后加入固体碳酸氢钠中和至中性,并减压除水;所述酸催化剂选自无机酸、有机酸或酸性树脂中的任意一种;当酸催化剂为有机酸或无机酸催化剂时,如式(ⅴ)所示中间体与酸催化剂的摩尔比为1:0.01~1:1,当酸催化剂为酸性树脂催化剂时,如式(ⅴ)所示中间体与酸催化剂的质量比是1:0.1~1:1。
21、当酸催化剂为酸性树脂时,反应结束后先过滤除去不溶的酸性树脂。
22、进一步地,所述无机酸选自盐酸或硫酸中的任意一种,所述有机酸选自甲磺酸、对甲苯磺酸、樟脑磺酸、醋酸或三氟醋酸中的任意一种,所述酸性树脂选自amberlite系列酸性树脂或dowex系列酸性树脂中的任意一种。
23、与现有技术相比,本发明具有如下有益效果:
24、(1)本发明只需要通过常规的溶剂和试剂就能实现目标产物d-来苏糖(ⅰ)的制备,所用的溶剂和试剂具有明显低的安全隐患。
25、(2)本发明的制备方法能以较高总收率(45%)得到目标产物d-来苏糖(ⅰ),显著高于现有合成路线,更适合于放大生产。
技术特征:
1.一种d-来苏糖的制备方法,其特征在于,包括如下步骤:
2.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s1步骤中,所述有机碱选自吡啶、三乙胺、二异丙基乙基胺或n-甲基吗啉中的任意一种。
3.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s1步骤中,如式(ⅱ)所示1,2-异丙基-β-d-阿拉伯糖苷:苯甲酰氯:有机碱的摩尔比为1:0.5:1~1:2:5。
4.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s1步骤中,反应的温度为-25℃~25℃,反应的时间为0.5~12h。
5.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s2步骤中,所述有机溶剂选自二氯甲烷或四氢呋喃中的任意一种。
6.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s2步骤中,如式(ⅲ)所示中间体与所述dast试剂的摩尔比为1:1~1:15。
7.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s2步骤中,反应的温度为-25℃~25℃,反应的时间为1~36h;反应结束后,将反应体系在0℃下滴加到碳酸氢钠水溶液中混合分层。
8.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s3步骤中,还原反应为:将如式(ⅳ)所示中间体与有机溶剂混合,并分批加入硼氢化钠在25℃~85℃下还原反应1~12h,反应结束后除去溶剂;所述有机溶剂选自甲醇或乙醇;如式(ⅳ)所示中间体与硼氢化钠的摩尔比为1:1~1:5。
9.根据权利要求1所述的一种d-来苏糖的制备方法,其特征在于,s4步骤中,酸性水解为:将如式(ⅴ)所示中间体、酸催化剂和水在25℃~85℃下反应1~36h,反应结束后加入固体碳酸氢钠中和至中性,并减压除水;所述酸催化剂选自无机酸、有机酸或酸性树脂中的任意一种;当酸催化剂为有机酸或无机酸催化剂时,如式(ⅴ)所示中间体与酸催化剂的摩尔比为1:0.01~1:1,当酸催化剂为酸性树脂催化剂时,如式(ⅴ)所示中间体与酸催化剂的质量比是1:0.1~1:1。
10.根据权利要求9所述的一种d-来苏糖的制备方法,其特征在于,所述无机酸选自盐酸或硫酸中的任意一种,所述有机酸选自甲磺酸、对甲苯磺酸、樟脑磺酸、醋酸或三氟醋酸中的任意一种,所述酸性树脂选自amberlite系列酸性树脂或dowex系列酸性树脂中的任意一种。
技术总结
本发明涉及一种D‑来苏糖的制备方法,包括如下步骤:S1、将1,2‑异丙基‑β‑D‑阿拉伯糖苷(Ⅱ)、有机碱、二氯甲烷混合并滴加苯甲酰氯反应,反应结束后加水混合分层,取有机相经稀盐酸水溶液洗涤、无水硫酸镁干燥、蒸干、纯化,得到中间体(Ⅲ):S2、将中间体(Ⅲ)与有机溶剂混合并滴加DAST试剂反应,反应结束后将反应体系滴加到碳酸氢钠水溶液中混合分层,取有机相依次用柠檬酸水溶液和食盐水洗涤、无水硫酸镁干燥、蒸干、纯化,得到中间体(Ⅳ):S3、将中间体(Ⅳ)进行还原反应并纯化得到中间体(Ⅴ):S4、将中间体(Ⅴ)进行酸性水解并纯化得到D‑来苏糖(Ⅰ)。本发明具有收率高、操作简便、安全风险低等优点。
技术研发人员:夏铮,潘仙华,陈宇
受保护的技术使用者:上海应用技术大学
技术研发日:
技术公布日:2024/1/13
- 还没有人留言评论。精彩留言会获得点赞!