N-烷氧基-1-酰基-1H-吡咯-2-酰胺类化合物及其应用
本发明涉及药物化学,尤其涉及n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物及其应用。
背景技术:
1、新德里金属-β-内酰胺酶(new delhi metallo-β-lactamse-1,ndm-1),是一种新发现的可水解β-内酰胺类化合物的酶(bioorg.med.chem.lett.2014;24,386-9)。蛋白结构研究表明,ndm-1的关键活性位点含有两个锌离子,属于典型的金属β-内酰胺酶(proteincell 2011,2(5),384-394)。它通过水解β-内酰胺环使几乎所有含有β-内酰胺环的抗生素失活(protein science:a publication of the protein society.2011;20,1484-91.)。产ndm-1的“超级细菌”对包括碳青霉烯类在内的多种类型抗生素表现出高度耐药,仅替加环素、柔红霉素及多粘菌素对其具有一定的敏感性,使得这类病人的临床治疗非常困难(bioorg.med.chem.2013,21(11),3138-3146)。
2、近年来,ndm-1抑制剂的研发引起了相关领域研究者的广泛兴趣,具有一定ndm-1抑制活性的化合物陆续见诸报道,总数超过500个(acs infect.dis.2019,5(1),9-34),大致分为两类。一类是源于天然产物的抑制剂(microbiol res.2022,261,127079),主要是一些多羟基化合物、羧酸化合物、酮羰基化合物、色酮类化合物。它们的结构复杂,合成困难,且活性并不理。另一类是合成的小分子化合物,主要包含以edta(angew.chem.,int.ed.2014,53(8),2130-2133)为代表的金属螯合剂,含巯基的卡托普利类似物(j.am.chem.soc.2012,134(28),11362-11365),硼酸类化合物(j.med.chem.2019,62(18),8544-8556),吡啶羧酸类化合物(j.med.chem.2017,60(17),7267-7283),缩氨基硫脲类化合物(bioorg.chem.2021,107,104576),唑类化合物(molecules 2019,24(6),1174),罗丹宁衍生物(acs med.chem.lett.2018,9(4),359-364),依布硒啉衍生物(bioorg.chem.2020,100,103873)。这些合成的小分子化合物,存在抑制活性相对较低、或选择性较差、或毒性较大、或成药性较差等缺陷。
3、上述报道报道的很多化合物对ndm-1有抑制作用,但目前仍无相应的有效抑制剂进入临床试验,使得产金属β-内酰胺酶的“超级细菌”所致感染性疾病,尚无有效的临床治疗手段。因此,基于ndm-1酶晶体结构特点,利用计算机辅助设计,设计并合成一系列n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,希望其对ndm-1具有良好的抑制效果。
4、本发明是在国家自然科学基金(21702239)资助下而进行的研究。
技术实现思路
1、本发明的目的是提供一种n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物及其应用。
2、本发明是通过以下技术方案予以实现的:
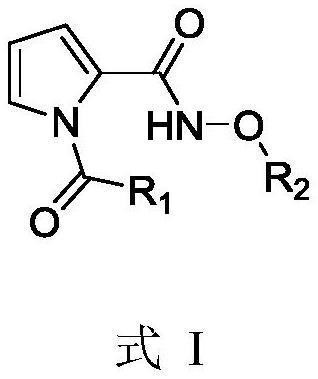
3、一种如式i所示的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物:
4、
5、其中,r1选自4-甲基苯甲基,4-甲基苯乙基,4-甲基苯丙基,4-甲氧基苯甲基,3-甲氧基苯甲基,噻吩-2-甲基,4-氰基苯甲基或4-乙氧基苯甲基;r2选自甲基或苄基。
6、优选地,式ⅰ所示的化合物,具体如下表1所示:
7、表1
8、
9、
10、本发明还涉及所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物的制备方法,由如下步骤组成:
11、(1)以三氯乙酰吡咯和o-取代羟胺类化合物为原料,o-取代羟胺类化合物中r2选自甲基或苄基,三乙胺为溶剂,反应得到化合物a,反应方程式如下:
12、
13、(2)步骤(1)得到的化合物a和羧酸类化合物为原料,羧酸类化合物中r1选自4-甲基苯甲基,4-甲基苯乙基,4-甲基苯丙基,4-甲氧基苯甲基,3-甲氧基苯甲基,噻吩-2-甲基,4-氰基苯甲基或4-乙氧基苯甲基,4-二甲氨基吡啶、2,6-二甲基吡啶和二碳酸二叔丁酯为催化剂,乙腈为溶剂,反应得到目标产物:n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,反应方程式如下:
14、
15、优选地,步骤(1)中所述的三氯乙酰吡咯和o-取代羟胺类化合物的摩尔比为1:0.5-3;三氯乙酰吡咯的浓度为0.05-2.0mol/l,反应温度为25℃-100℃,反应时间为4-8h。
16、优选地,步骤(2)所述的化合物a与羧酸类化合物的摩尔比为1:0.5-3,化合物a的浓度为0.05-1mol/l,室温下搅拌反应10-14h。
17、优选地,步骤(2)所述的羧酸类化合物与4-二甲氨基吡啶的摩尔比为4-6:1,4-二甲氨基吡啶、2,6-二甲基吡啶和二碳酸二叔丁酯的摩尔比为1:1:5-6。
18、本发明还涉及所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,或其前体药物,或其药学上可接受的盐作为新德里金属-β-内酰胺酶1(ndm-1)抑制剂的应用。本发明提出的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物对新德里金属-β-内酰胺酶1(ndm-1)具有良好的抑制作用。
19、本发明还涉及所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,或其前体药物,或其药学上可接受的盐在制备抑制耐药细菌活性药物中的应用。本发明提出的所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物通过抑制新德里金属-β-内酰胺酶ndm-1活性以缓解ndm-1引起的细菌对β-内酰胺类抗生素的耐药性。
20、本发明还涉及一种抑制耐药细菌活性药物,包含有效量的权利要求1或2所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,以及任选的药学可接受的载体或赋形剂。本发明提出的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物通过与β-内酰胺类抗生素联用,可望治疗由ndm-1引起的耐药细菌感染。
21、与现有技术相比,本发明的有益效果是:本发明的制备方法具有快速、方便、成本低等优点,得到的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物对新德里金属-β-内酰胺酶1(ndm-1)具有良好的抑制作用,可作为ndm-1的抑制剂,通过与β-内酰胺类抗生素联用,可望治疗由ndm-1引起的耐药细菌感染,具有良好的药物应用前景。
技术特征:
1.式ⅰ所示的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物:
2.根据权利要求1所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,其特征在于,式ⅰ所示的化合物如下表所示:
3.权利要求1或2所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物的制备方法,其特征在于,由如下步骤组成:
4.根据权利要求3所述的制备方法,其特征在于,步骤(1)中所述的三氯乙酰吡咯和o-取代羟胺类化合物的摩尔比为1:0.5-3;三氯乙酰吡咯的浓度为0.05-2.0mol/l,反应温度为25℃-100℃,反应时间为4-8h。
5.根据权利要求3所述的制备方法,其特征在于,步骤(2)所述的化合物a与羧酸类化合物的摩尔比为1:0.5-3,化合物a的浓度为0.05-1mol/l,室温下搅拌反应10-14h。
6.根据权利要求3或5所述的制备方法,其特征在于,步骤(2)所述的羧酸类化合物与4-二甲氨基吡啶的摩尔比为4-6:1,4-二甲氨基吡啶、2,6-二甲基吡啶和二碳酸二叔丁酯的摩尔比为1:1:5-6。
7.权利要求1或2所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,或其前体药物,或其药学上可接受的盐作为新德里金属-β-内酰胺酶1(ndm-1)抑制剂的应用。
8.权利要求1或2所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,或其前体药物,或其药学上可接受的盐在制备抑制耐药细菌活性药物中的应用。
9.一种抑制耐药细菌活性药物,其特征在于,包含有效量的权利要求1或2所述的n-烷氧基-1-酰基-1h-吡咯-2-酰胺类化合物,以及任选的药学可接受的载体或赋形剂。
技术总结
本发明公开了N‑烷氧基‑1‑酰基‑1H‑吡咯‑2‑酰胺类化合物及其应用。N‑烷氧基‑1‑酰基‑1H‑吡咯‑2‑酰胺类化合物结构式如式Ⅰ所示,其中,R1选自4‑甲基苯甲基,4‑甲基苯乙基,4‑甲基苯丙基,4‑甲氧基苯甲基,3‑甲氧基苯甲基,噻吩‑2‑甲基,4‑氰基苯甲基或4‑乙氧基苯甲基;R2选自甲基或苄基。本发明提出的制备方法具有快速、方便、成本低等优点,得到的N‑烷氧基‑1‑酰基‑1H‑吡咯‑2‑酰胺类化合物对新德里金属‑β‑内酰胺酶1(NDM‑1)具有良好的抑制作用,可作为NDM‑1的抑制剂,通过与β‑内酰胺类抗生素联用,可望治疗由NDM‑1引起的耐药细菌感染,具有良好的药物应用前景。
技术研发人员:黄漫娜,罗盼,梁耀文,万一千
受保护的技术使用者:中山大学
技术研发日:
技术公布日:2024/1/14
- 还没有人留言评论。精彩留言会获得点赞!