具有启动子活性的核酸及其用途的制作方法
本申请涉及遗传学、基因疗法和分子生物学领域。更具体地,本发明涉及具有启动子活性的核酸(变体)、基于其的表达盒和载体、用于生产靶产物或表达载体的宿主细胞。
背景技术:
1、启动子是一种dna元件,其促进与启动子可操作地连接的多核苷酸的转录。启动子也可以是启动子/增强子元件的一部分。尽管启动子和增强子元件之间的物理边界并不总是清楚的,启动子通常是指核酸分子上的位点,rna聚合酶和/或任何相关因子结合到该位点,并且在该位点启动转录。增强子在时间上以及空间上增强启动子活性。已知许多启动子在广泛的细胞类型中具有转录活性。启动子可以分为两类,组成型发挥功能的启动子和通过诱导或去阻抑来调节的启动子。这两类都适用于蛋白质表达。用于在真核细胞中(并且特别是在哺乳动物细胞中)高水平生产多肽的启动子应该是强的,并且优选在广泛的细胞类型中是有活性的。能够在许多细胞类型中驱动表达的强组成型启动子是本领域公知的,并因此在此不必详细描述它们。
2、启动子和/或增强子的实例是衍生自逆转录病毒ltr、巨细胞病毒(cmv)(例如cmv启动子/增强子)、猿猴病毒40(sv40)(例如sv40启动子/增强子)、腺病毒(例如腺病毒主要晚期启动子(admlp))、cag启动子以及强哺乳动物启动子(例如ttr启动子或ef1-α启动子)的启动子和/或增强子。
3、根据亚型,cmv启动子的长度为589-1650bp(changyu zheng et all.,all humanef1αpromoters are not equal:markedly affect gene expression in constructsfrom different sources,int j med sci.2014;11(5):404-408,doi:10.7150/ijms.8033)。cag启动子(cmv早期增强子/鸡β肌动蛋白)的长度为868bp(nieuwenhuis,b.,haenzi,b.,hilton,s.等人.optimization of adeno-associated viral vector-mediated transduction of the corticospinal tract:comparison of fourpromoters.gene ther.2021;28:56–74,https://doi.org/10.1038/s41434-020-0169-1)。
4、所有上述启动子的长度都超过588bp。表达盒中长度超过588bp的启动子不是使用多种表达载体表达大转基因的最佳选择。
5、因此,需要产生短启动子。
6、许多启动子(包括cmv启动子)不是组织特异性的,即,它们不提供治疗性转基因在某些器官的细胞中的选择性表达,当用于产生基因疗法产物时,这个事实是这些启动子的明显缺点。
7、因此,需要产生组织特异性启动子,其提供治疗性转基因在某些器官的细胞中的选择性表达。
技术实现思路
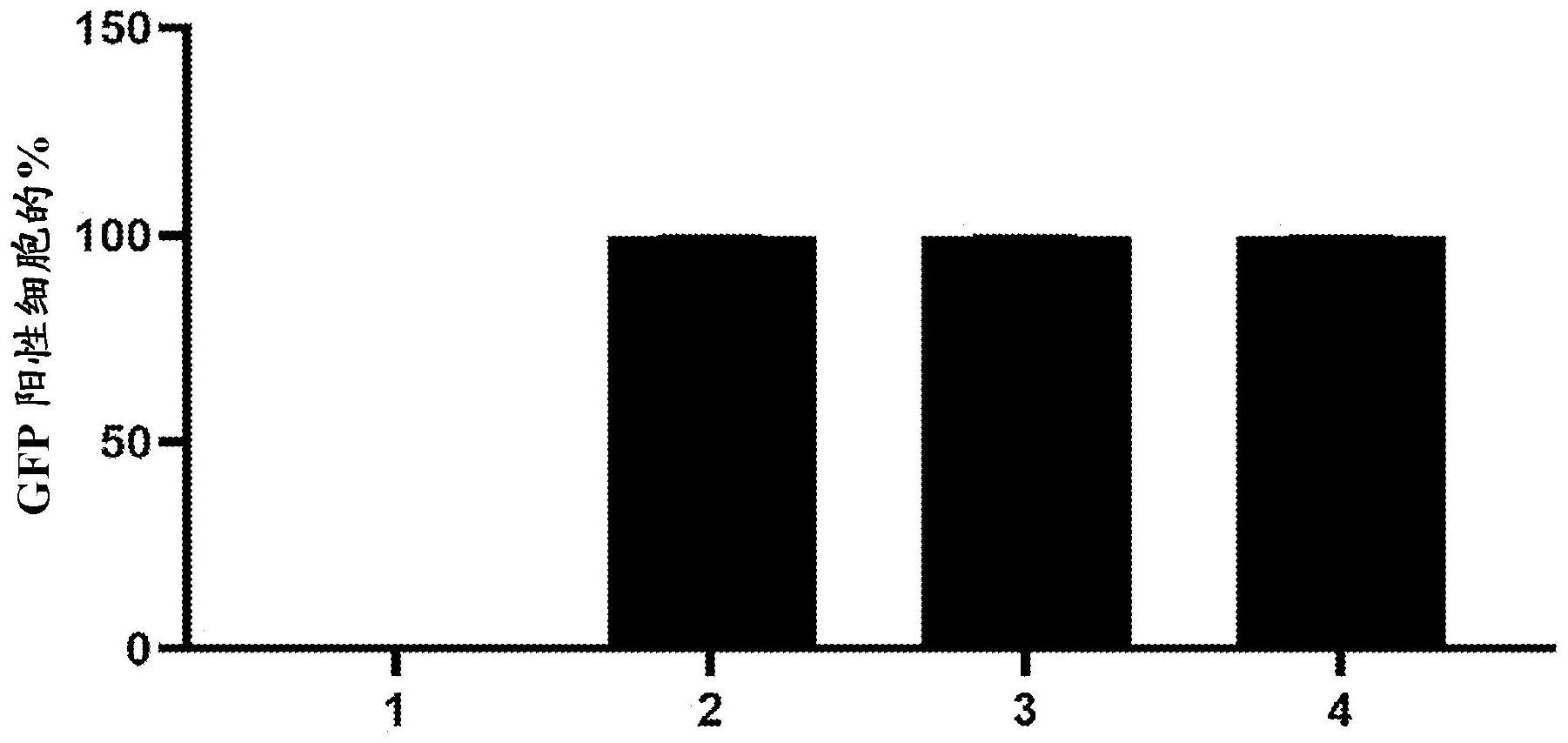
1、本发明的作者惊奇地发现具有选自seq id no:1、2、3、4、5、6、7、8、9、10、11、12、13、14或15的核苷酸序列的核酸具有启动子活性。具有seq id no:1、2、3、4、5、6、7、8、9、10、11、12、13、14或15的核苷酸序列的启动子的长度在123-252bp的范围内。此外,本发明的作者惊奇地发现具有seq id no:1、2、3、4、5、6、7、8、9、10、11、12、13、14或15的核苷酸序列的启动子在肝细胞来源的细胞中具有组织特异性启动子活性。
2、定义和一般方法
3、除非本文另有定义,否则与本发明结合使用的所有技术和科学术语将具有与本领域技术人员通常理解的相同的含义。
4、此外,除非上下文另有要求,否则单数术语应包括复数术语,并且复数术语应包括单数术语。通常,本文所述的细胞培养、分子生物学、免疫学、微生物学、遗传学、分析化学、有机合成化学、医学和药物化学以及蛋白质和核酸的杂交和化学的本分类和方法是本领域技术人员公知的并且广泛用于本领域。酶反应和纯化方法根据制造商的指导方针进行,如本领域常见的,或如本文所述。
5、如本说明书和所附权利要求书中所用,除非上下文另有规定,否则词语“包括(include)”和“包含(comprise)”或其变体(例如“包括(includes)”、“包括(including)”、“包含(comprises)”或“包含(comprising)”)将被理解为暗示包括所述的整体或整体组,但不排除任何其它整体或整体组。
6、核酸分子
7、术语“核酸”、“核酸序列(nucleic sequence)”、“核酸序列(nucleic acidsequence)”、“多核苷酸”、“寡核苷酸”、“多核苷酸序列”和“核苷酸序列”在本说明书中可互换使用,是指核苷酸的精确序列,其经修饰或未经修饰,确定核酸的片段或区,含有或不含非天然核苷酸,并且是双链dna或rna、单链dna或rna、或所述dna的转录产物。
8、如本说明书中所用,通过非限制性实例,多核苷酸包括通过本领域可找到的任何方法获得的所有核酸序列,作为非限制性实例,包括重组方法,即,使用普通克隆技术和pcr等从重组文库或细胞基因组克隆核酸序列,和通过合成方法。
9、本发明不涉及其天然染色体环境中(即天然状态下)的核苷酸序列,这也应包括在此。本发明的序列已经被分离和/或纯化,即,它们被直接或间接取样,例如通过复制,从而其环境已经至少部分地被修饰。因此,本文还应提及通过重组遗传学(例如使用宿主细胞)获得的或通过化学合成获得的分离的核酸。
10、除非另有指示,否则术语核苷酸序列包括其互补序列。因此,具有特定序列的核酸应理解为包括其互补链及其互补序列的核酸。
11、载体
12、如本文所用的术语“载体”是指能够转运与其连接的另一核酸的核酸分子。此外,术语“载体”在本文中是指能够转运核酸的重组病毒颗粒。
13、如本说明书中所用,术语“表达”定义为由其启动子驱动的特定核苷酸序列的转录和/或翻译。
技术特征:
1.具有启动子活性的核酸,其包含选自seq id no:1、2、3、4、5、6、7、8、9、10、11、12、13、14或15的核苷酸序列。
2.表达盒,其包含根据权利要求1所述的核酸分子和可操作地连接的转基因。
3.根据权利要求2所述的表达盒,其中所述转基因编码蛋白质或小抑制性核酸。
4.根据权利要求3所述的表达盒,其中所述转基因编码选自因子viii或其功能变体、因子ix或其功能变体、smn1蛋白(存活运动神经元蛋白)、sars-cov2的rbd-s多肽或治疗性抗体的蛋白质。
5.表达载体,其包含根据权利要求1所述的核酸或根据权利要求2-4中任一项所述的表达盒。
6.根据权利要求5所述的表达载体,其是质粒、aav、慢病毒或腺病毒。
7.根据权利要求6所述的表达载体,其是选自以下aav血清型的aav:aav1、aav2、aav3、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、aav12、aav13、aav14、aav15、aav16、raav.rh8、raav.rhlo、raav.rh20、raav.rh39、raav.rh74、raav.rhm4-l、aav.hu37、raav.anc80、raav.anc80l65、raav.7m8、raav.php.b、raav2.5、raav2.6、raav2.8、raav2.9、raav2tyf、raav3b、raav.lk03、aav.hsc1、aav.hsc2、aav.hsc3、aav.hsc4、aav.hsc5、aav.hsc6、aav.hsc7、aav.hsc8、aav.hsc9、aav.hsc10、aav.hsc11、aav.hsc12、aav.hsc13、aav.hsc14、aav.hsc15或aav.hsc16。
8.用于生产靶产物或根据权利要求5-7所述的表达载体的宿主细胞,其包含根据权利要求1所述的核酸或根据权利要求2-4中任一项所述的表达盒。
技术总结
本申请涉及遗传学、基因疗法和分子生物学领域。更具体地,本发明涉及具有启动子活性的核酸(变体)、基于其的表达盒和载体、用于生产靶产物或表达载体的宿主细胞。
技术研发人员:E·V·韦拉索瓦,A·N·斯特雷科娃,K·I·泰舒克,P·M·格什维奇,M·P·佩雷佩尔金纳,P·A·雅克列夫,D·V·莫洛佐夫
受保护的技术使用者:拜奥卡德联合股份公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!