一种重组人溶菌酶的纯化制备方法与流程
本公开涉及重组人溶菌酶纯化,具体涉及一种重组人溶菌酶的纯化制备方法。
背景技术:
1、人源溶菌酶属于c型溶菌酶,是一种由130个氨基酸组成的分子量约为14.7kda的单体蛋白,是一种能够溶解革兰氏阳性细菌细胞壁的酶,水解细菌中黏多糖的碱性酶。溶菌酶主要通过破坏细胞壁中的n-乙酰胞壁酸和n-乙酰氨基葡萄糖之间的β-1,4糖苷键,使细胞壁不溶性黏多糖分解成可溶性糖肽,导致细胞壁破裂内容物逸出而使细菌溶解。溶菌酶还可与带负电荷的病毒蛋白直接结合,与dna、rna、脱辅基蛋白形成复合体,使病毒失活。
2、溶菌酶是一种天然、安全性能良好的杀菌剂和防腐剂,具有抗菌、消炎、抗病毒等作用,可广泛应用于食品生物防腐、医药、日用化工等行业。构建重组人溶菌酶,可以大幅度提高溶菌酶活性,并且纯化得到的酶产物残留少,纯度高,具有环保、不受原料限制等优点。
3、然而目前依然缺少高效表达有活性的人溶菌酶的工程菌,商品化的重组人溶菌酶还很少。
4、需要说明的是,在上述背景技术部分公开的信息仅用于加强对本公开的背景的理解,因此可以包括不构成对本领域普通技术人员已知的现有技术的信息。
技术实现思路
1、本公开的目的在于提供一种重组人溶菌酶的纯化制备方法,进而至少在一定程度上克服由于相关技术的限制和缺陷而导致的目前依然缺少高效表达有活性的人溶菌酶的工程菌,商品化的重组人溶菌酶还很少的情况。
2、本公开的其他特性和优点将通过下面的详细描述变得显然,或部分地通过本公开的实践而习得。
3、本申请提供了一种重组人溶菌酶的纯化制备方法,包括:
4、人溶菌酶载体pet-28a(+)通过转化大肠杆菌感受态细胞转入大肠杆菌中,对大肠杆菌进行转化并诱导表达,得湿菌;
5、对所述湿菌进行裂解,得包涵体;
6、对所述包涵体进行复性、纯化,得重组人溶菌酶。
7、可选的,步骤对所述包涵体进行复性、纯化,得重组人溶菌酶包括:
8、对包涵体变性后进一步进行复性,得到复性液;
9、透析过液所述复性液,并将透析过液后的复性液进行离子交换层析纯化,得到纯度≥95%的重组人溶菌酶。
10、可选的,步骤透析过液所述复性液,并将透析过液后的复性液进行离子交换层析纯化中,采用洗涤缓冲液对复性液进行离子交换层析纯化;
11、所述洗涤缓冲液包括:20mm tris、2m尿素、0.15m氯化钠、20%蔗糖;洗涤缓冲液的ph=8.0~8.5。
12、可选的,按1:5(m:v)的比例向所述包涵体内加变性溶液,搅拌后取上清液,得变性液;
13、将所述变性液滴加至复性溶液中,使得复性溶液的浓度范围为:0.1-0.3mg/ml为止,得复性液;
14、对所述复性液进行多次透析,并对透析后的复性液进行阳离子交换纯化,得纯度≥99%的重组人溶菌酶。
15、可选的,所述变性溶液包括:20mm tris、8m尿素、10mm dtt;ph=8.0~8.5;
16、所述复性溶液包括:20mm tris、1m l-精氨酸、0.1mm gssg、1mm gsh;ph=8.0~8.5;
17、步骤对所述复性液进行多次透析中,使用透析缓冲液对复性液进行多次透析;所述透析缓冲液为20mm tris,ph=8.0~8.5。
18、可选的,步骤对透析后的复性液进行阳离子交换纯化包括:
19、采用离子交换缓冲液a平衡柱子,上样后清洗、离子交换缓冲液b洗脱、收集洗脱峰;其中,离子交换缓冲液a为20mm tris,ph=8.0~8.5;离子交换缓冲液b包括:20mmtris、1m氯化钠,ph=8.0~8.5。
20、可选的,所述方法还包括:
21、对所述重组人溶菌酶进行活性检测,将检测合格的重组人溶菌酶分装保存至-20℃的环境中。
22、可选的,所述活性检测的过程包括:
23、重组人溶菌酶置于25℃,0.1mol/l磷酸盐缓冲液(ph 6.2)中,以溶壁微球菌为底物,于450nm处每分钟使吸光度值下降0.001时所需的酶量;
24、活性单位为u/mg或u/g或u/ml。
25、可选的,步骤人溶菌酶载体pet-28a(+)通过转化大肠杆菌感受态细胞转入大肠杆菌中,对大肠杆菌进行转化并诱导表达,得湿菌包括:
26、构建人溶菌酶载体pet-28a(+);用碱裂解法制备质粒,
27、用氯化钙制备和转化感受态大肠杆菌,人溶菌酶载体pet-28a(+)通过转化大肠杆菌感受态细胞转入大肠杆菌中,对大肠杆菌进行转化;
28、对转化成功的大肠杆菌单克隆,并接种至终浓度为50ug/ml卡纳抗性的5ml试管中培养,培养条件为:37℃,200rpm培养16h;
29、培养成功的大肠杆菌用甘油保存;
30、按1%-2%的接种量接种甘油菌至500ml摇瓶中,37℃,200rpm培养至od600=0.6~0.8,加入1mm iptg在15℃诱导24h,12000rpm,4℃离心收获湿菌。
31、可选的,步骤对所述湿菌进行裂解,得包涵体包括:
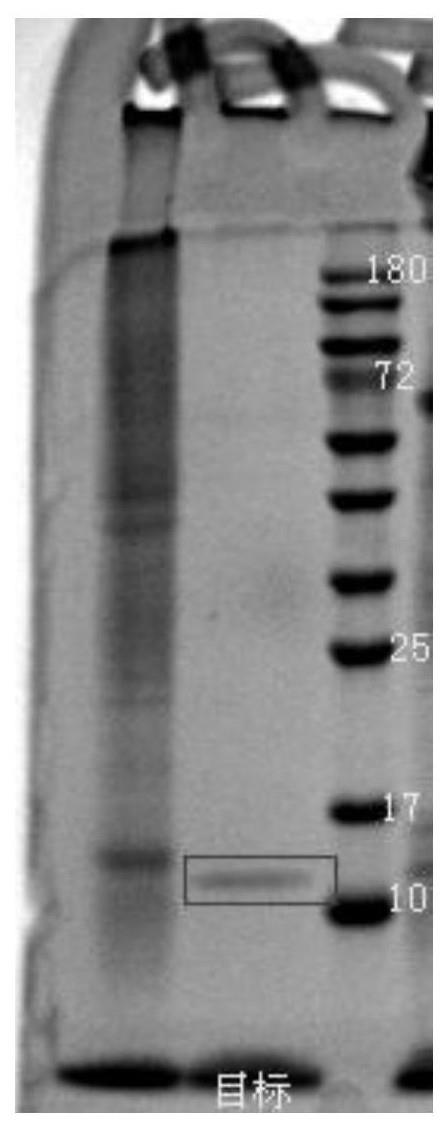
32、收获的湿菌利用sds-page电泳验证表达量,成功表达后,进一步用发酵罐发酵,收获湿菌备用;
33、收获的湿菌利用大肠杆菌裂解澄清试剂盒裂解后,12000rpm,4℃离心,弃去上清液,收获沉淀;
34、洗涤沉淀,获得包涵体。
35、本申请提供了一种重组人溶菌酶的纯化制备方法,包括:人溶菌酶载体pet-28a(+)通过转化大肠杆菌感受态细胞转入大肠杆菌中,对大肠杆菌进行转化并诱导表达,得湿菌;对所述湿菌进行裂解,得包涵体;对所述包涵体进行复性、纯化,得重组人溶菌酶。该工程菌株在大肠杆菌培养基中表达人溶菌酶,实现了人溶菌酶在大肠杆菌中的高效表达,后期再经过培养基及培养条件优化可实现人溶菌酶的高效连续生产,经变复性后,进一步纯化获得高活性人溶菌酶,比活≥200000u/mg,可在-20℃长期保存。可广泛应用于饲料、食品和医药等行业,具有良好的商业应用前景。
36、应当理解的是,以上的一般描述和后文的细节描述仅是示例性和解释性的,并不能限制本公开。
技术特征:
1.一种重组人溶菌酶的纯化制备方法,其特征在于,包括:
2.根据权利要求1所述的重组人溶菌酶的纯化制备方法,其特征在于,步骤对所述包涵体进行复性、纯化,得重组人溶菌酶包括:
3.根据权利要求2所述的重组人溶菌酶的纯化制备方法,其特征在于,步骤透析过液所述复性液,并将透析过液后的复性液进行离子交换层析纯化中,采用洗涤缓冲液对复性液进行离子交换层析纯化;
4.根据权利要求1所述的重组人溶菌酶的纯化制备方法,其特征在于,
5.根据权利要求4所述的重组人溶菌酶的纯化制备方法,其特征在于,
6.根据权利要求4所述的重组人溶菌酶的纯化制备方法,其特征在于,步骤对透析后的复性液进行阳离子交换纯化包括:
7.根据权利要求1所述的重组人溶菌酶的纯化制备方法,其特征在于,所述方法还包括:
8.根据权利要求7所述的重组人溶菌酶的纯化制备方法,其特征在于,所述活性检测的过程包括:
9.根据权利要求1所述的重组人溶菌酶的纯化制备方法,其特征在于,步骤人溶菌酶载体pet-28a(+)通过转化大肠杆菌感受态细胞转入大肠杆菌中,对大肠杆菌进行转化并诱导表达,得湿菌包括:
10.根据权利要求1所述的重组人溶菌酶的纯化制备方法,其特征在于,步骤对所述湿菌进行裂解,得包涵体包括:
技术总结
本申请提供了一种重组人溶菌酶的纯化制备方法,包括:人溶菌酶载体pET‑28a(+)通过转化大肠杆菌感受态细胞转入大肠杆菌中,对大肠杆菌进行转化并诱导表达,得湿菌;对所述湿菌进行裂解,得包涵体;对所述包涵体进行复性、纯化,得重组人溶菌酶。该工程菌株在大肠杆菌培养基中表达人溶菌酶,实现了人溶菌酶在大肠杆菌中的高效表达,后期再经过培养基及培养条件优化可实现人溶菌酶的高效连续生产,经变复性后,进一步纯化获得高活性人溶菌酶,比活≥200000U/mg,可在‑20℃长期保存。可广泛应用于饲料、食品和医药等行业,具有良好的商业应用前景。
技术研发人员:赵江峰,李艳霞,孟苗,张江凡,张彤彤,杨小静,窦当当,黄溶,龚世位
受保护的技术使用者:西安麦博泰克生物科技有限公司
技术研发日:
技术公布日:2024/1/16
- 还没有人留言评论。精彩留言会获得点赞!