一种合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法
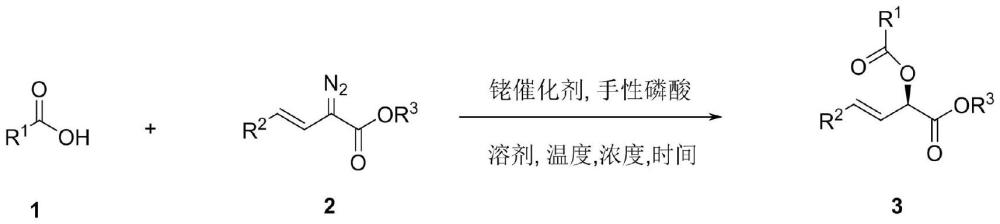
本发明属于不对称催化有机合成领域,具体涉及一种苯甲酸衍生物、α-酰氧基-β,γ-不饱和重氮乙酸酯衍生物的非对映和对映选择性合成α-酰氧基-β,γ-不饱和酯及其衍生物反应。
背景技术:
1、α-酰氧基-β,γ-不饱和羧酸及其衍生物广泛存在于天然产物和生物活性分子中。该结构包含一个烯丙醇基团和一个α-羟基羰基基团,这两个基序在合成化学中分别作为烯丙基化试剂和α-羟基羧酸的前体具有重要意义。
2、前期有几种不对称合成α-酰氧基-β,γ-不饱和酯的方法。早期的报道主要是酶催化,包括β,γ-不饱和α-酮酯的不对称还原(casy,g.,lee,t.v.,lovell,h.,etal,j.chem.soc.chem.commun.,1992,924.)和前手性α-二取代丙二酸衍生物的脱羧(larissegger-schnell,b.,kroutil,w.,faber,k.,synlett,2005,1936)。feng实现了通过路易斯酸催化β,γ-不饱和α-酮酯的不对称烯丙基化以提供α-羟基-β,γ-不饱和酯(tang,q.,fu,k.,ruan,p.,dong,s.,su,z.,liu,x.,feng,x.,angew.chem.int.ed.,2019,58,11846)。最近,liu及其同事报道了不对称rh/胍催化α-酰氧基-β,γ-不饱和重氮酯与羧酸的o-h插入反应(tan,f.,x.liu,hao,x.,tang,y.,lin,l.,feng,x.,acscatal.,2016,6,6930.)。
3、我们采用rh/手性磷酸催化α-酰氧基-β,γ-不饱和重氮酯与羧酸的o-h插入。反应操作简单、原料简单易得、反应条件温和、底物适用范围广、效率高、非对映和对映选择性好。
技术实现思路
1、本发明公开了一种α-酰氧基-β,γ-不饱和重氮酯衍生物作为卡宾前体与苯甲酸衍生物的高立体选择性合成光学纯α-酰氧基-β,γ-不饱和酯及其衍生物反应。
2、本发明具体的反应通式如下:
3、
4、其中:
5、r1为c6h5,4-mec6h4,4-tbuc6h4,4-fc6h4,4-cf3c6h4,4-vinylc6h4,3-mec6h4,3-clc6h4,2-mec6h4,2-fc6h4,2-萘基,环己基,环戊基,甲基;
6、r2为c6h5,4-mec6h4,4-tbuc6h4,4-cnc6h4,3-mec6h4,3-clc6h4,2-mec6h4,2-fc6h4,2-clc6h4,2-brc6h4,me,n-butyl;
7、r3为me,et,ipr,tbu。
8、一种重氮卡宾化学选择性和对映选择性插入苯甲酸衍生物的方法,具体为:向干燥的反应管中加入铑催化剂、手性配体、苯甲酸衍生物加一定量溶剂室温搅拌均匀,然后用注射器将α-酰氧基-β,γ-不饱和重氮乙酸酯衍生物溶于一定量溶剂并且滴加入反应液中,一定温度下搅拌反应,反应液通过柱层色谱分离得到手性α-酰氧基-β,γ-不饱和酯及其衍生物。
9、使用的手性配体为如下所示:
10、
11、其中,最优手性配体为cpa1。
12、苯甲酸衍生物具体结构式如下:
13、
14、α-酰氧基-β,γ-不饱和重氮乙酸甲酯衍生物结构式如下:
15、
16、反应的溶剂为:二氯甲烷、二氯乙烷、甲苯、三氯甲烷、正戊烷等,其中,最优的溶剂为正戊烷。
17、反应催化剂为:rh2(esp)4、rh2(pttl)4、rh2(oct)4、rh2(tfa)4,优选rh2(tfa)4。
18、反应中铑催化剂、手性配体、苯甲酸衍生物、α-酰氧基-β,γ-不饱和重氮乙酸甲酯衍生物的摩尔比为:0.002~0.004:0.010~0.020:0.2:0.2~0.4,最优的摩尔比为:0.004:0.01:0.2:0.4。
19、苯甲酸衍生物为1当量时,反应液浓度为:0.025~0.10mol/l,最佳浓度为0.05mol/l。
20、反应温度为:0-35℃,反应时间为3-15min;反应的最佳温度为室温25℃。
21、有益效果和优点
22、本发明设计了一种重氮卡宾化学选择性和对映选择性插入苯甲酸衍生物的方法,高选择性合成手性α-酰氧基-β,γ-不饱和酯及其衍生物。为合成具有良好立体选择性的含一个立体中心的高取代α-酰氧基-β,γ-不饱和酯化合物,提供了一条简单的途径。
23、本发明方法的优点有:反应操作简单、条件温和、原料简单易得、底物适用范围广、效率高、非对映和对映选择性好。
技术特征:
1.一种合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于:向反应容器中加入铑催化剂和手性磷酸,加入溶剂,在室温搅拌,然后加入苯甲酸衍生物、α-酰氧基-β,γ-不饱和重氮乙酸酯衍生物,在氩气保护下进行搅拌反应,通过柱层色谱分离得到手性α-酰氧基-β,γ-不饱和酯及其衍生物;
2.根据权利要求1所述合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于:所述铑催化剂为:rh2(esp)4、rh2(pttl)4、rh2(oct)4、rh2(tfa)4中的一种;
3.根据权利要求1所述合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于,所述手性配体为以下一种:
4.根据权利要求1所述合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于,所述铑催化剂、手性磷酸、苯甲酸衍生物、α-酰氧基-β,γ-不饱和重氮乙酸甲酯衍生物的摩尔比为:0.002~0.004:0.010~0.020:0.2:0.2~0.4。
5.根据权利要求1所述合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于,苯甲酸衍生物具体结构式如下:
6.根据权利要求1所述合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于,α-酰氧基-β,γ-不饱和重氮乙酸甲酯衍生物结构式如下:
7.根据权利要求1所述合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于,所述溶剂为:二氯甲烷、二氯乙烷、甲苯、三氯甲烷、正戊烷中的一种。
8.根据权利要求1所述合成α-酰氧基-β,γ-不饱和酯及其衍生物的方法,其特征在于,苯甲酸衍生物为1当量时,反应液浓度为:0.025~0.10mol/l;反应温度为0~35℃;反应时间为3~15min。
技术总结
本发明属于不对称催化合成领域,具体公开了一种合成α‑酰氧基‑β,γ‑不饱和酯及其衍生物的方法,本发明采用铑催化的苯甲酸衍生物与α‑酰氧基‑β,γ‑不饱和重氮乙酸酯衍生物的非对映和对映选择性合成α‑酰氧基‑β,γ‑不饱和酯及其衍生物的方法,高立体选择性得到了光学纯的α‑酰氧基‑β,γ‑不饱和酯及其衍生物,本发明方法的优点有:反应操作简单、原料简单易得、反应条件温和、底物适用范围广、效率高、非对映和对映选择性好。
技术研发人员:邵莺,陈佳魏,孙江涛,唐生表
受保护的技术使用者:常州大学
技术研发日:
技术公布日:2024/2/19
- 还没有人留言评论。精彩留言会获得点赞!