β-咔啉-沙利度胺偶联物及其在制备逆转ABT-199耐药的药物中的应用
本发明属于医药合成,特别涉及β-咔啉-沙利度胺偶联物及其在制备逆转abt-199耐药的药物中的应用。
背景技术:
1、bcl-2家族抗凋亡蛋白(bcl-2,bcl-xl,mcl-1等)是一类重要的凋亡靶点,它们通过与促凋亡蛋白发生蛋白-蛋白相互作用调控线粒体凋亡通路。其中bcl-2蛋白是该家族最早发现的肿瘤靶点,研究人员针对该靶点开发了多种小分子抑制剂。其中abt-199是一种强效选择性bcl-2抑制剂,它对bcl-2的亲和力高达0.01nm,并且对bcl-xl和bcl-w亲和力较低。abt-199能够选择性地杀死bcl-2依赖性肿瘤细胞rs4;11。在动物实验中,abt-199能够完全抑制bcl-2依赖性肿瘤的生长,且不杀死血小板细胞。由于其良好的活性和安全性,abt-199于2016年获得fda批准用于肿瘤治疗。
2、然而研究发现,abt-199在研究中被发现存在耐药问题,表现两个方面:(1)abt-199仅对bcl-2依赖性的肿瘤细胞有效,对其他多种类型的肿瘤细胞自发耐药;(2)临床研究显示abt-199平均给药2.5个月后会出现肿瘤复发。因此急需解决abt-199耐药问题。
3、目前,尚未见关于化合物具体为β-咔啉-沙利度胺偶联物在制备abt-199耐药的药物方面的报道。
技术实现思路
1、针对背景技术中存在的技术问题,本发明的目的在于提供了β-咔啉-沙利度胺偶联物及其在制备逆转abt-199耐药的药物中的应用。该化合物具有较强的协同抗肿瘤活性,能够与abt-199联合用药杀死耐药肿瘤细胞,可应用于逆转abt-199耐药的药物制备中。
2、为了实现上述目的,本发明采用如下技术方案:
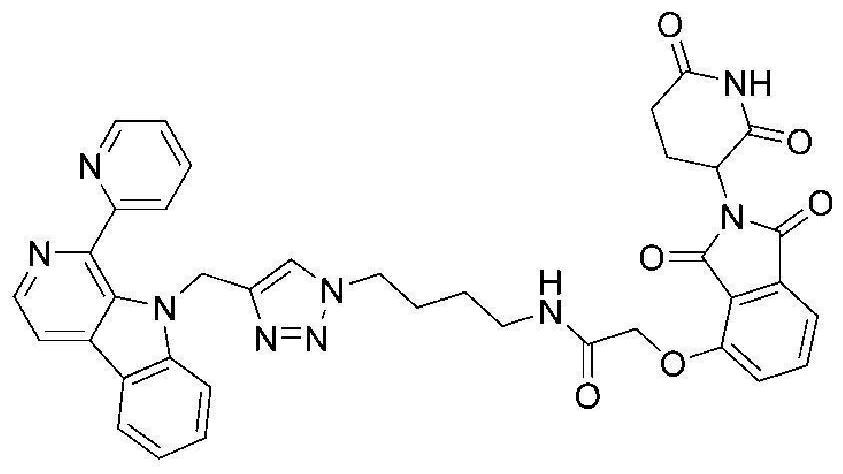
3、本发明的第一方面提供了β-咔啉-沙利度胺偶联物,所述β-咔啉-沙利度胺偶联物的分子式为c38h33n9o6,分子量为711.26,结构式如式i所示:
4、
5、本发明的第二方面提供了上述β-咔啉-沙利度胺偶联物通过首先将1-吡啶-β-咔啉和3-溴丙炔进行烷基化反应得到9-丙炔-1-吡啶-β-咔啉,然后将9-丙炔-1-吡啶-β-咔啉和沙利度胺的叠氮衍生物进行click反应制备而得。其制备方法,包括以下步骤:
6、s1、将1-吡啶-β-咔啉、强碱性物质和3-溴丙炔溶于有机溶剂中,在保护性气体下进行烷基化反应,纯化,得到9-丙炔-1-吡啶-β-咔啉;
7、s2、将所得9-丙炔-1-吡啶-β-咔啉和沙利度胺的叠氮衍生物溶于溶剂中,在硫酸铜和抗坏血酸钠作用下进行click反应,纯化,得到β-咔啉-沙利度胺偶联物。
8、优选的,步骤s1中,所述1-吡啶-β-咔啉、3-溴丙炔、强碱性物质的物质的量之比为1:1~10:1~10。
9、优选的,步骤s1中,所述强碱性物质为nah、k2co3、naoh或者cs2co3中的任意一种。
10、优选的,步骤s1中,所述有机溶剂与1-吡啶-β-咔啉的用量配比为1~100ml:10mmol;
11、优选的,步骤s1中,所述有机溶剂为dmf、dma、dmso和thf中的一种或两种以上的组合。
12、优选的,步骤s1中,所述烷基化反应在室温下进行,反应时间为4~8h。
13、优选的,步骤s2中,所述9-丙炔-1-吡啶-β-咔啉、沙利度胺的叠氮衍生物、硫酸铜、抗坏血酸钠的物质的量之比为10:10~15:2~6:5~8。
14、优选的,步骤s2中,所述click反应在室温下进行,反应时间为10~20h。
15、优选的,步骤s2中,所述溶剂为有机溶剂与水的混合溶剂,所述溶剂为叔丁醇、甲醇、乙醇、dmf中的任意一种,进一步优选为叔丁醇。
16、优选的,步骤s1中,所述纯化采用硅胶柱层析进行,所用的洗脱剂为二氯甲烷、乙酸乙酯和氯仿中的任意一种与石油醚组成的混合溶剂,且混合溶剂的组成中,所述石油醚与二氯甲烷、乙酸乙酯和氯仿中的任意一种的体积之比为10~1:1~10。
17、优选的,步骤s2中,所述纯化采用硅胶柱层析进行,所用的洗脱剂为二氯甲烷、乙酸乙酯和氯仿中的任意一种与甲醇组成的混合溶剂,且混合溶剂的组成中,所述甲醇与二氯甲烷、乙酸乙酯和氯仿中的任意一种的体积之比为10~1:1~20。
18、本发明的第三方面提供了上述β-咔啉-沙利度胺偶联物在制备抗肿瘤药物中的应用。
19、本发明的第四方面提供了上述β-咔啉-沙利度胺偶联物在制备逆转abt-199耐药的药物中的应用。
20、本发明的第五方面提供了一种药物组合物,其含有治疗上有效剂量的上述β-咔啉-沙利度胺偶联物以及药学上可接受的载体。
21、本发明具备如下有益效果:
22、本发明通过两步反应制备了β-咔啉-沙利度胺偶联物:首先将1-吡啶-β-咔啉和3-溴丙炔进行烷基化反应,得到9-丙炔-1-吡啶-β-咔啉;然后将9-丙炔-1-吡啶-β-咔啉和沙利度胺的叠氮衍生物在催化剂(硫酸铜和抗坏血酸钠)作用下进行click反应,制得β-咔啉-沙利度胺偶联物,具体为2-(2-(2,6-二氧-3-哌啶)-1,3-二氧异吲哚-4-)-氮-(4-(4-((1-(吡啶-2-)-9h-吡啶[3,4-b]吲哚-9-)甲基)-1h-1,2,3-三唑-1-)丁基)乙酰胺。并考察了其对abt-199耐药的影响,实验结果表明,本发明制备的β-咔啉-沙利度胺偶联物具有较强的逆转abt-199耐药的活性,有望应用于各种抗肿瘤或逆转abt-199耐药的药物制备方案中。
23、(2)本发明制备方法合成工艺简单、易于操作、成本低廉,适于推广。
技术特征:
1.一种β-咔啉-沙利度胺偶联物,其特征在于,所述β-咔啉-沙利度胺偶联物的分子式为c38h33n9o6,分子量为711.26,其结构式如式i所示:
2.一种如权利要求1所述的β-咔啉-沙利度胺偶联物的制备方法,其特征在于,包括以下步骤:
3.根据权利要求2所述的β-咔啉-沙利度胺偶联物的制备方法,其特征在于,步骤s1中,所述1-吡啶-β-咔啉、3-溴丙炔和强碱性物质的物质的量之比为1:1~10:1~10;所述强碱性物质为nah、k2co3、naoh或者cs2co3中的任意一种。
4.根据权利要求2所述的β-咔啉-沙利度胺偶联物的制备方法,其特征在于,步骤s1中,所述有机溶剂与1-吡啶-β-咔啉的用量配比为1~100ml:10mmol;所述有机溶剂为dmf、dma、dmso和thf中的一种或两种以上的组合。
5.根据权利要求2所述的β-咔啉-沙利度胺偶联物的制备方法,其特征在于,步骤s1中,所述烷基化反应在室温下进行,反应时间为4~8h;所述click反应在室温下进行,反应时间为10~20h。
6.根据权利要求2所述的β-咔啉-沙利度胺偶联物的制备方法,其特征在于,步骤s2中,所述9-丙炔-1-吡啶-β-咔啉、沙利度胺的叠氮衍生物、硫酸铜、抗坏血酸钠的物质的量之比为10:10~15:2~6:5~8。
7.根据权利要求2所述的β-咔啉-沙利度胺偶联物的制备方法,其特征在于,步骤s2中,所述溶剂为有机溶剂与水的混合溶剂,所述溶剂为叔丁醇、甲醇、乙醇、dmf中的任意一种。
8.如权利要求1所述的β-咔啉-沙利度胺偶联物在制备抗肿瘤药物中的应用。
9.如权利要求1所述的β-咔啉-沙利度胺偶联物在制备逆转abt-199耐药的药物中的应用。
10.一种药物组合物,其特征在于,含有如权利要求1所述的β-咔啉-沙利度胺偶联物以及药学上可接受的载体。
技术总结
本发明公开了β‑咔啉‑沙利度胺偶联物及其在制备逆转ABT‑199耐药的药物中的应用,β‑咔啉‑沙利度胺偶联物的分子式为C<subgt;38</subgt;H<subgt;33</subgt;N<subgt;9</subgt;O<subgt;6</subgt;,分子量为711.26,具体为2‑(2‑(2,6‑二氧‑3‑哌啶)‑1,3‑二氧异吲哚‑4‑)‑氮‑(4‑(4‑((1‑(吡啶‑2‑)‑9H‑吡啶[3,4‑b]吲哚‑9‑)甲基)‑1H‑1,2,3‑三唑‑1‑)丁基)乙酰胺。该化合物通过首先将1‑吡啶‑β‑咔啉和3‑溴丙炔进行烷基化反应得到9‑丙炔‑1‑吡啶‑β‑咔啉;然后将9‑丙炔‑1‑吡啶‑β‑咔啉和沙利度胺的叠氮衍生物进行Click反应制备而得。实验结果表明,该化合物具有较强的逆转ABT‑199耐药的活性,有望应用于各种抗肿瘤或逆转耐药的药物制备方案中,本发明制备方法合成工艺简单、易于操作、成本低廉,适于推广。
技术研发人员:卢幸,邬慧贤,谢文彬,喻宇慧
受保护的技术使用者:桂林医学院附属医院
技术研发日:
技术公布日:2024/2/8
- 还没有人留言评论。精彩留言会获得点赞!