一种多功能模拟酶复合球的制备方法及其应用与流程
本发明属于酶催化与环境毒物催化降解技术领域,涉及一种多功能模拟酶复合球的制备方法及其应用。
背景技术:
酶是重要的生物催化剂,具有专一性强、催化效率高、无污染等优良性能。绝大多数酶是大分子蛋白质,必须在温和适宜的条件下才能发挥催化作用,在高温、高离子浓度、强酸、强碱及部分有机溶剂中均不稳定,容易变性失活而降低其催化性能。为了解决这些问题,研究工作者们尝试对天然酶进行修饰形成模拟酶以改良其催化性能。模拟酶是一类人工合成的非蛋白结构但是却与天然酶具有相类似的催化活性的催化剂。并且,固定化修饰的酶稳定性有所增加,有一定的形状和机械强度,可以装填在反应器中长期使用,便于实现生产自动化和连续化。常见的酶的固定化有吸附、包埋、结合和交联等方式。其中,包埋固定化法是近年来发展迅速的一种新兴固定化技术,是把酶固定在聚合物材料的格子结构或微囊结构等多空载体中,而底物仍能渗入格子或微囊内与酶相接触,并使其保持活性且能反复利用。常用的包埋固定化载体有琼脂、明胶、海藻酸钠(sa)、聚乙烯醇和丙烯酰胺。其中,海藻酸钠是一种线性天然生物大分子多糖类,在单元糖环上具有羧基和羟基等功能基团,温和条件下可与二价阳离子(如ca2+、zn2+)形成凝胶,并且由于海藻酸可生物降解、生物相容性和黏附性好而广泛应用。药学中利用海藻酸钠的成膜性制备微囊,利用其溶解度特性、凝胶和聚电解质作为缓释制剂的载体、包埋剂或生物粘附剂等。
血红素(hemin)作为辣根过氧化物酶(hrp)等血红素类蛋白质的催化活性中心,是由二价铁离子镶嵌在原卟啉环中构成的一种小分子铁卟啉化合物,能够催化h2o2氧化底物反应产生颜色变化,表现出类过氧化物酶的活性。然而,血红素本身催化活性低且不溶于水,在水溶液中易聚集成活性很低的二聚体,在氧化性媒介中结构易被破坏而致催化活性减弱。为了解决这些问题,研究工作者们尝试对血红素进行化学修饰以改良其催化性能。近年来,随着纳米技术的高速发展,贵金属纳米材料(如纳米金)由于粒径小、表面活性高和比表面积大而被广泛用作催化剂。目前,对金纳米颗粒的类过氧化物酶催化性能的研究已显成熟,特别是,采用纳米金颗粒修饰过氧化物酶以提高其催化性能的研究已被广泛报道,一些经过生物矿化生成的小尺寸(小于5nm)金纳米颗粒不仅本身具有一定的过氧化物酶活性,而且可接近或深入被修饰的过氧化物酶的催化活性中心,极大地发挥其纳米导线功能,促进酶催化反应的电子传输能力。
与此同时,磁性四氧化三铁(fe3o4)纳米材料因具有量子尺寸、小尺寸、表面和宏观量子隧道效应,以及独特的磁性可回收利用性质,在现代社会越来越受到人们的关注,在物质分离、催化及环境毒物降解领域发挥极大作用。而且这些纳米材料制备简单、廉价、稳定性高,且具有抗变形性和可回收利用性,在酶催化降解应用中比天然酶更具有优势。另外,球形石墨烯(sg)因具有优良的机械性质、特殊的单原子层平面二维结构和超高的比表面积,广泛用于结合一些纳米材料形成复合催化剂,提高对污染物的吸附能力。
技术实现要素:
本发明通过模拟天然酶的催化原理,提供一种多功能模拟酶复合球的制备方法,制备出一种具有显著酶催化活性和高吸附降解性的磁性模拟酶复合球(sa-hemin-au-sg-fe3o4)。具有催化活性高、稳定性好、可回收利用等优点。
同时,本发明还提供了上述多功能模拟酶复合球的应用,将该模拟酶复合球用于一些环境有机毒物,如苯酚(ph)、亚甲基蓝(mb)和罗丹明b(rb)等的快速催化、吸附降解。
本发明的技术方案如下:
一种多功能模拟酶复合球的制备方法,在碱性条件下,以血红素(hemin)为还原剂和稳定剂,与氯金酸(haucl4)混合后矿化反应,形成具有高催化活性的金纳米簇模拟酶(hemin-au),再与球形石墨烯(sg)和四氧化三铁(fe3o4)混合反应后,加入海藻酸钠(sa)与钙离子进行包埋处理,得到多功能模拟酶复合球(sa-hemin-au-sg-fe3o4)。
上述一种多功能模拟酶复合球的制备方法,步骤包括:
1)室温条件下,将fecl3·6h2o溶解于乙二醇中,溶解浓度0.157~0.252m,搅拌,待完全溶解后加入乙酸钠,乙酸溶解浓度0.763~0.851m,继续搅拌30min后,转移到高压釜中,调节温度为200℃,反应8h,然后冷却至室温,用磁铁分离,收集磁铁吸附的固体,用水和乙醇洗涤,在60℃下烘干12h,得到中空纳米球fe3o4,备用;
2)室温条件下,将血红素溶解于0.01m的naoh水溶液中,配制浓度为0.25~2.0mg/ml的血红素溶液,然后将血红素溶液与10.0mm的氯金酸水溶液等体积混合,搅拌下缓慢滴加1.0m的naoh水溶液,调节溶液ph为10.0,37℃水浴反应8h,随后加入球形石墨烯,加入浓度为2.5~7.5mg/ml,加入步骤1)制得的中空纳米球fe3o4,加入浓度为7.5~37.5mg/ml,0~65℃搅拌反应6.0~18h,制得hemin-au-sg-fe3o4复合物;
3)将步骤2)制得的hemin-au-sg-fe3o4复合物加入到0.5~4.5wt%的海藻酸钠水溶液(5.0ml)中,分散浓度以血红素浓度计算为0.025~0.2mg/ml,超声30min混合均匀后,吸取溶液,滴入到1.0~5.5wt%的氯化钙水溶液中,形成圆形小颗粒,然后静置1.5h使其固定化,再用超纯水洗涤,低温干燥,得到sa-hemin-au-sg-fe3o4磁性模拟酶复合球,即多功能模拟酶复合球。
进一步地,步骤1)中,fecl3·6h2o溶解于乙二醇中,溶解浓度优选0.183m;乙酸溶解浓度优选0.804m。
进一步地,步骤2)中,血红素溶液浓度优选为1.0mg/ml,球形石墨烯加入浓度优选5mg/ml、中空纳米球fe3o4加入浓度优选25mg/ml。
进一步地,步骤2)中,优选37℃搅拌反应12h。
进一步地,步骤3)中,海藻酸钠水溶液浓度优选2.0wt%。
进一步地,步骤3)中,优选用1.0ml的注射器吸取溶液,以每秒一滴的速度滴入到20.0ml的氯化钙水溶液中;所述的氯化钙水溶液浓度优选3.0wt%。
所述的制备方法中,室温为20~25℃。
本发明所述多功能模拟酶复合球,适用于催化降解环境有机毒物,尤其适用于苯酚(ph)、亚甲基蓝(mb)和罗丹明b(rb)等的快速催化、吸附降解。
所述多功能模拟酶复合球在催化降解环境有机毒物的应用,方法为:将多功能模拟酶复合球直接加入到含有环境有机毒物的水溶液中,震荡反应0.5~2h。
进一步地,多功能模拟酶复合球加入浓度优选5mg/ml;光照条件下震荡反应优选1h。
本发明功能模拟酶复合球制备方法,通过模拟天然酶的催化原理,首先在碱性条件下以hemin作为还原剂和稳定剂,将氯金酸(haucl4)矿化形成具有高催化活性的金纳米簇模拟酶(hemin-au),然后将该模拟酶与sg和fe3o4“一锅式”混合反应,形成hemin-au-sg-fe3o4中间体复合物,进而通过安全、环保以及工艺优良的天然高分子材料sa包埋,原位合成催化活性高、稳定性好、可回收利用的磁性模拟酶复合球(sa-hemin-au-sg-fe3o4)。并对其中hemin-au复合物的形貌进行透射电镜(tem,图1)表征。然后,利用光度分析法一方面研究了该磁性模拟酶复合球的制备条件,另一方面研究了该复合物的类过氧化物酶催化活性;研究表明,该复合材料一方面由于sg和fe3o4具有巨大的表面积和内部空腔,会吸附小颗粒分子在其表面上,另一方面由于hemin、sg、fe3o4分子均具有六元环结构,容易形成π-π共轭效应,使它们之间的联系更加紧密,加速电子的传递和转移,从而提高了模拟酶的催化活性,可用于一些环境有机毒物如苯酚(ph)以及染料如亚甲基蓝(mb)和罗丹明b(rhb)的快速催化、吸附降解中。
本发明与现有的模拟酶复合球相比,其主要优势包括:
1)以hemin作为还原剂和稳定剂,实现金的原位生物矿化,形成具有显著酶催化功能的hemin-au复合物,不涉及复杂光电仪器使用,具有操作简单、成本低廉等优点;
2)sg特殊的单原子层平面二维结构和超高的比表面积,吸附连接丰富的hemin-au复合物在其表面,显著增强单位体积内酶分子的个数,从而增强复合物催化性能;
3)hemin、sg、fe3o4分子均具有六元环结构,容易形成π-π共轭结构,使它们之间的联系更加紧密,加速电子的传递和转移,另外,sg、fe3o4本身具有一些类过氧化物酶活性,与hemin-au结合后,使得整体活性增强;
4)选用sa包覆,一方面sa具有丰富的羧基和羟基等功能基团,易与hemin中的羧基结合实现酶的固定化包埋;另一方面,sa可生物降解、生物相容性和黏附性好,不仅环境无毒,而且可以很好的黏附在磁性颗粒表面;另外,fe3o4具有磁性,可回收利用,回收操作简便快捷,使其更广泛的应用于不同领域、不同环境中。
附图说明
图1(a)hemin-au复合物的透射电镜tem表征;(b)hemin-au复合物紫外表征图;
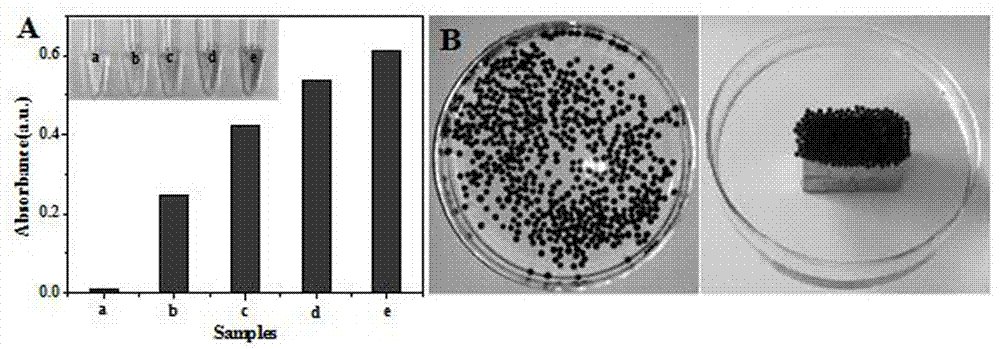
图2(a)(a)sa,(b)hemin,(c)hemin-au,(d)hemin-au-sg和(e)hemin-au-sg-fe3o4催化活性比较(插图为反应产物颜色的比较);(b)海藻酸钠固定化的磁性模拟酶实物图;
图3合成sa-hemin-au-sg-fe3o4颗粒的主要条件的优化,(a)naoh用量的优化,(b)合成时间的优化,(c)sa的用量的优化和(d)cacl2的用量的优化颗粒与tmb-h2o2显色反应是温度条件的优化;
图4sa-hemin-au-sg-fe3o4颗粒与tmb-h2o2显色反应条件的考察,(a)ph条件的考察,(b)反应温度的考察;
图5sa-hemin-au-sg-fe3o4颗粒(a)储存稳定性和(b)催化活性的考察;
图6以(a)sa球为对照,sa-hemin-au-sg-fe3o4球在(b)黑暗,(c)室内,(d)太阳光下分别催化降解亚甲基蓝时(a)亚甲基蓝的吸光度随着时间变化的曲线和(b)染料催化降解率;
图7以(a)sa球为对照,sa-hemin-au-sg-fe3o4球在(b)黑暗,(c)室内,(d)太阳光下分别催化降解罗丹明b时(a)罗丹明b的吸光度随着时间变化的曲线和(b)染料催化降解率;
图8以(a)sa球为对照,sa-hemin-au-sg-fe3o4球在(b)黑暗,(c)室内,(d)太阳光下分别催化降解苯酚时(a)苯酚的吸光度随着时间变化的曲线和(b)有机毒物催化降解率。
具体实施方式
下面通过实施例进一步的描述本发明技术方案。这些描述并不是对本发明内容作进一步的限定。凡对本发明内容所作的等同替换,或相应的改进,仍属于本发明的保护范围之内。
下述实施例中:氯化血红素,纯度为98%;氯金酸,含金量≥47.8%;海藻酸钠、氯化钙、氢氧化钠,30%过氧化氢、苯酚、亚甲基蓝和罗丹明b均为分析纯;
若无特别说明,室温为20~25℃;溶液均由二次去离子水配制。
实施例1
一种多功能模拟酶复合球的制备方法,各原料的配比如下:
haucl4:10.0mm,1.0ml
hemin:0.25mgml-1,1.0ml
naoh:1.0m,105μl
sg:5.0mg
sa:0.5wt%,1.0ml
fe3o4:15.0mg
cacl2:1.0wt%,20.0ml
其步骤为:
1)室温条件下,将fecl3·6h2o(1.73g)溶解于乙二醇(35ml)中,溶解浓度0.183m,磁力搅拌,待完全溶解后加入3.83g乙酸钠,乙酸钠在溶液中0.804m,继续搅拌30min后转移到高压釜中,调节温度为200℃,反应8h,然后冷却至室温,用磁铁分离,收集磁铁吸附的固体,用水和乙醇洗涤,在60℃下烘干12h,得到中空纳米球fe3o4,备用;
2)室温条件下,将血红素溶解于0.01m的naoh水溶液中,配制浓度为0.25mg/ml的血红素溶液,然后将血红素溶液与1.0ml、10.0mm的氯金酸水溶液等体积混合,磁力搅拌下缓慢滴加105μl、1.0m的naoh水溶液,调节溶液ph为10.0,37℃水浴反应8h,随后加入5.0mg球形石墨烯,15.0mg步骤1)制得的中空纳米球fe3o4,0℃一锅式搅拌反应6.0h,制得hemin-au-sg-fe3o4复合物;
3)将步骤2)制得的hemin-au-sg-fe3o4复合物加入0.5wt%的海藻酸钠水溶液5.0ml中(分散浓度以血红素浓度计算为0.025~0.2mg/ml),超声30min混合均匀后,用1.0ml的注射器吸取溶液,将其以每秒一滴的速度滴入到20.0ml、1.0wt%的氯化钙水溶液中,滴入后会立刻形成圆形小颗粒,然后静置1.5h使其固定化,再用超纯水洗涤,低温干燥,得到sa-hemin-au-sg-fe3o4磁性模拟酶复合球,即多功能模拟酶复合球。
实施例2
一种多功能模拟酶复合球的制备方法,各原料的配比如下:
haucl4:10mm,1.0ml
hemin:0.60mgml-1,1.0ml
naoh:1.0m,115μl
sg:10.0mg
sa:1.0wt%,1.0ml
fe3o4:25mg
cacl2:1.5wt%,20ml
其步骤为:
1)室温条件下,将fecl3·6h2o(1.73g)溶解于乙二醇(35ml)中,溶解浓度0.183m,磁力搅拌,待完全溶解后加入3.83g乙酸钠,乙酸钠在溶液中0.804m,继续搅拌30min后转移到高压釜中,调节温度为200℃,反应8h,然后冷却至室温,用磁铁分离,收集磁铁吸附的固体,用水和乙醇洗涤,在60℃下烘干12h,得到中空纳米球fe3o4,备用;
2)室温条件下,将血红素溶解于0.01m的naoh水溶液中,配制浓度为0.60mg/ml的血红素溶液,然后将血红素溶液与1.0ml、10.0mm的氯金酸水溶液等体积混合,磁力搅拌下缓慢滴加115μl、1.0m的naoh水溶液,调节溶液ph为10.0,37℃水浴反应8h,随后加入10.0mg球形石墨烯、25.0mg步骤1)制得的中空纳米球fe3o4,25℃一锅式搅拌反应8.0h,制得hemin-au-sg-fe3o4复合物;
3)将步骤2)制得的hemin-au-sg-fe3o4复合物加入1.0wt%的海藻酸钠水溶液5.0ml中(分散浓度以血红素浓度计算为0.025~0.2mg/ml),超声30min混合均匀后,用1.0ml的注射器吸取溶液,将其以每秒一滴的速度滴入到20.0ml、1.5wt%的氯化钙水溶液中,滴入后会立刻形成圆形小颗粒,然后静置1.5h使其固定化,再用超纯水洗涤3遍,低温干燥,得到sa-hemin-au-sg-fe3o4磁性模拟酶复合球,即多功能模拟酶复合球。
实施例3
一种多功能模拟酶复合球的制备方法,各原料的配比如下:
haucl4:10.0mm,1.0ml
hemin:1.0mgml-1,1.0ml
naoh:1.0m,125μl
sg:12.0mg
sa:2.5w%,1.0ml
fe3o4:35.0mg
cacl2:3.0w%,20ml
其步骤为:
1)室温条件下,将fecl3·6h2o(1.73g)溶解于乙二醇(35ml)中,溶解浓度0.183m,磁力搅拌,待完全溶解后加入3.83g乙酸钠,乙酸钠在溶液中0.804m,继续搅拌30min后转移到高压釜中,调节温度为200℃,反应8h,然后冷却至室温,用磁铁分离,收集磁铁吸附的固体,用水和乙醇洗涤,在60℃下烘干12h,得到中空纳米球fe3o4,备用;
2)室温条件下,将血红素溶解于0.01m的naoh水溶液中,配制浓度为1.0mg/ml的血红素溶液,然后将血红素溶液与1.0ml、10.0mm的氯金酸水溶液等体积混合,磁力搅拌下缓慢滴加125μl、1.0m的naoh水溶液,调节溶液ph为10.0,37℃水浴反应8h,随后加入12.0mg球形石墨烯,35.0mg步骤1)制得的中空纳米球fe3o4,55℃一锅式搅拌反应10.0h,制得hemin-au-sg-fe3o4复合物;
3)将步骤2)制得的hemin-au-sg-fe3o4复合物加入2.5wt%的海藻酸钠水溶液5.0ml中(分散浓度以血红素浓度计算为0.025~0.2mg/ml),超声30min混合均匀后,用1.0ml的注射器吸取溶液,将其以每秒一滴的速度滴入到20.0ml、3.0wt%的氯化钙水溶液中,滴入后会立刻形成圆形小颗粒,然后静置1.5h使其固定化,再用超纯水洗涤,低温干燥,得到sa-hemin-au-sg-fe3o4磁性模拟酶复合球,即多功能模拟酶复合球。
实施例4
一种多功能模拟酶复合球的制备方法,各原料的配比如下:
haucl4:10.0mm,1.0ml
hemin:1.0mgml-1,1.0ml
naoh:1.0m,120μl
sg:10.0mg
sa:2.0wt%,1.0ml
fe3o4:50.0mg
cacl2:3.0wt%,20ml
其步骤为:
1)室温条件下,将fecl3·6h2o(1.73g)溶解于乙二醇(35ml)中,溶解浓度0.183m,磁力搅拌,待完全溶解后加入3.83g乙酸钠,乙酸钠在溶液中0.804m,继续搅拌30min后转移到高压釜中,调节温度为200℃,反应8h,然后冷却至室温,用磁铁分离,收集磁铁吸附的固体,用水和乙醇洗涤,在60℃下烘干12h,得到中空纳米球fe3o4,备用;
2)室温条件下,将血红素溶解于0.01m的naoh水溶液中,配制浓度为1.0mg/ml的血红素溶液,然后将血红素溶液与1.0ml、10.0mm的氯金酸水溶液等体积混合,磁力搅拌下缓慢滴加120μl、1.0m的naoh水溶液,调节溶液ph为10.0,37℃水浴反应8h,随后加入10.0mg球形石墨烯,50.0mg步骤1)制得的中空纳米球fe3o4,37℃一锅式搅拌反应12.0h,制得hemin-au-sg-fe3o4复合物;
3)将步骤2)制得的hemin-au-sg-fe3o4复合物加入2.0wt%的海藻酸钠水溶液5.0ml中(分散浓度以血红素浓度计算为0.025~0.2mg/ml),超声30min混合均匀后,用1.0ml的注射器吸取溶液,将其以每秒一滴的速度滴入到20.0ml、3.0wt%的氯化钙水溶液中,滴入后会立刻形成圆形小颗粒,然后静置1.5h使其固定化,再用超纯水洗涤,低温干燥,得到sa-hemin-au-sg-fe3o4磁性模拟酶复合球,即多功能模拟酶复合球。
将在实施例4条件下所制得的模拟酶的拓扑结构及相关酶活性和环境稳定性进行考察。
如图1a为合成的金纳米簇的透射电镜图(tem),从图中可知所制备的hemin-au纳米粒子粒径均匀,分散性较好,平均尺寸大小为2.0-3.0nm。已有研究表明,金纳米颗粒的尺寸小于5.0nm时具有高效的催化活性,即金纳米簇的“小尺寸效应”,可望赋予hemin-au较高的催化活性。图1b为hemin-au的紫外吸收图,由图可知,hemin-au在330nm和385nm处有两个吸收峰,分别对应au和hemin的特征吸收峰,进一步证明hemin-au模拟酶的成功合成。
图2系统研究了hemin、hemin-au、hemin-au-sg和sa-hemin-au-sg-fe3o4的催化性能。由图2a可知,hemin、hemin-au、hemin-au-sg和sa-hemin-au-sg-fe3o4对应的催化产物的吸光度值逐渐增大,即催化活性依次升高,sa-hemin-au-sg-fe3o4催化活性最高。原因可能是:一方面,hemin-au具有较hemin高的催化活性,另一方面,纳米sg、fe3o4本身就具有类过氧化物酶的活性,将其与hemin-au和sg一锅反应,其巨大的表面积和内部空腔,会吸附小颗粒分子到其表面,并且hemin、sg、fe3o4分子都具有六圆环结构,容易形成π-π共轭结构,这种共轭结构会使它们之间的联系更加紧密,加速了电子的传递和转移。图2b为使用sa包埋模拟酶复合球形成的颗粒,可以看出制得的颗粒为球形,表面光滑,大小均匀。由于颗粒中有磁性fe3o4,可用磁铁回收,重复利用,回收操作比较简便快捷,可使其更广泛的应用于不同领域、不同环境中。
另外,对合成过程进行了条件优化。如图3a所示,合成sa-hemin-au-sg-fe3o4最适宜的碱量为100mm,过酸或过碱会影响固定化的效果。图3b考察了制备小球时的固定化时间,结果表明最适宜的固定花时间为1.5小时。这可能是由于固定化时间短,sa与钙离子反应不充分,sa形成的膜不稳固,容易破裂;而固定化时间太长会使sa收缩严重,阻断sa包裹的分子从里面出来的通道,影响催化反应。另外,sa作为模拟酶复合球的载体,对模拟酶复合球的活性有显著的影响。其浓度太小,凝胶的孔径较大,颗粒容易破裂使模拟酶复合球流失,导致酶活性降低;其浓度过大,凝胶的孔径越小,酶与底物进出的通道小,影响酶与底物的结合,使颗粒催化活性较小,所以sa的最佳浓度为2.0w%,如图3c所示。图3d考察了氯化钙浓度的影响,由图可知,氯化钙浓度过大,产品颗粒表面会布满钙离子,堵塞凝胶的孔径,切断酶与底物进出的通道,另外,钙离子会与hemin反应使其活性降低;钙离子浓度太低会使凝胶强度太小,导致酶流失,所以适宜的钙离子浓度为3.0w%。
图4为对模拟酶复合球的催化反应条件的优化。由图4a可知,ph值对模拟酶复合球的活性有较大的影响。原因可能是,颗粒表面的sa在酸性条件下形成不溶于水的海藻酸,使颗粒表面收缩变紧,孔径变小,阻断了颗粒内部酶的出入,导致其催化活性降低;而随着ph值的增加,颗粒表面的sa会逐渐溶解,孔径变大,加速sa-hemin-au-sg-fe3o4与反应底物的接触,催化活性增强。但是ph值过高,会使孔径过大,虽然会使其催化活性增大,但是会导致模拟酶复合球颗粒的破裂,使sa-hemin-au-sg-fe3o4完全流出。因此,过酸过碱都会影响颗粒活性,弱酸弱碱范围内使用最好。同时,由图4a看出,温度过低或过高都会影响颗粒的活性,固定化颗粒发挥活性的适宜温度为37°c。
图5考察了模拟酶复合球的环境稳定性。由图5a可知,将颗粒储存在水中12个月,催化tmb-h2o2显色的活性几乎没有太大改变。图5b展示了固定化颗粒在催化tmb-h2o2显色使用5次后,依然保持很高的催化活性。从而说明,sa-hemin-au-sg-fe3o4模拟酶复合球在水中具有很高的稳定性,模拟酶复合球可以重复利用。
实施例5多功能模拟酶复合球应用
将本发明实施例1制备的多功能模拟酶复合球用于环境有机毒物(ph)及染料(mb、rhb)的吸附与催化降解
以ph、mb和rhb为例,将该磁性模拟酶复合球用于环境污染物的降解研究,结果如图6、图7和图8所示。如图6所示,以sa小球作对比,将sa小球(0.25g)加入到mb溶液(10-4m,50ml)中,由于sa小球内部多孔的结构,可以较容易的吸附大量小分子,所以mb溶液颜色逐渐变浅,sa小球颜色由透明变成蓝色。同理,将sa-hemin-au-sg-fe3o4模拟酶复合球(0.25g)在不同的条件下与mb(10-4m,50ml)作用,大约1小时后mb有不同程度的褪色,从图6a中也可以看出,mb的紫外吸光度逐渐降低。从图6b中看出单纯sa小球(a)的降解吸附率为29%,sa-hemin-au-sg-fe3o4模拟酶复合球在黑暗(b)、室内(c)、太阳光(d)条件下对mb的降解率分别为69.5%、70.5%、81%,从而说明sa-hemin-au-sg-fe3o4模拟酶复合球对mb具有显著的催化降解能力,且在太阳光下的降解效果更明显。这可能是由于hemin-au-sg-fe3o4之间的π-π共轭结构加速了模拟酶复合球与底物之间的电子传递或者转移速率,从而提高了模拟酶复合球的酶催化能力。
图7为sa-hemin-au-sg-fe3o4模拟酶复合球降解rhb的考察。与降解mb现象类似,大约2小时后rhb会不同程度的褪色(图7a),从7b中看出sa小球的降解吸附率为28.7%,在黑暗、室内、太阳光条件下的降解率分别为59.6%、72.8%、83.1%,进而说明sa-hemin-au-sg-fe3o4模拟酶复合球对rhb具有显著的催化降解能力,且在太阳光下的降解效果更明显。原因可能是光催化降解,也可能是hemin-au-sg-fe3o4之间的π-π共轭结构使加速了模拟酶复合球与底物之间的电子传递或者转移速率,从而提高了模拟酶复合球的酶催化能力。
另外,将sa-hemin-au-sg-fe3o4模拟酶复合球(0.25g)在不同的条件下与ph(99.8%,20ml)作用,并加入200μl30%的双氧水,室温搅拌,可以观察到混合体系中有大量的热和气泡产生。随后,每隔5分钟取降解体系上清液(50μl)与fecl3溶液(1.0m,150μl)混合反应。由图8a可知,sa对ph几乎没有降解功能,而sa-hemin-au-sg-fe3o4模拟酶复合球对ph降解效果明显,尤其以在太阳光下降解效果最为明显。另外,对没有加sa-hemin-au-sg-fe3o4模拟酶复合球的空白体系,在加入fecl3后溶液由黄色变为紫色,这是由于fecl3与苯酚反应生成2,4,6-三氯苯酚紫色络合物所致,说明体系中的苯酚没有被降解,而对加入sa-hemin-au-sg-fe3o4模拟酶复合球的体系,开始加入fecl3时溶液变为紫色,大约1h后,加入fecl3后上清液颜色不再发生变化,此时体系中的苯酚被降解完全,这是由于在sa-hemin-au-sg-fe3o4的催化作用下,双氧水将苯酚氧化变成苯醌,而苯醌与fecl3不反应,没有紫色络合物生成。从8b中看出sa小球的降解吸附率为8.07%,在黑暗、室内、太阳光条件下的降解率分别为60.41%、73.36%、92.77%,进而说明sa-hemin-au-sg-fe3o4模拟酶复合球对ph具有显著的催化降解能力,且在太阳光下的降解效果更明显。
对比例1
一种基于血红素介导金矿化途径的双催化功能模拟酶的制备方法,步骤包括:
(1)取氯化血红素,室温下加水搅拌,配制为浓度0.10mg/ml的hemin溶液,4℃储存;取氯金酸加水,配制为浓度10mm的haucl4溶液;取naoh加水,配制为浓度1.0m的naoh溶液;
(2)将步骤(1)制备的1.0mlhaucl4溶液与1.0mlhemin溶液等体积混合,5min后,剧烈搅拌下加入20μlnaoh溶液,然后在水浴中继续搅拌,37℃反应8h,8000r/s离心20min,取上清液采用14kda的透析袋去离子水透析处理12h,得基于血红素介导金矿化途径的双催化功能模拟酶(即hemin-auncs复合物),于4℃保存。
实施例1及对比例1产品性能对比
本发明实施例1所制备的sa-hemin-au-sg-fe3o4模拟酶复合球与对比例1中的hemin-au模拟酶同时应用于对染料(mb、rhb、ph)的降解实验中,结果发现,sa-hemin-au-sg-fe3o4具有显著高于hemin-au的降解性能。原因如下:(1)sg特殊的单原子层平面二维结构和超高的比表面积,可吸附连接丰富的hemin-au复合物,显著增强单位体积内酶分子的个数,从而增强复合物催化性能;(2)hemin、sg、fe3o4分子均具有六元环结构,容易形成π-π共轭结构,使它们之间的联系更加紧密,加速电子的传递和转移,另外,sg、fe3o4本身具有一些类过氧化物酶活性,与hemin-au结合后,使得整体活性增强;(3)sa具有丰富的羧基和羟基等功能基团,易与hemin中的羧基结合实现酶的固定化包埋,并且可生物降解、生物相容性和黏附性好,环境无毒,可以很好的黏附在磁性颗粒表面;(4)fe3o4具有磁性,可回收利用,回收操作简便快捷,使其更广泛的应用于不同领域、不同环境中。基于此,sa-hemin-au-sg-fe3o4模拟酶复合球可广泛应用于催化降解染料中。
- 还没有人留言评论。精彩留言会获得点赞!