一种阿奇霉素干混悬剂溶出曲线的测定方法与流程
本发明属于药物分析,具体涉及一种阿奇霉素干混悬剂溶出曲线的测定方法。
背景技术:
1、阿奇霉素属于大环内酯类抗生素,是临床上应用广泛的抗感染药物,多用于敏感菌所致的呼吸道、皮肤软组织感染和衣原体所致的传播性疾病。阿奇霉素于1981年上市后,已开发出了片剂、胶囊、分散片、颗粒剂、干混悬剂等多种剂型。阿奇霉素干混悬剂具有起效快,顺应性好的优势,且尤其适用于给药困难如小孩、老人或吞咽困难的特殊用药群体。
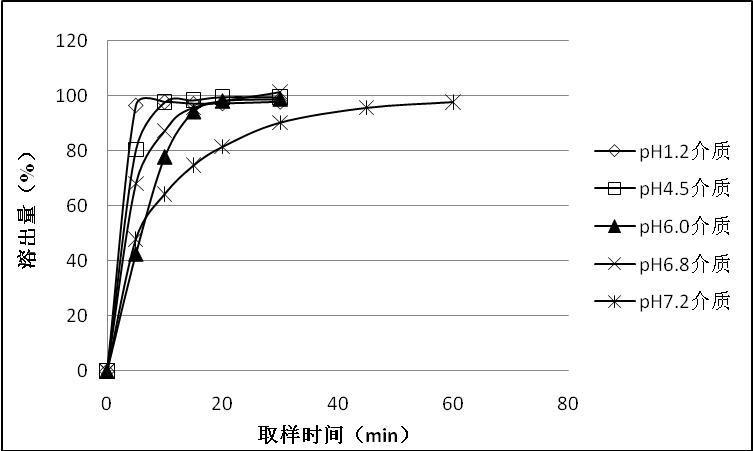
2、阿奇霉素属于ph依懒性药物,溶解度受ph值的影响较大。研究过程中发现,阿奇霉素干混悬剂在《普通口服固体制剂溶出曲线测定与比较指导原则》中推荐的ph1.2、ph4.5、ph6.8介质条件下,溶出过快,溶出度均15分钟超过85%;在美国药典收录的溶出度测定介质条件下(ph6.0介质),溶出度15分钟超过85%。由此可见,在现有溶出介质条件下,阿奇霉素干混悬剂溶出均较快,无法参考《普通口服固体制剂溶出曲线测定与比较指导原则》提供的相似因子(f2)法进行评价,因此,开发具有区分力的溶出曲线,对评价阿奇霉素干混悬剂仿制制剂与参比制剂的一致性、指导制剂工艺处方筛选等有重要意义。
3、中国药典规定阿奇霉素干混悬剂的性状为颗粒或粉末,目前辉瑞制药有限公司生产的阿奇霉素干混悬剂为原研地产化,采用的工艺为直接物理混合分装的工艺,产品呈粉末状态,而国内生产的阿奇霉素干混悬剂采用工艺多为湿法制粒,产品呈颗粒状态。干混悬剂溶出度检测多采用直接投样于介质表面,当为粉末状态时容易成团漂浮于溶出介质表面,减缓阿奇霉素的释放,导致溶出较慢,而当为颗粒状态时沉于溶出介质底部,与溶出介质接触更充分,阿奇霉素释放较快。两者溶出行为存在差异,为消除该差异,有必要采取一定方法将粉末状制剂分散均匀后投入溶出介质底部,再测定溶出曲线,以便于两种状态干混悬剂的溶出行为比较。
技术实现思路
1、为解决上述问题,本发明通过考察不同ph介质的溶出曲线,提供了一种具有区分力的测定阿奇霉素干混悬剂体外溶出的方法,可用于仿制制剂与参比制剂的质量一致性评价工作,也可用于评价药品批间质量的一致性。本发明通过加水5ml搅拌分散均匀后再投样,样品落于溶出介质底部,可以消除阿奇霉素干混悬剂参比制剂(粉末状态)与仿制制剂(颗粒状态)两者因产品状态不同导致的溶出行为差异,可用于不同工艺仿制制剂与参比制剂的质量一致性评价工作。
2、本方案提供一种阿奇霉素干混悬剂溶出曲线的测定方法,包括如下步骤:
3、(1)溶出介质的制备:配制ph7.2磷酸盐缓冲液作为溶出介质;
4、(2)供试品溶液的制备:将参比制剂和仿制制剂分别置适量容器中,加水5ml搅拌分散均匀后投入步骤(1)中所述溶出介质中,使用桨法进行溶出试验,经不同时间取溶出液5ml,过滤,取续滤液作为供试品溶液,并及时补充等温度等体积的溶出介质;
5、 (3)对照品溶液的制备:称取阿奇霉素对照品于1l容量瓶中,加入少量乙腈溶解,用步骤(1)中所述溶出介质稀释至刻度,作为对照品溶液;
6、(4)测定:采用高效液相色谱法测定溶出量;
7、(5)相似性比较:采用相似因子(f2)法比较待测样品中仿制制剂与参比制剂的溶出曲线相似性。
8、优选地,所述步骤(1)中磷酸盐缓冲液为磷酸二氢钾缓冲溶液。
9、优选地,所述步骤(2)中,溶出转速为25~50rpm,最优选为35rpm;溶出介质体积为900ml;溶出温度为37.0±0.5℃;溶出取样时间为5、10、15、20、30、45、60分钟
10、优选地,所述步骤(3)中,对照品溶液中阿奇霉素的浓度为0.1mg/ml。
11、优选地,所述步骤(4)中,采用高效液相色谱法测定溶出量时,色谱条件为:以十八烷基硅烷键合硅胶为填充剂(waters xbrigde shield rp18,4.6mm×150mm,5μm或效能相当的色谱柱);以0.05mol/l磷酸二氢钾溶液(稀磷酸调节ph为8.2)-乙腈(35:65)为流动相;流速为每分钟2ml;柱温为50℃;进样体积为50μl。
12、优选地,所述步骤(5)中,采用相似因子(f2)法时,选择5、10、20、45分钟四个时间点时仿制制剂与参比制剂的平均溶出量计算相似因子f2。相似因子f2大于或等于50时,仿制制剂与参比制剂相似;相似因子f2小于50时,仿制制剂与参比制剂不相似。
13、有益效果
14、(1)本发明解决了现有技术中常规的溶出曲线无区分力,不能准确反映阿奇霉素干混悬剂仿制制剂与参比制剂体外溶出行为的差异,应用本发明提供的溶出曲线,满足《普通口服固体制剂溶出曲线测定与比较指导原则》采用相似因子(f2)法比较溶出曲线相似性的要求,能够反映阿奇霉素干混悬剂的内在品质,并具有良好的体内外相关性,对提高生物等效性试验的效率,加快仿制药研发进程,有重要意义。
15、(2)本发明解决了干混悬剂常规采用直接投样法测定溶出条件下,阿奇霉素干混悬剂粉末状态产品与颗粒状态产品的溶出行为存在差异,不能准确反映两种状态制剂之间体外溶出行为的差异,应用本发明提供的方法,能够消除该溶出行为的差异,为两种工艺制备的阿奇霉素干混悬剂的一致性评价提供比较方法。
技术特征:
1.一种阿奇霉素干混悬剂溶出曲线的测定方法,其特征在于,包括如下步骤:
2.根据权利要求1所述的阿奇霉素干混悬剂溶出曲线的测定方法,其特征在于,所述步骤(1)中的磷酸盐缓冲液为磷酸二氢钾缓冲溶液。
3.根据权利要求1所述的阿奇霉素干混悬剂溶出曲线的测定方法,其特征在于,所述步骤(2)中的溶出转速为25~50rpm,优选为35rpm;溶出介质体积为900ml;溶出介质温度为37.0±0.5℃;溶出取样时间为5、10、15、20、30、45、60分钟。
4.根据权利要求3所述的阿奇霉素干混悬剂溶出曲线的测定方法,其特征在于,所述步骤(2)中的溶出转速为35rpm。
5.根据权利要求1所述的阿奇霉素干混悬剂溶出曲线的测定方法,其特征在于,所述步骤(4)中的高效液相色谱法的色谱条件为:
6.根据权利要求1所述的阿奇霉素干混悬剂溶出曲线的测定方法,其特征在于,所述步骤(5)中的相似因子(f2)法,选择5、10、20、45分钟四个时间点时仿制制剂与参比制剂的平均溶出量计算相似因子f2。
技术总结
本发明属于药物分析技术领域,具体涉及一种阿奇霉素干混悬剂溶出曲线的测定方法,包括以下步骤:(1)溶出介质的制备:配制pH7.2磷酸盐缓冲液作为溶出介质;(2)样品溶液的制备:将阿奇霉素干混悬剂置适量容器中,加水5ml搅拌分散均匀后投入溶出介质中,使用桨法进行溶出试验,得到样品溶液;(3)对照品溶液的制备:称取阿奇霉素对照品,置量瓶中,加入少量乙腈溶解,用溶出介质稀释至刻度,得到对照品溶液;(4)测定:分别取对照品溶液和各个溶出时间点的样品溶液,采用高效液相色谱法测定溶出量;(5)比较:采用相似因子(f2)法,计算相似因子f2,比较仿制制剂溶出曲线与参比制剂的相似性。本发明提供了一种具有区分力的溶出曲线的测定方法,解决了现有技术中溶出方法不能满足《普通口服固体制剂溶出曲线测定与比较指导原则》中关于采用相对因子(f2)法比较溶出曲线相似性的要求,因而影响阿奇霉素干混悬剂仿制药工艺处方筛选和体外一致性评价的问题。
技术研发人员:田文桥,杨德斌
受保护的技术使用者:迪沙药业集团有限公司
技术研发日:
技术公布日:2024/1/16
- 还没有人留言评论。精彩留言会获得点赞!