消毒用组合物的制作方法
[0001]
本发明涉及含有葡萄糖酸奥拉昔定的具有广泛的杀菌谱的消毒用组合物。
背景技术:
[0002]
奥拉昔定为化学名1-(3,4-二氯苄基)-5-辛基双胍这样的具有高杀菌活性的化合物。葡萄糖酸奥拉昔定在水中具有充分的溶解性,具有宽的杀菌谱,杀菌效果在短时间显现,进而其活性会长时间持续,而且安全性也高,因此作为医疗用消毒剂有用(专利文献1)。含有葡萄糖酸奥拉昔定的外皮用杀菌消毒剂对属于皮肤常住菌的各种细菌和有包膜病毒具有优异的效力,而另一方面,对没有包膜的猫杯状病毒几乎没有效力(非专利文献1)。因此,在医疗、护理、饮食品产业等领域中,正在谋求效力更高、具有广泛的杀菌谱的含葡萄糖酸奥拉昔定的消毒剂。
[0003]
奥拉昔定属于具有1个双胍结构的单双胍系化合物。作为具有相同双胍结构的消毒剂,作为二双胍系化合物的氯己定、作为多双胍系化合物的聚六亚甲基双胍可作为代表种类而举出。
[0004]
氯己定为1分子中具有2个双胍结构的二双胍系化合物。与奥拉昔定同样地难溶于水,通过制成葡萄糖酸盐变为可溶,因此作为医药品主要以葡萄糖酸氯己定的形式使用(非专利文献2)。葡萄糖酸氯己定与葡萄糖酸奥拉昔定同样地,对有包膜病毒显示杀病毒作用,而另一方面对无包膜病毒没有效力(非专利文献3)。另外,已知葡萄糖酸氯己定在ph4~6.5时稳定,若使稀释水溶液为ph8以上的碱性,则会产生沉淀;即使升高ph,杀菌效力也不会产生差异(专利文献2、非专利文献2、非专利文献4)。
[0005]
另一方面,聚六亚甲基双胍被分类为多双胍系化合物,是1个单元中具有1个双胍结构的六亚甲基双胍的聚合物。聚六亚甲基双胍在水中极其易溶,具有广范围的杀菌谱,因此其弱酸性溶液作为低毒性除菌剂而被广泛市售(非专利文献5、6等)。另外,报道了市售的聚六亚甲基双胍消毒剂对无包膜病毒也具有杀病毒活性(非专利文献7),也有进一步升高ph时杀菌效力及杀病毒效力会上升的报道(非专利文献4、专利文献3、4)。
[0006]
现有技术文献
[0007]
专利文献
[0008]
专利文献1:日本特开第2005-289959号公报
[0009]
专利文献2:日本特开第2007-217394号公报
[0010]
专利文献3:日本特开第2007-045732号公报
[0011]
专利文献4:日本特开第2017-171606号公报
[0012]
非专利文献
[0013]
非专利文献1:附件“奥拉奈津液(
オラネジン
液)1.5%消毒用施用器10ml/25ml”(2015年8月修订)
[0014]
非专利文献2:药品综述资料(
インタビューフォーム
)“葡萄糖酸氯己定液”(2010年7月修订)
[0015]
非专利文献3:临床微生物学评论(clin microbiol rev.);12(1):147-179(1999年1月)
[0016]
非专利文献4:皮肤药理与生理(skin pharmacol physiol.);28(3):147-158(2015年)
[0017]
非专利文献5:消费者安全科学委员会(scientific committee on consumer safety)“关于聚六亚甲基双胍盐酸盐(phmb)安全性的意见“(“opinion on the safety of poly(hexamethylene)biguanide hydrochloride(phmb)”)(2015年7月)
[0018]
非专利文献6:万妥昔鲁ib抗菌剂技术信息资料(vantocil ib antimicrobial技術情报資料)
[0019]
非专利文献7:网址“奥科化学公司报告称,研究证实万妥昔鲁(商标)产品可控制作为急性胃肠炎的主要原因的诺如病毒”(“arch chemicals reports that studies confirm that vantocil(tm)product controls norovirus,a leading cause of acute gastroenteritis”)
[0020]
(https://www.businesswire.com/news/home/20060113005294/en/arch-chemicals-reports-studies-confirm-vantocil-tm)
技术实现要素:
[0021]
发明所要解决的课题
[0022]
本发明的课题在于,提供一种消毒用组合物,其进一步提高用作安全性高的外皮用杀菌消毒剂的葡萄糖酸奥拉昔定的效力,并且通过扩大杀菌谱,使施用范围进一步扩大。
[0023]
用于解决课题的手段
[0024]
本发明人等为了解决上述课题持续进行了深入研究。由于施用于皮肤的组合物通常与皮肤的ph(ph4~7)适应而为弱酸性,奥拉昔定通过用碱水溶液进行中和而以游离体的形式析出(专利文献1),因此以往含有葡萄糖酸奥拉昔定的杀菌剂在ph5进行制剂化(非专利文献1),但本发明人等制备葡萄糖酸奥拉昔定的碱性溶液并对其活性进行了试验,结果出乎意料地发现,不仅杀菌效力提高,而且对用弱酸性制剂基本没有效力的无包膜病毒也显现效力。另外,本发明人等确认了,通过在含有葡萄糖酸奥拉昔定的碱性溶液中进一步加入表面活性剂,稳定性提高。本发明基于以上的见解。
[0025]
即,本发明如下。
[0026]
(1)消毒用组合物,其特征在于,含有葡萄糖酸奥拉昔定,且为碱性。
[0027]
(2)如上述(1)所述的消毒用组合物,其特征在于,在ph8~11的范围内。
[0028]
(3)如上述(1)或(2)所述的消毒用组合物,其特征在于,葡萄糖酸奥拉昔定的浓度为0.01~20%(w/v)。
[0029]
(4)如上述(1)~(3)中任一项所述的消毒用组合物,其特征在于,包含水和/或消毒用醇。
[0030]
(5)如上述(4)所述的消毒用组合物,其特征在于,消毒用醇浓度为10~85%(v/v)。
[0031]
(6)如上述(4)或(5)所述的消毒用组合物,其特征在于,消毒用醇选自乙醇及异丙醇。
[0032]
(7)擦洗剂(
ラビング
剤),其包含上述(1)~(6)中任一项所述的消毒用组合物。
[0033]
发明的效果
[0034]
利用本发明的组合物,能够制作在医疗、护理、饮食品产业等领域中可利用的、效力更高、具有广泛的杀菌谱的消毒剂。
附图说明
[0035]
图1为示出实施例1的含葡萄糖酸奥拉昔定的组合物(ph5、8~10)对偶发分枝杆菌(mycobacterium fortuitum)jcm 6387的杀菌力的图。
[0036]
图2为示出实施例1的含葡萄糖酸奥拉昔定的组合物(ph5、8~10)对龟分枝杆菌(mycobacterium chelonae)jcm 6388的杀菌力的图。
[0037]
图3为示出实施例1的含葡萄糖酸奥拉昔定的组合物(ph5、8~10)对犬小孢子菌(microsporum canis)nbrc 32464的杀菌力的图。
[0038]
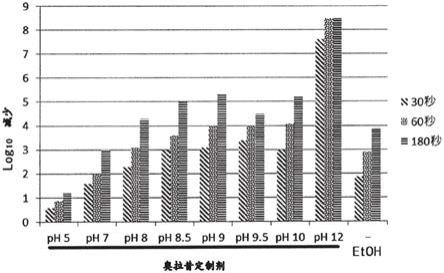
图4为示出实施例2的含葡萄糖酸奥拉昔定的组合物(ph5、7~12)对噬菌体的杀病毒(噬菌体)活性的图。
[0039]
图5为示出实施例3的含乙醇的奥拉昔定制剂对噬菌体的杀病毒(噬菌体)活性的图。
具体实施方式
[0040]
本发明涉及消毒用组合物,其特征在于,含有葡萄糖酸奥拉昔定,且为碱性。此处,对于碱性而言,只要组合物的ph超过7即可,鉴于对皮肤的毒性及杀菌活性,例如可以举出ph超过7且小于或等于12、ph超过7且小于或等于11.5、ph超过7且小于或等于11、ph超过7且小于或等于10.5、ph超过7且小于或等于10,优选ph7.5~12、ph7.5~11.5、ph7.5~11、ph7.5~10.5、ph7.5~10,更优选ph8~11.5、ph8~11、ph8~10.5、ph8~10,进一步优选ph8.5~11.5、ph8.5~11、ph8.5~10.5、ph8.5~10、进一步更优选ph9~12、ph9~11.5、ph9~11、ph9~10.5、ph9~10。需要说明的是,本发明的组合物为水溶液。另外,在本说明书中,“消毒”、“杀菌”是指对细菌、真菌和/或病毒进行灭杀。
[0041]
ph的调节中可以使用公知的任意ph调节剂,例如可以举出氢氧化钠、氢氧化钾、氢氧化钙、碳酸铵、碳酸钾等碱性溶液,其中可以优选例示出氢氧化钠。另外,可以使用碱性缓冲液来制备本发明的组合物,作为使用的缓冲液,可以例示出硼酸-碳酸钠缓冲液、caps-naoh缓冲液、bicine-naoh缓冲液、gricine-naoh缓冲液、tricine-naoh缓冲液、hepps-naoh缓冲液、taps-naoh缓冲液、bicine-naoh缓冲液、hepes-naoh缓冲液等。
[0042]
作为葡萄糖酸奥拉昔定的浓度,只要为具有充分的杀菌效力的浓度,就没有特别限制,例如可以举出0.01~20%(w/v),优选0.1~10%(w/v),更优选0.5~5%(w/v)。与后述的消毒用醇组合使用的情况下,例如可以举出0.01~10%(w/v),优选0.1~7%(w/v),更优选0.5~5%(w/v),进一步优选0.5~3%(w/v)。
[0043]
本发明的组合物对丝状菌、抗酸菌、特别是小孢子菌属菌、分枝杆菌属菌具有提高了的杀菌活性。进而,对通过以往的含葡萄糖酸奥拉昔定的消毒剂不能失活的无包膜病毒、特别是属于杯状病毒科的病毒(属于诺如病毒属的病毒等)也有优异的杀病毒活性。
[0044]
为了增强杀菌活性、为了赋予速干性,本发明的组合物可以还包含消毒用醇。此
处,作为消毒用醇,优选可以举出乙醇或异丙醇,作为消毒用醇浓度,可以举出例如10~85%(v/v)、20~85%(v/v)、30~85%(v/v)、40~85%(v/v)、50~85%(v/v)、10~80%(v/v)、20~80%(v/v)、30~80%(v/v)、40~80%(v/v)、50~80%(v/v)、10~70%(v/v)、20~70%(v/v)、30~70%(v/v)、40~70%(v/v)、50~70%(v/v)。本发明的组合物也可以实质上不含消毒用醇。通过包含消毒用醇,也能够制成由兼具消毒用醇所带来的杀菌活性的增强效果和由葡萄糖酸奥拉昔定所带来的杀菌活性的持续效果的速干性消毒剂。进而,通过消毒用醇使得杀菌活性增强,因此也能够降低葡萄糖酸奥拉昔定的浓度。作为葡萄糖酸奥拉昔定与消毒用醇的浓度比,例如可以举出1:400~1:20,优选1:300~1:30,更优选1:200~1:40。
[0045]
本发明的组合物中可以进一步配合公知的杀菌剂。作为杀菌剂,例如,可举出苯扎氯铵、烷基磷酸苄烷铵等苄烷铵盐、苄索氯铵、三氯生、异丙基甲基苯酚、氯化十六烷基吡啶鎓、间苯二酚、三氯碳酰苯胺、盐酸氯己定、葡萄糖酸氯己定、聚六亚甲基双胍、次氯酸钠、过氧化氢、聚维酮碘、碘酊等。这些杀菌剂可以单独配合,也可以组合使用2种以上。
[0046]
本发明的组合物可以进而配合公知的溶解辅助剂。作为溶解辅助剂,可以举出例如非离子性表面活性剂、离子性表面活性剂、乙二胺、苯甲酸钠、烟酰胺、环糊精、乙醇、苯甲醇、丙二醇等。作为离子性表面活性剂,可以优选可以举出油烯基二甲基氧化胺、硬脂基二甲基氧化胺、棕榈基二甲基氧化胺、肉豆蔻基二甲基氧化胺、月桂基二甲基氧化胺、椰油烷基二甲基氧化胺等烷基二甲基氧化胺,其中优选月桂基二甲基氧化胺。作为非离子性表面活性剂,可以举出山梨糖醇酐脂肪酸酯、聚氧乙烯山梨糖醇酐脂肪酸酯、聚氧乙烯烷基醚、聚氧乙烯聚氧丙烯烷基醚、聚氧乙烯聚氧丙烯二醇、聚甘油脂肪酸酯、聚氧乙烯氢化蓖麻油、蔗糖脂肪酸酯等,其中优选聚氧乙烯聚氧丙烯二醇、聚氧乙烯烷基醚、聚氧乙烯聚氧丙烯烷基醚。作为聚氧乙烯聚氧丙烯二醇,可以例示出聚氧乙烯(42)聚氧丙烯(67)二醇(pluronic(注册商标)p-123)、聚氧乙烯(54)聚氧丙烯(39)二醇(pluronic(注册商标)p-85)、聚氧乙烯(196)聚氧丙烯(67)二醇(pluronic(注册商标)f-127)、聚氧乙烯(3)聚氧丙烯(17)二醇(pluronic(注册商标)l-31)、聚氧乙烯(20)聚氧丙烯(20)二醇(pluronic(注册商标)l-44)、聚氧乙烯(120)聚氧丙烯(40)二醇(pluronic(注册商标)f-87)、聚氧乙烯(160)聚氧丙烯(30)二醇(pluronic(注册商标)f-68),其中优选聚氧乙烯(20)聚氧丙烯(20)二醇(pluronic(注册商标)l-44)。作为聚氧乙烯烷基醚,可举出聚氧乙烯鲸蜡基醚、聚氧乙烯油烯基醚、聚氧乙烯月桂基醚(聚桂醇(
ラウロマクロゴール
))等,特别优选聚氧乙烯月桂基醚(聚桂醇)。另外,作为聚氧乙烯聚氧丙烯烷基醚,可举出聚氧乙烯(20)聚氧丙烯(4)鲸蜡基醚、聚氧乙烯(30)聚氧丙烯(6)癸基十四烷基醚、聚氧乙烯(25)聚氧丙烯(25)月桂基醚等,特别优选聚氧乙烯(20)聚氧丙烯(4)鲸蜡基醚。溶解辅助剂的浓度只要为防止葡萄糖酸奥拉昔定的沉淀、并且不使杀菌活性降低的浓度即可,通常在0.1~30%(w/v)的浓度范围根据葡萄糖酸奥拉昔定的浓度来设定。
[0047]
本发明的组合物可以任意包含抗炎剂、保湿剂、润滑剂、感觉改善剂、增稠剂等。
[0048]
作为抗炎剂,例如,可以举出甘草提取物、甘草次酸、甘草酸二钾、甘草次酸硬脂酯、乙酸生育酚酯、尿囊素、及芦荟提取物等。
[0049]
作为保湿剂,例如,可以举出氨基酸、脂肪酸酯、吡咯烷酮羧酸、吡咯烷酮羧酸钠、乳酸钠、透明质酸、透明质酸钠、n-椰油酰基-l-精氨酸乙基酯dl-吡咯烷酮羧酸盐、尿素、山
梨糖醇、海藻糖、1,3-丁二醇、丙二醇、泊洛沙姆(pluronic(注册商标)f-68等)、及甘油等。
[0050]
作为润滑剂,例如,可以举出肉豆蔻酸异丙酯、棕榈酸异丙酯、硬脂酸异丙酯、油酸异丁酯、及马来酸异丁酯等脂肪酸酯,这些可以单独包含1种或包含2种以上。
[0051]
作为感觉改善剂,例如,可以举出二甲基聚硅氧烷、及环状有机硅等有机硅系化合物。
[0052]
作为增稠剂,例如可以举出羟乙基纤维素、羟丙基纤维素、疏水化羟丙基甲基纤维素、甲基纤维素及羧甲基纤维素等纤维素衍生物、(甲基)丙烯酸系共聚物、聚乙烯醇、聚乙烯基吡咯烷酮、甲基乙烯基醚马来酸酐共聚物、聚丙烯酰胺、海藻酸、海藻酸钠、海藻酸丙二醇酯、明胶、阿拉伯胶、黄蓍胶、槐豆胶、瓜尔胶、罗望子胶、黄原胶、结冷胶、及角叉菜胶等。
[0053]
本发明的组合物优选可以用于医疗器具、调理器具、护理器具等物品表面、手指等皮肤外表面的消毒用的用途中。本发明的组合物可以包含于纸、布、无纺布、棉棒、脱脂棉等基材中而使用,可以填充于涂布用的施用器而使用,也可以以擦洗剂、清洗剂的形式使用,优选本发明的组合物以擦洗剂形式使用。此处,擦洗剂是指速干性擦式制剂,清洗剂是指,将杀菌
·
消毒剂和具有清洗能力的表面活性剂混合而成的制剂。需要说明的是,将本发明的组合物用于两手的手指的消毒的情况下,对于每1次的用量而言,通常以1~5ml、优选1.5~4.5ml、更优选2~4ml、进一步优选2.5~3.5ml使用,对于1天的使用次数而言,鉴于皮肤毒性,可以举出100次以内,优选80次以内,更优选60次以内,进一步优选40次以内。
[0054]
以下,通过实施例更具体地对本发明进行说明,但本发明的技术范围不限定于这些例示。
[0055]
实施例1
[0056]
1.对真菌及非结核性抗酸菌的杀菌力
[0057]
通过time-kill试验来评价含葡萄糖酸奥拉昔定的组合物(ph5、8~10)对已知引起感染症的丝状真菌及非结核性抗酸菌的杀菌力。
[0058]
1-1试验材料及方法
[0059]
1-1-1试验物质
[0060]
(1)被验物质1
[0061]
名称:奥拉昔定制剂ph5
[0062][0063]
(2)被验物质2
[0064]
名称:奥拉昔定制剂ph8
company公司制)19g中加入甘油(制品编号:070-04941,和光纯药工业株式会社制)5ml及纯水900ml,进行搅拌。对其进行高压蒸汽灭菌(121℃、20分钟)。灭菌后从高压蒸汽灭菌器中取出,一边搅拌一边冷却至50~55℃后,加入bbl middlebrook oadc增菌液(制品编号:212240,becton,dickinson and company公司制)100ml进行搅拌。在琼脂凝固前,以各约20ml地分注到培养皿中并使其固化。
[0079]
(2)sab平板
[0080]
在沙氏琼脂培养基“nissui”(制品编号:05701,日水制药株式会社制)65g中加入纯水1000ml并进行搅拌。对其进行高压蒸汽灭菌(121℃、20分钟)。在琼脂凝固前,以各约20ml地分注到培养皿中并使其固化。
[0081]
(3)sablp平板
[0082]
在沙氏
·
葡萄糖lp琼脂培养基“daigo”(制品代码:392-01875,日本制药株式会社制)73g中加入纯水1000ml并进行搅拌。对其进行高压蒸汽灭菌(121℃、20分钟)。在琼脂凝固前,以各约20ml地分注到培养皿中并使其固化。
[0083]
1-1-3中和剂
[0084]
在蒸馏水约800ml中加入100g聚山梨酯80、硫代硫酸钠水合物5.0g、磷酸二氢钾0.4g、1ml的tritonx-100、无水磷酸一氢钠10.1g及大豆卵磷脂11.7g,进行搅拌。进而,加入10.0g tamol(注册商标)nn8906,进行加热及搅拌直至溶解。溶解后,加入1mol/l氢氧化钠溶液,调整至ph7.8~7.9。加入蒸馏水直到总量变为1000ml后,进行高压蒸汽灭菌。
[0085]
1-1-4试验菌
[0086]
作为试验菌,使用丝状菌犬小孢子菌(microsporum canis)nbrc32464、以及抗酸菌龟分枝杆菌(mycobacterium chelonae)jcm 6388及偶发分枝杆菌(mycobacterium fortuitum)jcm 6387。各个试验菌在7h10平板(龟分枝杆菌及偶发分枝杆菌)或sab平板(犬小孢子菌)中培养后悬浮于蒸馏水中,制备mcfarland no.1(龟分枝杆菌及偶发分枝杆菌)或mcfarland no.5(犬小孢子菌)的试验菌液。
[0087]
1-2杀菌力评价试验
[0088]
1-2-1初期活菌数的测定(龟分枝杆菌及偶发分枝杆菌)
[0089]
(1)在蒸馏水3ml中加入试验菌液150μl并混合。
[0090]
(2)立即将菌混合液50μl加入到中和剂4.95ml中,进行混合。将其作为102倍稀释液。
[0091]
(3)将102倍稀释液0.3ml加入至中和剂2.7ml中并进行10倍稀释。进而通过同样的操作反复进行稀释来制作10倍稀释系列(102~104倍稀释液为止合计3个等级)。
[0092]
(4)将102~104倍稀释液按每100μl分注于7h10平板,并进行涂抹。(2)~(4)的工序在30分钟以内进行。
[0093]
(5)将涂抹平板倒置,进行培养直至可以进行菌落计数。
[0094]
(6)通过目视对在涂抹平板增殖的菌落进行计数,用菌落数乘以稀释倍数算出活菌数(cfu/ml)。其中,菌落数过多从而菌落间无法区别的涂抹平板记为tntc(too numerous to count),不进行计数。
[0095]
1-2-2试验物质作用后的活菌数的测定(龟分枝杆菌及偶发分枝杆菌)
[0096]
(1)在试验物质3ml中加入试验菌液150μl并混合。将其作为反应液,反应在室温下
进行。
[0097]
(2)进行规定时间的反应后,抽出反应液50μl,加入到中和剂4.95ml中,进行混合。将其作为102倍稀释液。
[0098]
(3)将102倍稀释液0.3ml加入至中和剂2.7ml并进行10倍稀释。进而通过同样的操作反复进行稀释来制作10倍稀释系列(102~104倍稀释液为止合计3个等级)。
[0099]
(4)将102~104倍稀释液按每100μl分注于7h10平板,并进行涂抹。
[0100]
(5)将涂抹平板倒置,进行培养直至可以进行菌落计数。
[0101]
(6)通过目视对在涂抹平板增殖的菌落进行计数,用菌落数乘以稀释倍数算出活菌数(cfu/ml)。
[0102]
1-2-3初期活菌数的测定(犬小孢子菌)
[0103]
(1)在蒸馏水3ml中加入试验菌液150μl并混合。
[0104]
(2)立即将菌混合液500μl加入至中和剂4.5ml,进行混合。将其作为101倍稀释液。
[0105]
(3)将101倍稀释液0.3ml加入至中和剂2.7ml并进行10倍稀释。进而通过同样的操作反复进行稀释来制作10倍稀释系列(101~103倍稀释液为止合计3个等级)。
[0106]
(4)将101~103倍稀释液按每100μl分注于sablp平板,并进行涂抹。(2)~(4)的工序在30分钟以内进行。
[0107]
(5)将涂抹平板倒置,进行培养直至可以进行菌落计数。
[0108]
(6)通过目视对在涂抹平板增殖的菌落进行计数,用菌落数乘以稀释倍数算出活菌数(cfu/ml)。其中,菌落数过多从而菌落间无法区别的涂抹平板记为tntc,不进行计数。
[0109]
1-2-4试验物质作用后的活菌数的测定(犬小孢子菌)
[0110]
(1)在试验物质3ml中加入试验菌液150μl并混合。将其作为反应液,反应在室温下进行。
[0111]
(2)进行规定时间的反应后,抽出反应液500μl,加入至中和剂4.5ml,进行混合。将其作为101倍稀释液。
[0112]
(3)将101倍稀释液0.3ml加入至中和剂2.7ml并进行10倍稀释。进而通过同样的操作反复进行稀释来制作10倍稀释系列(101~103倍稀释液为止合计3个等级)。
[0113]
(4)将101~103倍稀释液按每100μl分注于sablp平板,并进行涂抹。
[0114]
(5)将涂抹平板倒置,进行培养直至可以进行菌落计数。
[0115]
(6)通过目视对在涂抹平板增殖的菌落进行计数,用菌落数乘以稀释倍数算出活菌数(cfu/ml)。
[0116]
1-2-5log
10
减少(lr)的计算式
[0117]
lr=a-b
[0118]
a:初期活菌数(常用对数值)的平均值
[0119]
b:各试验物质作用后的活菌数(常用对数值)
[0120]
对于龟分枝杆菌及偶发分枝杆菌而言,反应液与中和剂的混合的比例为1:99,涂抹量为100μl,因此活菌数的检测下限值为1000cfu/ml(常用对数值为3)。另外,对于犬小孢子菌而言,反应液与中和剂的混合的比例为1:9,涂抹量为100μl,因此活菌数的检测下限值为100cfu/ml(常用对数值为2)。未检测到菌落的情况下,采用检测下限值,对于lr而言,标注不等号“>”来表示。
[0121]
1-3结果
[0122]
将结果示于下述的表1~3及图1~3。
[0123]
表1
[0124]
对抗酸菌偶发分枝杆菌jcm 6387的杀菌力
[0125][0126]
表2
[0127]
对抗酸菌龟分枝杆菌jcm 6388的杀菌力
[0128][0129]
表3
[0130]
对丝状真菌犬小孢子菌nbrc 32464的杀菌力
[0131][0132]
根据以上的结果可明确,与奥拉昔定制剂ph5相比,奥拉昔定制剂ph8~10对任意试验菌的杀菌力均强。需要说明的是,与奥拉昔定制剂ph8相比,奥拉昔定制剂ph10的杀菌力降低,认为是因为活性受到作为溶解辅助剂添加的pluronic l-44的抑制。
[0133]
实施例2
[0134]
2.奥拉昔定制剂对噬菌体ms2的作用
[0135]
已知噬菌体ms2对消毒剂的感受性低,用于消毒剂对杀诺如病毒的作用等的代替试验。因此,通过使用了噬菌体ms2的试验来评价改变ph而制备的奥拉昔定制剂及市售的消毒剂对病毒的杀病毒效果。
[0136]
2-1试验材料及方法
[0137]
2-1-1试验物质
[0138]
(1)被验物质1
[0139]
名称:奥拉昔定制剂ph5
[0140][0141]
(2)被验物质2
[0142]
名称:奥拉昔定制剂ph7
[0143][0144]
(3)被验物质3
[0145]
名称:奥拉昔定制剂ph8
[0146][0147]
(4)被验物质4
[0148]
名称:奥拉昔定制剂ph8.5
[0149][0150]
(5)被验物质5
[0151]
名称:奥拉昔定制剂ph9
[0152][0153]
(6)被验物质6
[0154]
名称:奥拉昔定制剂ph9.5
[0155][0156]
(7)被验物质7
[0157]
名称:奥拉昔定制剂ph10
[0158][0159][0160]
(8)被验物质8
[0161]
名称:奥拉昔定制剂ph12
[0162][0163]
(9)对照物质
[0164]
名称/简称:消毒用乙醇“kenei(
ケンエー
)”/70%etoh
[0165]
制造销售商:健荣制药株式会社
[0166]
组成:含有76.9~81.4%(v/v)的乙醇(c2h6o)。
[0167]
2-1-2培养基
[0168]
(1)702液体培养基
[0169]
在1l纯水中加入多聚蛋白胨(polypepton)10g、酵母提取物2g、mgso4·
7h2o 1g,进行高压蒸汽灭菌(121℃、20分钟)。
[0170]
(2)软琼脂培养基
[0171]
在纯水0.5l中加入多聚蛋白胨5g、酵母提取物1g、mgso4·
7h2o0.5g、培养基用琼脂3.5g,进行高压蒸汽灭菌(121℃、20分钟)。
[0172]
(3)琼脂平板
[0173]
在trypto-soya琼脂培养基(scd琼脂培养基)“nissui”64g加入纯水1.6l,进行搅拌。对其进行高压蒸汽灭菌(121℃、20分钟)。在琼脂凝固前,按各约20ml地分注到培养皿中并使其固化。
[0174]
2-1-3中和剂
[0175]
在蒸馏水约800ml中加入100g聚山梨酯80、硫代硫酸钠水合物5.0g、磷酸二氢钾0.4g、1ml triton x-100、无水磷酸一氢钠10.1g及大豆卵磷脂11.7g,进行搅拌。进而,加入10.0g tamol(注册商标)nn8906,进行加热及搅拌直至溶解。溶解后,加入1mol/l氢氧化钠溶液,调整至ph7.8~7.9。加入蒸馏水直到总量变为1000ml后,进行高压蒸汽灭菌。
[0176]
2-1-4噬菌体及宿主
[0177]
(1)噬菌体
[0178]
名称/简称:大肠杆菌噬菌体ms2/ms2噬菌体
[0179]
获得地址:独立行政法人制品评价技术基盘机构生物技术中心(nbrc)
[0180]
nbrc编号:102619
[0181]
(2)宿主
[0182]
名称/简称:escherichia coli(migula 1895)castellani and chalmers1919/e.colinbrc13965
[0183]
获得地址:nbrc
[0184]
nbrc编号:13965
[0185]
2-2试验方法
[0186]
2-2-1宿主
[0187]
将保存于酪蛋白胨(
カジトン
)培养基的e.coli nbrc13965接种至702液体培养基5ml
×
4个,在35℃下进行振动一晩的培养。将其加入到702液体培养基180ml中,进而进行3小时振动的培养,将所得者作为宿主培养液。
[0188]
2-2-2噬菌体液
[0189]
噬菌体液使用按照常规方法制备成约6
×
10
12
pfu/ml者。
[0190]
2-2-3杀病毒(噬菌体)试验
[0191]
(1)在试验物质475μl中加入噬菌体液25μl。另外,在作为对照作用液的蒸馏水475μl中加入噬菌体液25μl。
[0192]
(2)室温下进行30秒、1分钟及3分钟作用。对照作用液的作用时间仅设为约3分钟。
[0193]
(3)作用后,采取作用液50μl,加入至中和剂450μl并进行搅拌。将其作为101倍稀释液。
[0194]
(4)将各101倍稀释液20μl加入至中和剂180μl并进行搅拌。将其作为102倍稀释液。重复同样的稀释操作,制作直到109倍为止的10倍等级的稀释液。
[0195]
(5)在102~109倍等级的稀释液100μl中加入宿主培养液0.2ml,进行搅拌。加入在约47℃下保存的软琼脂培养基约5ml,平稳地搅拌后,在琼脂平板上层叠。
[0196]
(6)软琼脂培养基固化后,在35℃下培养一晩。
[0197]
(7)对产生的菌斑数进行计数。
[0198]
(8)通过加权平均法[下述(式1)]算出效价(log
10
pfu/ml)。另外,算出log
10
减少。
[0199]
2-2-5数据解析
[0200]
(1)噬菌体效价
[0201]
通过下式(式1)计算噬菌体效价。
[0202]
pfu/t=(σc1+c2+
…
+c
n
)
÷
((n1+n2×
ν2+
…
+n
n
×
ν
n
)
×
d)
………
(式1)
[0203]
t:加入至平板的稀释液量(本试验中为0.1ml)
[0204]
c1:可计数的最小的稀释倍数的全部平板的菌斑数的合计
[0205]
c2:c1的下一个稀释倍数的全部平板的菌斑数的合计
[0206]
c
n
:最大的稀释倍数的全部平板的菌斑数的合计
[0207]
n1:c1的平板数
[0208]
n2:c2的平板数
[0209]
ν2:c1与c2的稀释倍数的比(本试验中为10-1
)
[0210]
n
n
:c
n
的平板数
[0211]
v
n
:c1与c
n
的稀释倍数的比
[0212]
d:c1的稀释倍数
[0213]
对效价(pfu/ml)进行常用对数变换(log
10
pfu/ml),通过四舍五入用直到小数点后第1位进行表示。效价(pfu/ml)为1以下的情况下,将其常用对数值记为0。
[0214]
(2)log
10
减少(lr)
[0215]
杀病毒(噬菌体)作用通过log
10
减少值来进行评价。
[0216]
lr=a-b
[0217]
a:对照作用液噬菌体效价(常用对数值)的平均值
[0218]
b:各试验物质作用后的噬菌体效价(常用对数值)
[0219]
对于lr而言,通过四舍五入用直到小数后第1位进行表示。需要说明的是,试验物质作用后的效价(常用对数值)为0的情况下,噬菌体效价的检测下限值为3-log
10
,因此用“>(a-3)”表示lr。
[0220]
2-3结果
[0221]
将试验物质的杀病毒作用的评价结果示于表4及图4。
[0222]
表4
[0223]
试验物质的杀噬菌体作用
[0224][0225]
ph5的奥拉昔定制剂几乎未显示杀病毒作用,ph7的奥拉昔定制剂的杀病毒作用与作为对照物质使用的70%乙醇为同等,而对于将ph改变为碱性的奥拉昔定制剂而言,可看到ph越高lr越大的倾向。对于ph8以上的制剂而言,60秒下的lr为3以上,对于ph8.5以上的制剂而言,30秒下的lr为3以上,满足了理想的消毒剂的杀病毒作用的要件即lr3以上。因此可明确,葡萄糖酸奥拉昔定的碱性溶液具有有实用性的杀病毒活性,ph越高,其杀病毒活性变得越强。
[0226]
实施例3
[0227]
3.含乙醇的碱性奥拉昔定制剂对噬菌体ms2的作用
[0228]
本实施例中,出于确认对于碱性奥拉昔定制剂的、由消毒用醇带来的速干性赋予效果及杀菌活性的增强效果的目的,在ph9.5的碱性奥拉昔定制剂中添加乙醇,通过使用了噬菌体ms2的试验评价杀病毒效果。
[0229]
3-1试验物质
[0230]
利用以下的表5的组成,制备被验物质1~3、比较例1、及基剂(对照物质)。
[0231]
表5
[0232][0233]
另外,使用以下的消毒用乙醇作为对照。
[0234]
名称:消毒用乙醇“kenei”[0235]
制造销售商:健荣制药株式会社
[0236]
组成:含有76.9~81.4%(v/v)的乙醇(c2h6o)。
[0237]
3-2试验方法
[0238]
对于杀病毒效果而言,通过上述实施例2的2-1及2-2中记载的使用了噬菌体ms2的方法进行评价。需要说明的是,噬菌体液使用制备成约4
×
10
12
pfu/ml者。
[0239]
3-3结果
[0240]
将试验物质的杀病毒作用的评价结果示于表6及图5。
[0241]
表6
[0242][0243]
根据上述的结果显示,对于含有乙醇的碱性奥拉昔定制剂而言,杀病毒作用也伴随着葡萄糖酸奥拉昔定的浓度而上升,显示了即使为了赋予速干性而添加乙醇,也不妨碍由葡萄糖酸奥拉昔定带来的杀病毒作用。进而显示了,含有乙醇的碱性奥拉昔定制剂比不含有乙醇的碱性奥拉昔定制剂的杀病毒作用高,因此即使在使葡萄糖酸奥拉昔定浓度降低的情况下,也呈现有实用性的杀病毒作用。另外,ph小于7的含乙醇的奥拉昔定制剂(比较例1)中,未看到有实用性的杀病毒活性(lr3以上),因此启示含有乙醇的碱性奥拉昔定制剂中,葡萄糖酸奥拉昔定、乙醇、碱性协同地有助于杀病毒作用。需要说明的是,本实施例中,pluronic f-68是为了减少皮肤粗糙、保湿等而添加的,pluronic f-68为0.5g/100ml的情况下在效力方面也未观察到差异。
[0244]
产业上的可利用性
[0245]
通过使用本发明的组合物,能够制作具有改善的杀菌谱、并且对无包膜病毒也具有效力的含葡萄糖酸奥拉昔定的消毒剂,因此医疗、护理、饮食品产业等领域中的产业上的有用性高。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1