用于热外科汽化及切割组织的方法和装置与流程
相关申请案
本申请案主张2015年1月15日提交的美国申请第62/103,746号临时专利案、2014年9月15日提交的美国申请第62/050,244号临时专利案,以及,2014年12月16日提交的国际申请第pct/il2014/051103号专利案,所述国际申请主张2013年12月18日提交的美国申请第61/917,435号临时专利案的优先权利益,其内容通过引用整体并入本文。
本申请还涉及由麦可·史拉特金(michaelslatkine)、罗南·沙菲特(ronenshavit)、拉菲尔·沙菲特(raphaelshavit)的共同申请、共同审查中及共同转让的pct专利申请案,名称为“用于热组织汽化和压缩的方法和装置”(代理人案卷号63941),其公开内容通过引用并入本文。
技术领域及
背景技术:
本发明在一些实施例中,涉及使用一组织加热及/或汽化元件以切割组织的装置及方法,特别地但不排他地涉及数种用于感测组织汽化元件何时接触组织的装置及方法,并且可选地主要同步加热所述组织汽化元件,或甚而仅在所述组织汽化元件接触所述组织时加热所述组织汽化元件。
已知有用手术探针接触组织进行切割及良好止血的各种技术。一种常见的技术是基于电手术技术。单极电手术单元(esu)可以在正确控制时提供精确的切割。然而,电流会返回到接地垫或金属器械,如腹腔镜管或金属体植入物(例如牙科植入物),可能导致严重烧伤,并导致医疗并发症。示例可参见一篇文章,名称为“预防来自电外科仪器的患者热灼伤”,annereed所著,2013年于现今感染控制的授权转载。
单极电手术单元(esu)并不允许使用于脑部手术。另一方面,双极esu提供显着的组织损伤。虽然esu单元被广泛用于手术,但在许多手术应用中对于精确止血接触切口的需求已经在30年前得到认可。
诸如此种装置的示例为一肖氏(shaw)解剖刀。所述肖氏手术刀是一种锋利的刀片,可以通过内部电线加热到摄氏280度的温度,所述控制器可以在一狭窄的极限内控制所述解剖刀片温度,所述刀片也足够锐利以允许冷切割。所述肖氏手术刀的缺点在于不能用于内窥镜手术,以及相对较慢的加热及冷却时间。所述肖氏手术刀用作连续切割装置,常常导致取决于切割速度的周边热损伤。此外,切割的深度不是自动控制的,并且根据用户应用的垂直及横向力而变化。示例可参见如由willarde.费尔出版的文章,名称为“使用头颈部手术中的shay手术刀”,发表于1981年(7月至8月)的耳鼻喉头颈外科杂志89:515-519。
daikozono的美国第4,736,743号专利案描述用于接触激光手术的医用激光探针,其中例如通过对组织的直接及间接激光加热来进行一手术切割。直接加热通过对所述主体组织的直接激光照射而被以常规方式实现。间接加热通过使用特别涂覆有红外线吸收材料的一探针尖端而被实现。所述材料用作部分吸收及部分透射所述激光能量。所述吸收的激光能量加热所述探针尖端,从而在所述探针被用于接触组织时促成组织汽化。所述传输的激光能量通过其所述常规照射来汽化所述组织。在应用所述红外线材料前,将所述尖端表面粗糙化以增强粘附性,而同时将一光学透明材料放置在所述尖端上,以预防正常尖端使用期间的材料损坏或糜烂。
数个蓝宝石尖端是连接到一光纤的一远端的数个探针。激光馈入所述光纤的一近端,例如激发自钕:钇铝石榴石(nd:yag)的一激光,并且所述光通过全内反射沿着所述光纤传导。所述光学辐射集中在所述尖端并被组织吸收,随后将热量从所述组织传递到所述光纤的所述尖端,并且在所述光纤与组织接触时产生碳化组织的一薄半透明层。所述光纤的一高温远程终端的所述组合,以及通过碳化组织吸收的光的所述组合,用以汽化所述组织,并在所述尖端移动到组织上时提供一切口。这样的一切口比用一聚焦二氧化碳激光器获得的切口的精确度较低,但具有提供触觉反馈的优点。部分地离开所述尖端远程终端并传播进入组织的光,进一步加热所述凝血热损伤外的组织。类似于上述的肖氏手术刀,用蓝宝石尖端获得的一切口深度不能很好地控制。如果一操作者的手沿着不平行于所述组织表面的一曲线移动,则所述切口深度将不均匀,并且通常将跟随所述手的移动曲线。另外,如果手的运动太慢,会产生相当大的热损伤,如果手的运动太快,组织不会汽化,热损伤甚至更大。
其他基于接触切割组织的激光形式利用无蓝宝石探针的裸光纤。在这种情况下,所述薄(大部分达600微米直径)的裸光纤的远端在所述激光器开启的情况下被涂覆碳化组织,随后光吸收被增强。这些切割组织的光纤类似于蓝宝石探针,然而所述光纤是高度脆弱的,并且在短暂使用后经常熔化或断裂。使用一激光作为一光能来源的一热外科接触光纤的示例,是通过medilas、dorniermedtech生产,并在www.dornier.com中叙述的fibertom。
neuberger的美国第6,383,179号专利描述同时切割区域并切除所需组织的一装置。所述装置通过某种手段将激光能量并入一机械解剖刀,使得所述切割区域也遭到切除。例如,一激光源通过某种手段耦合到诸如一金刚石刀的一光学透明刀片上。所述金刚石刀被适当地涂覆,使得辐射仅在数个期望的区域离开。在另一示例中,光纤被嵌入到一锐利的边缘刀片的解剖刀中,意欲耦合到一合适辐射源。
世界知识产权组织公开的第wo2011/013118号专利申请案叙述一种用于在组织中汽化一孔的一装置,包括一汽化元件;一加热元件,被配置成加热所述汽化元件;以及一机构,被配置成将所述汽化元件推进到组织中的特定深度,并且在一期间内,所述期间长到足够使所述汽化元件汽化组织且在短到足以限制热扩散超过源自所述孔的一预定附带损伤距离,从组织中缩回所述汽化元件。还叙述相关装置及方法。
欧洲第ep1563788号专利申请案叙述一种用于诊断宗旨的增强皮肤对分析物的渗透性的方法,或一种用于治疗宗旨的药物,叙述利用微孔及可选地利用音能及一化学增强剂。如果选择,则可以通过频率调制、幅度调制、相位调制及/或其组合来调制音能。微孔的完成是通过(a)通过局部快速加热水来切除所述角质层,使水汽化,从而剥蚀细胞;(b)刺穿所述角质层,一手术刀被校准以形成直径达约1000微米的一微孔;(c)通过将紧密聚焦的一声能束聚焦在所述角质层上,以来切除所述角质层;(d)用一高压喷射流体液压刺穿所述角质层,以形成直径达约1000微米的一微孔;或者,(e)用短脉冲刺穿所述角质层,以形成直径达约1000微米的一微孔。
hakky的美国第5,498,258号专利叙述一种凝结、光激、切除及去除前列腺及膀胱组织的装置及方法。所述装置是包含激光诱导机械切割的一激光切除型内窥镜。所述切割刀片的所述尖端涂有特氟隆(teflon)及不锈钢,以防止所述激光的或切除组织的沾黏。所述接触式激光头及切割刀片通过一激光束加热。这允许所述操作者在不损害组织的细胞完整性的情况下,对所述目标组织进行光激及切除。因此,所述切割的组织被保存用于组织学分析。还提供了一种方法,使用上述具有激光诱导加热的激光切除型内窥镜,从前列腺及膀胱区域凝结、光激、切除及去除组织。
美国第8,808,311号专利叙述数种可耦合到或具有一端部反应器或具有一个端部反应器的一个一次性加载单元的外科器械,以及至少一种操作性地连接到所述外科器械的微机电系统(mems)装置,用于感测一条件、测量一参数及控制所述条件及/或参数。
美国第8,834,461号专利叙述数种用于所述切除组织的装置、系统及方法,实施例包括一切除导管,具有附接到可展开的一载体组件的一切除元件阵列。所述载体组件可以被限制在一导管的所述内腔中,并且被部署为呈现出一扩张状态。所述载体组件包括被配置成以低功率切除组织的多个电极。另外的实施例包括一系统,包括一接口单元,用于递送一种或多种形式的能量到所述切除导管。
美国第8,876,811号专利,一挠性光纤通过机械地弯曲所述光纤,递送激光器的光学辐射到各种手术部位。
上述所有参考文献以及通过本发明提及的公开内容,还有这些参考文献中提及的所有参考文献的公开内容通过引用并入本文。
技术实现要素:
本发明在一些实施例中,涉及使用一组织加热及/或汽化元件以切割组织的装置及方法,特别地但不排他地涉及数种用于感测组织汽化元件何时接触组织的装置及方法,并且可选地主要同步加热所述组织汽化元件,或甚而仅在所述组织汽化元件接触所述组织时加热所述组织汽化元件。
根据本发明的一些实施例的一方面,提供一种用于热切割组织的一装置,包括一组织加热元件;一振荡机构,推进所述组织加热元件朝向组织并使所述组织加热元件从所述组织缩回;一检测器,检测所述组织加热元件何时接触组织的;以及一热控制器,控制所述组织加热元件进行加热,其中控制所述组织加热元件进行加热的热控制器基于检测所述组织加热元件何时接触组织,而控制所述组织加热元件的加热。
根据本发明的一些实施例,所述组织加热元件包括一材料选自由金属及涂有一生物相容性涂层的金属组成的一群组。
根据本发明的一些实施例,还包括一激光器,用于加热所述组织加热元件;及一光纤,用于传导所述激光器的输出到所述组织加热元件。
根据本发明的一些实施例,所述组织加热元件包括一材料选自由蓝宝石、金属及涂有一生物相容性涂层的金属组成的一群组。
根据本发明的一些实施例,所述组织加热元件包括一材料,所述材料对所述激光器发出的光能不透明。
根据本发明的一些实施例,还包括一激光器,用于加热所述组织加热元件;及一光纤,用于传导所述激光器的输出到所述组织,其中所述光纤的一尖端传递热量到所述组织中,从而包括所述加热元件。
根据本发明的一些实施例,还包括一导电元件,用于加热所述组织加热元件。
根据本发明的一些实施例,用于检测所述组织加热元件何时接触所述组织的所述检测器包括:一检测器,以对所述组织加热元件的推进测量一机械阻抗。
根据本发明的一些实施例,推进所述组织加热元件朝向组织并从所述组织缩回所述组织加热元件的所述振荡机构被布置为:用以检测所述组织加热元件何时接触所述组织的所述检测器在所述组织加热元件正在接触所述组织时进行检测,此时使所述组织加热元件朝向组织推进至所述检测器进行检测所处在的位置一段距离以外,所述距离介于0至20毫米的范围内。
根据本发明的一些实施例,推进所述组织加热元件朝向组织并从组织缩回所述组织加热元件的所述振荡机构包括:一电动机。
根据本发明的一些实施例,检测所述组织加热元件何时接触组织的所述检测器包括:一检测器,以测量流到所述电动机的电流。
根据本发明的一些实施例,推进所述组织加热元件朝向组织并从组织缩回所述组织加热元件的所述机构包括:一线性电动机。
根据本发明的一些实施例,提供一种切割组织的方法,其特征在于:所述方法包括步骤:使用用于热切割组织的一装置,用以:自动推进一组织加热元件朝向组织;自动检测所述组织加热元件何时接触组织;及基于检测所述检测组织加热元件何时接触组织,而自动控制所述组织加热元件的加热。
根据本发明的一些实施例,所述方法另包括:将所述组织加热元件自动推进一期望距离,所述期望距离自接触所述组织的一点测量起。
根据本发明的一些实施例,所述方法另包括:从接触组织处自动缩回所述组织加热元件。
根据本发明的一些实施例,所述方法另包括:自动多次推进及缩回所述组织加热元件,以达到进入所述组织而累积推进的一期望深度。
根据本发明的一些实施例,所述方法另包括:使所述组织加热元件相对于所述组织侧向移动,同时使所述组织加热元件多次推进及缩回,而完成切入所述组织的一切口。
根据本发明的一些实施例,所述自动检测所述组织加热元件何时接触组织的步骤包括:测量流到一电动机的电流。
根据本发明的一些实施例,所述自动检测所述组织加热元件何时接触组织的步骤包括:测量所述组织加热元件的一推进速率。
根据本发明的一些实施例,所述测量所述组织加热元件的一推进速率包括:测量所述组织加热元件的一推进量,及通过将所述推进量除以所述推进的一持续时间而计算所述速率。
根据本发明的一些实施例,加热所述组织加热元件被控制为仅在自动检测所述组织加热元件何时接触组织后开始。
根据本发明的一些实施例,加热所述组织加热元件被控制为在自动检测所述组织加热元件何时接触组织后开始进行一期望时期。
根据本发明的一些实施例,加热所述组织加热元件被控制为持续一期望时期后再停止。
根据本发明的一些实施例,基于用于汽化一期望体积的组织所需的热量,而计算用于加热所述组织的所述期望时期。
根据本发明的一些实施例,基于所述组织加热元件接触组织的一横截面乘以在推进所述组织加热元件进入组织并从所述组织缩回所述组织加热元件的一单一回合中的一陷口所需的一深度,而计算汽化组织的一期望体积所需的热量。
根据本发明的一些实施例,所述用于热切割组织的装置包括:一激光器,用于加热所述组织加热元件;及一光纤,用于传导所述激光器输出到所述组织加热元件,其中所述自动控制所述加热组织加热元件加热的步骤包括:引发所述激光器产生输出。
根据本发明的一些实施例,提供一种通过在一组织中汽化一陷口而用于导引材料穿过所述组织的装置,其特征在于:所述装置包括:一组织加热元件;一机构,推进所述组织加热元件朝向组织;一检测器,检测所述组织加热元件何时接触所述组织;及一热控制器,控制所述组织加热元件的加热,其中用于所述组织加热元件的所述热控制器是基于检测所述组织加热元件何时接触组织,而控制所述组织加热元件的加热。
根据本发明的一些实施例,提供一种通过汽化一组织中的陷口而用于导引材料穿过所述组织的方法,其特征在于:所述方法包括步骤:使用用于热切割组织的一装置,用以:自动推进一组织加热元件朝向组织;自动检测所述组织加热元件何时接触组织;及基于所述检测组织加热元件何时接触组织,而自动控制所述组织加热元件的加热。
根据本发明的一些实施例,所述陷口保持开放以导引所述材料的一持续时期在通过愈合形成关闭前是1小时以上。
根据本发明的一些实施例,所述组织加热元件与组织的一接触时间自动保持短于10毫秒。
根据本发明的一些实施例,所述组织加热元件的一尖端的一远程终端的一宽度小于150微米。
根据本发明的一些实施例,在所述组织加热元件的一尖端中包括一材料选自由不锈钢及钛组成的一群组。
根据本发明的一些实施例,所述持续时间是6小时以上。
除非另有定义,本文使用的所有技术和/或科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。尽管类似于或等同于本文所描述的方法和材料可以用于本发明的实施例的实践或测试中,但是下面描述示例性方法和/或材料。在发生冲突的情况下,专利说明书(包括定义)将受到控制。此外,材料,方法和实施例仅是说明性的,并不意图是限制性的。
附图说明
在此仅通过示例的方式参照所述附图和图像来描述本发明的一些实施例。现在具体参考附图和图像,应强调的是,所示的所述细节是作为示例并且为了说明性地讨论本发明的实施例的目的。在这方面,使用附图和图像的描述对于本领域技术人员来说是显而易见的,可以如何实施本发明的实施例。
在所述的图中:
图1a是根据本发明的一示例性实施例用于外科手术中切割组织的一装置的一简化框图;
图1b是使用本发明的一示例性实施例的线性切割过程的一简化框图;
图1c及图1d是根据本发明的一示例性实施例产生线性切口的更详细的图例;
图1e是根据本发明的一示例性实施例产生一线性切口的一简化图例;
图1f是根据本发明的另一示例性实施例的一手持件的一特征示例;
图1g是根据本发明的另一示例性实施例用于在外科手术中切割组织的一装置的一简化框图;
图2a及图2b是根据本发明的数个示例性实施例的加热尖端与组织之间相互作用的简化框图的数个图例;
图3a及3b是现有手术激光器技术基于蓝宝石接触尖端及组织之间相互作用的简化框图的数个图例;
图4a及图4b是根据本发明的一示例性实施例产生固定深度的切口的简化框图的数个图例;
图5是根据锥形蓝宝石尖端的现有技术实施例的一切口的一简化框图的图例;
图6是本发明的一示例性实施例的一简化横截面图的图例;
图7是根据本发明的一示例性实施例制造的用于陷口深度控制方法的简化流程图的图例;
图8a是根据本发明的一示例性实施例在一尖端阵列及在空气中驱动一尖端阵列的一线性电动机的一驱动电流的位置的一示波器迹线;
图8b是根据本发明的一示例性实施例在一尖端阵列及一线性电动机的一驱动电流包括阻碍皮肤接触的一时段的位置的一示波器迹线;
图9a及图9b是描绘根据本发明的另一示例性实施例的涂有镍涂层随后涂金的铜尖端的横截面图像;
图9c是绘示图9a及图9b的所述示例性实施例沿着所述铜尖端及所述镍随后镀金的距离以元素浓度作为一函数的图形;
图10是根据本发明的数个示例性实施例的治疗探针尖端的一简化图例;
图11是根据本发明的一示例性实施例在治疗后立即在人体内皮肤产生汽化的陷口的一组织学横截面的照片;
图12是根据本发明的一示例性实施例切割组织的一示例应用的一简化横截面图例;
图13是根据本发明的一示例性实施例切割组织的一示例应用的一简化横截面图例;
图14是根据本发明的一示例性实施例的一尖端阵列、一手持件及所述手持件的一特征列表的一简化图例;
图15a、图15b及图15c是根据本发明的一示例性实施例的一热机械切除(tma)过程的数个简化图例;
图16是根据本发明的一示例性实施例的通过施加加热尖端产生的各种效果列表的一简化图例;
图17包含根据本发明的各种示例性实施例使用各种治疗尖端在各种治疗模式治疗组织的的九个横截面图像;
图18是根据本发明的一示例性实施例的一尖端阵列及所述尖端阵列的描述的一简化图例。
图19是根据本发明的一示例性实施例可选地使用于一尖端阵列的一条形码及关于所述尖端阵列的另一种可选的特征叙述的一简化图例;
图20是根据本发明的一示例性实施例的一手持件与关于所述手持件可选的特征叙述的一简化图例;
图21是根据本发明的一示例性实施例用于热手术汽化及组织切割的系统及关于所述系统2102可选的特征描述的一简化图例;
图22a及22b包括根据本发明的一示例性实施例在一实验中治疗组织及关于所述实验中所发现的叙述的一横截面图像;
图23是将根据本发明的一示例性实施例的名为替梭(tixel)与一分段二氧化碳激光治疗进行比较的一表格;
图24是根据本发明的一示例性实施例的一尖端阵列及一治疗系统的一简化图例;
图25是根据本发明的一示例性实施例的一手持件的一简化图例;
图26a至图26d是根据本发明的另一个示例性实施例的一手持件的简化图例;
图27是根据本发明的一示例性实施例的一手持件的横截面的半前视的一简化图例;
图28是根据本发明到目前为止的另一个示例性实施例的一手持件的一简化图例;
图29是根据本发明的一示例性实施例的一尖端及所述尖端的一叙述的一简化图例;
图30是根据本发明的一示例性实施例的一尖端及两个表格的一简化图例;
图31是根据本发明的一示例性实施例的一尖端阵列的一图像;
图32a是根据本发明的一示例性实施例用于施加到小牛肝脏的热手术汽化及组织切割的一手持件的一图像;
图32b是根据本发明的一示例性实施例将图32a的所述手持件应用到小牛的肝的一图像;
图32c是根据本发明的一示例性实施例以一加热的线性尖端阵列切割小牛的肝的一图像;
图32d是根据本发明的另一个示例性实施例将图32a的一尖端阵列应用到小牛的肝的一图像;
图33是根据本发明的一示例性实施例的一尖端、一尖端握把及一表格的一简化图例;
图34是根据本发明的一示例性实施例的一尖端、一尖端阵列及一表格的一简化图例;
图35是根据本发明的一示例性实施例用于切割组织的方法的一简化流程图例;及
图36是根据本发明的一示例性实施例在一组织中通过汽化一陷口而用于导引材料穿过所述组织的一简化流程图例。
具体实施方式
本发明在一些实施例中,涉及使用一组织加热及/或汽化元件以切割组织的装置及方法,特别地但不排他地涉及数种用于感测组织汽化元件何时接触组织的装置及方法,并且可选地主要同步加热所述组织汽化元件,或甚而仅在所述组织汽化元件接触所述组织时加热所述组织汽化元件。
综述:
本发明的一些实施例的一方面包括自动推进一加热及/或汽化元件朝向组织,决定所述汽化元件何时接触所述组织,加热所述汽化元件以便用于汽化所述汽化元件接触的组织,以及自动从接触的组织缩回所述汽化元件。
遍及本说明书及权利要求书中被使用的所述术语“汽化元件”的所有语法形式,与一术语“加热元件”及其对应的语法形式可互换地使用。
在一些实施例中,可以基于数个温度设置、控制温度升高速率、控制加热持续时间等,可选地实现对组织的上述效果。
本发明的一些实施例的一方面包括如何感测所述汽化元件何时接触组织。在一些实施例中,推进所述汽化元件的是一电动机,可选地是一线性电动机。当所述汽化元件接触组织时,所述推进需要抵抗一增加的对立而推进,在一些实施例中,可选地被感测到。在一些实施例中,所述增加的对立以可选地减慢所述推进的移动,并且所述减速可选地被感测到。
本发明的一些实施例的一方面包括通过推进所述汽化元件的多少以及相对于什么时间点或空间点来确定。在一些实施例中,相对于所述汽化元件与组织的一接触点确定所述推进距离。在一些实施例中,通过所述汽化元件的推进在组织中产生的一汽化的陷口的深度,而决定所述推进的距离。
本发明的一些实施例的一方面包括产生所述汽化元件的重复推进。在一些实施例中,在组织的一个位置进行重复的推进,可选地在组织中汽化较一单个推进还深的一陷口。在一些实施例中,推进所述汽化元件的一装置被保持就定位,并且可选地可从所述汽化元件接触组织的第一点测量所述汽化元件的推进,可选地测量所述组织汽化的累积深度。在一些实施例中,将汽化组织的一期望深度作为进入一控制单元的输入,并且可选地以一次或重复推进所述汽化元件,直到汽化所述组织的深度到达所述期望深度。
本发明的一些实施例的一方面包括重复推进所述汽化元件,同时侧向移动所述汽化元件。在一些实施例中,这种组织的重复陷口可选地在组织中产生一切口。在一些实施例中,如上所述的测量或控制所述切口的一深度。
本发明的一些实施例的一个方面包括决定何时加热所述汽化元件。在一些实施例中,所述汽化元件仅在接触组织时被加热,可选地如上所述而被决定。
本发明的一些实施例的一方面包括决定在单次脉冲推进及缩回时应用于所述汽化元件的热量。在一些实施例中,基于汽化组织的一期望体积所需的热量而计算热量。在一些实施例中,基于所述汽化元件接触组织的横截面乘以在单个脉冲中的一陷口的一期望深度,而计算组织的期望体积。在一些实施例中,计算出的热量大于汽化组织的一期望体积所需的热量,以允许汽化的组织呈现稍微绝缘屏障,以从所述汽化元件传热到所述组织。在一些实施例中,计算出的热量大于汽化组织的一期望体积所需的热量,以允许在所述应用中的热量损失。
本发明的一些实施例的一方面包括决定如何加热所述汽化元件。在一些实施例中,通过沿着一光纤光导管输送激光能量来进行加热,使得所述激光能量在所述光纤光导管的所述端加热一汽化元件。这种汽化元件详述如下。用于制造这种汽化元件的一些非限制性示例的材料包括:蓝宝石、涂有生物相容性涂层的一金属等。
在一些实施例中,通过沿着一光纤光导管输送激光能量来执行加热,使得需要这种加热时以激光能量加热组织。在这样的实施例中,实际上没有汽化元件。然而,本领域技术人员将理解,仍然可以感测到光纤朝向组织推进并接触组织,因此,上述实施例在所述汽化元件接触组织时利用感测,可以被理解为意指促使光纤与组织接触。
在一些实施例中,通过在所述汽化元件处的一导电元件或一导电箔的电热以进行加热。在一些实施例中,所述导电元件或箔是所述汽化元件本身。
本发明的一些实施例的一方面包括所述汽化元件的尺寸及/或大小及/或形状。在一些实施例中,所述尺寸被设计成大致对应于期望在所述组织中制造的孔或陷口的尺寸。在一些实施例中,通过在组织中边对边地重复制造孔,而在组织中制造被期望的一切口宽度,以大致对应于所设计的大小。在一些实施例中,产生所述汽化元件的形状,以便于制造所需的孔或切口。作为非限制性示例,在一些实施例中,所述汽化元件可选地被成形为一细长元件,有利于进行一线性切割。作为另一个非限制性示例,在一些实施例中,所述汽化元件可选地成形为汽化元件的一线性阵列,也有助于进行一线性切割。
本发明的一些实施例的一方面包括选择用于制造所述汽化元件的一材料。在一些实施例中,选择为具有高导热性的所述材料。在一些实施例中,所选择的材料具有一特定范围的一热容量,以便在加热时含有足够的热量,以汽化一期望量的组织,对应于在组织中形成所需深度的孔或切口及/或以便在不加热时快速失热,从而使得在组织附近具有最小可能损伤的一热汽化元件。
本发明的一些实施例的一方面包括涂覆所述汽化元件。在这样的实施例中,可选地以一个或多个层中的一种或多种涂层材料涂覆一第一材料以建构所述汽化元件的芯材。在一些实施例中,所述涂层防止所述芯材与组织接触,特别是,当芯材冷时及/或当芯材被加热到一组织汽化温度,如果芯材不被认为安全地接触生物组织者。
在一些实施例中,根据温度设置,温度上升设置速率等可选地实现上述对组织的效果。
目前基于激光器的热接触探针的一些主要缺点是:
a)激光器辐射从一蓝宝石探针或一光纤远程终端泄漏到组织中。所述泄漏导致更深的凝血及更少的出血。然而,由于大的周边热损伤区域,所述切口不太精确,导致愈合愈慢。组织的碳化也是常见的注意,在本发明的一些实施例中,用于手术的一加热尖端可选地是不透明的,在一些情况下是光纤上的金属涂层,潜在地防止激光器辐射泄漏。
b)主要使用nd:yag或二极管激光器的激光器是大功率激光器,在主要手术应用的功率可能超过30瓦,一些用于牙科的激光器可能使用5至10瓦,这样的激光器相对较大而且昂贵。此外,这些激光器甚至5w激光器受到高等级,大多是iv等级医疗法规的要求,并且要求严格的安全预防措施,因为它们直接与组织相互作用。因此,这样的激光器在任何情况下都是非常昂贵的。此外,手术室工作人员必须使用不舒适的安全眼镜。应当注意,在本发明的一些实施例中,所述尖端具有低热容量,例如通过非限制性示例具有薄的中空金属尖端,使得能够使用相对较低功率的激光器,平均功率为~1至10瓦的极限示例激光器。
还应注意,在本发明的一些实施例中,可选地使用一脉冲激光器,可选地与接触组织的尖端同步。这些实施例潜在地使用较少的功率。
c)切口深度是不好控制的。
d)切口深度不固定并受到控制,因为操作者的手可以用一变化的速度移动,并且改变垂直及侧向切割力以及在组织上的停留时间。
本发明在一些实施例中包括外科手术方法及装置,更具体地但不排他地包括用于外科手术中的组织切割及汽化的方法及装置,甚至更具体地但不排他地包括方法以及用于显微外科手术的装置,例如神经外科手术,耳鼻喉科(ent)手术,牙科学,通过组织递送药物及腹腔镜检查等。
在本说明书何权利要求书中到处被使用的所述术语“组织”的所有语法形式,并且与术语“皮肤”及其对应的语法形式可互换地使用。本发明的各种实施例及实施例对治疗组织描述的参考,也意图适用于治疗皮肤。
在整个本说明书及权利要求书中到处被使用语法形式中的术语“陷口”,并且与术语“压缩”及其相应的语法形式可互换地使用。本发明的各种实施例及实施例被描述为在组织中产生陷口的,也适用于在组织中产生凹陷。
是本发明的实施例的一个目的是克服现有技术的缺点。
本发明的实施例的一个目的是控制带有高温尖端的组织的一汽化深度。
本发明的实施例的一个目的是改善患者的愈后状况。
本发明的一些实施例的一方面包括使用一加热棒的尖端,以最小的附带损伤产生组织的切口,并且不损伤底下的组织。
在一些实施例中,所述尖端的一远端大部分是金属的。
在一些实施例中,所述尖端的一远端是不透明的。
在一些实施例中,所述尖端的加热温度在摄氏100及850度之间。
在一些实施例中,一汽化元件,例如一汽化杆,具有成形为特定截头形状的一远端,适用于在短时间内供应大量的热量以汽化组织,而在一些实施例中也避免所述组织的碳化。
在一些实施例中,在所述组织中产生数个孔(holes)、数个凹槽(grooves)、数个陷口(craters)及/或数个凹陷(indentations)。
在一些实施例中,锥形或方锥体汽化尖端用于切割组织,潜在地减少或消除碳化。
在一些实施例中,切割被执行到一固定深度,而无关施加的速度及/或摇动。
本发明的一些实施例的一方面是精确地汽化组织而不会对下面的细微组织或金属部件造成损害,例如通过非限制性示例,诸如牙种植体的植入物。
本发明的一些实施例的一方面包括检测一手术远程尖端何时接触皮肤。
在一些实施例中,通过感测所述尖端推抵皮肤的机械阻力来进行所述检测。当针对特定深度及/或外科手术部位的所述陷口或切口形状时,检测尖端何时接触皮肤接触是有意义的。
在一些实施例中,通过测量所述(数个)尖端的一推进速度以及检测所述(数个)尖端运动何时被所述组织减慢来进行检测。
在一些实施例中,通过测量如推进所述(数个)尖端所需的电流或电压或脉冲宽度(在脉宽调制下)来执行检测。当所述(数个)尖端与组织接触时,改变保持推进所需的电参数,并且可选地检测与组织的接触。
本发明的一些实施例的另一方面是朝向组织振动所述切割尖端并退出,以便与组织产生非常短的接触期间,致使切口及/或陷口的一潜在清洁汽化。
本发明的一些实施例的另一方面是将尖端朝向组织振动并以高频率退回,致使汽化陷口的重迭及一洁净切割。
本发明的一些实施例的另一方面是使切口尖端朝向组织振动并以高频退出,实际上允许一用户在组织表面上保持固定的距离,所述频率高于一用户反应速度。
本发明的一些实施例的另一方面包括以足够高的频率振动所述切割尖端朝向及退出与组织的接触,从而能够通过利用一组织接触检测机构自动产生一固定深度切口。
本发明的一些实施例的另一方面包括使用通过一光波导或光纤递送的一系列脉冲激光器辐射朝向一汽化/切割组织,并与所述尖端的推进及其与组织的接触同步。
在一些实施例中,通过所述光波导或光纤的激光器辐射与光纤缩回同步地被停用。所述同步潜在地使得能够产生极精确及安全的手术切割及/或减少热损伤及/或减少碳化。
本发明的一些实施例的另一方面是利用具有短热松弛时间的不透明金属中空尖端,以便将所述尖端快速加热至高达摄氏100至850的温度,并在短时间内递送大部分能量至组织。
本发明的一些实施例的另一方面是在牙科及口腔颌面外科、神经外科学、耳鼻喉科(ent)、内窥镜检查、妇科(gyn),包括腹腔镜检查,脊柱手术及普通外科手术中,进行非常精确的组织切割或汽化。
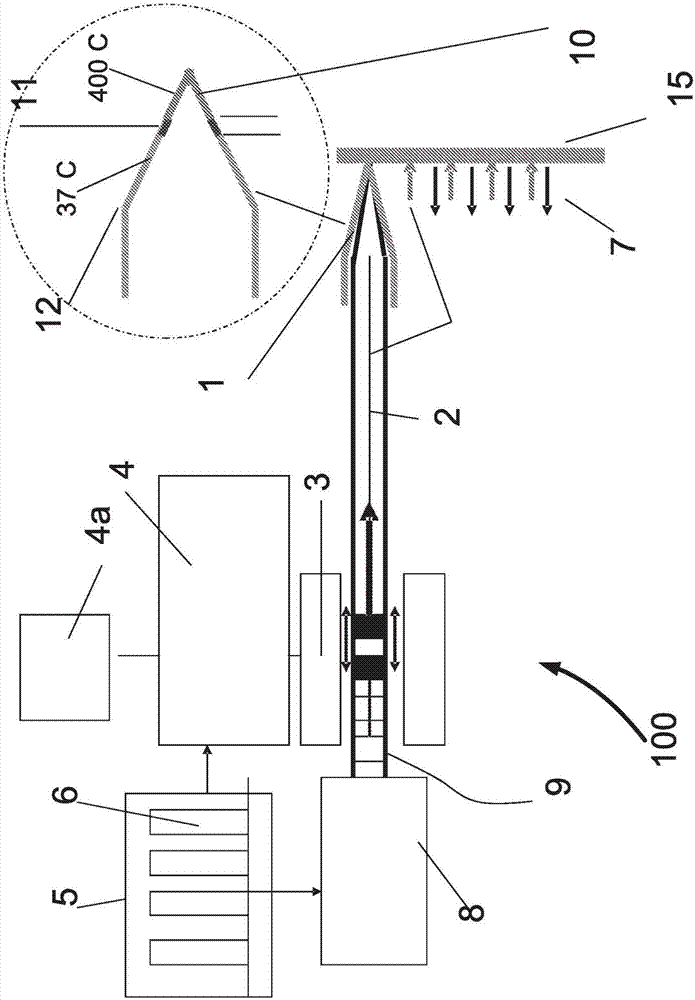
现在参考图1a,这是根据本发明的示例性实施例用于在外科手术中切割组织的装置100的一简化框图。
图1a绘示出附接到一光波导或光纤2的一远端的一中空金属尖端1。尽管可以使用其他尖端,但是图1a叙述一种专门利用中空尖端的应用。所述中空金属尖端1可选地可具有不同的形状,例如圆锥形或凿状或球形或圆柱形或方锥形。所述尖端材料可以具有高的导热率,例如150至400w/m℃(诸如钨或铜的热导率),并且可以具有低导热率,例如低于30w/m℃(例如不锈钢或钛),在下面将要解释的各种应用中。
在某些示例性应用中,需要高导热性。所述金属尖端1是不透明的。所述光波导2可选地通过一附接元件3,而可选地附接到一电动机4。一电动机4(可以是线性的或旋转的)能够使所述光纤2及尖端1朝向一组织表面15及从所述组织表面15后退。运动速度以及位置及加速度(基于5至30微米的位置精度)被潜在而精确地知道,并且一电动机控制器4a可选地感测尖端1及组织15之间的接触,可选地基于组织15对尖端1的阻抗。基于感测组织接触,所述控制器4a可选地控制电动机4的速度、加速度及位置,从而致使潜在而精确地控制尖端1接触组织的期间t,以及精确测量及/或控制一接触深度。一激光器8可选地是一二极管激光器、沿着所述光纤或光波导2朝向所述中空尖端1传播而发射的一脉冲束9。
一主时脉5可选地产生电脉冲6,所述电脉冲6可选地馈送到激光二极管8及所述电动机4的其中一个或两个,致使光纤运动与来自所述激光器8的发射的光束之间的同步。所述电脉冲导致所述尖端1的一振荡运动7,从而尖端与组织接触时可选地被加热,并且可选地在收缩时不被加热。所述短接触时间潜在地确保一高尖端温度,例如摄氏400至850度,这能够清洁及精确的汽化,无关外科医生的手速度。此外,由于相对于感测组织接触的切割尖端测量,一切口深度潜在地是固定,而无关外科医生的垂直手部移动(甚至手抖动)以及潜在地独立于组织表面曲率。
在一些实施例中,可选地受控的深度在0至20毫米的范围内。
在一些实施例中,通过测量所述组织加热元件的所述尖端在检测到所述尖端接触组织后推进的一距离,以控制所述可选择的受控深度。
所述可选地受控的深度在微创手术过程中是潜在的有益的,诸如打开组织以覆盖一牙科植入物,或诸如声带上的小损伤的汽化或输卵管壁的线性切割或脑损伤的汽化。
用于一般手术或牙科的一外科手术用具的典型参数包括,作为非限制性示例的:
一激光功率水平为5至15瓦;一光纤直径为400至1000微米;一尖端形状:锥形或凿状,具有锥形半角~10至20度(全角20至40度);振荡运动幅度为1至10毫米(可选地还取决于组织曲率,如下面参考图4b所述;以及振荡频率20至100赫兹(hz),这取决于切割深度及速度。在一些实施例中,所述振荡频率取决于切割速度-当一用户的手高速移动时,用于一快速切割,所述频率增加并且防止陷口之间的间隙。在一些实施例中,振荡频率取决于所需的深度-可选地防止陷口之间的重迭,以便通过在相同位置推进两次而不产生一深陷口,从而深化所述陷口。尖端材料:钨,是生物相容的,具有高导热性(~150w/m℃)。尖端壁厚~100至200微米。加热时的远端温度:摄氏400至850度。手持件长度100至200毫米。
在本发明的一些实施例中,所述光纤2在所述激光器8及所述附接机构3之间的部分是挠性的,潜在地允许所述激光器及其电源供应器的位置远离外科手持件18,包括电动机/控制器,光纤2的远端部分及所述切割尖端1。在这种示例性实施例中,所述高温尖端1远离一光学加热源。
图1a还绘示出所述远程尖端更详细的一放大图。中空尖端1的壁可选地在其远程部分中形成为锥体,并且作为其近端部分中的圆柱形部分,以便能够牢固地附接到光波导。2.可选地选择尖端壁的尺寸(如下面的计算所示),以确保用于组织切口的高温远端10,同时在近似(向后)约300微米的一位置12处约维持约摄氏37度的体温。温度从约摄氏400至850度降到约摄氏37度的一短段11约为300微米长。
现在参考图1b,这是使用本发明的示例性实施例的线性切割过程的一简化框图的图例。
图1b绘示出一种在以一速度v移动一外科手持件时,通过推进与缩回尖端1产生一系列的陷口13。组织切除与激光脉冲的同步如图所示,以及在一缩回阶段以停止光学加热致使一尖端冷却。一尖端远程终端14a可选地汽化带有非常浅的侧支热损伤的陷口14。当所述速度v高时,潜在地仅产生一列陷口,可选地不产生一连续的切口。这样的一列陷口,是潜在地有用于汽化如声带的薄型病变。这种实施例的一优点在于,尽管一速度v可能是高的,但组织汽化会发生且是干净及均匀的。这对比于使用最先进的蓝宝石尖端,所述蓝宝石尖端的高速度更快过能量递送速度,会留下组织撕裂或热损伤。
现在参考图1c及图1d,这些是根据本发明的示例性实施例产生线切口的更详细的数个图例。
图1c绘示出诸如图1a的示例性实施例通过一尖端创造一组织切口,此处所述速度v根据一脉动速率而被调节。所述调节致使在所述陷口13之间可选的轻微重迭,并且产生恒定深度的一无焦切口16。
图1d绘示出图1c的所述切口的另一视图。需要注意的是,如果速度v较慢,则可选地产生一更深的陷口,并且仍然不会焦化。
在一些实施例中,一外科医生可选地可注意到所述较深的陷口,并且可选地增加速度v。
现在参考图1e,这是根据本发明的示例性实施例产生一线切口的一简化图例。
图1e绘示出一外科医生操作一切割手持件18的一示例性实施例的一简化图例。所述外科医生可选地在所述手持件18的尖端是冷的时候,将所述手持件18放置在组织上。在激活所述手持件18上,可选地通过用手指20按压一开关19,所述手柄18开始所述切割过程并创造一切口21。当所述外科医生想要停止时,所述外科医生可选地按压所述开关19。所述开关19可选地可为一脚踏开关。
现在参考图1f,这是根据本发明的另一示例性实施例的手持件的一特征的一图例。
图1f意图绘示出当所述手持件的所述尖端不接触组织时,尽管可以激活一开关19a,但是所述尖端是冷的,并且情况是安全的。
现在参考图1g,这是根据本发明的另一示例性实施例用于在外科手术中切割组织的装置150的一简化框图的图例。
图1g绘示出本发明的一实施例,在此所述激光加热器通过与电动机运动同步的一电流发生器148而被取代。通过一电线19递送的加热能量也如图中放大的部分所示。所述电线149被热耦合到所述尖端,并且在一些实施例中,所述治疗尖端可选地涂覆有不导电的一氧化层。
图1g未绘示的加热所述治疗尖端的其他方式,包括以一振荡磁场(感应加热)或超声波加热在所述尖端中产生涡电流。
现在参考图2a及图2b,这是根据本发明的示例性实施例的一加热尖端与组织之间相互作用的数个简化框图的图例。
图2a更详细地绘示出具有一加热光束25的一示例锥形末端26。图2a中的一些示例特征是一不透明的尖端,并且通过将热从所述尖端的一高温远程终端24传递到组织而产生汽化能量。
图2b更详细地绘示出具有加热光束25的一示例凿形的尖端。图2b中的一些示例特征是通过将热从所述尖端26的一高温远程终端传递到组织而产生汽化能量的一不透明尖端。
现在参考图3a及图3b,这些是现有技术基于蓝宝石的手术激光器接触尖端与组织之间相互作用的简化框图;
图3a及图3b呈现蓝宝石或类似蓝宝石尖端形状的光纤尖端的一组织相互作用。除了由于组织碳化引起的热传递之外,光传播到组织中并参与一加热过程。
现在参考图4a及图4b,这是根据本发明的示例性实施例产生固定深度的一切口的数个简化框图的图例。
图4a中的曲线40a绘示出一外科医生的手在组织上的高度h(t)处以速度v的一不规则运动的一示例。h可能随时间变化,例如在1至4毫米之间。所述不规则性可能是由手抖动或分心或视力不佳引起的。结果,所述手持件的一远程终端(排除一尖端的所述手持件)遵循一曲线41a。在激活所述手持件的同时,由于尖端及光纤42可选地推进直到组织接触被建立,并且通过一电动机控制器可选地感测,深度d的汽化将会发生且与沿所述切割线相同。
图4b还绘示出类似的效果,在组织表面不平坦而弯曲的一示例中。再次,切口是无焦的并且深度恒定。
现在参考图5,这是根据现有锥形蓝宝石尖端技术实施例产生一切口的一简化框图。
外科医生手部运动的所述不规则性可能被转化为深度d(t)的一不规则切口。应注意的是,使用图4a及图4b所示的示例性实施例方法可以潜在地校正蓝宝石顶端外科器械的所述不规则切口深度以具有一固定切口深度。
下表(表1)列出了几种类型的接触手术单元的特征及本发明的示例性实施例之间的一些潜在的差异:
应注意,并非所有发明特征都应用于每个外科手术切口。例如,如果振荡频率高(例如30赫兹或稍高),则一外科医生可能会感觉到所述外科手持件与组织的接触。
在另一示例中,所述加热可以连续地操作,并且所述尖端将表现为常规热刀,可选地具有一受控深度。
一手术切口的一示例实施例:
一外科医生想要通过创造10毫米长度、2毫米深度及200微米宽的一切口,以暴露一牙种植体。沿同一行的切割可选地是逐层重复。假设每层是100微米深。因此,所述外科医生将必须重复所述切割过程20次(20遍)。
每个切割(汽化)层的体积为0.2×10×0.1立方毫米(mm3)=0.2mm3。汽化1mm3的组织所需的所述能量约为3焦耳/立方毫米(joule/mm3)。结果,汽化单一切割层所需的所述能量为0.6焦耳。扩充功能选项更多如果植入物曝光步骤的期间为10秒,则每个切割层的期间为10/20=0.5秒。结果,在0.5秒内切割单一组织层所需的功率水平为0.6/0.5焦耳/秒=1.2瓦特。因此,我们看到一个5至10瓦特的小型便宜的工业二极管激光器可以很容易地提供所述功率用于这样的一切口,并且所述切割速度可能潜在地会更快。
基于200微米的一切口宽度,可以使用及加热200微米宽的一远程尖端。假设一凿状尖端,沿所述切口线的陷口数量可以是10毫米/0.2毫米=50个陷口。每个陷口的所述汽化期间可以为0.5秒/50=10毫秒。10毫秒的期间可以分为两个步骤,组织接触及汽化为5毫秒,非接触运动为5毫秒(缩回及回到组织)。应注意的是,5瓦特的激光将使用5毫秒的一汽化时间。
接下来评估所述尖端的所需功能。假设利用具有300微米壁厚及凿状的一中空钨头。为了在5毫秒内实现陷口汽化,在l=300微米的距离,所述治疗尖端热松弛时间应小于5毫秒。一材料的所述热松弛时间tr通过tr~0.5(cρ/k)l^2给出,由此ρ=密度、c=比热容、k=热导率。在钨的情况下,k=170瓦/毫秒(w/msec)、c=0.13j/gr、ρ=19gr/cm3。结果tr=0.6毫秒,l=300微米。在1毫米尺寸的尖端的情况下,tr~9x0.6~5毫秒。
在这样一个例子中,一期望宽度是300微米,这是足够强的,使得所述尖端不会断裂或弯曲,并且潜在地能够在缩回时快速冷却。
用于手术的组织传感技术:
现在参考图6,这是本发明的示例性实施例的一简化横截面图。
还参考图1a,图1a的电动机4可以是瑞士faulhaberminimotorsa生产的一旋转电动机或一线性电动机。
图6呈现在图1a中的通常描述的组织传感技术的一更详细的描述。
一外科用手持件31可以具有一“左轮手枪”形状。所述外科用手持件31还可以具有图6中未示出的其它形状,例如图1e及图1f所示的一直线笔形状。一线性电动机30可选地位于所述手持件31中,所述手持件31也可以包括一位置编码器32,如图6所示。所述位置编码器32潜在地提供一杆33的一位置,所述杆33包括图1a中描述的所述光纤/光导及治疗金属探针(未示出),并且相对在所述手持件31中的一参考位置通过电动机30驱动。所述杆33及光纤及远程治疗探针被推向组织(未示出),并且从可选地放置一远程覆盖物34的组织处退回。
在一些实施例中,所述远程盖34可以是薄的并且细长的,例如当所述手持件具有笔形时。所述远程盖34可以并入数个孔,以便能够将空气吸入手持件31。
在本发明的一些实施例中,所述手持式封套由两部分组成。
所述位置编码器32潜在地提供1微米的位置精度,并且可以是磁阵列型编码器(例如由德州仪器公司生产的磁型编码器)或一光学编码器或一霍尔效应检测器。
所述线性电动机可以在一恒定电压工作,并且可以通过一控制器35来控制通过其施加在光纤及治疗探针上的力,可选地通过调制施加到所述电动机的脉冲宽度(脉冲宽度调制-pwm)来控制。
所述杆33的速度等于所述尖端的速度,可选地通过得知所述杆的位置来监视。随着朝向组织的推进及接触到治疗的组织(这可能在到达一目标切割深度后发生),如果皮肤机械顺应性较低,则杆33的所述速度可能会被降低。通过非限制性示例的方式,这在薄组织上可能发生,诸如覆盖骨的牙龈或在几乎到达一硬牙植体表面时。
通常,在组织的机械阻抗及空气的机械阻抗之间存在差异,导致通过测量杆/尖端的运动的机械阻抗,而获得在空气及组织之间的良好差异。在许多手术切割中,如图12所示,绘示出在一牙植入物上切割的一示例,通过用一镊子抓住组织,而可选地进一步增强组织的机械阻抗。
对于切口深度控制,可以实现深度控制策略的各种非限制性示例。
根据一第一深度控制策略,一旦检测到速度降低,一控制器可选地修改施加到所述电动机的所述脉冲宽度,直到恢复速度。所述杆33可选地继续其运动,直到达到一预选深度,由此逆转杆速度并且缩回尖端。
根据一第二深度控制策略,所述控制器测量杆减速,并且计算杆推进距离,以便实现一预设切口深度以及在组织中的一尖端停留时间。这种闭环控制机制潜在地使带有优良深度精度的陷口汽化潜在地与组织类型无关(从机械顺应性观点),并且潜在地与组织位置无关(例如图4b所示的弯曲组织)。
在一些实施例中,可以减少对外科医生的手的稳定性的要求,或者可以减少机器人手术中的治疗手的稳定性,导致成本降低。由于在许多治疗中,机械性皮肤顺应性与临床副作用(例如因为机械冲击或损伤引起的损伤)之间存在直接关系,因此还潜在地获得对副作用的一有益控制。
现在参考图7,这是根据本发明的示例性实施例的一种用于制造陷口的深度控制方法的一简化流程图。
图7绘示出的所述方法包括:
提供一个或多个输入参数,例如:尖端类型、尖端数量、尖端形状、尖端尺寸、在组织中的期间、来自装置的尖端突出、脉冲重复率、加热功率水平、激光功率水平等(702);
放置一手持件在一治疗处并激活一触发(705);
使用一电动机,可选地为一线性电动机,可选地基于所述输入参数的一速率,推进一治疗尖端或数个尖端朝向组织,可选地转换为用于控制电动机(707)的脉宽调制(pwm)参数;
推进所述(数个)治疗尖端进入组织,从而产生数个陷口,可选地同时监测速度或推进距离(710);
达到(数个)尖端推进的目标深度,可选地允许所述(数个)尖端在短时间内保持在目标深度,可选地允许数个尖端推抵组织(712);
降低(数个)尖端速度,可选地基于测量所述组织的机械阻力以向前运动进入组织(715);
在一些实施例中,所述尖端接触组织并开始汽化所述组织。当所述尖端汽化组织时,对所述尖端移动的所述皮肤阻抗相对较低-所述皮肤符合所述尖端运动。在一些实施例中,决定一汽化深度h取决于递送到所述尖端的能量。通过决定用于尖端接处组织的一期间及/或通过决定诸如一激光器的一加热单元的一功率水平,可选地执行一汽化深度h的决定。一旦达到所述汽化深度h,例如200微米,所述组织(陷口底部)开始抵抗所述尖端的移动,因为它不再被汽化,仅潜在地通过接触而被加热。可选地对于尖端运动的阻抗的一测量提供数据,这在一些实施例中被用作汽化已经结束的一标志,并且可选地可引起所述尖端撤回的决定。在一些实施例中,汽化深度的估计可选地可取决于加热参数及期间,并且很少取决于外科医生的手移动,因为在实施例中,所述深度h取决于接触检测。在一些实施例中,所述汽化深度具有对接触检测的依赖性,因为无接触检测,所述尖端可能在所述陷口中接触组织而停留一较长期间,例如30毫秒,并开始加热组织且引起周边热损伤。
可选地,一控制器基于测量模式自动地选择新的操作参数,可选地将新的操作参数转换为新的(脉波宽度调制)程序(717);及
可选地重复705至715或705至717中的某一些(720)。
图7绘示出数个陷口的汽化深度的闭环控制的一示例性实施例的一示意性描述,而无论皮肤顺应性及外科医生的手相对于组织的精确垂直位置为何。通过移动外科医生的手,可选地产生数个陷口的一线性阵列,潜在地导致一线性切口。
在本发明的一些实施例中,可能通过测量一金属手术探针及组织之间的电阻抗,而实现组织接触感测。只要一探针尖端与组织不接触,电阻可能近似无限大。在接触后,取决于组织类型,电阻抗显著降低。在许多情况下,这种技术劣于组织机械阻抗感测,例如感测导电牙植体。
在本发明的一些实施例中,测量向前移动时机械阻抗的减小。在这种情况下,所述阻抗的变化表示所述治疗尖端在鼓膜切开术的情况下,在一体膜例如所述鼓膜中钻孔并到达一组织腔。一旦检测到这样的测量,所述电动机控制器可选地可命令向后缩回。
现在参考图8a,这是根据本发明的示例性实施例在空气中驱动尖端阵列的数个尖端的一阵列及一线性电动机的一驱动电流的位置的一示波器迹线1602。
另外参考图8b,这是根据本发明的示例性实施例的一示波器迹线1632,这是包括接触阻碍皮肤的一时间周期的数个尖端的一阵列的位置及一线性电动机的一驱动电流。
图8a及图8b于使用脉波宽度调制(pwm)闭环控制方法控制的一线性电动机,具有对时间的x轴1604、1634,每个划分是400毫秒,以及,对尖端位置1606、1636的y轴,每个划分是5毫米,以及,驱动电流1608、1638,每个划分是1安培。
图8a绘示出一上部迹线160,这显示作为一时间函数的尖端位置,其中所述尖端在空气中移动。所述上部迹线1610的ab部分对应于所述尖端的推进,所述上部迹线1610的bc部分对应于所述尖端的最大推进,并且所述上部迹线1610的cd部分对应于所述尖端的缩回阶段。
图8a绘示出用于推进所述尖端的一驱动电流的一下部迹线1612。通过所述下部迹线1612绘示的所述驱动电流基本上是恒定的,禁止噪声伪像。通过所述下部迹线1612绘示的所述驱动电流对应于通过组织-无皮肤接触的所述尖端运动的机械阻抗。
图8b绘示出一上部迹线1640,这显示作为一时间函数的尖端位置,其中所述尖端移动到接触组织,在图8b的示例中,所述组织是位于所述尖端的路径中的一手指的所述皮肤。所述上部迹线1640的ef部分对应于所述尖端正在推进到组织中,而且gh部分对应于尖端缩回。
图8b绘示出一下部迹线1642,这显示用于推进尖端的一驱动电流。所述下部迹线1642绘示的所述驱动电流显示出ef部分的一电流增加。所述推进中的尖端在e点与皮肤接触,并且在逐渐推压皮肤同时压缩皮肤。在图8b绘示的示例性实施例中,所述尖端速度被控制为恒定,可被看出正如所述上部迹线1640在ef部分上的恒定斜率。所述驱动电流与所述驱动力成比例,所述驱动力与一抵抗力成比例,以便保持所述速度,并且所述抵抗力被认为与深度成正比。所述驱动力及电流在点f处达到最大值,这对应于最深的凹陷。图8b显示检测与皮肤接触的一能力,以及可选地基于力反馈而决定凹陷的一深度,这在一些实施例中涉及所述驱动电流。
在图8a及图8b中,本案发明人已经通过以驱动电流的脉波宽度调制控制的一线性电动机测试如上所述实施组织接触检测的能力。图8a的所述上部迹线1640将尖端位置描述为在空气中的时间函数。ab部分是一推进部分,bc部分是最大的推进,cd部分是缩回阶段。所述下部迹线显示所述驱动电流基本上是恒定的。这表示没有机械阻抗-无皮肤接触。图8b绘示出如图8a中的尖端位置(上曲线1640)在组织(手指皮肤)位于所述前进中的尖端前方的情况。一下部迹线1642显示所述驱动电流。
可以看出,在ef部分增加一线性电流。所述推进中的尖端与组织在e点处接触,并在逐渐向前推组织同时压缩组织。由于所述驱动电流与所述驱动力成正比(驱动力与阻力成正比,阻力与深度成正比),所述驱动力及电流在点f处达到最大值,点f处是最深的凹陷。因此,我们已经证实通过控制驱动电流的力反馈,而检测皮肤接触以及凹陷深度的能力。
(数个)治疗尖端结构的示例性实施例的描述:
根据本发明的实施例,一治疗尖端的一远程尖端可能具有以下形状:锥形、方锥形、圆形(球形)、圆柱形平面、凿状或刀片状。尖端可能是中空的一金属包络或非中空固体。所述治疗尖端的外表面在整个操作期间(如10至30分钟)内,在摄氏300至850度的工作温度下可能是生物相容的。根据本发明的一个实施例,尖端材料应当具有高热导率,以便允许热量快速递送到汽化的陷口体积,并提供汽化陷口所需的一汽化潜热。适用在高温的组织汽化以及满足生物相容性要求的一种材料是钨,钨的热导率为~170瓦/毫秒。在摄氏400度的钨制成的扁平尖端能够在~1毫秒内汽化~30至50微米的组织。然而,通过使用圆锥形或方锥形的钨尖端,三倍的汽化深度可达到~150微米。这是由于锥体或方锥的几何特性具有的体积等于高度及直径相同的圆柱体积的1/3。
生产低成本锥形或方锥形的基座直径/宽度~300至1000微米及高度1000微米的钨尖可能是具有挑战性的。在一些实施例中,所述钨尖端被加工。在一些实施例中,如图1a及图2a所示,一圆锥形或方锥形尖端可选地是中空的,并且可选地通过压印或冲压技术或烧结技术生产。在一些实施例中,圆锥形或方锥形尖端的一远程尖端直径为~100至300微米。
另一种高导热尖端材料是铜(~400w/m℃)。然而,由于铜不是生物相容性的,方锥形或圆锥形的非中空尖端可选地可在诸如钛的高温下用生物相容性材料包覆(涂覆)。可以用约50至150微米的包络厚度涂覆上述由铜制成的具有一钛方锥形包络的尖端尺寸,而不显著降低热导率。所述钛包络可能通过加工或压印或冲压技术生产。所述尖端的所述铜芯材料可能通过烧结技术生产。
在一些实施例中,所述尖端是钛中空方锥体或锥体,厚度为50至300微米,优选为50至100微米。
在一些实施例中,尖端材料是铜,并且生物相容性涂层是金,可选地镀在铜上。在本发明的一个实施例中,一金层不是均匀的:在接触组织的所述尖端的远程终端上的电镀厚度接近100微米,而同时在所述尖端基部的厚度仅为~5微米。金镀层厚度的一逐渐变化潜在地确保高温金材的高稳定性,所述高温金材与组织产生接触,而同时因为接近所述尖端基部的电镀厚度(包括尖端表面区域的一大部分),而潜在地保持较低材料量及成本。
现在参考图9a及图9b,这些是描绘根据本发明的另一示例性实施例涂覆有镍的涂层1936随后涂覆金的铜尖1933的横截面图像。
图9a绘示出一铜基部1933及涂覆有镍随后接着金涂层1936的铜尖端。
图9b绘示出图9a的部分放大图,显示一尖端1933,以及镍在尖端1936上被金涂覆。图9b显示出在尖端处的约83微米厚的一涂层及所述尖端的侧面上的约34微米厚的一涂层。
现在参考图9c,这是描绘图9a及9b的示例性实施例的元素浓度作为沿着铜尖及所述镍随后涂金的距离的一函数的一图形1940。
所述曲线图1940具有以微米为距离单位的一x轴1942,及显示在测量距离处的材料中元素百分比的一y轴1944。
所述图形1940中的一第一线条1946显示出金(au)的浓度。
所述图形1940中的一第二线条1947显示出铜(cu)的浓度。
所述图形1940中的一第三线条1948显示出镍(ni)的浓度。
在图9a、图9b及图9c的示例性实施例的所述样品中,尽管所述尖端被加热至摄氏520度的一温度为50分钟,所述金层在所述尖端处的厚度为83微米,并且存在超过60微米的一层纯金。由于在某些情况下,一皮肤复原治疗的期间可能持续接近20分钟,所以本案发明人加热所述尖端的期间超过20分钟。
在一些实施例中,数个尖端的所述阵列通过使用烧结的铜尖端生产,所述铜尖端电镀有一6至20微米的镍层,并进一步电镀一5至10微米的金层。应注意的是,电镀可以在所述尖端产生一较厚的涂层,所述电镀为尖锐的且集中的电场。令人相信,所述尖端的电镀产生一协同作用,由此所述较厚的电镀位于所述阵列与所述组织相遇的位置,并且数个尖端的一烧结阵列上的所述生物相容性镀层优选地通过电镀形成。
为了测试铜及镍不会扩散到所述金层中,将数个尖端的所述阵列加热至摄氏520的温度持续50分钟,并用一电子显微镜测试金层稳定性及用x射线光谱测试铜、镍及金浓度作为深度的函数。所述结果显示,即使在所述尖端的所述尖锐远程终端也具有高的金稳定性,并且没有铜或镍扩散到所述表面。
用不锈钢尖端的一烧结阵列进行一类似的测试,结果良好。
图9a及图9b绘示出镀有金的一铜尖端阵列的横截面(手术切割单元中的每个单一尖端的特性可与相同尖端的一阵列中的每个尖端特性相同)。所述尖端已经加热到500度的温度持续3小时,并测试镍与铜离子从金层下面的镍镀层的扩散。扩散没有接近外表面,并且还测试数个尖端的毒性及生物相容性。结果证实稳定性及生物相容性。
现在参考图10,这是根据本发明的示例性实施例的治疗探针尖端的一简化图例。
图10呈现根据本发明的各种实施例的外科手术尖端1001、1005、1010、1015、1020、1025的各种形状。所述形状为:a-半中空圆锥形1001;b-中空圆锥1005;c-凿状1010(可以是用于切割的尖锐且未加热,或不够尖锐用于冷切割);d-圆柱形1015(实心或中空);e-球形1020(潜在地用于打开导管如血管);f-香蕉形状1025-潜在地用于鼓膜切开术。在一些实施例中,所述尖端是金属的及不透明的。在一些实施例中,所述尖端由蓝宝石及/或金刚石及/或陶瓷如aln(氮化铝)制成。
本案发明人已经进行各种尖端材料的陷口汽化实验,以确认如上所述的尖端的尺寸及材料选择。在人体皮肤上已进行过实验。
现在参考图11,这是根据本发明的示例性实施例在治疗后立即产生的人体内皮肤的汽化陷口的组织学横截面的照片。
图11呈现治疗后立即在人体内皮肤的汽化陷口1104的组织学横截面1102。所述陷口1104的深度为~100微米。所述陷口1104的直径为~150微米。所述陷口1104的形状是圆锥形。附带的损伤大多数小于80微米,除了在所述陷口1104的中心,此为~100微米。没有周围碳化。所述陷口1104已经获得镀金的铜尖端,并操作在摄氏400度下。
在本发明的另一个实施例中,治疗尖端可以通过将所述尖端加热到摄氏450至500持续2至5分钟来清洁及消毒。在那个温度下,燃烧有机材料中存在的碳,并且有机材料完全被切除。发明人已经成功测试那个消毒技术。
一些应用性的示例:
牙科及口腔颌面外科学:
现在参考图12,这是根据本发明的示例性实施例切割组织的示例性应用的一简化横截面图。
图12呈现一牙科应用的一示例,关于为何组织122必须在钛金属植入物121上微创切割,以插入人造牙齿(在第一手术植入步骤愈合后)。可选地,凿状的一尖端60在所述牙科植入物121上方切开一切口61。用一镊子拉动组织122可选地确保清楚的暴露组织及逐层切割组织122的能力。浅热损伤进一步能够精确地逐层切割组织,每个切口可选地具有深度d,直到所述金属植入物121露出并暴露。潜在地没有出血,并且由于非常浅的热损伤,从切口61愈合是快速的。在这种情况下,单极器件不能使用在此类情况,蓝宝石尖端或双极电手术(esu)单元产生更多的热损伤,然后愈合愈慢。在上述示例性实施例中,传递到所述植入物121的热量足够小,以避免因为接触所述植入物121表面所导致的损伤,由于小的接触期间,潜在地归功于机械阻抗感测,并且有限体积的治疗尖端60小于所述植入物121的体积。
在一些实施例中,一汽化元件可选地包括诸如2至10个尖端的一线性阵列。所述线性阵列潜在地提高切割速度。如下所述是以4个尖端的一阵列切割一小牛的肝的一示例。在下面描述的示例中,所述切口深度约为1毫米,所述切口长度为4厘米,所述切割的期间为2秒,热损伤小于100微米,以及尖端温度为摄氏400度。
在一些实施例中,可选地加热一牙齿中的一中空通道的一底部。这样的一实施例可选地用于所述通道的所述底部的消毒。目前冷装置对所述通道底部的消毒是困难的。使用邻近所述通道的所述底部的细光纤发出的激光,可能会缓慢地加热所述底部,同时产生附带加热及损伤。通过根据本发明的实施例导引一涂覆的光导/光纤进入所述通道而向下到其底部并激活所述远程尖端,所述通道底部是可选地接触一短时间及可测量的期间,可选地通过对尖端移动的阻力被测量,以及在摄氏~300至800度的温度下对所述通道底部进行消毒,而不会损伤组织。
腹腔镜及内窥镜外科学:
现在参考图13,这是根据本发明的示例性实施例切割组织的一示例应用的一简化横截面图例。
图13以适用于一非限制性示例的腹腔镜及内窥镜手术的模式呈现本发明的一些实施例的一应用。作为一非限制性示例,叙述在腹腔镜下切割一输卵管壁。一手术单元1301包括一激光器或电热单元130,可选地还包括主时脉及一电动机控制器。所述电动机可以位于所述单元130中或者更靠近一远程尖端132。一能量递送光纤或电线131导向一腹腔镜134。所述远端尖端132可选地通过一系列的能量脉冲加热,并且可选地同步振荡133。所述腹腔镜134还可以包括一光学观视通道135。所述腹腔镜可选地通过腹部皮肤及子层136中的一穿刺插入一身体。所述治疗过的器官可以是经过微创切割的一输卵管138。
在一些实施例中,另外的内窥镜应用包括胆囊切割、切割沾黏、肠内切割息肉、气管中肿瘤切割或汽化等,诸如此类。
药物通过人体组织导引:
在一些实施例中,尖端的一阵列用于通过组织导引药物,在一些实施例中甚至采用深陷口汽化。作为一示例,发明人通过一男性手臂的表皮已汽化9×9个陷口的阵列。测量到所述陷口的开口直径为200至300微米。观察到所述陷口保持打开持续6小时。用一共聚焦显微镜(mavrick)测量每个陷口的直径作为皮肤深度的函数。在6小时后,一种药物,在此例是,黄色萤光液体-floreszeinsethilo德国,被应用于所述皮肤。所述药物在2分钟内被完全吸收。
值得注意的是,数个陷口保持开放的一期间在药物递送中具有重要意义。所述期间潜在地取决于打开一陷口,以及所述陷口的直径,而非引起深度的附带损伤,这可能成为药物转移的一障碍。作为一非限制性示例的方式,仅在角质层中的数个浅的陷口,在药物被施用前,所述陷口过小的一直径可能在一过短的期间内闭合,例如30分钟。
附加示例性实施例的描述:
现在参考图14,这是根据本发明的一示例性实施例的数个尖端1402的一阵列、一手持装置1404及所述手持装置1404的数个特征1406的一列表的一简化图例。
数个特征的所述列表包括:
平台技术,通过改变一金属护套的一长度及/或一形状及/或一加热尖端类型的选择及/或一操作参数,相同的单元可选地可用于不同的应用中,例如在不同的外科应用中。所述相同的平台可选地可被用于审美学以及药物递送中。
可重复使用的。作为一非限制性示例,一金属热尖端-在一些实施例中,所述治疗尖端是可重复使用的。所述治疗尖端可选地可在使用期间被消毒。可选地使用所述装置1404本身,通过加热到高温,所述治疗尖端可选地被消毒及/或清洁任何残留物,以汽化残留物及消毒所述尖端。
精确的运动控制-如上所述,治疗尖端的侵入深度可选地可被精确控制;
直接传热到组织;
清洁及精确的组织切除;
接触反馈机制;
简洁及低成本;
低痛及安全;
自动尖端清洁及消毒;
无辐射;及
万用性(多种模式及应用)。
现在参考图15a、图15b及图15c,这是根据本发明的示例性实施例的热机械切除(tma)的过程的简化图例。
图15a绘示出接触组织1504前的一尖端阵列1502的一简化图例。
图15b绘示出图15a的所述尖端阵列1502在短暂接触组织1504期间的一简化图例。在所述接触的至少一些所述期间内,所述尖端阵列可选地被加热,从而加热所述组织1504并在所述组织1504中产生数个陷口1506。
图15c绘示出通过所述尖端阵列1502形成陷口1506的组织1504的一简化图,同时所述尖端阵列1502被加热并接触所述组织1504。
现在参考图16,这是根据本发明的一示例性实施例通过施加被加热的尖端产生各种效果的一列表1602的一简化图例。
所述列表1602列举三种效果或治疗模式,包括:
在组织上的切除及/或汽化效用1604。通过一非限制性示例,一汽化深度可选地取决于数个操作参数及/或同一处的多个治疗脉冲,而可从20微米至500微米变化;
在组织上的一非切除效果1606,由此组织的外层不会被汽化,同时可选地可产生下面的孔。这样的效用可能在例如治疗皮肤时发生,其中在汽化具有较高含水量的表皮同时,更难汽化的角质层不被汽化。在一些实施例中,上述效用产生皮肤治疗及自身绷带,亦即,所述角质层作为经过治疗的表皮的一覆盖物。在一些实施例中,上述效果可选地在比所述切除效果更短的期间内实现;及
在组织中产生可渗透通道1608,所述可渗透通道可以用于将药物引入组织。
还列出所述治疗方式的一益处1610,亦即,所述治疗模式产生很少或没有疼痛,而且因此潜在地不需要使用一止痛剂。
在一些实施例中,可渗透的皮肤或组织通过所述角质层及任选的一些表皮的汽化产生而无凝血,并且在所述表皮下不会产生损伤。
在一些实施例中,上述可选地通过所述组织加热元件及所述组织之间在一短期间内接触而实现,例如通过一非限制性示例的方式,低于10毫秒或低于1至200毫秒的范围。
在一些实施例中,上述可选地通过使用所述组织加热元件的一尖端的一尖锐远程终端而实现,例如通过一非限制性示例的方式,所述组织加热元件的一尖端的一远程终端的宽度小于150微米,或小于100微米,或小于50微米或20微米。
在一些实施例中,至少与铜相比,上述可选地通过使用具有相对低的热传导的一尖端而实现。作为一非限制性示例的方式,所述尖端可以由不锈钢及/或钛构成。
现在参考图17,这包括根据本发明的各种示例性实施例使用各种治疗尖端的各种治疗模式治疗的组织的九个横截面图像。
图17绘示出:
已经以带有每个14毫秒的两个加热脉冲的一切除用的d型尖端治疗过的组织1702,使用涂覆有金的一铜尖端的一示例性实施例,并且在组织1702中形成一陷口的一第一横截面图像;
已经以带有每个9毫秒的两个加热脉冲的一切除用的d型尖端治疗过的组织1704,并且在组织1704中形成一陷口的一第二截面图像;
已经以带有一9毫秒的单个加热脉冲的一切除用的d型尖端治疗过的组织1706,并且在组织1706中形成一陷口的一第三截面图像;
已经以带有一14毫秒的单个加热脉冲的一非切除用的s型尖端治疗过的组织1708,使用涂覆金的一不锈钢尖端的一示例性实施例,并且在组织中形成一陷口的一第四横截面图像;
已经以带有每个9毫秒的两个加热脉冲的一s型尖端治疗过的组织1710,并且在组织1710中形成一陷口的一第五横截面图像;
已经以用于产生可渗透通道而带有一9毫秒的单个加热脉冲的一s型尖端治疗过的组织1714,并且在组织1714中形成一陷口的一第六横截面图像;
已经以用于产生可渗透通道而带有一9毫秒的单个加热脉冲的一s型尖端治疗过的组织1716,并且在组织1716中形成一陷口的一第七横截面图像;及
已经以用于产生可渗透通道而带有一9毫秒的单个加热脉冲的一s型尖端治疗过的组织1718,并且在组织1718中形成一陷口的一第八横截面图像。
在本申请案及权利要求书中,探针尖端也参考使用以下词语:
大于~150w/degm的较高导热系数的一d型端头;
具有相对较低热传导率的一s型尖端,例如~20-150w/mdegc;及
一t型尖端,由钛制成,并且通常类似于一s型尖端,具有相对较低的热导率,例如~20-150w/mdegc。
所述d型尖端可能更适用于切除、汽化、治疗模式。所述s型尖端潜在地更适合于一非切除治疗模式。
关于使用s型非切除尖端特此提出的一些意见:
在一些实施例中,当使用双脉冲时潜在地更加如此,所述角质层潜在地完全或部分去除,潜在地导致一切除效应,没有角质层残留作为用以产生一陷口的一潜在绷带;
在一些实施例中,当使用单个脉冲时,例如以s型尖端用于产生图像1714、1716、1718的9毫秒期间的单个脉冲,潜在地更加如此,药物渗透被认为是潜在地能够通过重新组织所述角质层及所述表皮的细胞,潜在地没有凝血可能作为药物的障碍。所述重组潜在地允许药物通过所述经治疗过的皮肤渗透。
在一些实施例中,例如当s型尖端是尖锐的,例如具有~100微米远程直径时,当使用9毫秒的脉冲期间时,所述锐利尖端可以切除所述角质层。然而,虽然发生一切除效果,但一产生的陷口似乎缺乏凝血的附带损伤边界。结果,所产生的陷口潜在地可渗透相当长的期间,高达3或6或12小时。
现在参考图18,这是根据本发明的示例性实施例的数个尖端的一阵列1802及数个尖端1802的所述阵列的描述1804的一简化图例。
所述数个尖端1802的所述阵列的叙述1804包括:
所述数个尖端的所述阵列1802是一数个金属尖端的一阵列;
数个尖端1802的所述阵列是具有大约100微米的一宽度及大约50微米的一曲率半径的数个微小锐利方锥形尖端的一阵列。在各种实施例中,尖端宽度可以在~100至1000微米之间的范围内,并且尖端曲率半径可以在~50微米与平坦表面(对应于无限曲率半径)之间。
应注意的是,在一些实施例中,通过包括如上所述的9×9个尖端的数个尖端阵列1802产生的一治疗区域为大约1平方厘米;
在一些实施例中,数个尖端1802的所述阵列可以被加热到摄氏400度的温度,这类似于用二氧化碳激光器治疗组织时达到的温度。
现在参考图19,这是根据本发明的一个示例性实施例可选地使用数个尖端的一阵列的条形码1902及数个尖端的所述阵列相关联的另一些可选特征的描述1904的一简化图例。
所述描述1904包括根据本发明的示例性实施例的数个尖端的所述阵列相关联的数个可选特征:
数个尖端的所述阵列可选地可包括用于可选地描述尺寸、尖端形状、单个尖端识别号等的一条形码;
根据本发明的示例性实施例,可以通过热手术汽化及组织系统切口中的一内置摄像头监视数个尖端的所述的阵列及/或所述条形码。所述监视可以用于读取所述条形码,并将数个参数输入到所述系统及/或用以在数个尖端的所述阵列靠近并接触组织时显示它。
在一些实施例中,所述条形码用于识别一尖端,可选地用于计数所述尖端的一使用次数,并且可选地用于限制所述尖端的使用次数小于一指定次数。对尖端的使用次数的一限制可潜在地用于防止在高温(例如在400摄氏度)下使用一特定数量后,对所述尖端的一涂层的一潜在的长期损伤。于一尖端的使用次数的一限制可以通过一非限制性示例的方式,使用15次,或使用3至50次的范围;
在一些实施例中,所述条形码用于记录哪个尖端用于哪个受试者或患者。作为一非限制性示例,一尖端可以用于相同患者的几种治疗,但在一些情况下可能不与其他患者一起使用;
在一些实施例中,如上所述的摄像头可以执行数个尖端的一阵列的自动质量检查,诸如通过一些非限制性示例,数个尖端使用后的清洁度、检查尖端的尖锐度是否保持,如果尖端上有碳化;如果所述阵列中的某些尖端可能弯曲;
可选地可通过将数个尖端的一阵列加热到足够高的温度,以汽化可能留在数个尖端的所述阵列上的残余物的温度来自动清洁尖端阵列,并且还对数个尖端的所述阵列进行消毒;
可选地可重复使用数个尖端的所述阵列;
数个尖端的所述阵列对于至少3,000次热脉冲及/或15个面部治疗会话是有益的。
现在参考图20,这是根据本发明的示例性实施例的手持件2002相关联的数个可选特征的描述2004的手持件2002的一简化图例。
所述描述2004包括关于所述手持件2002的数个可选功能:
基于可选的自动切口深度控制,通过所述手持件2002的手术精确运动控制,潜在地通过检测组织的接触并测量在所述接触点以外的额外推进,潜在地达成一受控的深度而无关组织阻抗;
所述手持件2002相对于用于热手术汽化及组织切割的当前仪器是小的及轻的(例如250克);
所述手持件2002的使用不会产生噪音;
在一些实施例中,所述手持件2002的使用不需要光学器件;
在一些实施例中,所述手持件2002的使用不需要液体;
在一些实施例中,所述手持件2002的使用不需要风扇;
所述手持件2002的形状、尺寸、重量可轻松进出许多手术的位置;
所述手持件2002的形状、尺寸、重量提供一治疗位置的良好可见度;及
所述手持件2002能够快速地进行治疗。作为一非限制性示例的方式,大约1厘米长度的手术切口大约可以在2秒内进行,而具有100微米的深度。在诸如此类的一示例中,所述汽化尖端的所述重复率为1赫兹(hz),类似于皮肤分段汽化中表面切除的情况。对于几毫米尺寸的小损伤,诸如通过一非限制性示例的高度为0.5至5毫米,可选地是在不到一分钟内被汽化。
现在参考图21,这是根据本发明的示例性实施例用于热手术汽化及组织切割的一系统2102,以及,所述系统2102相关联的数个可选特征的一描述2104的一简化图例。
所述描述2104包括关于所述系统2102的数个可选特征:
所述系统2102可以是充分精巧的,以布署作为一桌上型系统;
在一些实施例中,所述系统重量大约可以是1至7公斤;
所述系统2102可选地可折迭到一便携式外壳,以便携带;
所述系统2102可选地提供用于自动交换尖端的能力。
现在参考图22a及图22b,这包括绘示在一实验中治疗的组织的截面图像2202、2204,以及,根据本发明的一示例性实施例关于所述实验的数个发现的描述2206。
图22a绘示出通过所述角质层,及皮肤组织的所述表皮的汽化,及所述组织中的凝血部分2205引起的“第0天”产生的一陷口2203的所述图像2202。所述研究结果的所述描述2206还汇报在第0天没有检测到浮肿且无出血。所述治疗是一单个14毫秒的热脉冲。
图22b绘示出在图22a所示的组织治疗后“第7天”的图像2204。所述图像2204显示已经长出的一痂2207,这显示出表皮再生2209,并且显示具有新的成纤维细胞及巨噬细胞的150微米×50微米尺寸的一裂缝2211。
现在参考图23,这是将根据本发明的示例性实施例,称为替梭(tixel)的治疗与使用分段二氧化碳激光器的治疗进行比较的一表格2302。所述表格2302用于在每个组织产生的陷口所递送的能量相同的情况下,比较上述模式中的治疗、皮肤缩孔或汽化陷口:
替缩(tixel)治疗与分段二氧化碳激光器治疗相比较,治疗中的每个陷口的能量密度为1∶100;
在一示例中的替梭(tixel)治疗的脉冲时期为10毫秒,与分段二氧化碳激光器脉冲时期为0.1毫秒相比,比例为100∶1。
与分段二氧化碳激光器治疗相比,替梭(tixel)治疗中的每个陷口的能量递送是相同的;
作为一非限制性示例,一替梭(tixel)治疗与分段二氧化碳激光器治疗相比较,治疗触发的疼痛感觉的数量的比例为1∶81,因为所述替梭(tixel)治疗可选地产生例如81个陷口的一阵列,所述陷口在一个潜在的疼痛事件中持续数毫秒,同时二氧化碳激光器依次产生所述数个陷口,造成81个潜在的疼痛触发,每个持续几毫秒;
将一替梭(tixel)治疗系统与商用分段二氧化碳激光器治疗相比较,如上所述的治疗系统的尺寸比为1∶4;
将一替梭(tixel)治疗系统与商用分段二氧化碳激光器处理相比较,用于提供如上所述的治疗系统的成本比为1∶4;
将一替梭(tixel)治疗系统与商用分段二氧化碳激光器治疗相比较,提供如上所述的治疗系统的系统重量比为1∶4;
将一替梭(tixel)治疗系统与商用分段二氧化碳激光器治疗相比较,提供如上所述的治疗系统的预期停机时间(通常为患者停留时间)的比例为1∶4;
将一替梭(tixel)治疗系统与商用分段二氧化碳激光器治疗相比较,一预期疗效或最终治疗结果大致相同;
将一替梭(tixel)治疗系统与商用分段二氧化碳激光器治疗相比较,基于更小的尺寸及重量、提供更多用途及更容易使用,所述替梭(tixel)治疗系统的一被估计的变通性大概可谓是一举三得的。
现在参考图24,这是根据本发明的示例性实施例的尖端2402及治疗系统2404的阵列的一简化图例。
图24还包括列出三种类型的尖端的三个非限制性示例的文本,这三种类型的尖端可以与治疗系统2404结合,作为s型尖端(未示出);d型尖端(未示出);及t型尖端(未示出)。
现在参考图25,这是根据本发明的示例性实施例的一手持件2502的一简化图例。
所述手持件2502是“笔形”或细长形手柄的一示例,这可能适合于在一些较紧密,较受约束的空间中工作,例如用于在口中的牙龈上产生数个陷口,例如用于通过产生的所述陷口或用于在牙龈中产生一切口的一药物的应用。
现在参考图26a至图26d,这些是根据本发明另一示例性实施例的一手持件2602的一简化图例。
所述手持件2602包括一细长且窄的延伸部,这里称为护套2604,在所述护套2604的一远程中端处具有一治疗尖端2606。
图26a及图26b绘示出所述手持件2602的一半前视图及一侧视图。
图26c绘示出所述手持件2602的一横截面的一侧视图,包括一电子控制器2608、一机械振动器2610或振动驱动器2610以及一激光输送光纤2612。
图26d显示如图26c所示的所述手持件2602的所述横截面的一半前视图。
现在参考图27,这是根据本发明的示例性实施例的一手持件2702的一横截面的一半前视图的一简化图例。
所述手持件2702包括一可替换的细长薄窄延伸部,这里称为护套2704,以及具有不同形状尖端2708的各种附加延伸部2706。
现在参考图28,这是根据本发明另一示例性实施例的一手持件2802的一简化图例。
所述手持件2802可选地成形为用于自我给药的皮肤陷口,潜在地针对家庭使用。在一些实施例中,所述手持件2802被成形并配置有用于使皮肤缩孔的数个尖端的一阵列,潜在地用于治疗皮肤以改善药物穿越缩孔的皮肤。
现在参考图29,这是根据本发明的示例性实施例的一尖端2902及一尖端基部2910,以及所述尖端2902的一描述2904的一简化图例。
所述尖端2902可以通过所述尖端的曲率半径2906的尺寸及所述尖端的长度2908来描述。所述尖端2902是被加热并达到高温的装置的一部分。在一些实施例中,所述尖端2902可选地是中空的。在一些实施例中,所述尖端基部2910可选地是中空的。所述尖端基部2910用于将所述尖端2902附接到一护套(未示出)。
所述尖端2902的所述描述2904包括一个示例性实施例的描述,所述描述假设所述尖端的一曲率半径为0.3毫米。在一些实施例中,所述尖端可以不具有通过一曲率半径定义的一形状,并且作为非限制性示例的一测量,以0.3毫米叙述所述尖端的一宽度或一半宽度。所述尖端2902还被描述为具有1毫米的长度,而且一激光源也被描述为具有10瓦的强度。对于所述尖端2902使用不同的材料,导致用于将所述尖端2902加热到摄氏500度的时间不同,并且将所述尖端2902冷却至~摄氏42度或大约等于体温。
在使用一钛尖端的一些实施例中,加热时间可选地约为30至100毫秒,潜在地取决于圆锥形包络的厚度,冷却时间大约为20毫秒。
在使用一钨尖端的实施例中,加热时间约为3至15毫秒,冷却时间约为3毫秒。
现在参考图30,这是根据本发明的示例性实施例的一尖端3002及两个表格3004、3006的一简化图例。
所述第一表格3004叙述用于描述一治疗尖端的一示例性实施例的单元,还叙述通过加热将所述治疗尖端升温的激光功率及一目标温度。
所述第二表格3006包括数个单元及描述钛、钨及铜三种不同材料的尖端的数值。在所述表格3006中的值包括:
质量密度、摩尔质量、摩尔热容量、质量热容量、热导率、热损失、热扩散率、热容量、τ-温度损失时间常数、热容时间、扩散时间及5*tau。如图29所示,一治疗尖端通过一激光被加热的热响应时间取决于所使用的一金属类型。对于一高热扩散性材料(参见第二表格3006)的一热响应或松弛时间较一低热扩散性材料为短。热扩散率取决于金属的质量密度、热容量及热传导,如第二表格3006所示。如第一表格3004所示,所述尖端尺寸潜在地影响汽化深度及期间两者。
现在参考图31,这是根据本发明的示例性实施例的数个尖端的一阵列3102的一图像。
数个尖端3102的所述阵列包括一些方锥形尖端3104及一些截头锥形尖端3106。所述截头尖端能够使所述数个锐利尖端的应用在外科手术切割中被使用,而不会接触其他尖端及所述组织。图31绘示的示例性实施例示出四种接续的锐利尖端,然而,在一些实施例中,多于或少于四种锐利尖端,例如在1至100个锐利尖端的一范围内,所述锐利尖端可以是或可以不是接续的。
现在参考图32a,这是根据本发明的示例性实施例用于热手术汽化及切割应用到小牛的肝3206的组织的一手持件3204的一图像3202。
图32a显示出使用所述手持件3204运用热量切入小牛的肝3206,亦即,通过加热的尖端接触小牛的肝。一线性尖端阵列(由于图像3202被拍摄的方向,在图32b中不可见)被保持在大约摄氏400度的恒定温度下,并以13赫兹(hz)的频率可选地振动。所述形成的切口很难看到,并通过一椭圆3208而被标示。
现在参考图32b,这是根据本发明的示例性实施例将图32a的所述手持件3204应用于小牛的肝3216的一图像3212。在图32b中,数个尖端的所述阵列是冷的,或在室温下。应注意的是,没有通过所述手持件3204切割所述小牛的肝3216,并且小牛的肝3216的外观并无意描绘任何切口。应当注意,在图32b的所述示例性实施例中,数个尖端的所述阵列在不加热时不产生切口。
现在参考图32c,这是根据本发明的示例性实施例以一加热的线性尖端阵列切割小牛的肝的一图像。
为了制造图32c,通过一镊子(未示出)将小牛的肝组织拉到一边,以避免小牛的肝组织接触数个切割尖端的上部。
图32c示出一振荡尖端阵列的切口质量。
所述图像3232显示出围绕一切口3238的一椭圆3240,并且示出没有渗血、凝血深度小及没有碳化。
所述切口3238在所述图像3232的中心处可被看见为一垂直切口3238。所述切口显示无碳化,并且在所述切口3238的边际存在一非常薄(~50微米)的白色凝血线3239。
现在参考图32d,这是根据本发明的示例实施例将图32a的数个尖端3244的一阵列应用于小牛的肝3246的一图像3242。
现在参考图33,这是一尖端3302的一简化图例;根据本发明的示例性实施例的尖端握把3304及一表格3306。
所述尖端握把3304附接到所述尖端3302。
所述表格3306叙述关于加热所述尖端3302所做的计算。所述表格描述如下:
假设由钨制成的一锥形尖端3302,一半径为0.3毫米,一尖端长度为1毫米;一尖端握把3304或护套具有一内半径为4毫米,而且外半径为6毫米及一长度为5厘米;施加每个脉冲的热量为0.21焦耳的1000个脉冲,在所述尖端3302与所述握把3304之间具有完美的热耦合,并且没有额外的热损失到空气或水,所述握把的一温度上升将约为摄氏9.5度。
在本发明的一些实施例中,所述护套或握把,例如图33所示的所述握把/护套3304,可选地是以气流或以水流主动地冷却。
在本发明的一些实施例中,所述护套或握把,例如图33所示的握把/护套3304,并没有被主动冷却。不使用主动冷却的实施例适用于一手术情况仅持续数分钟,例如1至5分钟,此处所述握把只会被稍微加热。这种情况潜在地是常见的,因为使用本发明的实施例的大多数手术切割是相对较快的。
现在对图34进行说明,这是一尖端3402的一简化图例;根据本发明的示例性实施例的一尖端握把3404及一表格3406。
所述尖端握把3404附接到所述尖端3402。
所述表格3406叙述关于加热所述尖端3402所做的计算。所述表格描述如下:
假设由钨制成的一锥形尖端3302,具有一半径为0.3毫米及一尖端长度为1毫米、一尖端体积为9.42×10-11立方米、一尖端握把3304具有一长度为5厘米、一内半径为4毫米、一外半径为6毫米、一握把材料体积为3.1416立方厘米、一握把质量密度为7.7克/立方厘米、一握把具体比热容为0.51焦耳/(克*k)、一总握把容量为12.3焦耳/k,施加每个脉冲的热量为0.12焦耳的1000脉冲,及一总能量为120焦耳-在所述尖端握把预计温度上升9.73度开尔文(kelvin)。应注意的是,通常操作者不会使用这样的脉冲数量而不需要休息,并且对于200至300个脉冲的序列,通常温度上升不会超过摄氏2至3度。
现在参考图35,这是根据本发明的示例性实施例切割组织的一方法的一简化流程图。
图35所示的所述方法包括:
使用用于热切割组织的一装置(3502),用以:
自动推进一组织加热元件朝向组织(3504);
自动检测所述组织加热元件何时接触组织(3506);及
基于检测所述组织加热元件何时接触组织,自动控制所述组织加热元件进行加热(3508)。
现在参考图36,这是根据本发明的示例性实施例通过汽化所述组织中的一陷口导引材料通过组织的一方法的一简化流程图。
图36所示的所述方法包括:
使用用于热切割组织的一装置(3602),用以:
自动推进一组织加热元件朝向组织(3604);
自动检测所述组织加热元件何时接触组织(3606);及
基于检测所述组织加热元件何时接触组织,自动控制所述组织加热元件进行加热(3608)。
所述“包含(comprises)”、“包含(comprising)”、“包括(including)”、“具有(having)”及其词性变化是指“包括但不限于(includingbutnotlimitedto)”。
所述术语“组成(consistingof)”旨在表示“包括并限于(includingandlimitedto)”。
所述术语“基本上由...组成(consistingessentiallyof)”是指组合物,方法或结构可以包括另外的成分,步骤和/或部分,但是只有当附加成分,步骤和/或部分不会实质上改变所要求保护的基本和新特征时组成,方法或结构。
如本文所用,单数形式“一(a)”,“一(an)”和“所述(the)”包括复数参考,除非上下文另有明确规定。例如,所述术语“单元(unit)”或“至少一个单元(atleastoneunit)”可以包括多个单元,包括它们的组合。
遍及本申请案的内容中,本发明的各种实施例可以用一范围形式呈现。应当理解,范围格式的所述描述仅仅是为了方便和简洁,并且不应被解释为对本发明的范围的僵化限制。因此,应考虑对范围的所述描述,以具体公开所有可能的子范围(sub-range)以及所述范围内的各个数值。例如,1至6的范围的描述应被认为具体公开数个子范围,从1至3、从1至4、从1至5、从2至4、从2至6、从3至6等,以及所述范围内的个别数值,例如1、2、3、4、5及6。无论范围的广度如何,都适用。
无论何时在此显示数值范围,都意味着在指定范围内包括任何引用的数字(分数或整数)。所用惯用语(phrases)第一指示号码和第二指示号码“之间的范围/范围(ranging/rangesbetween)”和“范围/范围从(ranging/rangesfrom)”第一指示号码“到(to)”第二指示号码的在本文中可互换使用,并且意在包括第一和第二指示号码以及它们之间的所有分数和整数的数值。
应当理解,为了清楚,在单独实施例的上下文中描述的本发明的某些特征也可以在单个实施例中组合提供。相反,为了简洁起见,在单个实施例的上下文中描述的本发明的各种特征也可以单独提供或以任何合适的子组合提供或适用于本发明的任何其它描述的实施例。在各种实施例的上下文中描述的某些特征不被认为是这些实施例的基本特征,除非所述实施例在没有那些元件的情况下不起作用。
虽然已经结合本发明的具体实施例描述本发明,但是显而易见的是,许多替代方案,修改和变化对于本领域技术人员是显而易见的。因此,旨在包括落在所附权利要求的精神和广泛范围内的所有这样的替代、修改及变化。
本说明书中提及的所有出版物,专利及专利申请案通过引用并入本说明书中,其程度如同每个单独的出版物,专利或专利申请被具体和单独地指明通过引用并入本文。此外,本申请中引用或标识任何参考文献不应被解释为承认所述参考文献可用作本发明的现有技术。在使用章节标题的范围内,不应将其解释为必然的限制。
- 还没有人留言评论。精彩留言会获得点赞!