使心脏激活可视化的系统的制作方法
发明领域
本发明涉及心脏的多个衍生激活参数在3d心脏模型上的可视化。更具体地,本发明涉及提供心脏组织电激活的同步性的显示。此外更具体地,本发明涉及虚拟起搏器植入。
发明背景
传导系统中的一些心脏缺陷导致心脏的不同步收缩、传导障碍。因此,心脏不泵送足够的血液,最终导致心力衰竭。这些传导障碍可以具有多种原因,包括年龄、心脏(肌肉)损伤、药物和遗传。
此类传导障碍的常见原因是左心室和/或右心室快速激活纤维,希氏-浦肯野系统或瘢痕组织中的障碍部分。由于希氏-浦肯野系统或阻滞性瘢痕组织中的该障碍部分,左心室或右心室不以与另一侧相同的快速方式激活。这被称为左束支传导阻滞(lbbb)或右束支传导阻滞(rbbb)。在lbbb或rbbb的情况中,改善心脏功能的已知方式是植入心脏再同步治疗(crt),也被称为“双心室起搏”起搏器。心脏的电刺激再同步改善了心脏的泵送功能。
起搏器是利用通过电极(也称为导线)递送的电脉冲的医疗装置,其接触心脏肌肉以调节心脏的搏动。起搏器的主要目的是维持导致较高心输出量的适当的心率。crt起搏器装置包括两个或更多个导线,其中至少一个位于右心室并且一个位于左心室。这些导线可以用于感知固有的,即正常心脏驱动的激活,或者可以用于刺激,即引发该位置处的激活。
然后可以通过感知右心室中固有的激活来实现心脏再同步,并且将该触发用于激活左心室。可选地,可以通过改善或者通过取代既有的固有激活,通过人为刺激来驱动整个激活,即左心室和右心室。
与crt起搏器在当前临床实践中的使用相关的主要问题是找到心室腔室内的最佳起搏导线位置。目前,至少30%植入crt装置的患者不响应crt疗法。近几年,卫生保健系统以及起搏器工业均在寻找合适的容易且可靠的指导方法来找到这些最佳位置。
发明概述
本发明涉及用于处理来自对象的心电图ecg电极的测量数据的计算机实现方法。所述方法包括获得对象躯干的三维3d解剖学模型。优选地,所述解剖学模型既包含躯干的外表面又包含内部结构(如心脏和肺)的位置信息。对象躯干的三维解剖学模型可以,例如来源于医学成像模式,如mri、ct、pet-ct、超声等。3d解剖学模型可以包含躯干的几何形状以及肺、心脏、血腔、胸腔、脂肪和躯干中的任何其它相关组织中的一种或多种的几何形状。
本发明的发明人迄今为止已经在所谓的逆计算方面取得了进步,例如,其中根据表面心电图来估计例如心脏的激活顺序和/或其它参数。
本发明的发明人设计了心脏等时线定位系统(cardiacisochronepositioningsystem)(cips)。cips是能够根据例如12或更多导联心电图(ecg)来测定心脏激活的无创心电图成像(ecgi)方法和/或装置。cips模型将ecg信号与心脏、肺和躯干的mri或计算机断层扫描(ct)图像来源的模型整合,以计算心脏等时线的位置。在本文中,等时线指在3d心脏表面模型上描绘的(虚拟)线,其连接该心脏模型上激活同时发生或到达的点。3d心脏表面模型与等时线的组合提供心脏激活时间控制的3d模型,本文也称为心脏激活模型。
ecg在本文被定义为将心肌的实际电活动与心脏测量的或导出的(电活动)相关联的任何方法(优选无创的)。在经典心电图的情况下,体表电极之间电势的差异与心脏的电活动相关。也可以通过其它方式(例如通过所谓的icd(植入型心律转复除颤器)进行的测量)获得导出的ecg。为了获得此类功能图像,必须提供估计的电活动。
本发明的发明人发现,心脏激活模型还可以用于进行模拟。具体地,当向心脏激活模型添加刺激点时,所述模型可以用于预测产生的心脏激活。
因此,按照本发明,提供了用于提供心脏组织电激活的同步性的显示的计算机实现方法。所述方法包括获得心脏电激活的三维模型。所述方法可以包括获得特定患者心脏电激活的患者特异性的三维模型。所述三维模型包括表示心脏外表面(如心肌外表面)的网格。所述三维模型可以包括隔膜壁。网格具有多个节点。各节点具有与其相关的表示刺激位点处的心脏刺激与该相应节点处的心脏激活之间的时间延迟的数值。所述方法包括,对于心脏三维模型中的各节点,在心脏三维模型中该节点的位置处限定刺激位点。对于各节点,基于心脏电激活的三维模型确定由该节点处的刺激所产生的改变的心脏电激活的三维模型。对于各节点,基于该节点处的刺激确定心脏的心脏激活同步性度量。确定表示心脏的三维模型的心脏同步性图,其指示在各节点处心脏激活同步性的相应度量。
因此,心脏同步性图提供了对于3d心脏模型各节点,由单一节点处的激活所产生的整个心脏激活的同步性的简单概观。这允许对激活位置的影响进行简单评估。
任选地,心脏激活同步性的度量是下述之一:心脏去极化(dep)时间的标准差(std);去极化时间的范围;仅左心室(lv)的标准差;刺激与隔膜激活之间的延迟;av延迟;vv延迟等。具有最低去极化时间标准差std(dep)的区域可以是心脏起搏器电极的最佳植入位点。
任选地,所述方法包括限定常见刺激位点,其中对于各节点,确定由该节点处的刺激所产生的改变的心脏电激活的三维模型的步骤考虑常见刺激位置处的另外的刺激。因此,对于3d心脏模型各节点,心脏同步性图提供了由常见刺激位置和单个节点处的激活所产生的整个心脏激活的同步性的简单概观。对于两个激活位置,这允许对激活位置的影响进行简单评估。任选地,常见刺激位点是心脏的固有激活位点。因此,对于3d心脏模型各节点,心脏同步性图提供了由固有激活位点和单个节点处的激活所产生的整个心脏激活同步性的简单概观。任选地,常见刺激位点是人工刺激位点。因此,心脏同步性图可以用于提供由两处人工刺激位点的激活所产生的整个心脏激活的同步性的简单概观。可以理解,两处刺激位置的刺激可以同时进行。可选地,两处位置的刺激可能不同时进行。一处的刺激相对于另一处的刺激可能滞后。可以理解,也可以确定滞后时间的持续时间对心脏激活同步性的影响。
任选地,所述方法包括限定多个常见刺激位点,其中对于各节点,确定由该节点处的刺激所产生的改变的心脏电激活的三维模型的步骤考虑所述多个常见刺激位点处的另外刺激例如同时刺激。因此,对于3d心脏模型各节点,心脏同步性图提供了由例如多个常见刺激位点和单个节点处的同时刺激所产生的整个心脏激活的同步性的简单概观。任选地,常见刺激位点之一是心脏的固有激活位点。
任选地,所述三维模型包括表示心脏的整个外表面的网格,如心肌的整个外表面,例如包括隔膜壁。
任选地,获得心脏电激活的患者特异性的三维模型包括获得心脏以及任选地肺和胸部的患者特异性的三维解剖学模型;获得表示心脏的电功能的ecg数据;以及基于心脏和任选地肺和胸部的三维解剖学模型以及ecg数据确定心脏电激活的三维模型。可以通过医学成像如计算机断层扫描ct和/或磁共振成像mri获得患者特异性的解剖学模型。
任选地,通过从数据库中进行的选择来确定对象的三维解剖学模型。此外,提供了包含多个三维解剖学模型的数据库。3d模型可以包括躯干的几何形状,任选地包括肺、心脏、血腔、胸腔、脂肪以及躯干中的任何其它相关组织中的一种或多种的几何形状。3d解剖学模型相互之间是不同的。3d解剖学模型可以表示不同的可能的对象。3d解剖学模型可以,例如表示不同性别、年龄、重量、身长、胸围、骨架大小(framesize)、身体质量指数(bmi)等的对象。3d解剖学模型在医学标准如血压方面也可能不同。可以理解,数据库中的各3d解剖学模型可以,例如来源于相应参照对象的医学成像模态,如mri、ct、pet-ct、超声等。数据库中的一些或全部3d解剖学模型是虚构参照对象的虚构呈现也是可能的。
然后,所述方法可以包括从数据库中的多个3d解剖学模型选择显示与对象的解剖学最接近的一致性的3d解剖学模型。可以基于诸如性别、年龄、重量、身长、胸围、骨架大小、bmi等的参数做出选择。可以基于已经例如通过测量、询问或测试得知的对象的参数使此类选择自动化。可以根据对象的3d图像计算一些测量值,例如胸围、躯干的高度等。这些测量值可以用于从数据库中选择合适的3d模型。
选择还可以基于对象解剖学的3d图像与数据库中的3d模型的视觉比较。可以基于模式识别使此类选择自动化。这提供了不需要获得各对象的对象特异性的3d解剖学模型的优势。相反,可能获得多个不同的3d解剖学模型以及选择最能表示对象的准对象特异性的3d解剖学模型。任选地,所述方法包括:在从数据库中选择3d解剖学模型之后,将3d解剖学模型缩放为对象解剖学的3d图像和/或将3d图像缩放为3d解剖学模型。这提高了3d解剖学模型与3d图像的一致性。可对3d解剖学模型进行缩放,以使3d解剖学模型的外表面与获自3d图像的对象的解剖学的外表面相对应。当将3d解剖学模型进行缩放时,还可以对内部结构(如肺和心脏)的大小和位置进行缩放。
当对3d解剖学模型进行缩放时,也有可能考虑对象的参数。例如,缩放可以基于对象的体脂量和骨架大小。与具有较少体脂的对象相比,在具有更多体脂的对象中,相对于心脏和肺,胸围可以更大。
任选地,所述方法包括将标志物放置在对象的躯体上,例如放置在剑突处。将标志物设置为在对象躯干的3d图像中可识别的。标志物可以用于确定心脏的位置。剑突处的标志物可以用作心脏下端的参照。
当确定心脏在3d解剖学模型中的位置时,也有可能考虑对象的参数。此类参数可以是,例如对象的重量或年龄。重量可以指示大肚子,其向上推动心脏。因此,可以基于对象的重量改变3d解剖学模型中心脏的垂直位置。心脏趋向于随着年龄的增长位置更加水平。因此,可以基于对象的年龄改变3d解剖学模型中心脏的转动。
因此,通过从数据库中选择合适的标准3d解剖学模型来提供对象特异性的3d解剖学模型的良好近似是可能的。任选地,将所选的3d解剖学模型进行缩放以更好地符合对象解剖学的3d图像。任选地,此类所选3d解剖学模型的缩放包括内部结构如心脏和/或肺的缩放。任选地,基于一个或多个参数(如性别、年龄、重量、身长、胸围、骨架大小、bmi等)的对象特异性的数值改变所选的(以及任选地缩放的)3d解剖学模型中心脏的位置和/或方向。
可以理解,所选的以及任选地改变的3d解剖学模型提供了可以替代对象特异性的3d解剖学模型使用的准对象特异性的3d解剖学模型。鉴于对象特异性的选择,所选的以及任选地改变的3d解剖学模型在本文也被称作对象特异性的(或患者特异性的)3d解剖学模型。
仅从数据库中选择内部结构而解剖学模型来源于3d图像,这也是可能的。然后可以基于一个或多个参数(如性别、年龄、重量、身长、胸围、骨架大小、bmi等)的对象特异性的数值来选择内部结构。可以例如基于患者的重量和年龄选择内部结构(如心脏和/或肺)的大小、位置和方向(对于老年患者或超重患者,心脏更加水平)。
任选地,获得心脏电激活的三维模型包括记录ecg电极在胸部的准确位置。可以理解,知道电极的准确位置将提高心脏电激活的三维模型的准确性。
任选地,获得心脏电激活的三维模型包括将ecg每个电极的测量值与心脏以及任选地肺和胸部的解剖学模型相关联,并通过逆计算估计心脏的电激活。
任选地,获得心脏电激活的三维模型包括将瘢痕组织并入心脏的三维模型。可以通过降低传播速度而在电激活的三维模型中模拟瘢痕组织。对于存在瘢痕组织的心脏壁的区域,也可以通过将一个节点至另一节点的过渡设置得非常慢或者设置为不过渡的来说明瘢痕组织。并入瘢痕组织可以提高心脏同步性定位的准确性绘图。可以理解,瘢痕组织的实际位置可以获自,例如患者特异性的解剖学模型,获自ecg或延迟增强mri图像。
任选地,获得心脏电激活的三维模型包括将血管并心脏的三维模型。血管的布置可以根据心脏瓣膜的位置和心脏和/或心室的解剖学和/或模型。心脏血管或与此类血管位置相关的节点也可以用作刺激位置。例如,起搏器电极有时位于心脏血管如心静脉内。
任选地,所述方法包括基于心脏同步性图确定具有最高同步性的节点。具有最高同步性的节点可以代表这样的节点:当刺激时,其引起心脏最佳同步性激活。如果同步性图是基于任意时间单一节点的同步,则确定的节点可以是最适合人工刺激的节点,例如最佳起搏器电极位置。如果同步性图是基于一个节点与心脏固有激活位点的同步(例如同时),则确定的节点可以是除心脏固有激活之外最适合人工刺激的节点,例如最佳起搏器电极位置。如果同步性图是基于多个节点的同步(例如同时),则确定的节点可以是除所述多个节点(例如多个起搏器电极的位置)中其它节点处的刺激之外最适合人工刺激的节点,例如最佳起搏器电极位置。
任选地,所述方法包括基于心脏同步性图确定一个或多个起搏器电极的期望位置。可以例如如以上所述确定一个或多个起搏器电极的最佳位置。起搏器电极有时位于心脏血管如心静脉内。因此,任选地,根据心脏的三维模型确定此类心脏血管的位置。因此,可以包括心脏血管的位置作为心脏三维模型网格的节点。因此,可以确定心脏血管位置处心脏的刺激及其对同步性的影响,并将其并入同步性图中。
确定起搏器电极的期望位置可以包括确定具有最高同步性的节点。所述方法包括在第一步骤确定与心静脉相关的节点组中具有最高同步性的节点也是可能的。该节点则是起搏器电极的候选期望位置。可以理解,当查看所有节点时,该候选位置节点不必是具有最高同步性的节点。在第二步骤可以确定与候选位置的节点相关的同步性是否在预先确定的可接受的间隔内。如果同步性在预先确定的可接受的间隔外,则在第三步骤可以从与心静脉无关的节点选择具有最高同步性的候选位置。因此,建议通过心外膜线起搏或者无导线起搏。可以理解,在计算机实现的方法中,这些步骤可以自动进行。因此,可以向临床医生建议期望的起搏器电极位置。可以理解,当确定多个起搏器电极的期望位置时也可以应用相同的步骤。
因此,确定起搏器电极的期望位置可以包括鉴于如以上所述的同步性来优化起搏器电极的位置。确定起搏器电极的期望位置还可以包括考虑由节点处的刺激所产生的房室延迟(av延迟)。av延迟(心房与心室之间的延迟)可以用于促进至希氏浦肯野系统(如果该部分仍然完整)的固有av传导。同步性图可以反映作为心脏激活同步性的度量的av延迟。确定起搏器电极的期望位置还可以包括考虑室间延迟(vv延迟)、心室2(3、4...)个刺激位点之间的延迟。同步性图可以反映作为心脏激活同步性度量的vv延迟。
一旦确定一个或多个起搏器电极的期望位置,则可在真实的心脏放置一个或多个真实的起搏器电极。可在本发明的方法的范围之外进行心脏电极的实际放置。可将一个或多个起搏器电极置于期望的位置。可以理解,在实践中,一个或多个真实的起搏器电极在真实的心脏的实际位置可以偏离确定的期望的位置。
任选地,所述方法包括获得心脏一个或多个真实的起搏器电极的位置信息。心脏一个或多个真实的起搏器电极的位置信息可以获自患者特异性的三维解剖学模型。可以例如通过医学成像(如ct和/或mri)获得位置信息。心脏一个或多个真实的起搏器电极的位置信息也可以获自心脏电激活的三维模型。
任选地,所述方法包括在同步性图中指示一个或多个真实的起搏器电极的位置。因此,可以对一个或多个起搏器电极确定的期望的位置与所述一个或多个实际的起搏器电极的实际位置之间的偏离进行评估。因此,可以确定例如期望的位置与实际位置之间的物理距离。此外,可以确定由期望位置处的刺激所产生的同步性与由实际位置处的刺激所产生的同步性之间的差异。因此,可以评估期望的起搏器电极的位置与实际起搏器电极的位置之间的差异是否保证实际电极的重新定位和/或改变起搏器设置,如不激活实际的起搏器电极中的一个或多个。
任选地,一个或多个实际起搏器电极的位置可以用作以上所述的常见刺激位点。可能的是,心脏的固有激活位点可以用作其它常见刺激位点。因此,可以确定由一个或多个真实的起搏器电极处的激活(以及任选地固有激活)所产生的心脏的现实的同步性图。根据该现实的同步性图可以确定一个或多个实际起搏器电极的位置是否是可接受的。
任选地,当在心脏放置多个实际的起搏器电极时,所述方法包括确定一个或多个现实的同步性图,各现实的同步性图通过包含实际起搏器电极的位置作为常见激活位点来确定,对于除一个之外的所有实际的起搏器电极。因此,可以确定重定位哪一实际的起搏器电极对总的心脏同步性具有最有益的效果。但是,也可以确定实际的起搏器电极之一的刺激是否不(或者几乎不)导致或者甚至降低总的心脏同步性。在此类事件中,可将起搏器设置为不激活所述实际的起搏器电极。因此,心脏同步性不或者几乎不受不激活所述电极的不利影响,并且可以减少起搏器的电力使用。
类似地,可以评估其它实际的起搏器电极的重定位或不激活是否是有益的。
在实施方案中,本发明涉及用于提供心脏组织电激活同步性的显示的计算机实现的方法。该方法包括获得心脏、肺和胸部的患者特异性的三维显示。该三维模型包括表示心脏外表面(例如心肌表面)的网格,例如包括隔膜壁,所述网格具有多个节点。所述网格可以包含与心脏血管如心静脉相关的节点。该方法包括获得ecg数据,同时记录记录导线在胸部的准确位置。该方法包括将瘢痕组织并入三维显示。该方法包括使用逆计算程序确定心脏的三维固有电激活模型,所述模型包括表示心脏外表面(例如心肌表面)的网格,任选地包括隔膜,所述网格具有多个节点,各节点具有与其相关的心脏刺激与该节点处的心脏激活之间的时间延迟的数值。对于心脏三维电激活模型各节点,该方法包括在心脏三维解剖学模型中该节点位置处限定刺激位点,并确定由所述刺激位点处的刺激所产生的心脏同步性。
本发明还涉及用于虚拟起搏器电极实施的计算机实现的方法。所述方法包括获得心脏电激活的三维模型。所述方法可以包括获得特定患者的心脏电激活的患者特异性的三维模型。所述三维模型包括表示心脏外表面(例如心肌表面)的网格,任选地包括隔膜壁。所述网格具有多个节点,各节点具有与其相关的表示刺激位点处心脏的刺激与该相应节点处心脏的激活之间的时间延迟的数值。所述方法包括在心脏三维模型的节点处虚拟植入起搏器电极。所述方法包括基于心脏电激活的三维模型和起搏器电极的刺激确定改变的心脏电激活的三维模型。因此,可以模拟由起搏器电极的刺激所产生的心脏的电激活。这提供可在体内安装起搏器电极之前例如在手术之前评估起搏器电极刺激的影响的优势。任选地,方法包括,对于多个节点,重复在心脏三维模型的节点处虚拟植入起搏器电极,并基于心脏电激活的三维模型和该起搏器电极的刺激确定改变的心脏电激活的三维模型的步骤。然后所述方法可以包括基于获得的改变的心脏电激活三维模型的比较选择优选的起搏器电极植入位点。因此,可以考虑心脏的同步性来优化起搏器电极的放置。任选地,对于每一节点,实施在心脏三维模型节点处虚拟植入起搏器电极,并基于心脏电激活的三维模型和该起搏器电极的刺激确定多个节点的改变的心脏电激活的三维模型。在此种情况下,可以产生同步性图,并且如果需要,可将其用于选择优选的起搏器电极植入位点。任选地,所述方法包括在心脏三维模型的相应节点处虚拟植入多个起搏器电极,并基于心脏电激活的三维模型以及(例如同时的)多个起搏器电极的刺激来确定改变的心脏电激活的三维模型。因此,可以在体内安装起搏器电极之前评估多个起搏器电极刺激的影响。可以理解,如以上所述考虑心脏的固有激活是可能的。
任选地,所述方法包括获得一个或多个实际的起搏器电极在心脏的位置信息。任选地,所述方法包括指示一个或多个实际的起搏器电极在心脏电激活的三维模型中的位置。
本发明还涉及用于提供心脏组织电激活的显示的计算机实现的方法。所述方法包括获得心脏电激活的三维模型。所述方法可以包括获得特定患者的心脏电激活的患者特异性的三维模型。所述三维模型包括表示例如心肌表面(例如具有隔膜壁的)的心脏外表面的网格。所述网格具有多个节点,各节点具有与其相关的表示刺激位点处的心脏刺激与该相应节点处的心脏激活之间的时间延迟的数值。所述方法包括在模型中限定心脏三维模型节点处的刺激位点。所述方法包括基于心脏电激活的三维模型和刺激位点处的刺激确定改变的心脏电激活的三维模型。
本发明还涉及用于提供心脏组织电激活的同步性的显示的系统。所述系统包括处理单元。所述处理单元被设置为获得心脏电激活的三维模型,如特定患者的心脏电激活的患者特异性的三维模型。所述三维模型包括表示诸如例如具有隔膜壁的心肌表面的心脏外表面的网格。所述网格具有多个节点,各节点具有与其相关的表示刺激位点处的心脏刺激与该相应节点处的心脏激活之间的时间延迟的数值。对于心脏三维模型各节点,所述处理单元被设置为1)在心脏三维模型中该节点的位置处限定刺激位点,2)基于心脏电激活的三维模型确定由该节点处的刺激所产生的改变的心脏电激活的三维模型,以及3)基于该节点处的刺激确定心脏的心脏激活同步性的度量。所述处理单元被设置为确定表示心脏三维模型的心脏同步性图,其指示在各节点处心脏激活同步性的相应度量。可以理解,可以在例如屏幕上显示同步性图。可以提供对照用于定位,例如在屏幕上旋转和/或缩放同步性图。
本发明还涉及存储计算机可执行指令的非暂时性计算机可读介质或包含计算机程序编码部分的计算机程序产品,所述指令或编码部分当被可编程计算机执行时,使得计算机:
-获得心脏电激活的三维模型,所述三维模型包括表示心肌表面的网格,所述网格具有多个节点,各节点具有与其相关的表示心脏在刺激位点处的刺激与心脏在该相应节点处的激活之间的时间延迟的数值;
-对于心脏三维模型各节点:
-在心脏三维模型的该节点位置处限定刺激位点;
-基于心脏电激活的三维模型确定由该节点处的刺激所产生的改变的心脏电激活的三维模型;
-基于该节点处的刺激确定心脏的心脏激活同步性度量;以及
-确定表示心脏三维模型的心脏同步性图,其指示在各节点处心脏激活同步性的相应度量。
应该理解,鉴于所述方法所述的任何方面、特征和选项同样适用于系统和计算机程序产品,并且反之亦然。同样清楚的是,可将以上方面、特征和选项中的一种或多种进行组合。
附图简要描述
现在将参考附图详细描述本发明的实施方案,其中:
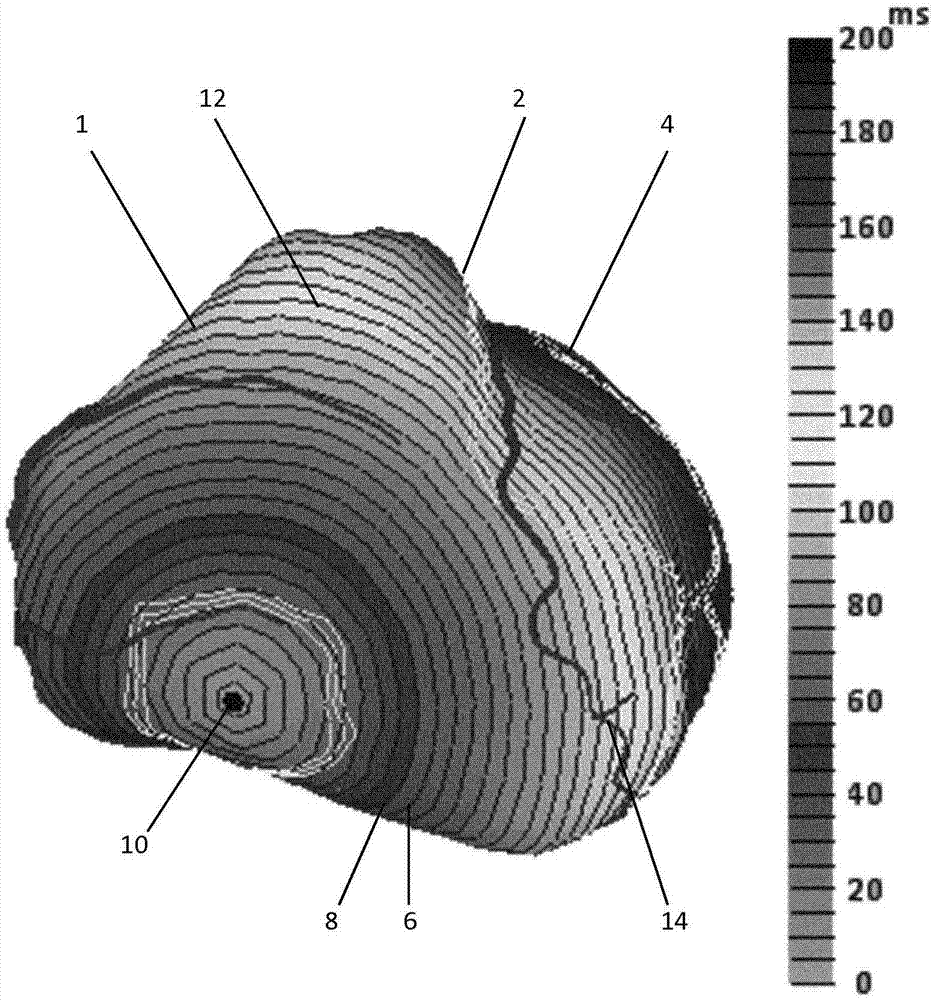
图1是心脏三维模型的实例;
图2a是心脏电激活3d模型的平面图的示意图;
图2b是心脏电激活3d模型平面图的示意图;
图2c是同步性图平面图的示意图;
图2d是同步性图平面图的示意图;
图3是系统的示意图;
图4a是心脏电激活3d模型平面图的示意图;
图4b是心脏电激活3d模型平面图的示意图;
图4c是同步性图平面图的示意图;
图4d是同步性图平面图的示意图;
图5是系统的示意图;
图6是方法的示意性流程图;
图7a是心脏电激活3d模型lao和pa视图的示意图;
图7b是同步性图lao和pa视图的示意图;
图8a是心脏电激活3d模型lao和pa视图的示意图;以及
图8b是同步性图lao和pa视图的示意图。
详细描述
图1显示了在两个不同方向观察的心脏1的三维模型的实例。所述三维(3d)模型包括表示心脏外表面的网格6,在此处是心肌表面。在该实例中,3d模型还包括隔膜壁。网格6具有多个节点8。在该实例中,网格是三角形网格,其中通过邻接的三角形接近心脏表面。
图2a显示了来自单一刺激位置的心脏初始激活。图2a中显示的心脏1是心脏电激活的模型。图2a显示了具有隔膜壁2的心肌的心室表面的图示。图2a是心脏1电激活的三维模型4的平面图。一般而言,三维模型4包括表示心脏的心室表面的网格6,在此是具有隔膜壁的心室心肌的外表面,例如如图1中所示。网格6具有多个节点8。在刺激位置10处电刺激心脏1。在刺激位置10处进行电刺激时,电信号将穿过心脏组织。因此,将在不同的时间激活心脏的不同部分。心脏上的各位置相对于初始刺激具有特定的延迟。各节点8具有与其相关的数值,其表示在刺激位置10处的心脏1的刺激与在该相应节点8处的心脏激活之间的时间延迟。享有相同延迟时间的位置通过图2a中的等时线12连接。在本文中,将等时线定义为3d心脏表面模型上描绘的线,其连接该模型上激活同时发生或到达的点。在该实例中,也通过使呈现的颜色不同来显示整个心脏表面节点的延迟时间。竖线指示与相应颜色相关的以毫秒为单位的时间延迟。可以理解,刺激位置10可以是心脏1的固有激活位置。
图3显示了用于提供心脏组织电激活的同步性的显示的系统100的示意图。所述系统包括处理单元102。图3中的系统还包括存储器104。
心脏1电激活的三维模型4可以获自组合的心电图和医学成像数据。该数据储存于存储器104中。处理单元102可以通讯连接至心电图系统106和医学成像系统108,用于检索数据并将其储存于存储器104中。能够由例如12导联线ecg测定心脏激活的(例如无创)心电图成像(ecgi)方法,可以通过处理单元102应用于确定心脏电激活的三维模型4。可将ecg信号与心脏、肺和躯干的患者特异性的三维解剖学模型组合,以计算心脏等时线的位置。因此,提供了心脏电激活的患者特异性的三维模型。患者特异性的3d解剖学模型可以获自磁共振图像(mri)或计算机断层扫描(ct)图像。可选地或者此外,可以从包括多个3d解剖学模型的数据库中选择显示与患者最接近的一致性的3d解剖学模型,以及任选地改变该模型。所选的以及任选地改变的3d解剖学模型可以用作患者特异性的3d解剖学模型。
心脏1电激活的三维模型4还可以包括信息。在图2a的实例中,模型4包括关于心脏血管,特别是心静脉的信息。根据心脏的患者特异性的三维解剖学模型,可以获得关于血管在心肌的位置的信息。将该信息添加至电激活的3d模型4,因为节点被指示与此类血管相关。然后在心脏1电激活的模型4中鉴定血管14,并任选地使其可见。任选地,处理单元102包括第一识别单元110,其被设置为从患者的心脏三维解剖学模型中自动检索表示此类血管的位置的信息。然后处理单元102可以将该信息自动插入心脏1电激活的3d模型4中。
模型4还可以包括关于瘢痕组织的信息。关于瘢痕组织的位置的信息可以获自延迟增强mri图像,并可以与患者的心脏3d解剖学模型结合。可以通过降低传播速度而在电激活三维模型4中模拟瘢痕组织。对于存在瘢痕组织的心脏壁的区域,也可以通过将一个节点至另一节点的过渡设置的非常慢或者设置为不过渡的来说明瘢痕组织。任选地,处理单元102包括第二识别单元112,其被设置为从心脏的患者特异性的三维解剖学模型中检索表示此类瘢痕组织的位置的信息。然后处理单元102可以将该信息自动插入心脏1电激活的3d模型4中。
因此根据本发明的方面,获得的心脏1电激活的三维模型4可以用于获得关于心脏电激活的其它信息。
在心脏1电激活的三维模型4中,可以确定一个节点至另一节点的激活的时间延迟。这可以用于有利于基于心脏1电激活的3d模型4产生由网格6的其它节点处的初始刺激所产生的其它视图。另外,处理单元102包括插入单元114。插入单元114采用心脏1电激活的3d模型4,并限定某节点作为刺激位置。可以理解,心脏1电激活的3d模型4在预先确定的节点处呈现刺激。出于计算目的,插入单元114可以移除所述预先确定的节点处的刺激。
图2b显示了由另一刺激位置10’处的初始刺激所产生的实例,在此是另一节点8。应认识到,对于网格6的各节点,可以产生由网格6其它节点处的初始刺激所产生的视图。
以单一参数:心脏激活同步性来概述由特定节点处的刺激所产生的整个心脏1的特定电激活顺序。心脏激活的同步性提供整个心脏如何同步激活的指示。对于常见情况,认为心脏更加同步性的激活是有益的。在该实例中,心脏激活同步性的度量是心脏去极化(dep)时间的标准差(std)。因此,心脏激活的同步性提供由相应节点处的刺激所产生的整个心脏激活的同步性的指示。处理单元102包括同步性测定单元116,其设置为测定心脏激活的同步性。
根据本发明的方面,分别确定各节点处的刺激的心脏激活同步性。因此,提供了网格各节点的心脏激活同步性的度量。处理单元102包括同步性图产生单元118,其设置为通过同步性测定单元116,基于各节点的心脏激活同步性的计算而产生同步性图。处理单元102可与输出单元120通讯连接,所述输出单元设置为向用户输出同步性图15和/或可选数据。输出单元可以是显示单元、打印机、信息传递单元等。
图2c显示了心脏同步性图15的实例。在该图2c中,指示了各节点处心脏激活同步性的相应度量。在该实例中,指示是伪彩色。在图2c中,指示了异同步性线16。这些异同步性线连接具有相同心脏激活同步性度量的节点。心脏同步性图提供了简单的单一的三维概观,显示心脏上哪些位置导致良好的心脏激活同步性以及心脏上哪些位置导致较差的心脏激活同步性,如果在此类位置刺激心脏的话。例如在该实例中,可以观察到原始刺激位置10不提供特别好的同步性,其中心脏激活同步性的数值为大约45ms心脏去极化时间的标准差。在该实例中,最不适合的刺激位置以s-指示,在此所述位置具有最高心脏激活同步性数值。在该实例中,最有利的刺激位置由s+指示,在此所述位置具有最低心脏激活同步性数值。应当注意,如图2d中所示,当从另一方向查看同步性图15时,可以最好地观察到最有利的刺激位置s+。
心脏激活同步性的度量的其它实例是去极化时间的范围(最大去极化时间–最小去极化时间)。去极化时间的范围可对周期长度进行校正。心脏激活同步性的度量的其它实例是仅左心室(lv)去极化时间的标准差。心脏激活同步性的度量的其它实例是刺激与隔膜激活之间的延迟。心脏激活同步性度量的其它实例是av延迟。心脏激活同步性的度量的其它实例是vv延迟。可以理解,可以根据手头的任务和/或根据患者经历的具体病况或异常来选择心脏激活同步性的度量。
在图4a中显示了第二实例。在该实例中,限定第二刺激位置18。然后利用心脏1电激活的三维模型4以及第一刺激位置10和第二刺激位置18处的同时刺激计算心脏1的电激活。可以理解,在该实例中,插入单元114不出于计算目的移除第一位置8处的刺激。图4a显示了所计算的产生的心脏1的电激活。可以理解,由于添加了第二刺激位置18,总激活时间缩短。在该实例中,第一刺激位置10表示心脏1固有激活的位置或者进行刺激的第一选择位置或者由心脏内已经存在的起搏器导线所产生的刺激的位置。
图4b显示了分别由与第一刺激位置10处的刺激同时的其它第二刺激位置18’处的初始刺激所产生的实例。可以理解,对于网格6各节点,可以产生由与与第一刺激位置10相关的第一节点处的刺激同时的网格6其它第二节点处的初始刺激所产生的视图。
在图4c和4d的实例中,将由与第一刺激位置10处的刺激同时的第二刺激位置18处的刺激所产生的整个心脏1的特定电激活顺序总结为心脏激活同步性。然后心脏激活同步性可以再次提供整个心脏激活如何同步的指示。根据本发明的方面,分别确定与第一10和第二18刺激位置处的刺激同时的各节点处的刺激的心脏激活的同步性。因此,提供作为第三刺激位置的网格的各节点心脏激活同步性的度量。图4c显示了心脏同步性图的实例。图4c的心脏同步性图提供了简单的单一的三维概观,其显示心脏上哪些位置导致良好的心脏激活同步性以及心脏上哪些位置导致较差的心脏激活同步性,如果在此类位置与第一刺激位置10和第二刺激位置18处的刺激同时刺激心脏的话。在该实例中,当与第一刺激位置10和第二刺激位置18同时刺激时,最不利的第三刺激位置,在此是具有大约为41ms心脏去极化时间的标准差的最高心脏激活同步性数值的位置,由s-指示。在该实例中,当与第一刺激位置10和第二刺激位置18同时刺激时,最有利的第三刺激位置,在此是具有最低心脏激活同步性数值的位置,由s+指示。应当注意,如图4d中所示,当从另一方向查看同步性图15时,可以最好得观察到最有利的刺激位置s+。
图5显示了用于提供心脏组织电激活的同步性的显示的系统100的另一示意图。图6显示了确定心脏同步性的方法的示例性示意流程图。
所示系统包括从硬件模块接收数据的处理单元102。任选地,处理单元102从心电图系统106接收ecg数据。处理单元从医学成像系统108接收患者特异性的解剖学数据。任选地,处理单元102从定位系统109接收关于ecg导线相对于患者的解剖结构(例如3d图像和定位至3d图像的躯干模型)的位置的信息。ecg导线位置也可以手动输入系统。
处理单元102根据患者特异性的解剖学数据确定同步性图15。此外,在该实例中,处理单元102包括下述单元并进行下述步骤。
为了产生同步性图,处理单元102需要患者胸部的患者特异性的3d解剖学模型以及胸部内心脏的大小、方向和位置。需要选择此类模型201以进一步用于处理单元。可以是此类模型已经可用202。在该实例中,如果模型还不可用,则检索单元103检查204数据库117中是否存在该患者的合适的解剖学模型。若是这样,检索单元103从数据库117中检索所述合适的解剖学模型。检索单元可以使来自数据库的解剖学模型适合患者的3d图像,以将所选解剖学模型转换206为(准)患者特异性的3d解剖学模型。如果在数据库117中无合适的患者特异性的解剖学模型,则检索单元103基于接受的患者特异性的解剖学3d图像数据产生患者特异性的解剖学模型。
任选地,患者特异性的3d模型还包括其它结构(如肺)的大小、方向和/或位置。患者特异性的3d模型可以是体积导体模型。
根据关于ecg导线的位置的信息和患者特异性的模型,导线定位器模块105可以确定ecg导线在患者特异性的模型中的相应位置,从而提供210增强的患者特异性的模型。
利用可用的患者特异性的解剖学模型和/或增强的患者特异性的模型,检查212表示固有激活或刺激激活的ecg数据是否可用。如果固有激活数据或者已经存在的一个或多个起搏器导线的起搏刺激可用,则激活单元107基于(增强的)患者特异性的模型和ecg数据确定214患者心脏当前激活的3d电模型。
如果没有可用的关于固有激活或刺激激活的ecg数据,则虚拟刺激单元111基于之前确定的和/或假定的节点之间的过渡速度向心脏的电模型添加216初始虚拟刺激。假定的过渡速度可以是例如0.8m/s。可以理解,电模型可以包括以上所述的动脉、静脉和/或瘢痕组织。这获得218患者心脏的虚拟激活的3d电模型。
同步性确定单元116根据患者心脏的固有激活、刺激激活或虚拟激活的3d电模型确定222以上所述的同步性图。
基于同步性图,处理单元102可以确定230人工刺激位置或虚拟刺激位置是否导致最佳激活和同步性。若是这样,该过程可以提供234患者心脏优选刺激位置的计算。
如果还未达到最佳同步性,则根据同步性图确定232是否应该添加额外的虚拟刺激位置,或者是否应该结合定时参数移动或改变虚拟刺激位置。
如果应该移除或改变虚拟刺激位置,则系统将相应地调节225人工刺激位置或虚拟刺激位置。然后可以重新确定激活226并且可以重新计算同步性222直至如所期望的激活230。
系统还可以结合其当前刺激参数虚拟调整当前人工刺激位置,即起搏器导线,以达到最佳同步性。
所述系统还可以用于评估多重刺激。所述多重刺激可以是例如固有激活和刺激激活(起搏)的组合。所述多重刺激可以是例如多重刺激激活(起搏)。可能的是,用户或处理单元102确定232是否另外的刺激位置例如另外的起搏器导线是期望的。
如果另外的刺激位置是期望的,则通过插入单元114插入另外的刺激位置。然后可以重新确定具有初始刺激位置(固有的、刺激的或虚拟的)和添加的虚拟刺激位置的情况下的激活226,并且可以重新计算同步性222。基于同步性图,处理单元102可以确定230另外的虚拟刺激位置是否导致最佳同步性。如果还未达到最佳同步性,则根据同步性图确定232是否应该添加额外的刺激位置,或者是否应该结合定时参数移动、改变虚拟刺激位置,或者甚至移除虚拟刺激位置。在此种情况下,重复该过程(三次、四次、五次等)。
因此,基于患者特异性的心脏激活模型,可以确定心脏同步性模型。同步性模型可以是包括异同步性线的3d心脏表面模型。在同步性模型中,异同步性线表示心脏激活的同步性。该同步性可以基于特定的激活条件,如起搏器导线位置处的右心室激活。
作为实例,可以如下产生同步性模型。
确定固有(左束支传导阻滞,lbbb)模式的激活等时线。这可以在下述步骤中完成。
1a)例如基于患者的mri或ct图像确定心脏、肺和胸部的患者特异性的解剖学3d模型或者其来源于取自适合患者大小的数据库的模型(例如通过使用3d相机)。解剖学3d模型可以例如包括心脏的3d表面模型、肺的3d表面模型和胸部的3d表面模型。通过在其转角连接的多个多边形(如三角形)的网格,3d表面模型可以是真实表面的密切近似。相互连接的转角形成网格的节点。
1b)测量ecg,例如12导联ecg。可以记录ecg装置的电极在胸部的准确位置。将三维解剖学模型中电极的位置用于评估心脏组织中电活性的分布、波动和/或运动。可将ecg装置的记录导线的准确位置输入胸部的解剖学3d表示。
1c)任选地,将瘢痕组织并入心脏的解剖学3d表示。瘢痕组织的存在和位置可以来源于延迟增强mri图像。
1d)使ecg装置的每个记录导线的测量值与心脏和躯干的几何形状相关。可以利用逆向程序确定固有激活。心脏组织中电活性的分布、波动和/或运动可以例如基于心肌距离函数、最快路径算法、最短路径算法和/或快速行进算法。
2)一旦确定固有(lbbb)模式的激活等时线,则向心脏各节点的固有激活添加刺激位点,并由结果计算心脏的期望同步性。节点在此意为解剖学3d心脏模型所基于的三角形的交点。
以上方法还可用于确定心脏起搏器电极放置的最佳位置。为了确定最佳起搏位点,可以计算同步性图。
与找到的/选择的最佳刺激位置组合的固有激活导致新的心脏等时线定位图。
图7a显示了lbbb模式固有激活的实例。图7a左图显示了完全相同的心脏1电激活的三维模型4的左前斜(lao)视图,右图显示了其后前位(pa)视图。图7b显示了图7a中显示的心脏1的同步性图15的实例。图7b左图显示了lao视图,右图显示了pa视图。图7b的同步性图显示了由与心脏的固有激活组合的一个额外的刺激位置所产生的心脏去极化时间的标准差。从图7b可以看出在基底左游离壁20上的区域中选择另外的刺激位置最大降低了心脏去极化时间的标准差。因此,在该实例中,可以选择基底左游离壁上的区域作为起搏器电极(如crt导线)的最佳位置。可以理解,可以产生更新的心脏电激活的三维模型,其包括与基底左游离壁上的区域中的刺激同时的固有激活。
然后可将所述图用于产生新的同步性图,以检查右室中的导线位置。通过这样做:
-可以确定所述导线是否必须进行刺激而非仅进行传感,
-可以确定是否应该移动所述导线,
-可以确定是否应该添加额外的刺激导线。
-可以确定固有av传导是否是有益的。固有av传导通常将传导至右束支,之后需要通过刺激lv来激活lv。所有这些还均可逆转,即利用rbbb等待lv激活并在最佳位置处刺激rv游离壁。
-通过在左心室和右心室重复该程序,可以微调心脏起搏的准确位置和时间。
当由于心脏的严重损伤固有激活信号不可用时,整个程序可以仅使用模拟(起搏器)刺激替代固有激活。在此种情况下可以省略程序步骤1b和1d。整个程序则将基于人工激活。
图8a显示了lbbb模式左刺激激活的实例。图8a左图显示了lao视图,右图显示了pa视图。图8b显示了图8a中显示的心脏1的同步性图的实例。图8b左图显示了lao视图,右图显示了pa视图。图8b的同步性图显示了由与心脏的左刺激激活组合的一个额外的刺激位置所产生的心脏去极化时间的标准差。从图8b可以看出在基底左游离壁20上的区域中选择另外的刺激位置最大降低了心脏去极化时间的标准差。因此,在该实例中,可以选择基底左游离壁上的区域作为起搏器电极(如crt导线)的最佳位置。可以理解,可以产生更新的心脏电激活的三维模型,其包括与基底左游离壁上的区域中的刺激同时的固有激活。
也可以在植入程序期间确定整个程序以找到最佳起搏位点。
在本文中,参考本发明的实施方案的具体实例来描述本发明。但是,显而易见的是,在不脱离本发明的本质的情况下,可在其中做出多种修改和改变。出于清楚和简要描述的目的,本文描述的特征为相同的或单独的实施方案的一部分,但是也考虑具有这些单独的实施方案中的所有或一些特征的组合的可选实施方案。
当从数据库中选择患者躯干的3d解剖学模型时,所述数据库包括多个相互之间不同的3d解剖学模型。3d解剖学模型可以例如在躯干和内部结构(如心脏和肺)的大小方面不同。3d解剖学模型可以表示与不同参数数值对应的参考躯干,所述参数如性别、年龄、重量、身长、胸围、骨架大小和身体质量指数中的一种或多种。可以理解,数据库中的各3d解剖学模型可以例如来源于相应参照对象的医学成像模态,如mri、ct、pet-ct、超声等。数据库中的一些或全部3d解剖学模型是虚构参照患者的虚构呈现也是可能的。
可以基于诸如性别、年龄、重量、身长、胸围、骨架大小、bmi等的参数从数据库中选择最合适的3d解剖学模型。可以基于例如通过测量、询问或测试已知的对象的参数使此类选择自动化。所述选择还可以基于对象躯干的3d图像与数据库中的3d模型的视觉比较。可以基于躯干3d图像的形状和3d解剖学模型躯干的形状的计算机识别使此类选择自动化。应认识到,数据库中不同的3d模型的数目越多,数据库中的3d模型之一与患者躯干的匹配越好。出于本发明的目的,选自数据库的3d解剖学模型可以用作患者特异性的3d解剖学模型。
可以通过将所选3d模型缩放至患者躯干的3d图像和/或将3d图像缩放至3d躯干模型进一步提高患者的躯干与所选3d模型之间的一致性。可将3d解剖学模型进行缩放以使模型中躯干的外表面与获自3d图像的对象的躯干的外表面相对应。此类缩放可以包括将3d解剖学模型斜移或翘曲。在将3d解剖学模型进行缩放的同时,也可将内部结构(如肺和心脏)的尺寸和位置进行缩放。
当将3d解剖学模型进行缩放时,可以通过考虑对象的参数数值而进一步提高患者躯干与所选3d模型之间的一致性。例如,缩放可以依赖于对象的体脂量和骨架大小。相对于具有较少体脂的对象,具有较多体脂的对象的胸围相对于心脏和肺的尺寸更大。
可以通过基于对象的参数数值改变心脏在所选3d解剖学模型中的位置而进一步提高患者的躯干与所选3d模型之间的一致性。此类参数可以是例如对象的重量或年龄。重量可以指示大腹部,其向上推动心脏。因此,可以基于对象的重量改变心脏在3d解剖学模型中的垂直位置。心脏趋向于随着年龄的增长位置更加水平。因此,可以基于对象的年龄改变3d模型中的心脏的转动。
在所述实例中,所述三维模型包括表示心肌表面的网格,所述网格具有多个节点。3d模型包括体网格,例如包括立方体或四面体也是可能的。
应认识到,处理单元可以体现为专用电子电路,可能包括软件编码部分。处理单元还可以体现为在可编程设备上执行以及例如在可编程设备的存储器中储存的软件编码部分,所述可编程设备如计算机。
尽管参考附图描述的本发明的实施方案包括计算机设备和在计算机设备上执行的进程,本发明还扩展至计算机程序,特别是适用于将本发明付诸实践的载体上或载体中的计算机程序。所述程序可以是源代码或目标代码形式或者是适合用于根据本发明的进程的实施的任何其它形式。载体可以是能够携带程序的任何实体或装置。
例如,载体可以包括存储介质,如rom(例如cdrom或半导体rom)或磁记录介质(例如软盘或硬盘)。此外,载体可以是可传输载体,如可以经电缆或光缆或者通过无线电或其它方式,例如经互联网或云传送的电信号或光信号。
当将程序体现在可以通过缆线或者其它装置或方式直接传送的信号中时,载体可以由此类缆线或者其它装置或方式组成。可选地,载体可以是包含程序的集成电路,所述集成电路适用于进行相关过程或者用于相关过程的执行。
但是,其它修改、变化和可选方案也是可能的。因此,说明书、附图和实例被认为具有说明意义而非具有限制意义。
出于清楚和简要描述的目的,本文描述的特征作为相同或不同实施方案的一部分,但是,应理解,本发明的范围可以包括具有所述特征全部或部分的组合的实施方案。在权利要求中,置于括号中的任何参考符号不应被解释为限制所述权利要求。单词‘包括’不排除除权利要求中所列的那些特征或步骤之外的其它特征或步骤的存在。此外,单词‘一个/一种(a)’和‘一个/一种(an)’不应被理解为限于‘仅一个/一种’,而是用于意指‘至少一个/一种’,并且不排除多个/多种。在相互不同的权利要求中叙述某些度量的事实并不指示这些度量的组合不能用于获益。
- 还没有人留言评论。精彩留言会获得点赞!