用于中心静脉压测量状态的方法和设备与流程
本发明涉及用于测定中心静脉压的方法,以及被配置成测定中心静脉压的设备。
背景技术:
中心静脉压(cvp)是指平均腔静脉压或右心房压,相当于无三尖瓣狭窄时的右心室舒张末期压力。cvp越高,右心室的被动舒张期充盈越大。根据正常心脏中的史达林氏(starling’s)心脏功能曲线,右心室的充盈越大,在随后搏动中右心室的搏出量越大。cvp以高于大气压的毫米汞柱(mmhg)或厘米水柱(cmh2o)表示(1.36cmh2o=1.0mmhg)。在大多数患者中,由cvp度量的平均右心房压与平均左心房压(lap)非常相似。在心脏舒张的末期,假设左心房压等于左心室舒张末期压力(lvedp),继而假设左心室舒张末期压力反映左心室舒张末期容量(lvedv)。因此,cvp反映左心室前负荷,这是优化心脏功能的关键参数。然而,在具有阻塞、或瓣膜问题或肺部疾病的患者中,左右心室可以独立地工作。在这些不太常见的情况下,应通过使用肺动脉导管(pac)测量肺毛细血管“楔”压来估计左心室前负荷,因为这是比cvp更好的了解通往心脏左侧的静脉回流的指引。
中心静脉压(cvp)测量对于监测危重患者、患有心力衰竭的个体和接受手术的患者的血液动力学以评估心脏前负荷和循环血容量至关重要。目前用于测量cvp的标准技术是侵入性的,需要将导管插入锁骨下或颈内静脉,具有潜在的并发症。由于cvp是右心房的压力,因此系统必须相对于右心房或静脉静止轴(phlebostaticaxis)的位置“归零”。该参考点位于第四肋间隙和腋中线的交叉点,从而使测量尽可能靠近右心房。
可以通过颈部颈静脉的体格检查来估计cvp。颈外静脉在胸锁乳突肌上经过,而颈内静脉深入其中。当受试者处于斜卧位时,颈外静脉的下部通常扩张而上部则塌缩。因此,颈静脉压(jvp)提供了中心静脉压的间接测量。颈内静脉在没有任何中间瓣膜的情况下连接到右心房,用作右心房中的血液的血柱。不幸的是,由于患者位置和临床医生测量技术的差异,jvp测量是困难的并且容易产生测量错误。cook等人在1996年进行的一项系统性的回顾得出的结论是医生之间关于颈静脉压的意见非常不统一。cook,deborahj.和davidl.simel.“doesthispatienthaveabnormalcentralvenouspressure?”[这名患者的中心静脉压是否异常?]jama[美国医学会杂志]275.8(1996):630-634。当通过jvp检查测定心力衰竭患者的cvp时,存在一种错误的观念,即如果患者处于体液超负荷状态,则更容易观察到颈静脉搏动。然而,由于颈静脉搏动依赖于右心房和心室收缩,如果患者处于射血分数较低的心力衰竭中,则可能难以察觉到搏动。
一种简单、准确、非侵入性和自行施用的cvp测定法将代表用于评估心脏功能和整体血液动力学状态以包括容量状态、体液超负荷和左心室舒张末期压力(lvedp)的宝贵工具。这种自行施用的测试对患有充血性心力衰竭的患者的非卧床监测具有重要价值。
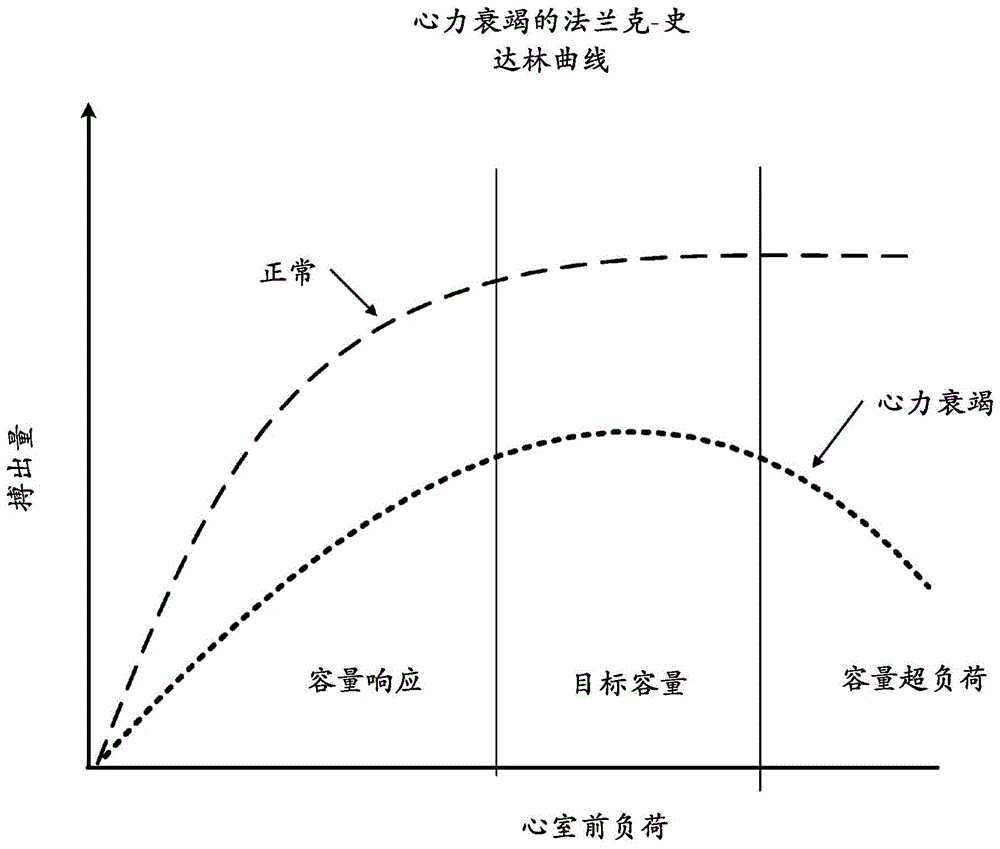
心力衰竭是由心输出量不足引起的。因此,管理目标集中于优化心脏功能受限患者的搏出量。搏出量严重依赖于心脏舒张末期左心室的血量,即舒张末期容量。图1是心力衰竭患者的心脏机能的图示。当舒张末期充盈压力超过最佳水平时,心力衰竭患者的心脏整体机能由降低的搏出量限定。心脏的最佳性能发生在有限的舒张末期压力范围内,并且在图中标记为“目标容量”且使用法兰克-史达林(frank-starling)曲线表示。因此,这些患者的体液管理至关重要;体液过少导致搏出量降低,而体液超负荷也会导致搏出量降低。
心力衰竭是一个重大的医学问题,美国每年花费在此的医疗费用估计约为300亿美元,其中80%的费用因入院而产生。通过提高非卧床管理来减少入院的能力一直是一项长期临床目标。与心力衰竭相关的住院治疗的主要原因是体液超负荷。体液超负荷的历史监测方法诸如呼吸短促、肿胀、疲劳和体重增加不足以敏感地反映出早期病理生理变化,这增加了代偿失调和随后入院的风险。lewinj,ledwidgem,o’loughlinc,mcnallyc,mcdonaldk.clinicaldeteriorationinestablishedheartfailure:whatisthevalueofbnpandweightgaininaidingdiagnosis?[已确立的心力衰竭的临床恶化:bnp和体重增加对于辅助诊断的价值是什么?]eurjheartfail.[欧洲心力衰竭杂志]2005;7(6):953-957。stevensonl,perloffjk.thelimitedreliabilityofphysicalsignsforestimatinghemodynamicsinchronicheartfailure[用于评估慢性心力衰竭中的血液动力学状态的生理指标的可靠性有限],jama.[美国医学会杂志]1989;261(6):884-888。图2显示了心力衰竭患者的典型临床过程,其中体液超负荷的增加导致住院治疗。对该图的检查表明,临床上可观察到的体征出现在整个代偿失调序列的后期。因此,使用临床症状管理心力衰竭患者存在问题。
最近完成的bettereffectivenessaftertransition—heartfailure[过渡后的更好疗效—心力衰竭](beat-hf)研究证明了测定早期血液动力学淤血存在困难。这项研究涉及超过1400名患者,利用现有的非侵入性技术对这些患者进行了广泛的监测。该研究采用包括出院前心力衰竭教育、定期电话指导和远程监测在内的方案调查了对心力衰竭患者的积极管理。远程监测包括集成有文本装置的支持蓝牙的体重计和血压/心率监测器,该文本装置将信息发送到集中式呼叫中心进行审查。如果超过预先确定的阈值,则呼叫患者并由临床人员确定改变药物。而且,如果报告了严重症状,则将通知患者的心力衰竭医师,并且在必要时将患者送往急诊科。这项广泛的临床研究得出的结论是干预对医院再入院率没有明显影响。
通过使用侵入性植入的肺动脉压监测系统,已经证明了入院率的降低。cardiomemshf系统测量并监测心力衰竭患者的肺动脉(pa)压和心率。该系统由可植入pa传感器、递送系统和患者电子系统组成。可植入传感器永久地置于肺动脉中,肺动脉是将血液从心脏移动到肺部的血管。在右心导管插入术期间植入传感器。患者电子系统包括电子单元和天线。患者电子系统从传感器无线地读取pa压力测量结果,然后将信息传递给医生。在分析该信息后,医生可以改变药物以帮助治疗患者的心力衰竭。在一项有550名参与者植入了该装置的临床研究中,其医生可以获得pa压数据的参与者的心力衰竭相关住院治疗在临床和统计上显著减少。该系统的植入成本约为2,000美元,并且定价为18,000美元。
cvp的准确、自行施用和非侵入性测量将是重要的医学进步,因为它将提供与昂贵的、侵入性cardiomems系统具有同等价值的信息。具体地讲,cvp是右心房压的量度,并且与平均左心房压(lap)非常相似。在心脏舒张末期,假设左心房压等于左心室舒张末期压力(lvedp),继而假设lvedp反映左心室舒张末期容量(lvedv)。因此,cvp与左心室前负荷直接相关,左心室前负荷是优化心力衰竭患者心输出量的关键参数。
技术实现要素:
本发明的实施例通过提供用于测定中心静脉压的非侵入性、非植入和自行施用的测试法解决了当前中心静脉压监测的局限性。该系统使用跨壁压的变化、静脉容量的光学测量结果和解剖测量结果来测定中心静脉压。该系统可以提供中心压力的绝对测量结果,或者可以用于监测中心静脉压随时间的相对变化。跨壁压的变化用于产生外周静脉血管容量的可检测变化以用于中心静脉压测量。通过血管内或血管外压力变化可以引起跨壁压变化。该系统在存在规定的跨壁压变化的情况下非侵入性地测量静脉容量的变化。跨壁压变化与血管静脉容量变化之间的关系与解剖测量结果一起用于测定患者的中心静脉压。中心静脉压的变化与心血管功能相关,并且可用于心力衰竭患者的有效管理。
该测量过程使用对静脉容量变化敏感的光学检测方法。这些光学变化可用于在存在限定的跨壁压变化的情况下测定中心静脉压。该光学测量系统以非接触方式或以限定的接触方式与静脉系统相互作用。该测量过程解决了测量的细微差别,包括静脉容量响应的延迟、自主功能、位置敏感性和患者之间的解剖差异。测得的中心静脉压提供心血管评估,以便以主动方式管理心力衰竭患者,从而避免体液超负荷和可能的入院。
附图说明
图1是法兰克-史达林曲线的示意图。
图2是血液动力学淤血随时间变化的示意图。
图3是心脏病中外周静脉压的图线。
图4是静脉扩张性的示意图。
图5是容量变化与静脉压关系的图线。
图6是臂抬高时静脉容量变化的图示。
图7是臂抬高时的生理效应的图示。
图8是使用臂升高改变跨壁压的图示。
图9是比较组织测量部位的图示。
图10是示出压力对测量部位的影响的图示。
图11是示出跨壁压变化率的影响的图示。
图12是腕部安装式传感器系统的图示。
图13是手环测量系统的图示。
图14是基于手指的测量系统的基部的图示。
图15是静脉成像系统的图示。
图16是使用外部袖带改变跨壁压的示意图。
图17是呼吸引起的时变跨壁压变化的图示。
图18是呼吸引起的时变跨壁压变化的第二图示。
图19示出了用于改变跨壁压的压力曲线的实例。
图20是跨壁压的血管外变化期间的静脉成像的实例。
图21是示出静脉静止轴的位置的图示。
图22示出了来自受试者图像的解剖测量的标识。
图23示出了使用光学方法标识心脏的位置。
图24是人体解剖结构的联动模型的图示。
图25是使用头部位置的受试者重新定位的实例。
图26是使用头部位置的第二示例性受试者重新定位。
图27示出了头部的横滚、俯仰和偏转的测定。
图28是解剖测量和受控制的臂运动系统的图示。
图29是用于最小化时间延迟的影响的测量方案的图示。
图30是具有受控制的臂抬高的静脉成像的实例。
图31是受试者发起的臂运动的图示。
图32是在受试者发起的臂运动期间基于腕部的光学数据的实例。
图33是利用动态空气压力的中心静脉压测量系统的图示。
图34是由空气压力引起的静脉容量变化的实例。
图35是利用静态空气压力的中心静脉压测量系统的图示。
图36是利用静态空气压力的中心静脉压测量系统的示意图。
图37示出了使用静态空气压力改变跨壁压的中心静脉压测定。
图38示出了使用静态空气压力的中心静脉压的敏感度。
图39是光学血压计(tonometer)示例性实施例的图示。
具体实施方式
定义
跨壁压是描述血管壁两侧的压力的一般术语(跨壁字面意思是“壁两侧”),并且通过以下等式定义:
p跨壁=p内侧-p外侧
如果存在正跨壁压(内部压力大于物体外部压力),则柔性容器扩展;而如果存在负跨壁压,则柔性容器收缩。正跨壁压有时被称为“扩张”压力。跨壁压变化是指改变内部压力与外部压力之间的关系的任何机制。用于改变内部压力或血管内压力的方法包括但不限于位置变化、静水压变化、搏出量变化、血管容量变化、心脏收缩性变化和运动。用于改变外部压力或血管外压力的方法包括但不限于胸内压变化,位置变化,水、空气或其他方式对脉管系统的压迫,使用真空方法,阻力呼吸,机械式呼吸,腹部压迫,瓦氏(valsalva)动作,穆勒(mueller)动作和肌肉收缩。
阻力呼吸是一个一般术语,适用于与正常呼吸相比升高、降低或改变胸内压的任何方法。阻力呼吸测试可包括单独或组合的吸气阻力呼吸和呼气阻力呼吸。呼气阻力呼吸的使用将产生胸内压的升高,而吸气阻力呼吸的使用产生胸内压的降低。可以使用各种方案诸如节奏性呼吸和事件限定的呼吸来执行阻力呼吸。节奏性呼吸限定吸气和呼气的目标时间,使得呼吸速率恒定。事件定义的呼吸是一种阻力呼吸,其中受试者在单次呼吸中克服阻力呼气或吸气,然后进入休息或恢复期。术语阻力呼吸还涵盖在有很少或没有空气运动的情况下产生胸内压变化的过程。产生升高或降低的闭塞压力作为阻力呼吸的广泛定义的一部分被包括在内。
静水力学位置变化是一个一般术语,适用于由于位置变化或其他方式而改变血管中的静水压的任何过程。
心力衰竭病因和cvp测量
由于心力衰竭的病因,心血管功能的变化与整体体液状态的变化相关,并且反映在中心静脉压或血液动力学淤血中。血液动力学淤血的测定是心力衰竭患者的心血管评估的关键指标,然而目前的测定方法不适用于家庭环境。侵入性测量提供中心静脉压的准确估计,但对于非卧床患者来说则不实用。植入技术具有适用性,但价格昂贵。超声或超声心动图方法可以估计升高的中心压力,但是耗时且需要训练有素的操作者。
静脉血液动力学
本发明认识到外周静脉压(pvp)反映通过类似于肺动脉闭塞导管与左心房之间存在的流体连续性的连续血柱耦合至cvp的“上游”静脉变量。syndercl,saltzmand,happej,eggenma,ferrellkl,leonardas.peripheralvenousmonitoringwithacutebloodvolumealteration:cuff-occludedrateofriseofperipheralvenouspressure[急性血容量改变的外周静脉压监测:袖带阻塞的外周静脉压上升率],critcaremed[危重病急救医学]1990;18:1142-5.3。
winsor等人于1945年研究了外周静脉压与心脏病的鉴别诊断和临床管理之间的关系。作者证实了心力衰竭患者中肘正中静脉的静脉压升高。图3从该出版物中复制并且示出了患有iii类和iv类心脏病的受试者的外周静脉压的显著升高。呈现的测量结果是通过静脉血压计测得的,静脉血压计是具有压力测量系统的侵入性静脉导管。本发明还认识到,当患有血管内容量不足或心力衰竭的患者坐起时,cvp显著下降,同样如图3所示。winsor,travis,andgeorgee.burch.“useofthephlebomanometer:normalvenouspressurevaluesandastudyofcertainclinicalaspectsofvenoushypertensioninman”[静脉血压计的使用:男性中的正常静脉压值和静脉高血压某些临床方面的研究],americanheartjournal[美国心脏杂志]31.4(1946):387-406。
静脉扩张曲线
外周微静脉和静脉是薄壁、盘绕的血管,并且容纳大约三分之二的循环血液。静脉系统充当胸腔隔室的可变血液贮存器并且影响心脏充盈压力。压力对静脉容量的影响在0与10mmhg之间特别陡峭,因为薄壁静脉容易变形,如图4所示。在零跨壁压以下,静脉塌缩成哑铃形状,并且任何流动都被限制于边缘通道。在1mmhg的跨壁压下,静脉几乎塌缩并且具有窄的椭圆形轮廓。随着压力朝向10mmhg上升,椭圆形轮廓逐渐变圆,使得静脉能够仅以几mmhg的压力变化即可适应较大容量变化。在10mmhg至15mmhg以上,该轮廓是完全圆形的,并且由于壁中的拉伸胶原相对不可伸展,因此该容量对超过15mmhg的压力不太敏感。最大扩张性(容量变化/压力变化)发生在约4mmhg。对于静脉系统,该扩张性估计约为100ml/mmhg,是动脉系统的50倍以上。
在完整的血管系统内,血液以约12mmhg至20mmhg的压力从毛细血管进入微静脉。当血液到达较大的指定静脉诸如肱静脉时,压力已降至约8mmhg至10mmhg。随后的静脉阻力非常小(除了在塌缩的血管中),因此8mmhg至10mmhg的压头足以将心输出量从外周驱动进入中心静脉和右心室,其中舒张压为0mmhg至6mmhg。
静脉塌缩与cvp之间的关系
为了清楚起见,图4的扩张性曲线已经在图5中被重新绘制,并且压力现在被表示为跨壁压,其中在横坐标的左侧为正跨壁压。当跨壁压为零或小于零时,发生完全静脉塌缩。因此,图5示出了在x轴上的由于臂运动而引起的跨壁压变化,以及在y轴上的容量减小。
图6是当臂从向下位置移动到向上位置时跨壁压和静脉容量的变化的图示。出于说明目的,在患者的腕部上定位光学监测装置。当臂在下(位置1)时,由于静脉血柱产生的静水压,跨壁压非常高。如曲线图上方所示,静脉被充盈,具有圆形轮廓。在该位置,由于定位在扩张性曲线的较平坦部分上,静脉容量对压力的微小变化相对不敏感。当臂移动到接近更水平的基准(位置2)时,由于静水压的降低,跨壁压降低。静脉大小和静脉容量相应减小。
在位置3处,臂上的光学感测位置已达到一定高度,使得跨壁压接近零,并且因此静脉将塌缩。外周静脉压继而cvp等于塌缩点处的压力加上由该点与右心房之间的竖直血柱施加的压力。例如,如果塌缩点(零跨壁压)发生在右心房中点上方7cm处,则cvp为7cm血液(7.4cmh2o)。该竖直高度在图中示为cvp压力线。
当臂抬得更高时例如抬高至图6中的位置4,静脉容量变化很小,因为静脉已经处于塌缩状态。
生理现实
上述说明呈现了cvp测定的简化和理想情况。在现实中,本发明的实施例减轻了人体生理学和测量过程的若干细微差别从而用于准确测定cvp。这些生理并发症和方法挑战如下所述。
动脉流和自主变化
从心脏到臂的血液流动发生在所有臂位置。由于系统是封闭系统,因此除非血管大小或容量存在任何变化,否则进入臂的动脉血的量必定等于离开臂的静脉血的量。如果假设采用刚性管,则通过肢体的循环实际上类似于通过u形虹吸管的流动,并且无论是竖直、水平还是倒置的,通过刚性虹吸管的流动都是相同的。如果血管完全刚性,则重力对循环没有整体影响。然而,该系统不是由刚性血管组成的,并且自主系统积极地参与调节通过臂的流动。hickey等人对血管变化以及自主变化进行了表征。hickey,m.,phillips,j.p.,&kyriacou,p.a.(2015).investigationofperipheralphotoplethysmographicmorphologychangesinducedduringahand-elevationstudy[对手升高研究期间引起的外周光体积描记形态变化的研究],journalofclinicalmonitoringandcomputing[临床监测与计算杂志]。当臂在下时,毛细血管压力由导致毛细血管前阻力升高的血管收缩控制。然而,由于增加的静水压,静脉延长。另外,在手指的末端,存在大量动静脉吻合,它们促进通过臂的整体血流并且直接涉及体温调节。从hickey等人复制的图7示出了生理学上的这些变化。在臂处于下部位置的情况下,毛细血管前小动脉处发生血管收缩,从而有效地通过动静脉吻合将血液重新引导到静脉系统中。概括地说,当臂低于cvp水平时,毛细血管流受到限制,动静脉吻合流量高且静脉扩张。如果使用光体积描记图(ppg)进行组织的光学测量,则信号的ac(脉动)分量将由于较小的动脉搏动很小,而信号的dc(平均)吸光度将由于组织中血容量的总体增加而增加。随着臂升高,自主神经系统试图保持毛细血管流,并且在毛细血管前水平上发生血管舒张。通过动静脉吻合的流量减小。当静脉由于大气压大于静脉压而开始塌缩时,即发生这种生理变化,从而导致跨壁压为零。这种塌缩通过降低毛细血管后阻力而增加全身性血管阻力。因此,当臂高于cvp水平时,毛细血管流量增加,并且静脉塌缩。光学ppg信号的ac分量将更大,而ppg信号的dc吸光度分量将减小。
手指毛细血管床中这一系列复杂的生理变化为测定中心静脉压导致了复杂的测量环境。如果像脉搏血氧仪的常见位置一样,ppg信号是从远端手指获得的,则光信号将受到毛细血管、大量动静脉吻合和静脉的影响。由于光子因散射而以半混沌的方式在组织中传播,因此它们对于任何单独的血管腔隙不是特定的,并且典型的ppg测量缺乏任何类型的空间分辨率。缺乏限定的空间分辨率限制了分离血管腔隙的能力。因此,远端手指不是用于评估静脉塌缩的优选测量位置。
可以通过选择相对于手指末端而言动静脉吻合数减少的组织位置来减轻由于臂升高引起的自主变化的影响,这将有助于测量准确度。此类位置包括手指的指根、手背和腕部。
替代性地,可以使用对静脉血具有增加的敏感性的光学测量方法减轻由于臂升高引起的自主变化的影响。这些系统可包括结合空间增强的光学系统,空间增强的光学系统广义地定义为改善静脉血容量变化的特异性的光学系统。这种系统的实例是使用置于静脉正上方的反射ppg系统。由此产生的传感器放置改善了系统对静脉变化的特异性。另一个实例包括低空间分辨率系统,该低空间分辨率系统包含例如位于腕部背面上的多个检测器。由于腕部组织的空间差异,每个检测器将对来自动脉源和静脉源的不同贡献敏感。基于ac和dc信号的测得变化或对高度变化的响应曲线,可以选择对静脉容量具有最大特异性的检测器。替代性地,来自多个检测器的信号可以组合使用并接受盲源分离技术诸如独立成分分析,使得静脉信号源可以与光信号分离。通过利用能够直接识别静脉的成像系统,可以实现进一步的空间能力。这种系统可以利用静脉识别和分割方法处理图像,以将信号分离到各静脉腔隙。
除了空间能力之外,基于脱氧血红蛋白和氧合血红蛋白的吸收不同的事实的光谱原理可以用于促进血液腔隙分离。脉搏血氧测量利用这些吸收差异以及脉搏或ac信号测定氧饱和度。这种一般过程可以有效地逆转,以分离信号的非脉动静脉分量。空间技术以及血管腔隙技术的使用可用于最小化生理噪声系数,以获得准确的中心静脉压测量结果。
时间响应延迟
本发明的实施例减轻或补偿的第二生理现实是血管系统不具有对跨壁压变化(包括静水压变化)的瞬时响应。如果臂从向下位置移动到向上位置,则静脉不会在中心静脉压以上的位置瞬间塌缩,因为血液进入引流静脉需要时间。静脉系统由不同直径的血管与防止逆流的静脉瓣膜组成。这些瓣膜具有打开压力以及由于受试者之间的生理差异而导致的顺应性差异。静脉系统的解剖结构导致阻尼或延迟响应,必须减轻或补偿这种阻尼或延迟响应以便获得准确测量结果。下面将讨论使这种影响最小化的方法。
静脉排空与充盈之间的不对称性
静脉排空与充盈之间的不对称性是测定cvp的重要要素。由于静脉瓣膜防止逆流,静脉必须从动脉流再充盈,因此充盈时间典型地将超过排空时间。例如,随着臂从较低位置移动到较高位置,静水压变化是与静脉塌缩相关联的主要影响,并且排空在几秒钟的时间内发生。然而,如果臂从升高位置移动到向下位置,则静脉不会瞬间扩张,因为臂的静脉容量必须通过动脉流入而有效地重新充盈。在将臂从某个位置移动到向下位置时,完全重新充盈臂中的静脉腔隙的时间可以在30秒左右,但是将根据血管形态和当前心输出量而变化。因此,当经由跨壁压变化改变静脉容量时,必须适当地考虑容量变化的方向性,即排空或充盈。
接触压力的影响
大多数光学组织测量是通过将光学测量系统置于组织上而执行的。静脉系统的压力相当低,典型地低于10cmh2o(0.14psi),这一事实要求应小心留意光学系统不影响跨壁压。如果将光学系统置于与组织接触,则必须将对静脉跨壁压的任何影响有效地结合到测量方法中。可以通过利用非接触式光学系统最小化局部跨壁压变化的影响。这样的系统被设计成最小化对跨壁压的任何影响并且以非侵入性和非干扰性方式有效测定静脉容量。
解剖参考的测定
如前所述,由于主要与解剖标志的可重复识别以及受试者位置相关联的操作者间差异,利用颈静脉压作为中心静脉压测定方法的能力受到限制。以非侵入性和自行施用方式准确且可重复地测定中心静脉压需要系统执行对解剖标志的评估、确保对受试者的适当定位或其组合。如果中心静脉压测量系统用于对给定受试者进行重复测量,则该系统可以使用所测定的高度水平的简单变化作为比较的基础。在这种情况下,受试者的可重复定位成为控制的重要参数。如果要在具有多个患者的诊所环境中使用该系统,则系统必须结合测定患者的身体位置来测定解剖尺寸。下文中披露了用于解决这些问题的系统和方法。
测量挑战的展示
以下实例示出了与准确的cvp测定相关联的挑战。在每个实例中,ppg传感器位于腕部上,并且在一些情况下,位于指尖。对于腕部位置,使用粘合剂将轻质ppg传感器直接附接在浅静脉上方以最小化接触压力。通过抬高臂实现跨壁压变化。图8a示出了缓慢抬高臂期间的ppg腕部数据的实例。最初,吸光度的变化随着抬高相对平坦,然而在相对于胸骨上切迹大约0cmh2o处,吸光度信号开始迅速下降,标志着静脉塌缩。吸光度相对于高度的导数如图8b所示。导数中用虚线表示的突出的负峰标志着从完整静脉向塌缩静脉过渡的中心。发生过渡的高度将与外周静脉压相关,并因此与中心静脉压相关。
末端手指毛细血管床困难
图9示出了使用手指的末端毛细血管作为传感器位置的复杂性。示出随着臂从0度(直线向下)旋转到180度(向上)末端手指处和腕部处的吸光度信号。腕部示出臂升高时的预期响应:一旦静脉完全塌缩,吸光度下降达到稳态。相比之下,指尖位置示出更复杂的图案。由于臂升高的增加,吸光度会出现初始下降,然而由于自主动脉血管舒张的较大影响,未达到稳态,这从信号的ac(脉动)分量的增加是显而易见的。总体血液信号在大约22秒达到最低点,但由于静脉和动脉系统的相反响应而经历波动。
外部压力敏感度
图10示出了在臂升高实验期间接触压力对测定外周静脉压的显著影响。当在ppg传感器周围增加非常轻微的接触压迫时,由于跨壁压的降低,静脉塌缩的压力下降超过10cmh2o。收紧ppg传感器上的带进一步降低静脉塌缩的程度。
高度变化率敏感度
静脉排空和塌缩不是瞬时过程,因此臂运动速率或跨壁压变化的速度是必须补偿或以其他方式进行控制的变量。图11示出了检测到的过渡高度取决于臂运动的速率。由于静脉塌缩所需的时间,因此更快的运动将导致cvp测定的准确度降低。
静脉响应是不对称的
如图9中可以看出的是,静脉系统中的容量对于臂抬高和臂下降的响应不对称。对于腕部和指尖两者,抬高臂时吸光度的变化较快。然而,对臂下降的响应要慢得多,因为必须重新充盈静脉腔隙。在腕部位置,吸光度信号在臂返回到向下(0度)位置之后超过20秒才返回基线值。
一般测量方法
光学测量系统
光学测量系统可以采用多种形式,从单一源和检测器配置到多波长/多传感器配置。出于说明的目的,将描述四个测量系统。
一个用于测定静脉容量的系统涉及将若干个光学传感器定位在基于腕部的装置下方。感测系统可以以传感器下方的区域不与装置物理接触的方式附接到腕部。然后可以使用测量算法确定哪个传感器或传感器组合提供与静脉容量变化相关联的最佳信息。图12是这种系统的图示。
第二个测量系统包括手环,该手环包含围绕装置的整个圆周的led检测器。在任何时间点,一些传感器将与组织接触,从而获得传统的ppg信号。其余传感器将靠近组织但不接触,并且可用于测定静脉容量。在一个或多个波长下同时获得ppg信息与静脉容量信息的组合产生了一种能够实现动脉影响补偿的系统。图13是这种系统的图示,其中圆圈表示led,而正方形表示光检测器。
第三个测量系统基于环,用于手指的指根。这种系统可以包括单一源和检测器关系,或者可以包括位于环的圆周周围的多个源和检测器。这种系统可以从多源检测器配置获取数据,用于获得动脉和静脉信号信息两者。图14是这种系统的图示。该图示出了一种可能的使用场景,其中环位于无名指上以进行一般心血管监测,同时可以通过在传感器不与组织接触的情况下将环置于小指上进行cvp测量。这实际上是一种非接触式ppg系统。
第四个测量系统可包括用于进行直接静脉成像的相机。这种静脉成像系统可以被配置成包括由红外发光二极管组成的led环,这些红外发光二极管对静脉血具有一定的特异性。一个这样的波长可以是850nm。成像可以使用将光信号集中朝向浅静脉的反射照明;使光线通过整个手指或手的透射照明;或者反射照明和透射照明的组合。当以反射模式使用时,可以在光信号检测之前利用随后的交叉偏振使照明偏振,以去除镜面反射或前表面反射。相机可对红外光敏感,并且可以包含附加的滤光器或处理算法以有效地去除环境光条件。可以修改这种系统以使得能够作为偏振差成像系统进行操作。图15是这种系统的图示。
替代性地,静脉容量的变化可以用多光谱成像系统测量,该多光谱成像系统为静脉血提供更大的特异性。这种成像系统使用多个波段的窄带照明和能够获取多光谱图像的相机。合适的成像系统可以包括利用以红色(660nm)、绿色(550nm)和蓝色(450nm)波长为中心的窄带led进行照明,结合商业rgb相机,该相机同时获取具有针对红色(r)、绿色(g)和蓝色(b)照明的差异特异性的三幅图像。照明可以利用正交取向的偏振片减少镜面反射。jakovels和spigulis已经证明这种系统可以测量静脉容量的变化。jakovels,d.,&spigulis,j.(2012).rgbimagingdeviceformappingandmonitoringofhemoglobindistributioninskin[用于标绘和监测皮肤中血红蛋白分布的rgb成像装置],lithuanianjournalofphysics[立陶宛物理学杂志]52(1)。
由光学系统观测到的静脉容量的实际测量结果可以采用多种形式。可以使用标准吸光度光谱测量法测定静脉容量,其中血液的吸光度与路径长度成比例。另外的方法可以基于血管的宽度或血管的高度。
跨壁压的血管内变化
血管内压力变化可以通过多种方法实现。通过包括臂升高变化在内的多种方式可以产生静水压变化。升高臂将压力从心脏降低约0.77mmhgcm-1的竖直位移(gavish和gavish2011),而放下手将使局部动脉压增加相同的因子。
血管内静脉压也可以通过在更近侧位置即更靠近心脏处进行的修改来改变。图16是使用中的这种系统的图示。在该实例中,患者具有7cmh2o的cvp。传感器位于右心房上方12cm的高度。在最左侧的附图中,外部袖带充气至20cmh2o。在这种条件下,跨壁压已经增加,使得静脉塌缩(0跨壁压)的位置在20cmh2o处,该位置高于传感器位置。传感器部位的静脉完全充盈,如图中所描绘。在第二时间点,袖带压力降至15cmh2o。静脉塌缩的位置已降至15cmh2o,但仍高于12cmh2o的传感器高度。随着袖带中的压力降低,与零跨壁压相关联的高度将减小,直到在光学系统下方发生静脉塌缩。在图示中,这发生在5cmh2o的压力下。由于静脉大部分塌缩,袖带压力降低至5cmh2o以下几乎没有变化。该测量方案的重要要素是袖带中的压力直到静脉容量达到平衡才下降。所描述的方法不需要臂运动并且产生用于系统性且容易地测定中心静脉压的方法。
用于改变跨壁压的额外方法是使用胸内压变化产生跨壁压改变。然而,需要以合理的速率呼吸要求胸内压的这些变化是随时间变化的。由于能够在频域中分离信号,因此使用时变信号具有益处。通过改变胸内压可以系统地改变到心脏的静脉回流。guyton静脉回流曲线很好地证明了这种生理关系。使用阻力呼吸方案产生负和正胸内压变化。图17和图18示出了将这种概念用于cvp测定。在图17a中,臂升高到一定水平,使得胸内压的变化对静脉容量几乎没有影响。如图所示,只有导致最大跨壁压的最大胸内压才引发静脉充盈。1701示出了最大胸内压的点。最大胸内压导致最大跨壁压,从而导致部分静脉充盈。如图所示,整体光信号变化将非常小。
如图17b所示,臂的总高度减小,使得传感器现在处于中心静脉压下。与1702所示相同程度的胸内压现在导致更完全的静脉充盈和吸光度信号的对应的更大变化。如图所示,胸内压的变化现在造成从塌缩静脉到部分充盈静脉的静脉充盈变化。因此,所得的光学变化增加。
图18a示出了臂高度的进一步降低,使得传感器现在位于略低于中心静脉压的高度。由于阻力呼吸引起的胸内压变化导致胸内压在正常胸内压附近的负和正变化。由此产生的胸内压偏移产生附加的跨壁压变化,这在跨壁压近似为零的情况下导致最大血容量变化水平。具体地讲,静脉从由于吸气引起的负胸内压导致的塌缩状态过渡为由于正压呼气导致的充盈状态。图18b示出了另外下降臂,使得胸内压的变化不会导致静脉塌缩。当接受检查的静脉保持正常充盈时,所产生的光信号具有减小的变化。
本领域的普通技术人员将认识到,由阻力呼吸、机械通气、瓦氏动作、穆勒动作和改变到心脏的静脉回流的其他扰动引起的胸内压的瞬时变化可用于产生变化,使得可测定中心静脉压。
跨壁压的血管外变化
通过改变外部压力可以实现静脉两侧的跨壁压的变化。这种外部压力变化的实例是将臂置于水浴中、静态压力或物理对象对静脉的物理压迫。这些类型的外部压力施加与物理压力测量法一致。考虑到静脉系统中存在的非常低的压力,由于需要非常高的精度,传统的物理压力测量法不适于自行施用。针对该应用的一些实施例的重要要素是使用非接触式压力测量法。在非接触式压力测量法中,用于产生跨壁压变化的力是动态(速度)压力、静态压力或其组合。
动态压力是空气流动方向和速度变化的结果。在动态压力系统中,可以控制速度和所产生的力(压力)以增加包含浅静脉的皮肤表面上的压力。在静脉变平的点,记录此时由空气柱施加的压力并将该压力转换为mmhg。该压力代表跨壁压为零的点。基于受试者解剖测量结果结合心脏相对于采样位置的高度,可以测定中心静脉压。在实践中,用于产生压平力的空气柱足够大以在限定区域内的多个静脉上施加压力。可以有效地对恒定力的区域进行成像,以测定静脉容量变化。
可以通过使用静态压力变化来实现跨壁压变化。静态压力是单位空气势能的量度。例如,管道壁上的空气压力被认为是静态的。想象风扇向完全封闭的管道吹风;这只会产生静态压力,因为没有空气流通过管道。用空气吹胀的气球属于类似的情况,其中仅存在静态压力。所描述的系统主要使用静态空气压力,因为可能存在一些空气损失。如果手或皮肤位置经受外部或周围空气压力的变化,则结果是跨壁压变化。在实践中,可以通过将手放置在具有一定程度空气流限制的外壳中从而产生外部或周围空气压力变化。如果进入腔室的空气体积超过离开的体积,则压力增加。该过程可用于产生对受试者手的大小和其他解剖差异不敏感的受控制的压力环境。
对于动态和静态压力系统两者,可以实施多种压力曲线,这些压力曲线实现对外周静脉压的测定,并因此实现对中心静脉压的测定。这些包括但不限于压力的斜坡、阶跃或周期性调制的任何组合。图19示出了可用于改变跨壁压的压力曲线的实例。在一种使用场景中,压力可以从低值线性地上升到高值,并且塌缩压力被确定为静脉容量经历最大变化(即,最小时间导数)的压力点。替代性地,可以以离散阶跃增加压力,其中每个阶跃的持续时间足够长以确保静脉容量已稳定至稳态值。在这种情况下,可以将塌缩压力确定为产生静脉容量最大减小的阶跃之间的中点压力。为了避免受压力步长限制的离散值,可以使用参数或非参数曲线拟合工具内插中点压力与静脉容量之间的关系,从而得到塌缩压力的改进估计。需注意,斜坡或阶跃也可以从高压下降至低压,然而由于静脉排空与充盈之间的时间不对称性,可能优选的是增加压力和排空静脉而不是降低压力并等待静脉充盈。
周期性调制例如正弦波或方波模式也可用于测定外周静脉压。周期性调制可以提供优势,因为它们将感兴趣的信号分离到特定频带。这一点很重要,因为静脉容量会经历与呼吸和血管紧张度(即血管收缩和血管舒张)相关的显著变化,该呼吸和血管紧张度是由交感神经支配和局部生理学介导的。通过调制特定频率下的压力并使用旨在增强或分离特定频带内的信号的基于傅里叶的方法或其他分析方法,可以降低对这些混杂噪声源的敏感度。在典型的使用场景中,相对小的压力调制(ac分量)与慢压力斜坡或阶跃(dc分量)结合使用以产生有效的压力曲线,如图20a所示。当dc压力分量较低且低于外周静脉压时,ac压力变化将产生相对小的静脉容量变化。当dc压力达到外周静脉压时,跨壁压将变为零,并且ac调制将产生静脉容量的较大变化。当dc压力高于外周静脉压时,静脉容量中的ac分量将随着静脉塌缩而再次变小。这些效应在图20b中示出,该图显示了由于压力调制引起的静脉吸光度的变化。因此,外周静脉压可以被识别为dc压力值,其中ac压力调制产生静脉容量的最大变化。
静脉相对于组织表面的深度以及皮肤弹性可以产生测量变化。如果系统的目的是测量静脉压而不是皮肤弹性,则皮肤弹性的变化可被视为噪声源。利用眼内压测量领域中使用的平衡技术,可以有效地补偿皮肤弹性的这种变化。具体地讲,角膜厚度的差异是眼内压变化的未知来源。通过使用滞后计算或眼反应分析,已有效地补偿了角膜厚度的差异。眼测量系统使用强度渐增的空气柱作为压平力。眼反应分析仪记录压平的时刻,但空气柱继续以增加的强度发射,直到角膜被压凹。然后空气柱的力减小,直到角膜再次处于压平点。两个压平点处的压力差是角膜弹性(滞后)的量度。可以使用数学公式针对高弹性或低弹性来“校正”压平点。这种“经校正的”眼内压较少依赖于角膜厚度。尽管眼内压测量利用反射角并因此与当前的系统显著不同,但发明人已发现使用利用增加和减小压力的基本概念可用于提高静脉压测定的准确度。出于测定静脉压的目的,该方法通过在物体上产生力直到已经发生血管的限定压迫而进行。持续施加空气压力超过该点,然后缓慢撤除,直到获得类似的观察。两个限定的测量点处的两个压力(力)的差异是皮肤弹性(滞后)的量度。该信息使得能够使用数学计算来校正皮肤的影响。
解剖测量
由于测量技术的差异,临床医生或其他护理提供者对解剖测量值的测定历来容易出错。为了减轻这些测量技术的差异,本发明的实施例使用光学识别技术来测定关键的解剖测量值。解剖测量可以由使用结构光的光学系统或使用3-d相机系统执行。存在这种系统的多种实证;目前可用的系统包括microsoftkinect、orbbecastra、intelrealsense和stereolabszeb立体相机。这些系统按照不同的原理操作,但能够在三维空间中进行测量。多种系统能够进行骨骼跟踪,从而捕获受试者(包括手和手指)的“骨骼”位置。han等人提出了基于3d骨骼数据的对人类的现有空间-时间表示的综合调查,并且从信息形态、表示编码、结构和过渡以及特征工程的角度提供了对这些方法的信息分类和分析。han,fei等人“space-timerepresentationofpeoplebasedon3dskeletaldata:areview”[基于3d骨骼数据的人类空间-时间表示:综述],arxivpreprintarxiv[arxiv预印本arxiv]:1601.01006(2016)。
图像捕获系统允许关节的适当定位并测量它们之间的距离,且可用于测定受试者在特定平面中的位置。在实践中,系统映射评估发生的环境,跟踪受试者在该环境中的位置,并映射受试者的关节以构建骨骼。所得到的骨骼可用于测定解剖测量值以及测定身体的三维位置。可以通过面部检测来增强这种信息以包括受试者眼睛的确切位置。眼睛位置与整体身体位置相结合产生了一种强大的用于确保受试者被适当定位以测定cvp的工具。
传感器高度测量
在若干示例性实施例中,可能希望确定传感器相对于地面、心脏或其他限定的参考点的位置。确定传感器位置的过程可以通过附接到受试者的测量系统(如下讨论)或者通过观测受试者完成。上述用于测定解剖尺寸的结构光或3-d相机系统也可用于确定传感器位置。另外的方法包括使用运动捕获系统,这些运动捕获系统涉及用于场景捕获的外部相机和置于受试者上的标记。光学被动技术在静脉传感器上使用可以由相机跟踪的回射标记。光学主动技术使用led标记。通过在静脉感测系统上包括标记或发光二极管等可以容易地实现这两种方法。
附接高度位置系统
可以经由惯性测量单元(imu)系统实现确定手指、手或腕部上的物体的位置的能力。包含加速度计和陀螺仪的典型imu系统可以测量物体在3d空间中的角度定位,该角度定位可以用于估计在受控制运动条件(诸如臂摆动)下物体的位置。通过将imu与相机结合使用可以实现额外的准确度。这种方法存在若干变型,但最著名的是tango(以前在测试中称为projecttango)。tango是谷歌公司(google)开发和创作的技术平台,它利用计算机视觉使得移动装置诸如智能电话、平板电脑和手表能够在不使用gps或其他外部信号的情况下检测它们相对于周围世界的位置。projecttango能够测定装置在环境中的位置和取向。该软件通过集成三种类型的功能来工作:(1)运动跟踪:使用环境的视觉特征结合加速度计和陀螺仪数据来密切跟踪装置在空间中的运动,(2)区域学习:将环境数据存储在标绘图中,该环境数据可在之后重复使用、与其他projecttango装置共享,并利用元数据诸如注释、指令或兴趣点进行增强,以及(3)深度感知:检测环境中的距离、大小和表面。它们一起以“六个自由度”(3个取向轴加3个运动轴)生成关于装置的数据,并且使得能够知道装置在绝对坐标空间中的位置。
需注意,如果仅需要相对位置而不是绝对位置,则可以使用来自惯性测量单元(imu)的加速度计和陀螺仪数据来估算系统的角运动和位移。
额外的高度感测系统可包括使用激光雷达。许多实施方式都是可能的;一个示例性系统具有安装在万向节中的激光雷达系统,因此其聚焦在地面上,而另一个实例使激光雷达系统在竖直平面内有效地旋转,从而可以测定地板与天花板之间的距离。额外的距离检测系统(包括超声系统、红外系统和飞行时间测量系统)也可以是合适的。
心脏与外周静脉之间的高度差的测定
对于使用外周静脉位置测量cvp,必须测定测量位置与右心房相关标志之间的高度关系。右心房在胸腔内的位置由于人与人之间的体格差异以及缺少可见标志而很难确定。当今的测量方式是,受过训练的医疗专业人员通过触诊解剖标志来确定心脏的位置。静脉静止轴是右心房的大致位置,并且位于腋中线与从胸骨右侧的第四肋间隙引出的线的交叉点处,如图21所示。在历史上,右心房位置的确定由于解剖变化、触诊错误和测量技术的差异而容易出错。
本发明的实施例使用不需要医疗训练或直接触诊的成像和建模技术提供用于心脏位置确定的更简单方法。通过使受试者站在仪器附近获得受试者的解剖测量结果。获取受试者的图像,并且图像处理和骨骼化程序使得能够测定关键的解剖测量值,诸如但不限于躯干长度、肢体长度和颈部长度,如图22所示。使用确立的比率限定肢体长度、躯干长度与右心房位置之间的关系。可用于限定这些比率的数据源包括信息源,这些信息源包括具有对应心脏位置信息例如mri、ct扫描和x射线的外部可观察肢体信息。按受试者特征诸如性别、种族和性别对数据源进行分段可以进一步细化比率,以改善对右心房位置的估计。结果是当人站在相机前时获得相对于可见标志和骨骼特征的估计心脏位置。可以使用传统相机或3-d相机进行该确定。
为了获得cvp测量结果,受试者坐在桌子旁,如图23所示。因此,随着受试者移动到就座位置,可以转换或保持经由光学评估获得的心脏位置。当受试者移动到就座位置时,位于装置上的相机用于评估心脏位置。系统可以使用可见标志诸如胸骨下切迹、关节位置或物理对象(诸如头部和肩部)确定心脏的位置。通过识别受试者上的心脏位置,系统可以测定测量位置与心脏之间的高度。该方法可用于非卧床诊所环境或家庭环境以测定中心静脉压。可以通过针对心脏的可重复定位所定义的过程增强该方法。
用于重复测量的相对心脏位置的确定
对于重复测量,期望重现测量位置与心脏之间的高度关系,或者以1至2cm的准确度测定从先前测量结果的变化。考虑到人体中接合关节的数量,这种重新定位任务具有许多细微差别和明显的复杂性。例如,考虑以下场景。受试者使用相同的刚性椅子和相同的桌子用于测试,但受试者向前倾斜。当受试者坐在竖直位置时,躯干的角位移相对于先前的测量结果产生较低的心脏高度。类似地,向侧面倾斜或者简单地蜷缩在椅子中会导致心脏位置移动数厘米。由于心脏不位于外部可见表面上而是存在于可变大小的胸腔内,因此准确地重新定位心脏高度或测定心脏移动程度的过程进一步复杂化。
通过使身体占据与初始或先前测量相同的体积空间,可以实现心脏重新定位。如果身体处于相同的体积空间,则心脏实际上处于相同的精确位置并且已经获得心脏高度的可重复性。具有深度能力的光学测量系统可用于确保躯干或上身的体积空间对准。可以在身体处于不同位置的情况下进行多次基线测量。如果随后的测量满足体积匹配要求,则可以进行测量。可以基于关节位置、身体边缘或其他物理对象的对准来确定体积匹配。
体积匹配过程可能受外部服装差异的影响,这可能会限制受试者使用的服装的类型和数量。为了减轻可能的服装限制,系统可以使用头部的位置作为定位工具。该方法可以基于将就座受试者建模为具有球窝连接点的一系列连接对象。第一连接是到椅子的附接,随后的连接部向上延伸。如图24所示,系统被建模为椅子上方的两个主要连接部即背部和颈部连接部,头部附接到顶部连接部。在这种模型中,任何连接部的非竖直对准都会导致头部位置的高度降低。因此,将头部重新定位在最大位置需要连接部是竖直的。因此,获得可重复的头部位置可用于产生可重复的心脏高度位置。然而,头部位置的确定是困难的,因为头部具有多个自由度。另外,受试者的面部位于脊柱和颈部的轴线的前面。注意到了这种不对称性,并在所提供的解决方案中解决这种不对称性。
图25a示出了处于竖直位置的受试者并使用瞳孔水平、面部上的竖直轴以及水平轴定义3轴坐标系。可以定义许多坐标系,并将以下坐标系用于说明目的。在图25b中,随着受试者在保持背部-颈部-头部对准的同时前倾,坐标系向前旋转,并且由坐标系定义的交叉点移动到较低高度。图25c示出了受试者后倾但颈部和头部竖直对准的情况。在这种情况下,轴系统不旋转,但交叉点处于较低的高度。图25d示出了心脏处于最大高度但头部轴已经旋转并且交叉点已下降的情况。这种场景限定了受试者位置不同但心脏高度保持不变的情况。在实践中,受试者可抬起头部并使其颈部伸直,从而实现完全对准。图26示出了该方法在存在身体的横向或倾斜运动的情况下保持功能。
如在先前的附图中所示,头部位置可以提供用于获得可重复的身体位置的关键要素,因为头部位置代表连接部的末端且典型地不被服装覆盖。由横滚、俯仰和偏转定义的头部取向加上头部的高度或者限定的轴线交叉点的高度可以是测定头部位置的基础。单轴或单个参考点测定可导致不准确。例如,使用瞳孔位置可导致高度测定误差,因为头向后仰会抬高眼睛位置并且可以补偿背部的未对准。结果是心脏高度降低,但未指出受试者处于错误位置。
头部位置测定系统使用具有3-d能力的相机,使得测定头部横滚、俯仰和偏转。图27示出了针对深度相机计算的这些要素。需注意,可以使用非深度相机,但使用深度相机时系统的整体准确度可以更好。对相机定位以捕获受试者的面部以及上部躯干。相机提供头部位置信息,并且可提供有关颈部、胸部和肩部位置的额外信息。
在使用中,受试者可以定义在测量持续时间内舒适且可持续的最大头部位置。该头部位置成为比较其他测量结果的基准。对于未来的测量,受试者将他们的臂放在外壳中并且坐在同一椅子上。使用视觉反馈工具,指示受试者以符合先前基准的方式重新定位他们的头部。结果是可重复的心脏高度。
在实践中,由于头部对准的身体位置的微小变化,一些受试者可能难以满足位置可重复性标准。这可以通过在短时间段内获得多个测量结果以绘制出位置的这些可能变化加以解决。该方法还可以使用额外信息促进受试者的重新定位。例如,也可以测定颈部与躯干之间的关系并将该关系用于促进重新定位。该方法与体积评估法具有相似性但基于对准角度,这些对准角度对服装差异不太敏感。
一些受试者(通常是年龄较大的受试者)具有严重脊柱后凸,也称为圆背或驼背。在存在这种状况的情况下,两种方法继续为中心静脉压测量产生可重复的定位机制。
其他光学方法可包括在身体上使用一个或多个(例如,三个)光学标记,诸如ir反射器。可以在一个装置中配置这些光学标记,使得可以测定相对于相机的位置,如同可以测定反射器在胸部上的角度一样。额外的方法可以包括在上身其他区域(以包括头部)放置标记。
非光学系统可包括使用测压计(manometer)和惯性测量单元(imu)。由于管两端之间的静水压的差异,柔性u形测压计提供管两端之间的相对高度。测压计的一端使用外部标志(例如,胸骨切迹)附接到身体,另一端与外周静脉的位置竖直对准。测压计测量外周静脉位置与参考点之间的竖直距离。由于心脏位于胸部内,因此考虑上身的角度很重要。imu可用于测定躯干的角度。得到的信息可用于产生可重复的身体位置,或者用于补偿身体位置相对于先前测量结果的变化。
使用相机和附接到外部标志的imu的组合系统也可用于测定心脏高度。可以结合来自相机和imu两者的所得信息以测量位置和取向。
示例性实施例
受控制的臂抬高情况下的静脉成像
利用受控制的臂抬高的系统和方法可以按各种方式实现,以下是一个示例性实施例的说明。图28示出了静脉成像系统和三维成像系统的组合使用,用于进行解剖测量。随着受试者接近该系统并如图28a所示坐下时,面向前的相机1201用于捕获受试者的解剖尺寸和标志。光学系统1202以能够进行静脉容量测定的方式对组织进行成像。然后,系统可在以限定和受控制的方式抬高臂的同时获取图像。图28b示出了臂被抬高到高于中心静脉压的点。
使用受控制的臂运动有助于减轻系统响应中生理延迟的影响。在一种使用场景中,系统可以以一系列小的分立步骤抬高臂,等待光学响应的平衡,然后进入下一个位置。图29示出了这种臂抬高方案。超过跨壁压为零的点时,额外的高度增加可能导致最小的额外静脉容量变化。运动前静脉容量的平衡很重要,因为它可以消除响应延迟的影响。高度变化的增量可以是恒定的,或者可以变化以优化压力-容量曲线的采样,在变化较大的区域中样本更多。因此,高度增量可以取决于先前位置变化的响应特性。如果先前响应变化大,则可以减小高度增量,而如果先前响应变化小,则可以增加高度增量。图29是上述方法的说明性实例。当静水压接近中心静脉压时1401,平衡的总时间增加1402。在静水压等于中心静脉压的高度1403,随着额外的臂抬高,不会发生额外的静脉压迫。这种类型的系统性方法使系统延迟对测定准确的中心静脉压的影响最小。
图30示出了在受控制的臂抬高期间来自静脉成像系统实施例的示例性数据。使用红外相机和805nm的照明获取手背静脉的图像。在这些图像中,静脉显示为较暗的区域,因为血液是红外光的较大吸收体。图30a示出了在逐渐更高的手高度处拍摄的一系列图像。静脉塌缩引起的吸光度差异很明显:暗静脉区域几乎在较高位置处消失。图30b示出了在受控制的臂抬高中手高度和图像强度的时间进程。从“静脉掩模”(venousmask)内测定强度,该“静脉掩模”是使用初始图像的二元分割产生的。在实验期间,使用旋转台升高臂,如图28所示。仅在强度信号平衡至最后高度变化之后,臂才以恒定的增量升高。通过对该图的检查表明,大约-5cm(相对于胸骨上切迹)的高度变化导致由于静脉塌缩引起的光信号的较大变化。稳态(平衡后)强度值在图30c中示为高度的函数。基于作为高度函数的光信号的变化,显然发生了3cm的静脉塌缩。
如本领域技术人员可以理解的,存在许多可用于分析静脉成像数据的替代性方法,这些方法包括分解方法、静脉宽度测量和感兴趣区域方法。
具有受控制的臂抬高的基于腕部的装置
受控制的臂抬高也可以通过受试者引发的运动实现。在一种场景中,基于腕部的光学评估系统(例如,如前所述的表带)可以与远程投影系统结合,该远程投影系统显示用户必须将其手移动到的位置。这种系统在图31中示出。只有在接收到视觉或听觉提示后,才能通知受试者将其手抬高到下一个显示的目标。投影系统可以使用相机测定到墙壁(或其他投影表面)的距离并确保受试者已经适当地移动。替代性地,表带上的光检测器可用于确定受试者已将其手抬高到适当位置。可以向受试者提供视觉反馈以及音频反馈,以指示适当的移动和定位。腕部系统可以通过无线或蓝牙连接与投影系统通信。
图32是在用户发起的臂运动期间从ppg基于腕部的传感器收集的数据的实例。视觉目标以均匀的高度增量显示,并且仅在ppg信号达到大致稳态值之后才提示用户移动。图32a示出了吸光度和腕部高度的时间进程,而图32b示出了作为高度函数的稳态吸光度。检查该曲线图显示出胸骨上切迹上方5cm之前的静脉塌缩。
非接触式动态血压计
图33a是利用动态(速度)压力测定静脉塌缩的中心静脉压测量系统实施例的图示。动态压力是空气流动方向和速度变化的结果。该系统不需要受试者移动他们的手,而是以导致跨壁压的系统性变化的方式改变组织上的外力。在操作中,该系统可以使用静脉成像系统来分离被受控制的气流影响的区域内的一个或多个测量部位。这种方法将臂抬高引起的自主变化的影响降至最低。非接触式血压计系统可包括3d相机以评估受试者相对于系统的心脏高度。可以通过检查从血管测得的吸光度变化、高度变化(如果光学系统与用于静脉高度测定的侧面对准)以及血管尺寸变化来确定静脉容量的实际测量结果。为了便于可重复测量,系统可以包括采用对准桩柱形式的手指对准系统,如图33b所示。图33c示出了用于照明、图像捕获和空气管理的装置。手的照明由光源2601完成,空气由2602引导。该系统还可以通过将光源放置在手下方实现透射照明。
图34示出了通过对施加的空气压力进行调制而实现的静脉容量的变化。在该示例性测量期间,获取手背静脉的红外图像,同时将空气流引导到手的表面上。在低状态与高状态之间以二元方式调制空气流速,周期约为20秒。图34a示出了在最小流量和最大流量时来自示例性测量的图像帧。检查图像序列显示出作为空气流量函数的静脉容量的可重复变化。静脉在最小空气流量期间比在最大空气流量期间更宽且更暗。图34b示出了使用初始图像的二元分割创建的静脉掩模内的平均光信号强度。由空气压力引起的静脉塌缩的时间进程清晰可见。图34a中显示的帧用圆圈表示最小流量,用正方形表示最大流量。图34c显示在最大流量和最小流量时穿过图像的横截面的平均像素强度。横截面在图34a的第一图中示出。当施加最大流量时,可以看到主静脉的宽度(大致以70像素为中心)显著收缩。因此,利用空气流量进行的非接触式压力调制导致显著的光信号变化,可以在强度幅度的变化以及空间和形态属性的变化这两方面对这些光信号变化进行分析。
非接触式静态血压计
该系统可以使用静态的或主要是静态的压力机构来改变跨壁压。该系统通过让用户通过入口或孔将手放入外壳中进行操作。盒子具有入口,入口的尺寸允许手伸入盒子,但同时最小化腕部周围的剩余空间。图35错误!未找到参考源。示出了这种设计。在一些实施例中,腕部周围的空间可以通过多种机构(包括例如可变光圈(irisdiaphragm))最小化。可变光圈通常用于光学系统从而以系统方式闭合圆形开口。用于在腕部周围形成密封的机构不应以产生cvp测量误差的方式阻碍来自手的静脉流。在2017年11月17日提交的pct专利申请pct/us17/62356中描述了合适的机构,该专利申请通过援引并入本文。可以通过使用不接触腕部、仅接触腕部中的非静脉组织或者以低于典型静脉压的压力接触腕部的系统减小测量误差。图35示出了受试者的腕部在伸入外壳时可搁在桌子或其他表面上。在远端前臂,静脉流的主要浅表导管是贵要静脉和头静脉,它们分别沿着前臂的内侧和外侧。因此,远端前臂的掌侧表面没有主静脉,并且可以在不影响cvp测量的情况下将接触压力施加到该表面。
可以通过改变盒子中的压力使得以可测量的方式改变跨壁压,从而测定中心静脉压。如果推入盒子的空气体积超过离开盒子的体积,则盒子中的压力将增加,从而降低静脉腔隙两侧的跨壁压。在操作期间,受试者不需要移动他们的手;跨壁压的所有变化都是由空气压力的变化介导的。在一个实施例中,系统可以使用静脉成像系统来分离由系统所成像的区域内的一个或多个测量部位。为确保准确测量,系统的外部部分可包括3d相机或简单的u形管测压计,以评估受试者心脏相对于系统的高度。可以通过检查从血管测得的吸光度变化、高度变化(如果光学系统与用于静脉高度测定的侧面对准)以及血管尺寸变化来确定静脉容量的实际测量结果。为了便于可重复测量,系统可包括手指或手对准系统。需注意,系统还可以产生低于大气压的压力,从而促进该部位中的静脉蓄积。这种能力对于限定测试的标准化初始条件可能是有价值的。在实践中,可以使用低于大气压的压力降低,并且在开始测试之前确定稳定的静脉容量信号。替代性地,可以使用高压条件作为初始条件以确保最小静脉容量。在另一种方法中,起始条件可以利用周期性压力调制以消耗静脉牵张感受器(stretchreceptor)并针对进一步扰动预处理静脉。这种限定的初始条件可用于提高测量准确度。
图36示出了使用静态空气压力改变跨壁压的中心静脉压测量系统和用于检测静脉容量变化的相机的实例。将手通过孔3601放入盒子中,该孔的尺寸适合于受试者的腕部和柔性硅胶套(未示出)。该套能够产生压力密封,该压力密封不会产生超过盒内压力的接触压力。通过在空气入口(未示出)处使用离心式鼓风机并且在出口(未示出)处使用蝶阀,可以改变盒内的空气压力。蝶阀的旋转允许或限制空气流动。可以通过定制软件设置期望的盒压,并且记录盒内压力的压力传感器可以与pid控制器耦合,以调节蝶阀的位置,从而达到目标压力。将手放在掌托3604上,该掌托提供与外壳压力相反的静摩擦力。通过中心波长为850nm的led3602的环从上方照射手。红外敏感单色相机3603可捕获手的手背表面的数字图像。反射照明增强对手背静脉的特异性,并且使较深静脉和动脉源对光信号的贡献最小化。正交取向的线性偏振片3605放置在led下方和相机镜头前方,并用于减少镜面反射。测压计(未示出)用于测定右心房与手背之间的竖直距离。测压计的一端附接到静脉静止轴(位于胸壁中间-前部-后部直径的第四肋间隙),而另一端附接到盒子处于手的位置处。该测量用于考虑到静水压的影响。
图37示出了使用图36的系统可以测定中心静脉压的方法。用图37a所示的红外相机捕获手背静脉的图像。如图37b所示,结合线性斜坡与方波调制的压力曲线用于改变跨壁压。调制幅度保持相对较小(4cmh2o),以避免延长的静脉充盈时间。图像经过逐帧配准以适应由受试者引起或者由压力变化引起的运动或失真。图像分析基于与压力曲线和局部邻域统计相关联的变化识别如图37c所示的静脉集群3701。来自静脉像素的强度信号被转换为相对吸光度并经历时域高通滤波以去除低频噪声源。还应用savitzky-golay滤波器以消除心率的影响,而不会过度模糊时间特征。图37d示出了经过处理的平均静脉信号。跨壁压经过零的时间段可以容易地被识别为引起静脉吸光度的最大调制的时间段。可以通过考虑某一窗口期间的平均压力并计算吸光度的关联变化来构建压力与调制的关系。使用局部平滑化算法确定的每个静脉集群的曲线在图37e中示出。可以比较这些曲线以确认不同静脉段之间的相对空间均质性。如果满足该条件,则可以从压力与调制关系曲线的峰值3702估计外周静脉塌缩压力,如图37f所示。在该实例中,外周压力被识别为21.3cmh2o。手背与静脉静止轴之间的竖直距离增加了17.2cmh2o的静水压,如用测压计所测定的。因此,在从外周静脉压减去静水压之后,将cvp测定为4.1cmh2o。这些分析步骤仅代表可以如何测定中心静脉压的一个实例,并且可以使用许多用于成像和信号处理的替代性方法来提取相似的信息。
图38示出了该方法对外周静脉压变化的敏感性。在对单个受试者进行的一组实验中,通过改变手相对于心脏的高度并因此改变手静脉中的静水压以操纵外周静脉压。图38a示出了手的起始位置的压力与调制关系曲线,而图38b示出了手降低时的曲线。降低手会增加静脉中的静水压,并使塌缩点(零跨壁压)向右偏移。如图38c所示,在若干个手位置上重复实验表明外周静脉压(pvp)具有与静水压(hsp)一致且高度可再现的关系。因此,无论手的高度如何,中心静脉压都可以确定为cvp=pvp-hsp。
空气压力袖带
静态和动态压力系统的另一个示例性实施例使用空气压力在腕部处形成空气袖带。系统性地改变毛细血管与心脏之间某位置的跨壁压的能力产生了几种测量选择。具体地讲,产生受控制的静脉回流机制的能力使得能够操纵血管内压力以测量中心静脉压。
如本领域技术人员可以理解的,存在许多替代性实施例,用于使用空气流量、空气压力或两者的组合产生血管外和血管内跨壁压变化以测定cvp。
光学血压计
光学血压计示例性实施例基于使用可以放置成与组织接触的一根或多根光纤。光纤可以以预定义的方式与组织相互作用,使得可以对组织施加不同水平的力。向组织施加力的机制是经由光纤,光纤也代表了测量模式。光纤可以测量随着由光纤施加的压力引起的增加压力的吸光度变化。未发生吸光度的额外变化或者发生最大过渡的压力点使得能够测定静脉塌缩和零跨壁压。获得零跨壁压力点所需的合力结合手相对于心脏的高度能够实现中心静脉压测定。出于创建自行施用的测试的目的,可以利用分布式光纤阵列,就像利用多个针脚以有效贴合手的表面的儿童玩具一样。所得的光纤阵列可以传输回成像光谱仪进行评估。图39是光学血压计示例性实施例的图示。
已经结合各个示例性实施例描述了本发明。将理解的是,以上描述仅用于说明本发明的原理的应用,本发明的范围由参照说明书的权利要求书来确定。本发明的其他变体和修改对于本领域的技术人员而言将是显而易见的。
- 还没有人留言评论。精彩留言会获得点赞!