一种膜联蛋白V的应用的制作方法
本发明属于生物医药技术领域,具体涉及一种膜联蛋白V在制备延缓糖尿病进程药物中的应用。
背景技术:
糖尿病是一种严重威胁人类健康的内分泌代谢性慢性病,近几年,糖尿病的发病率逐渐上升,其特征为持续性血糖升高。若高血糖患者得不到有效控制则会引发感染及多器官组织受损,免疫功能降低,健康受到极大的威胁。采用链脲佐菌素(Streptozotocin,STZ)诱导高血糖动物模型是目前常用的糖尿病研究模型。
膜联蛋白V(Annexin V)属于磷脂结合蛋白的膜联蛋白家族成员。膜联蛋白家族蛋白以依赖Ca2+的方式与磷脂结合。磷酯酰丝氨酸(phosphatidylserine,PS)和溶血磷脂酰胆碱(lysophosphatidylcholine,LPC)参与凋亡和坏死细胞的清除。膜联蛋白V被首次发现是作为体内抗血栓活性的抗凝血蛋白,膜联蛋白V与凋亡细胞外翻的PS结合可抑制促凝血和促炎症活性。迄今为止,许多学者发现了膜联蛋白V的其它生物学特性,包括Ca2+通道活性,调节磷脂酶A2,抑制凋亡细胞的吞噬作用,抗肿瘤免疫和免疫调节作用等。尽管目前对膜联蛋白V的研究较多,但其生理功能仍有待于研究。
Luis E.Munoz及其同事发现,膜联蛋白V缺陷型小鼠与野生(WT)小鼠相比,几乎没有迟发型超敏反应(DTH),表明内源性膜联蛋白V可增加对死亡细胞的免疫应答。Benjamin Frey和他的同事同样证明内源性膜联蛋白V作为一种炎症蛋白影响坏死细胞的吞噬作用,可以调节对同种异体细胞的免疫反应。然而,膜联蛋白V与糖尿病之间是否存在关联尚不清楚。
技术实现要素:
本发明的目的在于,提供一种膜联蛋白V在制备延缓糖尿病进程的药物中的应用。本发明不仅发现利用膜联蛋白V制备的制剂在体内对糖尿病有保护作用,而且在体外也发现其能减少STZ对胰岛素瘤细胞的损伤作用,同时还发现了利用膜联蛋白V制备的制剂对糖尿病肾脏并发症或肾功能的损害具有预防作用。
另外,还研究了膜联蛋白V在制备延缓糖尿病进程药物中的应用。
优选地,所述的膜联蛋白V在制备改善糖尿病生理指标和代谢状况的药物中的应用。
优选地,所述的糖尿病生理指标和代谢状况为禁食血糖、体重、血清胰岛素水平、葡萄糖耐量测试、食物摄入量、摄水量和尿量。
优选地,所述的膜联蛋白V在制备改善糖尿病模型胰岛素信号通路的药物中的应用。
优选地,所述的膜联蛋白V在制备改善糖尿病肝脏、胰腺和肾脏的病理变化的药品中的应用。
优选地,所述的膜联蛋白V在制备改善糖尿病血清肌酐和血尿素氮水平的药物中的应用。
优选地,所述的膜联蛋白V的应用在制备预防糖尿病肾脏并发症或肾功能损害的药物中的应用。
优选地,所述的膜联蛋白V在制备与常规糖尿病治疗或预防药物联合运用的延缓糖尿病进程药物中的应用。
优选地,所述的膜联蛋白V在保护胰岛素瘤细胞免于糖尿病诱导剂链脲佐菌素导致的细胞凋亡中的应用。
另外,还研究了利用常规制剂方法进行膜联蛋白V的制剂,并评价所制备的制剂在延缓糖尿病进程中的应用。
本发明产生的有益效果为:
(1)膜联蛋白V及其制剂能显著降低糖尿病模型的血糖水平、糖耐量实验(IPGTT)和血清胰岛素水平,体重增加;使得糖尿病模型小鼠的代谢状况如24h食物摄入量,摄水量和尿量显著降低。从而证实,膜联蛋白V及其制剂显著改善糖尿病生理指标和代谢状况。
(2)通过评估膜联蛋白V及其制剂对胰岛素信号传导途径的影响,结果发现,膜联蛋白V及其制剂处理组血糖水平下降,可能是由于胰岛素信号传导途径的增强。
(3)经膜联蛋白V及其制剂处理后,STZ诱导的高血糖小鼠的体内实验显示,肾脏的病理病变显著变轻,血清中肌酐和尿素氮含量减少,表明膜联蛋白V及其制剂可通过降低血清肌酐(Scr)和血尿素氮(BUN)对肾功能起到保护作用。膜联蛋白V及其制剂在延迟STZ诱导的糖尿病发作以及肾功能中发挥保护作用。
(4)体外实验中显示,膜联蛋白V制剂可以显著保护胰岛素瘤细胞免于糖尿病诱导剂链脲佐菌素导致的细胞凋亡。
附图说明
以下图中数据采用平均值±S.E.M分析(每组8只样本);其中#表示P<0.05,有统计学差异(与对照组比较);##表示P<0.01,有显著统计学差异(与对照组比较);##表示P<0.001,有及其显著统计学差异(与对照组比较);*表示P<0.05,有统计学差异(与模型组比较);**表示P<0.01,有显著统计学差异(与模型组比较);***表示P<0.001,有及其显著统计学差异(与模型组比较)。
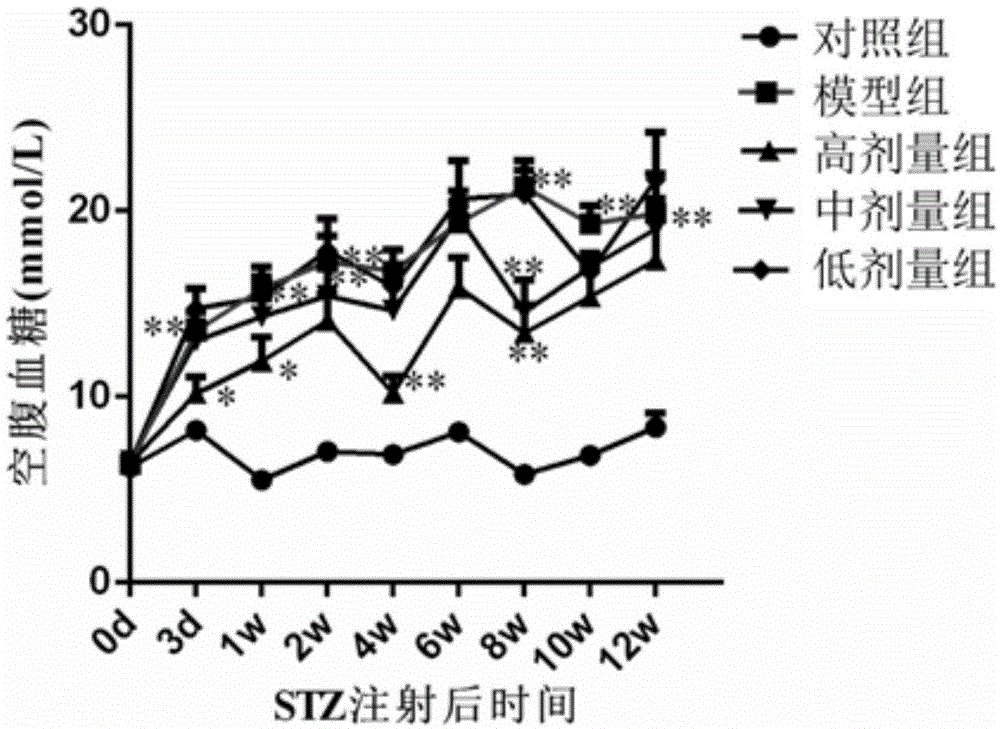
图1A为各组小鼠禁食6h的空腹血糖水平随注射STZ后的时间变化趋势图;
图1B为各组小鼠禁食6h的体重随注射STZ后的时间变化趋势图;
图1C为膜联蛋白V处理后12周时小鼠的空腹血清胰岛素水平图。
图2.膜联蛋白V对体内葡萄糖水平平衡的影响趋势图;
图3A为小鼠注射STZ后4周,8周,12周的24小时食物摄入量随STZ注射后的时间变化趋势图;
图3B为小鼠注射STZ后4周,8周,12周的用水量随STZ注射后的时间变化趋势图;
图3C为小鼠注射STZ后4周,8周,12周的尿量随STZ注射后的时间变化趋势图。
图4.膜联蛋白V对各组小鼠肝脏(A)和胰腺(B)形态学变化的影响病理学显微图(HE染色;20×10)。
图5.膜联蛋白对肝脏胰岛素信号通路的影响图;
其中p-IRS1(A),pGSK-3β(B)和pAKT(C)的肝脏相对蛋白水平分别标准化为IRS1,GSK-3β和AKT。
图6A为用苏木精-伊红(HE)染色(20×10)的肾切片的病理结构显微照片;
图6B为STZ诱导的小鼠血清尿氮素水平图;
图6C为STZ诱导的小鼠血清肌酐水平图。
图7A为胰岛素瘤细胞损伤模型图;
图7B为不同浓度的膜联蛋白V对胰岛素瘤细胞中增殖的影响图;
图7C为不同浓度的膜联蛋白V对STZ(1μM,24h)刺激的胰岛素瘤细胞增殖的影响图。
具体实施方式
下面结合具体实施方式,对本发明作进一步的详细说明。
实施例1
(1)膜联蛋白V的表达和制剂
在BL21(DE3)大肠杆菌中表达的重组膜联蛋白V,通过亲和层析和离子交换层析、获得纯化的重组膜联蛋白V;所有制备的溶液均由无菌无内毒素水制成;使用BCA试剂盒测量蛋白质浓度;纯化后,通过SDS-PAGE电泳分析蛋白产物的纯度,超过98%。然后或者以溶液形式的水剂、或者复溶性状好的冻干粉剂。后续研究证明:不同制剂形式的重组膜联蛋白的各种活性相当。
(2)诱导实验性高血糖模型
将50只8-9周龄雄性B6小鼠随机分成五组:
第I组-对照组:用磷酸盐缓冲盐水(PBS);
第II组-模型组:STZ;
第III组-低剂量组:STZ注射前2小时注射1.25mg/kg/day膜联蛋白V;
第IV组-中剂量组:STZ注射前2小时注射2.5mg/kg/day膜联蛋白V;
第V组-高剂量组:STZ注射前2小时注射5mg/kg/day膜联蛋白V。
在模型的剂量选取中,我们在STZ注射前2小时注射膜联蛋白V,选取了7个剂量点,分别为:0.3125,0.625,1.25,2.5,5,10,20mg/kg/day,但在本实施例中主要提供效果最好的三个点进行研究,即1.25,2.5,5mg/kg/day。
使用链脲佐菌素诱导小鼠糖尿病模型,具体步骤为:小鼠过夜禁食后,通过将溶于0.1M柠檬酸缓冲液(pH=4.5),剂量为60mg/kg的STZ连续5天腹腔注射小鼠(禁食12小时,可自由饮水),对照组小鼠给予柠檬酸缓冲液来代替STZ;在注射STZ前2小时,将膜联蛋白V通过腹腔皮下注射给药和对照组小鼠注射磷酸盐缓冲盐水(PBS);在STZ注射后三天使用血糖仪测量空腹血糖水平,血糖水平>11.1mM的小鼠被认为是高血糖小鼠。后续实验中,每周测量每只小鼠的禁食体重和血糖水平(如图1A~1B);STZ注射结束后12w,小鼠禁食后通过断颈处死小鼠测量小鼠空腹血清胰岛素水平(如图1C)。
小鼠处死前1周进行IPGTT实验。小鼠禁食6h后,通过腹腔注射1.0g/kg葡萄糖,在0、15、30、60、90min监测血糖水平(如图2)。
将小鼠放入代谢笼中注射STZ后4周,8周,12周,测量小鼠24h食物摄入量(如图3A)、用水量(如图3B)和尿量(如图3C)。
由图1A~1C可知,膜联蛋白V处理的小鼠与模型组小鼠相比,空腹血糖显著降低,体重增加,空腹胰岛素水平较高,说明膜联蛋白V在改善糖尿病生理指标和代谢状况有一定效果。
由图2可知,在IPGTT测定中,模型组小鼠中葡萄糖水平显著增加,表明膜联蛋白V处理后的葡萄糖清除率提高。
由图3A~3C可知,在膜联蛋白V处理后4周、8周、12周时记录24h食物摄入量,耗水量和尿量,其增加量随着膜联蛋白V剂量的减少而增加。
(3)Western blotting检测方法
取出小鼠肝脏,迅速放入在液氮后提取蛋白质,组织在细胞裂解液中匀浆,冰上裂解30min后,12000rpm、4℃离心10min,收集上清液,并用考马斯亮蓝法(Bradford方法)检测蛋白浓度,调整蛋白浓度,加入5×loading buffer并在沸水浴中煮样5min,样品置于-20℃下保存备用。用抗体IRS1,pIRS1,GSK-3β,pGSK-3β,AKT和pAKT(Cell Signaling Technology,Boston,MA,USA)检测蛋白质;作为上样对照,使用内参抗体GAPDH(Santa Cruz Biotechnology,Heidelberg,Germany)和β-actin(Epitomics,Burlingame,USA);二抗选用山羊抗兔IgG和山羊抗小鼠IgG(Jackson Immuno Research),通过使用Image J软件对条带进行量化(如图5A~C)。
由图5A~C可知,与模型组相比,膜联蛋白V处理组(第III~V组)的肝脏中的pIRS1和pAKT的表达显著增加,膜联蛋白V处理组中的pGSK-3β水平显著降低;膜联蛋白V处理组的胰岛素信号通路蛋白表达水平增强,表明膜联蛋白V可提高肝脏胰岛素信号通路的敏感性。
(4)HE染色
HE染色用于观察肝脏、胰腺和肾脏的形态学变化。将肝脏、胰腺和肾脏组织置于4%的多聚甲醛中固定过夜;常规石蜡包埋,5μm切片;切片常规用二甲苯脱蜡,经各级乙醇至水洗。透明:二甲苯Ι、二甲苯II中各浸泡5min,脱水:无水乙醇Ι,无水乙醇II,95%酒精,80%酒精,75%酒精,各5min。苏木素复染2min后流水冲洗返蓝,自来水浸泡15min或温水(约50℃)5min。置伊红液2min,自来水冲洗。脱水:75%酒精、80%酒精、95%酒精、无水乙醇Ι、无水乙醇II各5min。透明:二甲苯Ι、二甲苯II中各浸泡5min,晾干3min。封片:滴加中性树脂封片于组织片上,然后取干净的盖玻片,仔细加在封固剂上,慢慢压平,使盖片位置适中。显微镜下观察、拍照并长期保存(如图4和图6)。
由图4可知,肝脏(图4A)和胰腺(图4B)的组织学分析显示,膜联蛋白V处理的小鼠和对照小鼠之间在HE染色上存在显著差异。从图4A中看到,对照组小鼠是正常的,STZ处理组肝细胞水肿,胞浆疏松,随着膜联蛋白V剂量的增加,病变程度逐渐减弱。模型组中可见少量炎性细胞浸润模型组中的组织,其他组中未见炎性细胞浸润;如图4B所示,对照组小鼠是正常的,模型组中的少量腺体坏死和结构消失,膜联蛋白V处理组虽均有腺体结构疏松,第III组和第IV组的部分腺体增生,可见少量脂肪空泡,第IV组中箭头所示动脉透明病变,第V组中只有部分腺体可见少量脂肪空泡。总体而言,在减缓肝脏和胰腺病理损伤方面,随着膜联蛋白V剂量的增加,病变减轻。
由图6可知,膜联蛋白V对肾脏的影响主要是对肾小管和肾小球的影响。随着膜联蛋白V剂量的增加,肾脏HE结果显示急性肾小管坏死的症状明显改善,肾小球膜细胞增生和肾小球萎缩随膜联蛋白V用量的增加而逐渐减弱(图6A);在这项研究中,与PBS对照组相比,膜联蛋白V给药后显著降低STZ诱导的小鼠血清BUN(图6B)和Scr水平(图6C)。以上结果表明膜联蛋白V可以减缓STZ诱导的糖尿病肾病的肾功能损害。
(5)细胞培养
胰岛素瘤细胞购自ATCC提供的中国科学院细胞库。胰岛素瘤细胞使用含10%胎牛血清(FBS)(Gibco,BRL,USA)的RPMI 1640培养基(Hyclone,Logan,UT)中于37℃,5%CO2环境中培养。在96孔板以每孔1.0×105细胞密度接种胰岛素瘤细胞,12小时后,将胰岛素瘤细胞分别与0.1M柠檬酸盐缓冲液(pH=4.5),0.5、0.75、1、1.5、2μM STZ孵育24小时,使用CCK8进行细胞增殖实验;选择细胞损伤较明显的剂量建立细胞损伤模型,后续的实验选择STZ,剂量为1μM作用24小时;在96孔板按每孔接种105细胞,在正常条件下培养24小时,STZ处理2小时之前用膜联蛋白V处理细胞以及PBS作为阴性对照,48小时后,利用CCK8进行细胞增殖测试。
由图7A~7C可知,为研究膜联蛋白V对STZ损伤的胰岛素瘤细胞的作用,首先建立了胰岛素瘤细胞损伤模型(图7A)。在1μM的STZ的剂量下作用24h,较对照组胰岛素瘤细胞增殖明显降低。为研究仅膜联蛋白V对胰岛素瘤细胞的作用,将不同剂量的膜联蛋白V加入到胰岛素瘤细胞中,结果显示单独使用膜联蛋白V处理的胰岛素瘤细胞增殖不明显(图7B),在STZ损伤的情况下细胞增殖显著改善(图7C),表明膜联蛋白V对STZ损伤的胰岛素瘤细胞的增殖发挥重要作用。以上结果表明膜联蛋白V对STZ损伤的胰岛素瘤细胞起保护作用。
本发明不仅发现膜联蛋白V在体内对糖尿病有保护作用,而且在体外也发现其能减少STZ对胰岛素瘤细胞的损伤作用,同时还发现了膜联蛋白V对糖尿病肾脏并发症或肾功能的损害具有预防作用。
本发明也尝试将更多的常规的蛋白质药物的制剂方法应用于膜联蛋白V的制剂,不同的剂型形式都产生了较好地延缓糖尿病进程以及改善糖尿病生理指标和代谢状况、改善糖尿病胰岛素信号通路、改善糖尿病肝脏、胰腺和肾脏的病理变化、预防糖尿病肾脏并发症或肾功能损害、改善糖尿病血清肌酐和血尿素氮的效果;本发明还尝试像常规的糖尿病治疗或预防药物一样,将膜联蛋白V通过与常规糖尿病治疗或预防药物或治疗方法联合应用,能够进一步提高糖尿病治疗或预防效果。
以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!