用于制备他品洛夫的方法与流程
相关申请的交叉引用
本申请要求2017年11月10日提交的题为“方法(process)”的美国临时申请第62/584,192号的优先权,所述专利的内容以全文引用的方式并入本文。
技术实现要素:
本发明的一些实施例提供一种用于制备式(i)化合物或其盐的方法和其中使用的新型中间体
本发明的一些实施例描述式(iia)化合物或其盐
和其制备方法。
本发明的一些实施例描述式(iva)化合物或其盐
和其制备方法。
本发明的一些实施例描述式(v)化合物或其盐
和其制备方法。
本发明的一些实施例描述式(vi)化合物或其盐
和其制备方法。
本发明的一些实施例描述包含根据本发明的方法制备的式(i)化合物或其盐或溶剂化物和药学上可接受的赋形剂的药物组合物。
附图说明
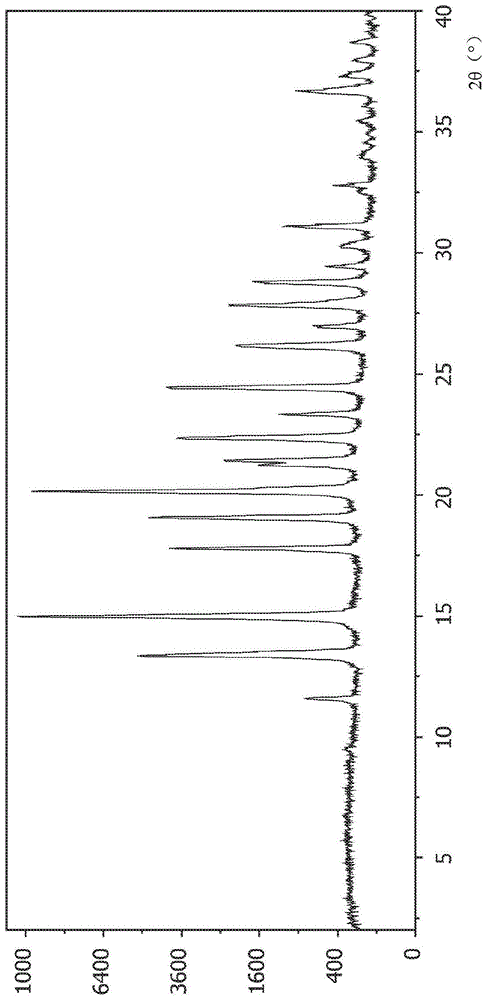
图1示出呈结晶固态形式(形式1)的式(i)化合物的x射线粉末衍射(xrpd)图。
图2示出呈结晶固态形式的式(i)化合物的乙酸溶剂化物的x射线粉末衍射(xrpd)图。
具体实施方式
式(i)的3,5-二羟基-4-异丙基-反式芪,也被称为(e)-2-异丙基-5-苯乙烯基苯-1,3-二醇或他品洛夫(tapinarof)为衍生自细菌的天然产物
该化合物具有几种潜在有用的生物学反应,包括抗菌、抗氧化剂和抗癌活性。pct专利申请wo200142231公开作为抗银屑病药和蛋白激酶抑制剂的多羟基芪和芪氧化物。
合成式(i)化合物的几种途径是所属领域已知的。中国专利申请cn101648851描述经由霍纳-沃兹沃思-埃蒙斯烯化反应形成(e)-烯烃的合成途径。还已知的途径是经由傅里德-克拉夫茨烷基化将异丙基引入到被取代的间苯二酚衍生物上。
kronenwerth等人描述一种类似于已知生物合成途径的替代合成方法(《欧洲有机化学杂志(eur.j.org.chem.)》2014,8026-8028)。然而,在此途径中,在整个合成过程中存在中间体和最终产物产率低的问题。还存在与异丙基芪中痕量汞的去除不完全相关联的毒性问题,这使得此途径不适用于大规模制造药物产品。
schamp等人(《四面体(tetrahedron)》,1973,29,3857-3859)公开由对应1,3-环己二酮合成简单的2-取代间苯二酚,如2-甲基、2-苯甲基和2-乙酰基间苯二酚。报道的条件涉及氯化1,3-环己二酮,随后在用25%的干燥氯化氢于二甲基甲酰胺中的溶液加热时除去hcl。
需要用于大规模制造式(i)化合物,具体地说没有潜在毒性问题的高产率合成的有效且可扩展的途径。
本发明提供与方法有关的许多实施例,其概括在下方案1中:
制备式(i)化合物-方法a
一些实施例描述用于制备式(i)化合物或其盐或溶剂化物的方法
其包含方法步骤(a)、(b)和(c)中的一个或多个,其中:
(a)包含使式(iii)化合物或其盐反应
以形成式(ii)化合物或其盐
其中x为cl、br或i,并且其后(ii)将式(ii)化合物或其盐转化成式(i)化合物或其盐或溶剂化物;
(b)包含将式(vi)化合物或其盐
转化成式(iii)化合物或其盐
并且其后将式(iii)化合物或其盐转化成式(i)化合物或其盐或溶剂化物;和
(c)包含将式(ix)化合物或其盐
转化成式(vi)化合物或其盐
并且其后将式(vi)化合物或其盐转化成式(i)化合物或其盐或溶剂化物。
一些实施例描述用于制备式(i)化合物或其盐或溶剂化物的方法,其包含方法步骤(a)到(c)中的至少一个。本发明的方法可包括方法步骤(a),(b)和(c)中的一个、两个或全部三个。
方法步骤(a)、(b)和(c)中的每个的产物可任选地结晶。
在一些实施例中,通过方法(a)、(b)或(c)制备的式(i)化合物呈结晶固态形式。在一个实施例中,提供呈晶体固态形式的式(i)化合物(形式1),其x射线粉末衍射图基本上如图1所示。在另一个实施例中,提供呈结晶固态的式(i)化合物,其特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在另一个实施例中,提供呈结晶固态的式(i)化合物,其特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。
方法步骤(a)
在一些实施例中,x为cl。
在一些实施例中,其中x为cl,并且反应使用选自由以下组成的组的氯化试剂进行:1,3-二氯-5,5-二甲基乙内酰脲(dcdmh)、n-氯丁二酰亚胺(ncs)和三氯异氰尿酸(tcca)。
在一些实施例中,氯化试剂为dcdmh。
在一些实施例中,式(ii)化合物或其盐转化成式(i)化合物或其盐在合适的溶剂中和任选地在具有添加剂材料的情况下进行。
发现用多种溶剂以良好的产率实现了这类转化。在一些实施例中,式(ii)化合物或其盐转化以得到式(i)化合物或其盐在合适的溶剂中进行,所述溶剂为选自由以下组成的组的极性非质子溶剂:二甲基甲酰胺(dmf)、1,3-二甲基-3,4,5,6-四氢-2(1h)-嘧啶酮(dmpu)、二甲基乙酰胺(dmac)和环丁砜。
尽管使用溶剂(如dmf)在操作上简单,但由于其生殖毒性,在药物产品的制造中使用这类溶剂是潜在关注的问题。因此,寻求一种替代溶剂,其将适合用于大规模制造药物产品。
然而,发现对于替代溶剂,包括一些常用溶剂,式(ii)化合物或其盐(例如其中x为cl)转化成式(i)化合物或其盐的进展不好。在这种情况下,发现使用添加剂材料,如苯甲基乙基氯化铵,以良好的产率促进此反应。这在下表1中说明。
表1
1反应在密封管中进行,其允许加热远高于溶剂的沸点。
2添加剂=2当量的苯甲基三乙基氯化铵。
3基于粗反应混合物的hplc测定的产率。
因此,进一步研究在式(ii)化合物或其盐(其中x为cl)转化成式(i)化合物或其盐或溶剂化物中使用一系列不同的添加剂材料。这些结果在下表2中表示。
表2
1基于粗反应混合物的hplc测定的产率。
在一些实施例中,式(ii)化合物或其盐转化成式(i)化合物或其盐在添加剂存在下进行,所述添加剂为季铵盐,例如溴化季铵盐或氯化季铵盐。在一些实施例中,溴化季铵盐为四丁基溴化铵。在一些实施例中,氯化季铵盐选自由以下组成的组:苯甲基三乙基氯化铵、四丁基氯化铵、四乙基氯化铵和四甲基氯化铵。在一些实施例中,氯化季铵盐为四乙基氯化铵。
在一些实施例中,式(ii)化合物或其盐转化以得到式(i)化合物或其盐或溶剂化物在添加剂存在下在选自由以下组成的组的溶剂中进行:乙腈、甲苯、2-甲基四氢呋喃、乙酸异丙酯、丙酮和甲基异丁基酮。发现乙腈提供溶解度和高沸点的最佳组合。在一些实施例中,此转化在为乙腈的溶剂中进行。
本公开的实施例描述式(iia)化合物或其盐
式(i)化合物可以其乙酸溶剂化物的形式制备。本公开的一些实施例描述以其乙酸溶剂化物的形式的式(i)化合物。已经发现,式(i)化合物的乙酸溶剂化物的形成为本发明的方法提供杂质和颜色清除的能力。式(i)化合物的乙酸溶剂化物其后可转化成式(i)化合物。
在一些实施例中,提供呈结晶固态形式的式(i)化合物的乙酸溶剂化物。在一些实施例中,提供呈结晶固态形式的式(i)化合物的乙酸溶剂化物,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,提供呈结晶固态的式(i)化合物的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,提供呈结晶固态的式(i)化合物的乙酸溶剂化物,其特征在于,x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。
在一些实施例中,方法另外包含使式(i)化合物或其盐或溶剂化物再结晶的步骤。在一些实施例中,再结晶使用甲醇和水进行。
方法步骤(b)
在一些实施例中,式(vi)化合物或其盐转化成式(iii)化合物或其盐包含使式(vi)化合物或其盐脱羧以形成式(v)化合物或其盐
随后使式(v)化合物或其盐酯化以形成所述式(iv)化合物或其盐
其中r为c1-4烷基;和其后使式(iv)化合物或其盐环化以形成式(iii)化合物或其盐。
在一些实施例中,式(vi)化合物或其盐转化成式(v)化合物或其盐包含在碱存在下脱羧。在一些实施例中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在具体实施例中,碱为三乙胺。
在一些实施例中,r为甲基、乙基、丙基或丁基。在一些实施例中,r为叔丁基。在一些实施例中,r为甲基。
在一些实施例中,式(v)化合物或其盐酯化成式(iv)化合物或其盐使用甲醇进行,例如酯化使用甲醇和盐酸进行。
在一些实施例中,式(iv)化合物或其盐环化成式(iii)化合物或其盐使用叔丁醇钾进行。
在一些实施例中,使式(iii)化合物或其盐酸化并且通过用甲基环己烷沉淀来分离。
在一些实施例中,式(vi)化合物或其盐转化成式(iii)化合物或其盐为套叠的,使得式(v)化合物或其盐和式(iv)化合物或其盐不分离。
一些实施例描述式(iva)化合物或其盐
式(iva)化合物,即(e)-7-甲基-5-氧代-3-苯乙烯基辛酸甲酯通过以下数据表征。
1hnmr(500mhz,dmso)δ7.33(m,2h),7.29(m,2h),7.20(m,1h),6.37(d,1h,j=16.0hz),6.15(dd,1h,j=8.1hz,j=16.0hz),3.56(s,3h),3.09(m,1h),2.60(m,2h),2.50(dd,1h,6.1hz,j=15.4hz),2.42(dd,1h,j=8.1hz,j=15.4hz),2.29(d,2h,7.0hz),2.00(m,1h),0.82(s,6h,6.7hz)。
13cnmr(125mhz,dmso)δ208.7(c),171.8(c),136.8(c),131.9(ch),129.5(ch),128.5(ch),127.2(ch),125.9(ch),51.4(ch2),51.2(ch3),46.7(ch2),38.5(ch2),34.4(ch),23.8(ch),22.29(ch3),22.26(ch3)。
c18h25o3的hrms-apci(m/z)[m+h]+计算值,289.1798;实测值,289.1719。
在一些实施例中,提供式(v)化合物或其盐
式(v)化合物,即(e)-7-甲基-5-氧代-3-苯乙烯基辛酸通过以下数据表征。
1hnmr(700mhz,dmso)δ12.13(s,1h),7.33(m,2h),7.29(m,2h),7.20(m,1h),6.37(d,1h,j=16hz),6.17(dd,1h,j=8.0hz,j=16.0hz),3.07(m,1h),2.60(m,2h),2.46(dd,1h,j=6.2hz,j=15.5hz),2.33(dd,1h,j=8.o,j=15.5hz),2.30(d,2h,j=7.1hz),2.0(m,1h),0.82(d,6h,j=6.6hz)。
13cnmr(176mh,dmso)δ208.8(c),172.9(c),136.9(c),132.2(ch),129.3(ch),128.5(ch),127.1(ch),125.9(ch),51.4(ch2),46.8(ch2),38.9(ch2),34.4(ch),23.8(ch),22.3(ch3),22.3(ch3)。
c17h23o3的hrms-apci(m/z)[m+h]+计算值,275.1642;实测值,275.1635。
在一些实施例中,提供式(vi)化合物或其盐。
式(iii)化合物或其盐可通过本文所描述的方法(例如方法步骤(a))或通过所属领域的技术人员已知的方法(例如通过kronenwerth,m.等人中描述的方法)转化成式(i)化合物或其盐或溶剂化物。在一些实施例中,式(iii)化合物或其盐可通过方法步骤(a)转化成式(i)化合物或其盐或溶剂化物。
方法步骤(c)
在一些实施例中,式(ix)化合物或其盐转化成式(vi)化合物或其盐包含使式(ix)化合物或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
随后添加丙二酸酯(r1o(o)c-ch2-c(o)or2)以形成式(vii)化合物或其盐
其中r1和r2独立地为c1-4烷基;
并且其后使式(vii)化合物或其盐水解以形成式(vi)化合物或其盐。
在一些实施例中,式(ix)化合物或其盐缩合成式(viii)化合物或其盐使用氢氧化锂、氢氧化钾或氢氧化钠进行,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。
在一些实施例中,式(viii)化合物或其盐转化成式(vii)化合物或其盐包含添加丙二酸酯,其为丙二酸二叔丁酯或丙二酸二乙酯。
在一些实施例中,式(ix)化合物或其盐转化成式(vi)化合物或其盐为套叠的,使得式(vii)和式(viii)化合物或其盐不分离。
在一些实施例中,提供式(viia)化合物或其盐。
式(viia)化合物,即(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二乙酯,通过以下数据表征。
1hnmr(700mhz,dmso)δ7.30(m,2h),7.30(m,sh0,7.21(m,1h),6.39(d,1h)j=15.8hz),6.14(dd,1h,j=15.99hz,j=8.9hz),4.12(q,2h,j=7.13hz),4.06(m,2h),3.68(d,1h,j=8.1hz),3.33(m,1h),2.73(dd,ih,j=16.9hz,j=9.0hz),2.63(m,1h,),2.28(d,2h,6.9hz),1.98(m,1h,6.7hz),1.16(t,3h,j=7.1hz),1.10(t,3h,j=7.0hz),0.81(d,3h,j=6.6hz),0.80(d,3h,j=6.7hz)。
13cnmr(176mhz,dmso)δ208.1(c),167.7(c),167.6(c),136.6(c),131.4(ch),128.9(ch),127.4(ch),125.9(ch),61.0(ch2),60.8(ch2),55.0(ch),51.3(ch2),44.8(ch2),37.7(ch),23.8(ch),22.3(ch3),22.2(ch3),13.9(ch3),13.9(ch3)。
c22h31o5的hrms-apci(m/z)[m+h]+计算值,375.2166;实测值,375.2158。
式(vi)化合物或其盐可通过本文所描述的方法(例如方法步骤(a)和(b))或通过所属领域的技术人员已知的方法(例如通过kronenwerth,m.等人中描述的方法)转化成式(i)化合物或其盐或溶剂化物。在一些实施例中,式(vi)化合物或其盐可通过方法步骤(a)和(b)转化成式(i)化合物或其盐或溶剂化物。
制备式(i)化合物-方法b
本文一些实施例描述用于制备式(i)化合物或其盐或溶剂化物的方法
其包含芳构化式(ii)化合物或其盐
其中x为cl、br或i;以获得式(i)化合物。在一些实施例中,方法另外包含纯化式(i)化合物或其盐或溶剂化物。在一些实施例中,纯化包含使式(i)化合物或其盐或溶剂化物结晶。在一些实施例中,式(i)化合物为在本文所描述的任何实施例中描述的晶体形式。在一些实施例中,式(i)化合物为晶体形式1。在一些实施例中,式(i)化合物为无水晶体。在一些实施例中,式(i)化合物的x射线粉末衍射图基本上如图1所示。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)处的特定峰。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在一些实施例中,x为cl。在一些实施例中,芳构化在合适的溶剂中和任选地在具有添加剂的情况下进行。在一些实施例中,芳构化在合适的溶剂中进行,所述溶剂为选自由以下组成的组使极性非质子溶剂:二甲基甲酰胺(dmf)、1,3-二甲基-3,4,5,6-四氢-2(1h)-嘧啶酮。在一些实施例中,芳构化在添加剂存在下在选自由以下组成的组的溶剂中进行:乙腈、甲苯、2-甲基四氢呋喃、乙酸异丙酯、丙酮和甲基异丁基酮。在一些实施例中,芳构化在添加剂存在下在乙腈中进行。在一些实施例中,添加剂为季铵盐。在一些实施例中,季铵盐选自由以下组成的组:四丁基溴化铵、苯甲基三乙基氯化铵、四丁基氯化铵、四乙基氯化铵和四甲基氯化铵。在一些实施例中,季铵盐为四乙基氯化铵。在一些实施例中,芳构化在具有乙基氯化铵的情况下在乙腈中进行。
在一些实施例中,方法另外包含用卤化剂卤化式(iii)化合物或其盐
以获得式(ii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。在一些实施例中,卤化剂为dcdmh,并且式(ii)化合物或其盐为式(iia)化合物或其盐:
在一些实施例中,卤化在甲醇中进行。在一些实施例中,卤化剂为dcdmh,并且卤化在甲醇中进行。
在一些实施例中,方法另外包含环化式(iv)化合物或其盐
其中r为c1-4烷基,以获得式(iii)化合物或其盐。在一些实施例中,r选自由以下组成的组:甲基、乙基、丙基或丁基。在一些实施例中,r为叔丁基。在一些实施例中,r为甲基。在一些实施例中,环化包含使式(iv)化合物或其盐与碱接触。在一些实施例中,环化使用叔丁醇钾进行。在一些实施例中,环化在2-甲基四氢呋喃中进行。在一些实施例中,环化包含在2-甲基四氢呋喃中用叔丁醇钾处理式(iv)化合物或其盐,例如化合物(iva)或其盐。在一些实施例中,使式(iii)化合物或其盐进一步酸化并且通过用甲基环己烷沉淀来分离。
在一些实施例中,方法另外包含酯化式(v)化合物或其盐
以获得式(iv)化合物或其盐。在一些实施例中,酯化使用甲醇和盐酸进行以获得化合物(iv)。在一些实施例中,酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。
在一些实施例中,方法另外包含使式(vi)化合物或其盐脱羧
以获得式(v)化合物或其盐。在一些实施例中,脱羧包含存在碱。在一些实施例中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,碱为三甲胺。在一些实施例中,脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。
在一些实施例中,方法另外包含水解式(vii)化合物或其盐
其中r1和r2各自独立地为c1-4烷基;以获得式(vi)化合物或其盐。在一些实施例中,r1和r2中的每个为乙基(viia)。在一些实施例中,水解包含用氢氧化钠处理式(vii)化合物或其盐。在一些实施例中,水解包含在乙醇中用氢氧化钠处理式(vii)化合物或其盐。在一些实施例中,方法包含水解式(viia)化合物或其盐,其包含在乙醇中用氢氧化钠处理式(viia)化合物或其盐。
在一些实施例中,方法另外包含将丙二酸二烷基酯(r1o(o)c-ch2-c(o)or2,其中r1和r2各自独立地为c1-4烷基)添加到式(viii)化合物或其盐中
以获得式(vii)化合物或其盐。在一些实施例中,丙二酸二烷基酯为丙二酸二叔丁酯或丙二酸二乙酯。在一些实施例中,添加包含在溴化锂/三乙胺存在下使丙二酸二烷基酯与式(viii)化合物或其盐接触。
在一些实施例中,方法另外包含使反式肉桂醛(式(ix)化合物)或其盐
与甲基异丁基酮缩合以形成式(viii)化合物或其盐。在一些实施例中,缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,缩合包含在氢氧化钠存在下在甲醇中用反式肉桂醛或其盐处理甲基异丁基酮。
制备式(i)化合物-方法c
在一些实施例中,本文所描述用于制备式(i)化合物或其盐或溶剂化物的方法
其包含:
a)使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐
b)酯化式(v)化合物或其盐以形成式(iv)化合物或其盐
c)环化式(iv)化合物或其盐以形成式(iii)化合物或其盐,
d)卤化式(iii)化合物或其盐以形成式(ii)化合物或其盐,
其中x选自br、cl和i;和
e)芳构化式(ii)化合物或其盐以形成式(i)化合物或其盐或溶剂化物。
在一些实施例中,方法另外包含在步骤c)中分离式(iii)化合物或其盐。在一些实施例中,方法包含在步骤d)中分离式(ii)化合物或其盐。在一些实施例中,方法另外包含纯化从步骤e)获得的式(i)化合物或其盐或溶剂化物。在一些实施例中,纯化包含使式(i)化合物或其盐或溶剂化物结晶。在一些实施例中,式(i)化合物为在本文所描述的任何实施例中描述的晶体形式。在一些实施例中,式(i)化合物为晶体形式1。在一些实施例中,式(i)化合物为无水晶体。在一些实施例中,式(i)化合物的x射线粉末衍射图基本上如图1所示。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)处的特定峰。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。
在一些实施例中,在步骤a)中式(vi)化合物或其盐脱羧包含存在碱。在一些实施例中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,碱为三甲胺。在一些实施例中,脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。
在一些实施例中,在步骤b)中式(iv)化合物或其盐的r选自由以下组成的组:甲基、乙基、丙基或丁基。在一些实施例中,在步骤b)中式(iv)化合物或其盐的r为叔丁基。在一些实施例中,在步骤b)中式(iv)化合物或其盐的r为甲基。在一些实施例中,在步骤b)中酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iv)或其盐或溶剂化物。在一些实施例中,酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。
在一些实施例中,在步骤c)中环化包含使式(iv)化合物或其盐与碱接触。在一些实施例中,环化使用叔丁醇钾进行。在一些实施例中,环化在2-甲基四氢呋喃中进行。在一些实施例中,环化包含在2-甲基四氢呋喃中用叔丁醇钾处理式(iv)化合物或其盐,例如化合物(iva)或其盐。在一些实施例中,使式(iii)化合物或其盐进一步酸化并且通过用甲基环己烷沉淀来分离。
在一些实施例中,在步骤d)中式(ii)化合物或其盐的x为cl、br或i。在一些实施例中,在步骤d)中式(ii)化合物或其盐的x为cl。在一些实施例中,卤化包含用卤化剂处理式(iii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。在一些实施例中,卤化剂为dcdmh,并且式(ii)化合物或其盐为式(iia)化合物或其盐。
在一些实施例中,在步骤e)中芳构化在合适的溶剂中和任选地在具有添加剂的情况下进行。在一些实施例中,在步骤e)中芳构化在合适的溶剂中进行,所述溶剂为选自由以下组成的组的极性非质子溶剂:二甲基甲酰胺(dmf)、1,3-二甲基-3,4,5,6-四氢-2(1h)-嘧啶酮。在一些实施例中,在步骤e)中芳构化在选自由以下组成的组的溶剂中在添加剂存在下进行:乙腈、甲苯、2-甲基四氢呋喃、乙酸异丙酯、丙酮和甲基异丁基酮。在一些实施例中,芳构化在添加剂存在下在乙腈中进行。在一些实施例中,添加剂为季铵盐。在一些实施例中,季铵盐选自由以下组成的组:四丁基溴化铵、苯甲基三乙基氯化铵、四丁基氯化铵、四乙基氯化铵和四甲基氯化铵。在一些实施例中,季铵盐为四乙基氯化铵。在一些实施例中,芳构化在具有乙基氯化铵的情况下在乙腈中进行。
在一些实施例中,步骤b)的r为甲基,并且步骤d)的x为氯。
在一些实施例中,在步骤a)中式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将式r1o(o)c-ch2-c(o)or2的丙二酸二烷基酯(其中r1和r2中的每个独立地为c1-4烷基)添加到式(viii)化合物或其盐中以形成式(vii)化合物或其盐
其中r1和r2各自如对于丙二酸二烷基酯所定义;
iii.水解式(vii)化合物或其盐,以形成所述式(vi)化合物或其盐。
在一些实施例中,在步骤i.中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤i.中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。
在一些实施例中,在步骤ii.中r1和r2中的每个为乙基。在一些实施例中,丙二酸二烷基酯为丙二酸二叔丁酯或丙二酸二乙酯。在一些实施例中,在步骤ii.中添加包含在溴化锂/三乙胺存在下使丙二酸酯与式(viii)化合物或其盐接触。
制备式(i)化合物-方法d
本文一些实施例描述用于制备式(i)化合物或其盐或溶剂化物的方法
其包含:
a)加热式(vi)化合物
与催化性三乙胺以形成式(v)化合物
b)加热式(v)化合物与甲醇和含水盐酸以形成式(iva)化合物
c)用叔丁醇钾处理式(iva)化合物的冷却的溶液以形成式(iii)化合物
d)加热式(iii)化合物与1,3-二氯-5,5-二甲基乙内酰脲以形成式(iia)化合物
e)加热式(iia)化合物与四乙基氯化铵以形成式(i)化合物其盐或溶剂化物
在一些实施例中,方法另外包含通过结晶纯化来自步骤e)的式(i)化合物。在一些实施例中,方法另外包含在步骤c)之后,步骤ci)分离式(iii)化合物。在一些实施例中,方法另外包含在步骤d)之后,步骤di)分离式(iia)化合物。在一些实施例中,方法另外包含纯化从步骤e)获得的式(i)化合物。在一些实施例中,纯化包含使式(i)结晶。在一些实施例中,式(i)化合物为在本文所描述的任何实施例中描述的晶体形式。在一些实施例中,式(i)化合物为晶体形式1。在一些实施例中,式(i)化合物为无水晶体。在一些实施例中,式(i)化合物的x射线粉末衍射图基本上如图1所示。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)处的特定峰。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。
在一些实施例中,在步骤a)中式(vi)化合物通过包含以下的方法制备:
i.在于甲醇中的氢氧化钠存在下用反式肉桂醛处理甲基异丁基酮以形成式(viii)化合物
ii.在溴化锂和三乙胺存在下用丙二酸二乙酯处理所述式(viii)化合物以形成式(viia)化合物
iii.用氢氧化钠和乙醇水解式(viia)化合物以获得式(vi)化合物。
制备式(i)化合物-方法e
一些实施例描述用于本发明的特定实施例方法,其在下方案2中示出并且如在实例中详细描述。
用于制备式(vi)化合物的方法
本文一些实施例描述用于制备式(vi)化合物或其盐的方法
其包含:
a)使反式肉桂醛或其盐或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。
用于制备式(v)化合物的方法
本文一些实施例描述用于制备式(v)化合物或其盐的方法
其包含在碱存在下使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐。在一些实施例中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,碱为三甲胺。在一些实施例中,脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。在一些实施例中,式(vi)化合物或其盐通过本文所描述的任何方法制备。在一些实施例中,式(vi)化合物或其盐通过包含以下的方法制备:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
本文一些实施例描述用于制备式(v)化合物或其盐的方法
其包含:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐
d)在碱存在下使式(vi)化合物或其盐脱羧,以形成式(v)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。在一些实施例中,在步骤d)中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,在步骤d)中,碱为三甲胺。在一些实施例中,在步骤d)中脱羧包含在三甲胺存在下加热[2式(vi)化合物或其盐。
用于制备式(iva)化合物的方法
本文一些实施例描述用于制备式(iva)化合物或其盐的方法
其包含酯化式(v)化合物或其盐
以形成式(iva)化合物或其盐。在一些实施例中,酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iva)。在一些实施例中,酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。在一些实施例中,式(v)化合物或其盐或其盐通过本文所描述的任何方法制备。在一些实施例中,式(v)化合物或其盐通过包含以下的方法制备:在碱存在下使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐。在一些实施例中,式(vi)化合物或其盐通过本文所描述的任何方法制备。在一些实施例中,式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
iii.水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
本文一些实施例描述用于制备式(iva)化合物或其盐的方法
其包含:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐
d)在碱存在下使式(vi)化合物或其盐脱羧,以形成式(v)化合物或其盐
e)酯化式(v)化合物或其盐以形成式(iva)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。在一些实施例中,在步骤d)中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,在步骤d)中,碱为三甲胺。在一些实施例中,在步骤d)中脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。在一些实施例中,在步骤e)中酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iva)。在一些实施例中,在步骤e)中酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。
用于制备式(iia)化合物的方法
本文一些实施例描述用于制备式(iia)化合物或其盐的方法
其包含卤化式(iii)化合物或其盐
以形成式(iia)化合物或其盐。在一些实施例中,卤化包含用卤化剂处理式(iii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。在一些实施例中,卤化剂为dcdmh。在一些实施例中,式(iii)化合物或其盐通过本文所描述的任何方法制备。在一些实施例中,式(iii)化合物或其盐通过包含以下的方法制备:环化式(iva)化合物或其盐,
以形成式(iii)化合物或其盐。在一些实施例中,式(iva)化合物或其盐通过本文所描述的任何方法制备。在一些实施例中,式(iva)化合物或其盐通过包含以下的方法制备:酯化式(v)化合物或其盐
在一些实施例中,式(v)化合物或其盐通过本文所描述的任何方法制备。在一些实施例中,式(v)化合物或其盐通过包含以下的方法制备:在碱存在下使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐。在一些实施例中,式(vi)化合物或其盐通过本文所描述的任何方法制备。在一些实施例中,式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
iii.水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
本文一些实施例描述用于制备式(iia)化合物或其盐的方法
其包含:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐
d)在碱存在下使式(vi)化合物或其盐脱羧,以形成式(v)化合物或其盐
e)酯化式(v)化合物或其盐以形成式(iva)化合物或其盐
f)环化式(iva)化合物或其盐以形成式(iii)化合物或其盐
g)卤化式(iii)化合物或其盐以形成式(iia)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。在一些实施例中,在步骤d)中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,在步骤d)中,碱为三甲胺。在一些实施例中,在步骤d)中,脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。在一些实施例中,在步骤e)中酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iva)。在一些实施例中,在步骤e)中酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。在一些实施例中,在步骤g)中卤化包含用卤化剂处理式(iii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。在一些实施例中,卤化剂为dcdmh。
通过方法a制备的式(i)化合物
本文一些实施例描述式(i)化合物或其盐或溶剂化物
其通过包含以下的方法制备:
a)使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐
b)酯化式(v)化合物或其盐以形成式(iv)化合物或其盐
c)环化式(iv)化合物或其盐以形成式(iii)化合物或其盐
d)卤化式(iii)化合物或其盐以形成式(ii)化合物或其盐
其中x选自br、cl和i;和
e)芳构化式(ii)化合物或其盐以形成式(i)化合物或其盐或溶剂化物。
一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法另外包含分离式(iii)化合物或其盐。一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法包含分离式(ii)化合物或其盐。一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法另外包含纯化从步骤e)获得的式i化合物。在一些实施例中,纯化包含使式(i)结晶。在一些实施例中,式(i)化合物为晶体形式1。在一些实施例中,式(i)化合物为无水晶体。在一些实施例中,式(i)化合物的x射线粉末衍射图基本上如图1所示。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)处的特定峰。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。
在一些实施例中,在步骤a)中式(vi)化合物或其盐脱羧包含存在碱。在一些实施例中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,碱为三甲胺。在一些实施例中,脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。
在一些实施例中,在步骤b)中,式(iv)化合物或其盐的r选自由以下组成的组:甲基、乙基、丙基或丁基。在一些实施例中,在步骤b)中式(iv)化合物或其盐的r为叔丁基。在一些实施例中,在步骤b)中式(iv)化合物或其盐的r为甲基。在一些实施例中,在步骤b)中酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iv)。在一些实施例中,酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。
在一些实施例中,在步骤c)中环化包含使式(iv)化合物或其盐与碱接触。在一些实施例中,环化使用叔丁醇钾进行。在一些实施例中,环化在2-甲基四氢呋喃中进行。在一些实施例中,环化包含在2-甲基四氢呋喃中用叔丁醇钾处理式(iv)化合物或其盐,例如化合物(iva)或其盐。在一些实施例中,使式(iii)化合物或其盐进一步酸化并且通过用甲基环己烷沉淀来分离。
在一些实施例中,在步骤d)中式(ii)化合物或其盐的x为cl、br或i。在一些实施例中,在步骤d)中式(ii)化合物或其盐的x为cl。在一些实施例中,卤化包含用卤化剂处理式(iii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。在一些实施例中,卤化剂为dcdmh,并且式(ii)化合物或其盐为式(iia)化合物或其盐。
在一些实施例中,在步骤e)中芳构化在合适的溶剂中和任选地在具有添加剂的情况下进行。在一些实施例中,在步骤e)中芳构化在合适的溶剂中进行,所述溶剂为选自由以下组成的组的极性非质子溶剂:二甲基甲酰胺(dmf)、1,3-二甲基-3,4,5,6-四氢-2(1h)-嘧啶酮。在一些实施例中,在步骤e)中芳构化在选自由以下组成的组的溶剂中在添加剂存在下进行:乙腈、甲苯、2-甲基四氢呋喃、乙酸异丙酯、丙酮和甲基异丁基酮。在一些实施例中,芳构化在添加剂存在下在乙腈中进行。在一些实施例中,添加剂为季铵盐。在一些实施例中,季铵盐选自由以下组成的组:四丁基溴化铵、苯甲基三乙基氯化铵、四丁基氯化铵、四乙基氯化铵和四甲基氯化铵。在一些实施例中,季铵盐为四乙基氯化铵。在一些实施例中,芳构化在具有乙基氯化铵的情况下在乙腈中进行。
在一些实施例中,步骤b)的r为甲基,并且步骤d)的x为氯。
一些实施例描述式(i)化合物或其盐,其中式(vi)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(i)化合物或其盐或溶剂化物,其中式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将式r1o(o)c-ch2-c(o)or2的丙二酸二烷基酯(其中r1和r2中的每个独立地为c1-4烷基)添加到式(viii)化合物或其盐中以形成式(vii)化合物或其盐
其中r1和r2各自如对于丙二酸二烷基酯所定义;
iii.水解式(vii)化合物或其盐以形成式(vi)化合物或其盐。
在一些实施例中,在步骤i.中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤i.中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。
在一些实施例中,在步骤ii.中r1和r2中的每个为乙基。在一些实施例中,在步骤ii.中丙二酸二烷基酯为丙二酸二叔丁酯或丙二酸二乙酯。在一些实施例中,在步骤ii.中添加包含在溴化锂/三乙胺存在下使丙二酸酯与式(viii)化合物或其盐接触。
通过方法b制备的式(i)化合物
本文一些实施例描述式(i)化合物或其盐或溶剂化物
其通过包含以下的方法制备:
a)使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐
b)酯化式(v)化合物或其盐以形成式(iva)化合物或其盐
c)环化式(iva)化合物或其盐以形成式(iii)化合物或其盐
d)卤化式(iii)化合物或其盐以形成式(iia)化合物或其盐
e)芳构化式(iia)化合物或其盐以形成式(i)化合物或其盐或溶剂化物。
一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法另外包含分离式(iii)化合物或其盐。一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法包含分离式(iia)化合物或其盐。一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法另外包含纯化从步骤e)获得的式(i)化合物。在一些实施例中,纯化包含使式(i)结晶。在一些实施例中,式(i)化合物为晶体形式1。在一些实施例中,式(i)化合物为无水晶体。在一些实施例中,式(i)化合物的x射线粉末衍射图基本上如图1所示。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)处的特定峰。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。
在一些实施例中,在步骤a)中式(vi)化合物或其盐脱羧包含存在碱。在一些实施例中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,碱为三甲胺。在一些实施例中,脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。
在一些实施例中,在步骤b)中酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iva)。在一些实施例中,酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。
在一些实施例中,在步骤c)中环化包含使式(iva)化合物或其盐与碱接触。在一些实施例中,环化使用叔丁醇钾进行。在一些实施例中,环化在2-甲基四氢呋喃中进行。在一些实施例中,环化包含在2-甲基四氢呋喃中用叔丁醇钾处理式(iva)化合物或其盐。在一些实施例中,使式(iii)化合物或其盐进一步酸化并且通过用甲基环己烷沉淀来分离。
在一些实施例中,在步骤d)中卤化包含用卤化剂处理式(iii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。在一些实施例中,卤化剂为dcdmh。
在一些实施例中,在步骤e)中芳构化在合适的溶剂中和任选地在具有添加剂的情况下进行。在一些实施例中,在步骤e)中芳构化在合适的溶剂中进行,所述溶剂为选自由以下组成的组的极性非质子溶剂:二甲基甲酰胺(dmf)、1,3-二甲基-3,4,5,6-四氢-2(1h)-嘧啶酮。在一些实施例中,在步骤e)中芳构化在选自由以下组成的组的溶剂中在添加剂存在下进行:乙腈、甲苯、2-甲基四氢呋喃、乙酸异丙酯、丙酮和甲基异丁基酮。在一些实施例中,芳构化在添加剂存在下在乙腈中进行。在一些实施例中,添加剂为季铵盐。在一些实施例中,季铵盐选自由以下组成的组:四丁基溴化铵、苯甲基三乙基氯化铵、四丁基氯化铵、四乙基氯化铵和四甲基氯化铵。在一些实施例中,季铵盐为四乙基氯化铵。在一些实施例中,芳构化在具有乙基氯化铵的情况下在乙腈中进行。
一些实施例描述式(i)化合物或其盐,其中式(vi)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(i)化合物或其盐,其中式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
iii.水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
在一些实施例中,在步骤i.中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤i.中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。
在一些实施例中,在步骤ii.中添加包含在溴化锂/三乙胺存在下使丙二酸酯与式(viii)化合物或其盐接触。
通过方法c制备的式(i)化合物
一些实施例描述式(i)化合物或其盐或溶剂化物
其通过包含以下的方法制备:
a)加热式(vi)化合物
与催化性三乙胺以形成式(v)化合物
b)加热式(v)化合物与甲醇和含水盐酸以形成式(iva)化合物
c)用叔丁醇钾处理式(iva)化合物以形成式(iii)化合物
d)用1,3-二氯-5,5-二甲基乙内酰脲氯化式(iii)化合物以形成式(iia)化合物
e)加热于乙腈中的式(iia)化合物与四乙基氯化铵以形成式(i)化合物其盐或溶剂化物。
一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法另外包含分离式(iii)化合物。一些实施例描述式(i)化合物,其中方法包含分离式(iia)化合物。一些实施例描述式(i)化合物或其盐或溶剂化物,其中方法另外包含纯化从步骤e)获得的式(i)化合物。在一些实施例中,纯化包含使式(i)结晶。在一些实施例中,式(i)化合物为晶体形式1。在一些实施例中,式(i)化合物为无水晶体。在一些实施例中,式(i)化合物的x射线粉末衍射图基本上如图1所示。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)处的特定峰。在一些实施例中,式(i)化合物处于结晶固态,其特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物。在一些实施例中,式(i)化合物为呈结晶固态形式的乙酸溶剂化物,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,式(i)化合物为呈结晶固态的乙酸溶剂化物,其特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。
一些实施例描述式(i)化合物或其盐,其中式(vi)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(i)化合物或其盐或溶剂化物,其中式(vi)化合物或其盐通过包含以下的方法制备:
i.在于甲醇中的氢氧化钠存在下用反式肉桂醛处理甲基异丁基酮以形成式(viii)化合物
ii.在溴化锂和三乙胺存在下用丙二酸二乙酯处理所述式(viii)化合物以形成式(viia)化合物
iii.用氢氧化钠和乙醇水解式(viia)化合物以形成式(vi)化合物。
通过方法制备的式(vi)化合物
本文一些实施例描述式(vi)化合物或其盐或
其通过包含以下的方法制备:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。
通过方法制备的式(v)化合物
本文一些实施例描述式(v)化合物或其盐
其通过包含以下的方法制备:在碱存在下使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐。在一些实施例中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,碱为三甲胺。在一些实施例中,脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。在一些实施例中,式(vi)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(v)化合物或其盐,其中式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
iii.水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
本文一些实施例描述式(v)化合物或其盐
其通过包含以下的方法制备:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐
d)在碱存在下使式(vi)化合物或其盐脱羧,以形成式(v)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。在一些实施例中,在步骤d)中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,在步骤d)中,碱为三甲胺。在一些实施例中,在步骤d)中脱羧包含在三甲胺存在下加热[2式(vi)化合物或其盐。
通过方法制备的式(iva)化合物
本文一些实施例描述式(iva)化合物或其盐
其通过包含以下的方法制备:酯化式(v)化合物或其盐
以形成式(iva)化合物或其盐。在一些实施例中,酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iva)或其盐。在一些实施例中,酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。一些实施例描述式(iva)化合物或其盐,其中式(v)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(iva)化合物或其盐,其中式(v)化合物或其盐通过包含以下的方法制备:在碱存在下使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐。一些实施例描述式(iva)化合物或其盐,其中式(v)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(iva)化合物或其盐,其中式(v)化合物或其盐通过包含以下的方法制备:在碱存在下使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐。一些实施例描述式(iva)化合物或其盐,其中式(vi)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(iva)化合物或其盐,其中式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
iii.水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
本文一些实施例描述式(iva)化合物或其盐
其通过包含以下的方法制备:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐
d)在碱存在下使式(vi)化合物或其盐脱羧,以形成式(v)化合物或其盐
e)酯化式(v)化合物或其盐以形成式(iva)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。在一些实施例中,在步骤d)中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,在步骤d)中,碱为三甲胺。在一些实施例中,在步骤d)中脱羧包含在三甲胺存在下加热式vi化合物或其盐。在一些实施例中,在步骤e)中酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iva)。在一些实施例中,在步骤e)中酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。
通过方法制备的式(iia)化合物
本文一些实施例描述式(iia)化合物或其盐
其通过包含以下的方法制备:卤化式(iii)化合物或其盐
以形成式(iia)化合物或其盐。在一些实施例中,卤化包含用卤化剂处理式(iii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。一些实施例描述式(iia)化合物或其盐,其中式(iii)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(iia)化合物或其盐,其中式(iii)化合物或其盐通过包含以下的方法制备:环化式(iva)化合物或其盐
以形成式(iii)化合物或其盐。一些实施例描述式(iia)化合物或其盐,其中式(iva)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(iia)化合物或其盐,其中式(iva)化合物或其盐通过包含以下的方法制备:酯化式(v)化合物或其盐
一些实施例描述式(iia)化合物或其盐,其中式(v)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(iia)化合物或其盐,其中式(v)化合物或其盐的化合物通过包含以下的方法制备:在碱存在下使式(vi)化合物或其盐脱羧
以形成式(v)化合物或其盐。一些实施例描述式(iia)化合物或其盐,其中式(vi)化合物或其盐通过本文所描述的任何方法制备。一些实施例描述式(iia)化合物或其盐,其中式(vi)化合物或其盐通过包含以下的方法制备:
i.使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
ii.将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
iii.水解式(viia)化合物或其盐以形成式(vi)化合物或其盐。
本文一些实施例描述式(iia)化合物或其盐
其通过包含以下的方法制备:
a)使反式肉桂醛或其盐与甲基异丁基酮缩合以形成式(viii)化合物或其盐
b)将丙二酸二乙酯添加到式(viii)化合物或其盐中以形成式(viia)化合物或其盐
c)水解式(viia)化合物或其盐以形成式(vi)化合物或其盐
d)在碱存在下使式(vi)化合物或其盐脱羧,以形成式(v)化合物或其盐
e)酯化式(v)化合物或其盐以形成式(iva)化合物或其盐
f)环化式(iva)化合物或其盐以形成式(iii)化合物或其盐
g)卤化式(iii)化合物或其盐以形成式(iia)化合物或其盐。
在一些实施例中,在步骤a)中缩合包含在氢氧化锂、氢氧化钾或氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮,例如缩合在甲醇中使用氢氧化钾或氢氧化钠进行。在一些实施例中,在步骤a)中缩合包含在甲醇中在氢氧化钠存在下用反式肉桂醛或其盐处理甲基异丁基酮。在一些实施例中,在步骤b)中添加包含在溴化锂/三乙胺存在下使丙二酸二乙酯与式(viiia)化合物或其盐接触。在一些实施例中,在步骤d)中,碱选自咪唑、吡啶和二甲基吡啶(2,6-二甲基吡啶)。在一些实施例中,在步骤d)中,碱为三甲胺。在一些实施例中,在步骤d)中脱羧包含在三甲胺存在下加热式(vi)化合物或其盐。在一些实施例中,在步骤e)中酯化式(v)化合物或其盐使用甲醇和盐酸进行,以获得化合物(iva)。在一些实施例中,在步骤e)中酯化包含用含水盐酸在甲醇中处理式(v)化合物或其盐。在一些实施例中,在步骤g)中卤化包含用卤化剂处理式(iii)化合物或其盐。在一些实施例中,卤化剂选自1,3-二氯-5,5-二甲基乙内酰脲(dcdmh);n-氯丁二酰亚胺(ncs);和三氯异氰尿酸(tcca)。在一些实施例中,卤化剂为dcdmh。
化合物
一些实施例描述呈结晶固态形式(形式1)的式(i)化合物,其x射线粉末衍射图基本上如图1所示。在一些实施例中,呈形式1的式(i)化合物特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)处的特定峰。在另一个实施例中,呈形式1的式(i)化合物特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度(所有值±0.1°2θ实验误差)的特定峰。在一些实施例中,式(i)化合物为至少80%形式1。在一些实施例中,式(i)化合物为至少85%形式1。在一些实施例中,式(i)化合物为至少90%形式1。在一些实施例中,式(i)化合物为至少95%形式1。在一些实施例中,式(i)化合物为至少99%形式1。在一些实施例中,式(i)化合物为约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%形式1。
一些实施例描述式(i)化合物的乙酸溶剂化物。在一些实施例中,式(i)化合物的乙酸溶剂化物呈结晶固态形式,其x射线粉末衍射图基本上如图2所示。在另一个实施例中,式(i)化合物的乙酸溶剂化物的特征在于x射线粉末衍射(xrpd)图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在另一个实施例中,式(i)化合物的乙酸溶剂化物的特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度(所有2θ值,±0.1°2θ实验误差)处的特定峰。在一些实施例中,式(i)化合物为至少80%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少85%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少90%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少95%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少99%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%式(i)的乙酸溶剂化物。
所属领域的技术人员应理解,特定形式的式(i)化合物的百分比相对于存在于样品的所有式(i)的形成表示。举例来说,短语“式(i)化合物为至少95%形式1”意指传达存在的式(i)化合物的所有形式的至少95%呈形式1。类似地,短语“式(i)化合物为至少80%式(i)的乙酸溶剂化物”意指式(i)化合物的样品的至少80%呈乙酸溶剂化物的形式。
一些实施例描述式(iia)化合物或其盐
一些实施例描述式(iva)化合物或其盐
一些实施例描述式(v)化合物或其盐
一些实施例描述式(vi)化合物或其盐
药物组合物
本文的实施例描述包含根据本文所描述的任何实施例制备的式(i)化合物或其盐或溶剂化物和药学上可接受的赋形剂的药物组合物。
一些实施例描述包含治疗有效量的形式1的式(i)化合物和药学上可接受的赋形剂的药物组合物。在一些实施例中,形式1的式(i)的组合物的特征在于x射线粉末衍射(xrpd)图具有在15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度2θ(±0.1°2θ)处的特定峰。在一些实施例中,形式1的式(i)化合物的特征在于x射线粉末衍射(xrpd)图具有至少九个,或至少八个,或至少七个,或至少六个,或至少五个,或至少四个,或至少三个选自15.0、17.8、19.1、20.2、21.5、22.4、23.3、24.5、26.2和27.9度2θ(±0.1°2θ)的特定峰。在一些实施例中,式(i)化合物为至少80%形式1。在一些实施例中,式(i)化合物为至少85%形式1。在一些实施例中,式(i)化合物为至少90%形式1。在一些实施例中,式(i)化合物为至少95%形式1。在一些实施例中,式(i)化合物为至少99%形式1。在一些实施例中,式(i)化合物为约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%形式1。
一些实施例描述治疗有效量的式(i)化合物的乙酸溶剂化物和药学上可接受的赋形剂的药物组合物。在一些实施例中,式(i)化合物的乙酸溶剂化物呈结晶固态形式,其x射线粉末衍射图具有在6.7、10.2、11.1、15.4、16.9、17.2和24.8度2θ(±0.1°2θ)处的特定峰。在一些实施例中,式(i)化合物的乙酸溶剂化物的特征在于x射线粉末衍射(xrpd)图具有至少六个,或至少五个,或至少四个,或至少三个选自在6.7、10.2、11.1、15.4、16.9、17.2和24.8度2θ(±0.1°2θ)处的峰的特定峰。在一些实施例中,式(i)化合物为至少80%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少85%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少90%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少95%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为至少99%式(i)的乙酸溶剂化物。在一些实施例中,式(i)化合物为约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%式(i)的乙酸溶剂化物。
一些实施例描述包含式(iia)化合物和药学上可接受的赋形剂的药物组合物。
一些实施例描述包含式(iva)化合物和药学上可接受的赋形剂的药物组合物。
一些实施例描述包含式(v)化合物和药学上可接受的赋形剂的药物组合物。
一些实施例描述包含式(vi)化合物和药学上可接受的赋形剂的药物组合物。
在任何前述药物组合物中,式(i)化合物以治疗有效量存在。
所属领域的技术人员熟悉制备式(i)化合物和其盐和溶剂合物的药物组合物的方法,其描述于《remington:医药科学和实践(remington:thescienceandpracticeofpharmacy)》,第21版2006。
在一些实施例中,通过本文所描述的任何方法制备的式(i)化合物或其盐或溶剂化物纯度为至少80重量%。在一些实施例中,通过本文所描述的任何方法制备的式(i)化合物或其盐或溶剂化物纯度为至少85重量%。在一些实施例中,通过本文所描述的任何方法制备的式(i)化合物或其盐或溶剂化物纯度为至少90重量%。在一些实施例中,通过本文所描述的任何方法制备的式(i)化合物或其盐或溶剂化物纯度为至少95重量%。在一些实施例中,通过本文所描述的任何方法制备的式(i)化合物或其盐或溶剂化物纯度为至少99重量%。在一些实施例中,通过本文所描述的任何方法制备的式(i)化合物或其盐或溶剂化物纯度为约90重量%、约91重量%、约92重量%、约93重量%、约94重量%、约95重量%、约96重量%、约97重量%、约98重量%或约99重量%。
定义
术语“c1-4烷基”意指含有至少一个并且至多四个碳原子的直链或支链烷基。如本文所用,“c1-4烷基”的实例包括但不限于甲基、乙基、正丙基、正丁基、异丁基和异丙基和叔丁基。
本文提及指定式的化合物和“其盐”涵盖作为游离碱或作为其盐的化合物,例如,作为其药学上可接受的盐。关于合适的药学上可接受的盐的综述参见berge等人《药学科学杂志(j.pharm.sci.)》,66:1-19,(1977).
可形成指定式的化合物的“溶剂化物”,其中在结晶期间溶剂分子并入结晶晶格中。溶剂化物可涉及非水溶剂,如乙醇、异丙醇、n,n-二甲亚砜(dmso)、乙酸、乙醇胺和乙酸乙酯,或它们可涉及水作为并入结晶晶格中的溶剂。
如本文所用,“药学上可接受的赋形剂”是指一种或多种药学上可接受的材料、组合物或媒剂,其涉及药物组合物的得到形式或稠度。每种赋形剂当共混时必须与药物组合物的其它成分相容,使得当向患者给药时相互作用将基本上降低式(i)化合物或其药学上可接受的盐的功效。
如本文所用,“基本上如图1所示”或“基本上如图2所示”的x射线粉末衍射图涉及所属领域技术人员认为表示具有与提供的图1或图2的xrpd图相同的晶体形式的化合物的x射线粉末衍射图。所属领域技术人员众所周知并理解,获得x射线粉末衍射图所涉及的采用的设备、湿度、温度、粉末晶体的取向和其它参数可导致在衍射图中线的外观、强度,和位置的一些变化。因此,“基本上如图1所示”或“基本上如图2所示”的x射线粉末衍射图可能不一定示出本文呈现的任何一种衍射图的每条线,和/或可示出由获得数据所涉及的条件不同,导致线的外观、强度或位置的轻微变化。所属领域技术人员能够通过比较其的xrpd图来确定(例如,通过重叠)结晶化合物的样品是否具有与本文公开的形式相同或不同的形式。
在说明书全文和随附权利要求书中,除非上下文另外要求,否则词语“包含(comprise)”和变化形式(如“包含(comprises)”和“包含(comprising)”)应理解成暗示纳入所述整数或步骤或整数或步骤的组,但不排除任何其它整数或步骤或整数或步骤的组。
根据本文所描述的任何实施例的化合物的“治疗有效量”,其药学上可接受的盐或溶剂化物或药物组合物为足以对特定疾病或病症的至少一种症状或参数产生选定作用的量。治疗作用可为客观的(即,可通过一些测试或标记物测量)或主观的(即,受试者给出作用的指示或感觉到作用或医生观测变化)。按需要,本文所涵盖的作用包括医学治疗和/或防治性治疗两者。为了获得治疗和/或防治性效果,根据本公开给药的化合物的特定剂量通过病例周围的具体情况确定,包括例如给药的化合物、给药途径、其它活性成分的共同给药、治疗的状况、采用的特定化合物的活性、采用的特定组合物、患者的年龄、体重、总体健康状况、性别和饮食;给药时间、给药途径和采用的特定化合物的排泄速率以及治疗的持续时间;。给药的治疗有效量将由医生考虑前述相关情况和合理的医学判断确定。根据本文所描述的任何实施例,治疗有效量通常使得当以生理上可耐受的赋形剂组合物给药时,足以实现有效全身浓度或组织中的局部浓度的量。
尽管已参考其某些优选的实施例相当详细地描述本发明,但其它版本是可能的。因此,所附权利要求的精神和范围不应限于本说明书包含的描述和优选的版本。将参考以下非限制性实例说明本发明的各种实施例。以下实例仅出于说明性目的,并且不应理解为以任何方式限制本发明。
如本文所用,在这些方法、方案和实例中使用的符号和惯例与当代科学文献中所使用的那些)一致(例如,《美国化学学会杂志(journaloftheamericanchemicalsociety)》或《生物化学杂志(thejournalofbiologica1chemistry)》。除非另外指出,否则所有起始物质都从商业供应商获得并且不经进一步纯化即使用。具体来说,以下缩写可用于实例和整个说明书中:
缩写
acoh乙酸
apci大气压化学电离
aq含水
ch3cn乙腈
ch3cooh乙酸
ch3oh甲醇
dcdmh1,3-二氯-5,5-二甲基乙内酰脲
dmac二甲基乙酰胺
dmfn,n-二甲基甲酰胺
dmpu1,3-二甲基四氢嘧啶-2(1h)-酮
dmso二甲基亚砜
et乙基
etoh乙醇
equiv当量
hcl盐酸
hrms高分辨质谱
ipr异丙基
koh氢氧化钾
kotbutoxide叔丁醇钾
libr溴化锂
me甲基
2-methf2-甲基四氢呋喃
mhz兆赫
mibk甲基异丁基酮
ms质谱
naoh氢氧化钠
net3三乙胺
nh4cl氯化铵
nmr核磁共振
tbac四丁基氯化铵
tbme叔丁基甲醚
tbu叔丁基
tbuok叔丁醇钾
tcca三氯异氰尿酸
teac四乙基氯化铵
实例
一般实验程序。所有反应均在配备有顶部搅拌器和并且装配有特氟龙隔板的夹套实验室反应器中,在氮气正压下进行。
材料:按原样使用市售溶剂和试剂。
仪器:
除非另外说明,否则质子核磁共振光谱(1hnmr)在25℃下在400mhz下记录。化学位移以四甲基硅烷的低场的百万分之一(ppm,δ标度)表示,并参考在nmr溶剂中的残留质子。数据表示如下:化学位移,多重性(s=单峰,d=双重峰,sep=七重峰,m=多重峰和/或多重共振,br=宽共振),积分,赫兹耦合常数和分配。质子去耦的碳核磁共振光谱(13cnmr)在25℃下在100mhz下记录。化学位移以四甲基硅烷的低场的百万分之一(ppm,6标度)表示,并参考溶剂的碳共振。使用orbitrap质量分析仪获得高分辨率质谱(hrms)。
在panalyticalx′pertpro粉末衍射仪,型号pw3050/60上,使用x′celerator检测器获得x射线粉末衍射(xrpd)数据。采集条件为:辐射:cukα,高压发电机:45kv,发电机电流:40ma,步长:0.017°2θ,每步时间:500秒,发散狭缝类型:固定,发散狭缝大小:0.4354°,测量温度:20℃-25℃,测角计半径:240mm。通过将样品装在0.9mm毛细管或零背景硅酮样品架中来制备样品。使用panalyticalx′perthighscoreplus软件获得峰位置。对于每个峰值分配,误差容限为约±0.1°2θ。
实例1
合成(5e,7e)-2-甲基-8-苯基辛-5,7-二烯-4-酮,(式(viii)化合物))
在-5℃下在1小时内将氢氧化钠(11.4g,284mmol,1.5当量)于甲醇(100ml)中的溶液逐滴添加到肉桂醛(式(ix)化合物)(25g,189mmol,1当量)和甲基异丁基酮(75ml,602mmol,3.2当量)的搅拌溶液中。一旦完成添加,将反应混合物在0℃下搅拌2小时。然后在0℃下将甲苯(250ml)和水(125ml)直接添加到反应器中,并且使搅拌的两相混合物升温到20℃。去除水层,并且用水(2×75ml)洗涤有机层。然后洗涤的有机层在真空下经由共沸蒸馏干燥到最终溶液体积为75ml或直到经由karlfischer滴定分析显示水含量小于0.2%。粗材料不经任何进一步处理即用于下一转化。
实例2
合成(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二叔丁酯,(式vii化合物,其中r1+r2=tbu)
在先前步骤(实例1)中获得的浓缩的溶液用甲苯稀释,使得溶液的总体积为175ml。然后在20℃下将丙二酸二叔丁酯(40.3ml,180mmol,0.95当量)、三乙胺(13.1ml,94.5mmol,0.5当量)和粉末溴化锂(3.28g,37.8mmol,0.2当量)添加到(5e,7e)-2-甲基-8-苯基辛-5,7-二烯-4-酮(式(viii)化合物)于甲苯中的溶液中。将非均相反应混合物在20℃下搅拌2小时。然后将水(200ml)直接装入搅拌的反应混合物中。使层分离并且丢弃水层。所得产物溶液不经任何进一步处理即用于下一转化。替代地,丙二酸二叔丁基酯加成产物(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二叔丁酯(式(vii)化合物)还可经由浓缩甲苯溶液并且从异丙醇/水(3∶2)结晶来分离,以提供呈淡黄色固体的(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二叔丁酯(式(vii)化合物)。
1hnmr(400mhz,dmso)δ7.32-7.29(m,4h),7.24-7.18(m,1h),6.38(d,1h,j=16hz),6.12(dd,1h,j=16,8.4hz),3.39(d,ih,j=8.4hz),3.27-3.20(m,1h),2.70(dd,1h,j=16.8,9.2hz),2.58(dd,1h,j=16.8,4.4hz),2.28(d,2h,j=7.2hz),1.98(sep,1h,j=6.8hz),1.39(s,9h),1.33(s,9h),0.81(d,3h,j=6.4hz),0.80(d,3h,j=6.4hz)。
13cnmr(100mhz,dmso)δ208.2(c),167.0(c),166.8(c),136.7(c),131.2(ch),129.1(ch),128.6(ch),127.3(ch),125.9(ch),81.2(c),80.9(c),56.8(ch),51.4(ch2),45.0(ch2),37.7(ch),27.5(ch3),27.4(ch3),23.9(ch),22.3(ch3),22.2(ch3)。
c26h39o5的hrms-apci(m/z)[m+h]+计算值,431.2792;实测值,431.2754。
实例3
合成(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二乙酯(式viia化合物)
浓缩的(5e,7e)-2-甲基-8-苯基辛-5,7-二烯-4-酮(约7.6摩尔)的溶液用甲苯稀释。然后在20℃下将丙二酸二乙酯(1.83kg,1.73l,1.5当量)、三乙胺(1.15kg,1.58l,1.5当量)和粉末溴化锂(131g,0.2当量)添加到(5e,7e)-2-甲基-8-苯基辛-5,7-二烯-4-酮(式(viii)化合物)于甲苯中的溶液中。将非均相反应混合物在35℃-40℃下搅拌至少8小时。然后将水(8l,8体积)直接装入搅拌的反应混合物中,并在35℃下搅拌15-30分钟。使层分离并且弃去水层。所得产物溶液不经任何进一步处理即用于下一转化。替代地,丙二酸二乙酯加成产物(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二乙酯(式(viia)化合物)还可经由浓缩甲苯溶液并且结晶来分离,以提供(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二乙酯(式(viia)化合物)。
1hnmr(700mhz,dmso)67.30(m,2h),7.30(m,sh0,7.21(m,1h),6.39(d,1h)j=15.8hz),6.14(dd,1h,j=15.99hz,j=8.9hz),4.12(q,2h,j=7.13hz),4.06(m,2h),3.68(d,1h,j=8.1hz),3.33(m,1h),2.73(dd,1h,j=16.9hz,j=9.0hz),2.63(m,1h,),2.28(d,2h,6.9hz),1.98(m,1h,6.7hz),1.16(t,3h,j=7.1hz),1.10(t,3h,j=7.0hz),0.81(d,3h,j=6.6hz),0.80(d,3h,j=6.7hz)。
13cnmr(176mhz,dmso)δ208.1(c),167.7(c),167.6(c),136.6(c),131.4(ch),128.9(ch),127.4(ch),125.9(ch),61.0(ch2),60.8(ch2),55.0(ch),51.3(ch2),44.8(ch2),37.7(ch),23.8(ch),22.3(ch3),22.2(ch3),13.9(ch3),13.9(ch3)。
c22h31o5的hrms-apci(m/z)[m+h]+计算值,375.2166;实测值,375.2158。
实例4
合成(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸(式(vi)化合物)
方法a
在先前步骤中获得的(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二叔丁酯(式(vii)化合物)的甲苯溶液用乙酸(50ml)稀释,并且在60℃下在1小时内逐滴添加到由乙酸(100ml)和浓含水盐酸(75ml)组成的搅拌溶液中。一旦完成添加,将所得溶液在60℃下搅拌4小时。使产物混合物在30分钟内冷却到20℃并且添加水(200ml)。在20℃下剧烈搅拌两层,并且然后使沉降。然后丢弃水层,并将甲苯层浓缩到干燥。将甲苯(250ml)添加到所得油中,并且在搅拌下将溶液加热到60℃。然后将温甲苯溶液在1小时内缓慢冷却到20℃,此时从溶液沉淀(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸(式(vi)化合物)。然后过滤固体并且用甲苯(100ml)洗涤湿滤饼。然后将湿滤饼在30℃下真空干燥12小时,以得到呈白色结晶固体的(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸(式(vi)化合物)(37.3g,62%来自肉桂醛(式(ix)化合物)。
方法b
在20℃-30℃下将来自实例3的(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸二乙酯(约7.6摩尔,式(viia)化合物)的甲苯溶液装入6m含水氢氧化钠(5.05l,4当量)、甲苯(0.5l或0.5体积)和200标准酒精度乙醇(2体积),并且将内容物在tj=20℃下搅拌至少4h。一旦完成,将温度调节到35℃-50℃并在搅拌至少30分钟之后停止搅动,并且分离各层。将水层冷却到0-5℃,并且用浓hcl将ph调节到ph为0-1(需要2.9l或4.7当量),同时在添加期间将温度维持在10℃或更低。一旦达到所需的ph,容器装入tbme(3l,3体积),并且使两相混合物升温到20℃-25℃。将混合物搅拌15-30分钟,并分离各层。将甲苯(7l,7体积)和水(6l,6体积)添加到有机层中,并且将混合物搅拌15-30分钟。分离各层,并且添加甲苯以实现16-18体积(3l,3体积)的填充。使用真空蒸馏将混合物蒸馏降至约9-9.5体积,将温度调节到40℃-45℃,并且用5g化合物vi(相对于理论产量0.2%w/w)接种混合物。将混合物在40℃-45℃下搅拌30-60分钟。一旦观察到成核,将混合物用甲苯稀释到12体积,并在40℃-45℃下保持至少1小时。将浆液以0.5℃/min冷却到10℃-20℃,并在10℃-20℃下保持至少1小时。通过过滤分离固体,并且用甲苯(2×7体积)洗涤滤饼。固体在真空烘箱中在25℃-35下干燥过夜,以得到(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸(式(vi)化合物)
1hnmr(400mhz,dmso)δ12.78(brs,2h),7.32-7.27(m,4h),7.23-7.19(m,1h),6.39(d,1h,j=16hz),6.17(dd,1h,j=16,8.4hz),3.43(d,1h,j=8.4hz),3.31-3.24(m,1h),2.72(dd,1h,j=16.8,8.8hz),2.63(dd,1h,j=16.4,4hz),2.28(d,2h,j=7.2hz),1.98(sep,1h,j=6.8hz),0.81(d,3h,j=6.4hz),0.80(d,3h,j=6.4hz)。
13cnmr(100mhz,dmso)δ208.4(c),169.6(c),169.5(c),136.8(c),130.9(ch),129.6(ch),128.5(ch),127.3(ch),126.0(ch),55.7(ch),51.4(ch2),45.1(ch2),37.6(ch),23.9(ch),22.3(ch3),22.2(ch3)。
c18h23o5的hrms-apci(m/z)[m+h]+计算值,319.1540;实测值,319.1528。
实例5
合成(e)-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iii)化合物)
将三乙胺(4.4ml,31.4mmol,0.25当量)装入(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸(式(vi)化合物)(40.0g,126mmol,1当量)于甲苯(210ml)的搅拌浆液。将所得混合物加热到110℃并且使其搅拌2小时。然后使含有未分离的中间体(e)-7-甲基-5-氧代-3-苯乙烯基辛酸(式v化合物)的反应混合物冷却到20℃,并且装入甲醇(120ml)和浓含水盐酸(10.5ml)。将所得溶液在60℃下搅拌4小时。使含有未分离的中间体(e)-7-甲基-5-氧代-3-苯乙烯基辛酸甲酯(式(iva)化合物)的所得混合物冷却到20℃并用水(200ml)洗涤。然后将洗涤的有机层经由真空蒸馏干燥到最终溶液体积为120ml。然后将甲酯(e)-7-甲基-5-氧代-3-苯乙烯基辛酸甲酯(式iva化合物)的溶液冷却到0℃。然后在1小时内将叔丁醇钾(19.7g,176mmol,1.4当量)于2-甲基四氢呋喃(80ml)中的溶液逐滴添加到(e)-7-甲基-5-氧代-3-苯乙烯基辛酸甲酯(式(iva)化合物)的冷却溶液中。一旦完成添加,在30分钟内反应混合物升温到20℃。将升温的溶液在20℃下搅拌1小时。然后将所得产物混合物装入1.0m含水盐酸(180ml),并且将两相混合物搅拌10分钟。然后丢弃水层,有机层用10%含水氯化钠(2×160ml)洗涤。然后在1小时内将甲基环己烷(400ml)逐滴添加到(e)-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iii)化合物)的溶液中,此时产物开始沉淀出来。然后过滤浆液并且用甲基环己烷(120ml)洗涤湿滤饼。然后将湿滤饼在30℃下真空干燥12小时,以提供呈白色结晶固体的(e)-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iii)化合物)(25.3g,79%来自(e)-2-(7-甲基-5-氧代-1-苯基辛-1-烯-3-基)丙二酸,(式(vi)化合物)。
1hnmr(400mhz,dmso)δ10.33(brs,1h,oh),7.39-7.37(m,2h),7.34-7.29(m,2h),7.24-7.20(m,1h),6.43(d,1h,j=16hz),6.27(dd,1h,j=16,7.2hz),3.08(sep,1h,j=7.2hz),2.87-2.78(m,1h),2.40(br,4h),1.08(d,6h,j=7.2hz)。
13cnmr(100mhz,dmso)6136.8(c),132.5(ch),128.9(ch),128.6(ch),127.3(ch),126.0(ch),119.2(c),36.1(ch),22.6(ch),20.4(ch3),其它碳进行烯醇互变异构。
c17h21o2的hrms-apci(m/z)[m+h]+计算值,257.1536;实测值,257.1519。
实例6
合成(e)-2-氯-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iia)化合物)
1-l夹套实验室反应器装入(e)-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iii)化合物)(55g,215mmol,1当量)和甲醇(495ml),产生非均相悬浮液。将混合物加热到内部温度为的~45℃-50℃,此时实现均匀溶液。依次将五等份固体1,3-二氯-5,5-二甲基乙内酰脲(23.3g,118mmol,0.55当量)装入此溶液。然后在10分钟内将产物溶液冷却到40℃,并且接种146mg(e)-2-氯-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iia)化合物)。混合物老化30分钟然后在60分钟内冷却到23℃。然后将水(330ml)在1小时内逐滴添加到浆液中,并且将混合物在20℃下搅拌30分钟。然后过滤浆液,并且用1∶1甲醇/水(2×110ml)洗涤湿滤饼。然后将湿滤饼在45℃下真空干燥12小时,以提供呈白色结晶固体的(e)-2-氯-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iia)化合物),其以~2∶1非对映异构体的混合物(60.0克,96%)存在。
异构体1:
1hnmr(400mhz,dmso)δ7.41-7.39(m,2h),7.36-7.32(m,2h),7.23-7.22(m,1h),6.54(d,1h,j=16hz),6.32(dd,1h,j=16,7.2hz),3.20-3.14(m,3h),2.84-2.77(m,1h),2.73-2.72(m,1h),2.70-2.69(m,1h),0.82(d,6h,j=6.8hz)。
13cnmr(100mhz,dmso)δ198.5(c),136.5(c),130.4(ch),129.9(ch),128.6(ch),127.5(ch),126.1(ch),94.6(c),43.4(ch2),35.0(ch),32.8(ch),16.7(ch3)。
异构体2:
1hnmr(400mhz,dmso)δ7.33-7.28(m,4h),7.25-7.21(m,2h),6.35(dd,1h,j=16,2hz),6.03(dd,1h,j=16,5.6hz),3.48(dd,1h,j=14.8,6hz),3.24-3.18(m,1h),3.10(sep,1h,j=6.4hz),2.86(dd,1h,j=14.8,3.6hz),0.83(d,6h,j=6.4hz)。
13cnmr(100mhz,dmso)δ199.6(c),136.1(c),130.3(ch),130.1(ch),128.6(ch),127.7(ch),126.1(ch),94.5(c),42.2(ch2),34.7(ch),30.9(ch),16.9(ch3)。
c17h20clo2的hrms-apci(m/z)[m+h]+计算值,291.1146;实测值,291.1132。
实例7
合成(e)-2-异丙基-5-苯乙烯基苯-1,3-二醇(式(i)化合物)
夹套实验室为装入(e)-2-氯-2-异丙基-5-苯乙烯基环己烷-1,3-二酮(式(iia)化合物)(407g,1.4mol,1当量)、四乙基氯化铵(464g,2.8mol,2当量)和乙腈(1.2l)。将混合物加热到75℃-80℃持续6小时。然后在30分钟内将产物混合物冷却到20℃并且用叔丁基甲醚(3.26l)稀释。所得溶液用水(每次洗涤2l)洗涤四次。将所得溶液浓缩到体积~610ml。装入乙酸(815m1)并且将溶液减压浓缩到体积~1.3l。将所得浆液加热到55℃直到均匀,然后在1小时的过程中缓慢冷却到35℃,在此时间期间产物开始沉淀。在2小时的过程中将甲基环己烷(6.5l)添加到浆液中。一旦完成添加,混合物在一小时内另外冷却到~23℃。过滤固体并且用6∶1甲基环己烷/acoh洗涤两次。然后将分离的固体在80℃下真空干燥24小时,以提供呈白色结晶固体的(e)-2-异丙基-5-苯乙烯基苯-1,3-二醇(式(i)化合物)(305g,86%)。
1hnmr(400mhz,dmso)δ9.05(s,2h,oh),7.58-7.55(m,2h),7.37-7.33(m,2h),7.27-7.22(m,1h),7.00(d,1h,j=16.4hz),6.87(d,1h,j=16.4hz),6.47(s,2h),3.43(sep,1h,j=7.2hz),1.24(d,6h,j=7.2hz)。
13cnmr(100mhz,dmso)δ156.4(c),137.0(c),134.7(c),128.9(ch),128.7(ch),127.4(ch),126.7(ch),126.3(ch),120.1(c),105.1(ch),23.7(ch),20.6(ch3)。
c17h19o2的hrms-apci(m/z)[m+h]+计算值为255.1380;实测值为255.1376。
- 还没有人留言评论。精彩留言会获得点赞!