用于心房间吻合的经导管装置的制作方法
相关申请的交叉引用
本申请要求于2017年11月30日提交的美国临时专利申请号62/592,630和于2018年8月8日提交的美国临时专利申请号62/715,922的优先权,其中每个专利申请的全文都通过引用结合在本文中。
背景技术:
充血性心力衰竭(chf)是一种慢性病,影响了美国600万人和全球2300万人。预计在未来10年,发病率将上升,并且美国每年将诊断出65万个新病例。心力衰竭是美国65岁以上患者入院的最常见原因,每年约有100万人住院,而且这一数字还将大幅上升。因此,心力衰竭仍然是主要的流行病,并且伴随着显著的医疗费用。
技术实现要素:
在一些实施例中,本文描述了在哺乳动物的心脏的右心房和左心房之间生成特定尺寸/规定的孔以释放升高的左心房压力的装置组件和方法。在一些实施例中,本文公开了经导管房间隔切除装置组件和方法,其构造成在心脏的右心房和左心房之间生成一定尺寸的心房间孔,以释放升高的左心房压力。在一些实施例中,本文公开了用于治疗诸如充血性心力衰竭的心力衰竭的装置组件。在一些实施例中,本文公开了用于使用基于能量的组织切割器来实现组织切除的心房间吻合的装置组件和方法。在一些实施例中,能量是在射频(rf)频谱的范围内。在一些实施例中,能量具有任何一个或多个电磁波频率(例如红外频率)。在一些实施例中,能量是热能和/或激光能。在一些实施例中,与传统的机械组织切割相比,这种基于能量的组织切割器有利地便于更有效、准确、可控的组织切割,从而极大地简化了手术过程,并且提高了心房间吻合的成功率。
概述
在一些实施例中,本文公开的装置组件包括输送导管、组织稳定器(或本文等同地,组织保持元件)、可扩张组织切割器(或本文等同地,组织切割器)中的一个或多个,该组织稳定器附装至组织稳定器导管(或本文等同地,组织保持导管),该组织稳定器导管具有允许导丝通过的腔和穿透末端,该可扩张组织切割器附装至组织切割器导管(或本文等同地,组织切割器导管),该组织切割器导管具有允许组织稳定器导管通过的另一腔。在一些实施例中,本文公开的装置组件包括一个或多个(第三)导管,该导管具有允许本文中的一个或多个部件通过以进出右心房的中心腔。在一些实施例中,组织稳定器导管具有腔,该腔允许具有穿透末端的附加扩张器导管通过,该扩张器导管具有允许导丝通过的另一腔。在一些实施例中,组织稳定器导管具有允许组织切割器导管通过的腔,并且组织切割器导管具有允许扩张器导管或导丝通过的另一腔。在一些实施例中,组织稳定器导管的末端穿透组织,使得其腔允许导丝通过。
在一些实施例中,本文公开了包括导丝的装置组件,该导丝是装置组件的一部分,或者是能够使用该装置组件的单独的“现成的”部件。
在一些实施例中,本文公开的装置组件包括引导导管(导管1),该引导导管具有预弯曲的形状、可转向性或可偏转性,以使组件的其他部件相对于房间隔以基本上垂直的角度取向。在一些实施例中,引导导管起到约束和输送组织稳定器的作用。在一些实施例中,不需要这种引导导管。
在一些实施例中,本文公开的装置组件包括组织稳定器,其附装至导丝、引导导管(导管1)、组织稳定器导管(导管2)或组织切割器导管(导管3),并且具有第一直径的收缩状态和更大的第二直径的展开状态;该部件用作用于组织保持或稳定的机构,以确保切除的组织被装置保持。在一些实施例中,射频(rf)阴极或阳极结合到组织稳定器中,而rf阴极或阳极中的另一个结合到装置组件的其他元件中,或者在装置组件外部但与哺乳动物的身体接触。
在一些实施例中,本文公开的装置组件包括附装到导管(导管3,等同于“组织切割器导管”)的组织切割器(或等同地,组织切割器),该组织切割器由导电材料制成,并且通过导线连接至rf发生器。
在一些实施例中,本文公开的装置组件包括rf能量源或rf阴极。在一些实施例中,rf阴极或rf源结合在组织切割器中。
在一些实施例中,本文公开的装置组件包括rf能量阱(rf阳极或rf回路),以将来自rf阴极的rf能量吸出体外,由此限定rf能量传输的场。在一些实施例中,rf能量阱放置在体内并且连接至离开身体并返回rf发生器的导线,或者是放置在身体表面上并且连接至返回rf发生器的导线的垫片。在一些实施例中,rf阴极或阳极结合在组织稳定器中。
在一些实施例中,本文公开的装置组件包括输送导管(导管4),其在展开之前容纳所有其他装置部件及其相应的导管。
在一些实施例中,本文公开的装置组件包括rf发生器,其位于无菌场外部,并且通过无菌连接器连接至rf阳极和阴极,该无菌连接器穿过无菌场并且分别从或向rf阳极和阴极输送rf能量。
在一些实施例中,本文公开了用于哺乳动物的心房间吻合以治疗充血性心力衰竭的装置组件,该装置组件包括:输送导管,该输送导管具有输送腔,并且可转向或可弯曲;射频(rf)发生器,该rf发生器定位成远离输送导管;和封装在输送腔内的可扩张组织切割器,该可扩张组织切割器附装至组织切割器导管,并且构造成在处于该输送腔外部时扩张,其中,可扩张组织切割器电连接至rf发生器,组织切割器导管与输送导管同轴,并且可以在其中滑动,组织切割器导管包括第一腔。在一些实施例中,可扩张组织切割器包括一种或多种导电材料。在一些实施例中,可扩张组织切割器通过导线连接至rf发生器。
在一些实施例中,本文公开了用于哺乳动物的心房间吻合以治疗充血性心力衰竭的装置组件,该装置组件包括:输送导管,该输送导管具有输送腔,并且可转向或可弯曲;射频(rf)发生器,该rf发生器定位成远离输送导管。
在一些实施例中,本文公开了一种封装在输送腔内的可扩张组织切割器,该可扩张组织切割器附装至组织切割器导管,并且构造成在处于输送腔外部时扩张,其中,可扩张切割器电连接至rf发生器,组织切割器导管与输送导管同轴,并且可以在其中滑动,组织切割器导管包括第一腔;和封装在输送腔内的可扩张组织稳定器,该可扩张组织稳定器在远端处或远端附近附装至组织稳定器导管,并且构造成在处于输送导管或组织切割器导管外部时扩张,该组织稳定器导管与第一腔同轴,并且可以在第一腔中滑动,组织稳定器导管包括第二腔。在一些实施例中,组织切割器导管与组织稳定器导管的第二腔同轴,并且可以在其中滑动,可扩张组织切割器构造成在处于组织稳定器导管的输送导管外部时扩张。
在一些实施例中,本文公开了一种装置组件,用于在哺乳动物的心脏的右心房和左心房之间的间隔中产生确定尺寸的孔以治疗充血性心力衰竭,该装置组件包括:a)输送导管,该输送导管具有输送腔;b)到射频(rf)发生器的第一连接器和第二连接器;该rf发生器定位成远离输送导管;c)封装在输送腔内的可扩张组织切割器,该可扩张组织切割器附装至组织切割器导管,该组织切割器包括在处于输送腔外部时的扩张构型,其中,可扩张组织切割器包括电联接至用于rf发生器的第一连接器的阴极,组织切割器导管与输送导管同轴,并且可以在其中滑动;和d)封装在输送腔内的可扩张组织稳定器,该可扩张组织稳定器附装至组织稳定器导管,并且与组织切割器导管相邻,其中,可扩张组织稳定器包括在处于输送腔外部时的扩张构型,组织稳定器导管与输送导管同轴,并且可以在其中滑动;其中,组织切割器导管在输送导管中位于组织稳定器导管的远侧。在一些实施例中,可扩张组织切割器包括一种或多种导电材料。在一些实施例中,可扩张组织切割器可以通过导线连接至用于rf发生器的第一连接器。在一些实施例中,导线至少部分地在组织切割器导管的壁中,或者至少部分地沿着组织切割器导管。在一些实施例中,可扩张组织切割器包括rf阴极。在一些实施例中,装置组件还包括可以连接至rf发生器的第二连接器的rf皮肤贴片阳极。在一些实施例中,可扩张组织稳定器包括rf阳极。在一些实施例中,rf发生器产生rf能量,该rf能量从rf阴极穿过哺乳动物的组织到达rf阳极。在一些实施例中,rf阴极与哺乳动物的身体接触。在一些实施例中,rf阳极与rf阴极之间的距离在约1毫米至约2米的范围内。在一些实施例中,可扩张组织切割器包括rf阳极。在一些实施例中,rf发生器产生rf能量,该rf能量从rf阴极穿过哺乳动物的组织到达rf阳极。在一些实施例中,rf阳极与rf阴极之间的距离在约1毫米至约2米的范围内。在一些实施例中,rf阴极是环形电极。在一些实施例中,rf阳极是环形。在一些实施例中,装置组件还包括引导导管、扩张器导管、扩张器腔(以允许在导丝上平移)、包括腔的远端扩张器轴、与引导导管同轴的扩张器末端、组织稳定器支柱和组织切割器支柱。在一些实施例中,rf发生器产生交流频率在约300khz至约3mhz的范围内或者功率在约1瓦至约500瓦的第二范围内的交流电。在一些实施例中,可扩张组织切割器和可扩张组织稳定器包括超弹性形状记忆合金。在一些实施例中,当在组织切割器导管外部展开和释放时,可扩张组织切割器具有大体上平面环状的构型。在一些实施例中,当在组织稳定器导管外部展开和释放时,可扩张组织稳定器具有大体上平面环状的构型。在一些实施例中,可扩张组织切割器的切割部分的扩张的横截面轮廓包括非圆形的横截面轮廓,例如椭圆形、三角形、正方形、六边形、八边形或其他多边形。在一些实施例中,可扩张组织稳定器的稳定部分的扩张的横截面轮廓包括非圆形的横截面轮廓,例如椭圆形、三角形、正方形、六边形、八边形或其他多边形。在一些实施例中,可扩张组织切割器的大致为平面的切割部分在最宽尺寸处的扩张尺寸在4.0mm至12.0mm之间。在一些实施例中,可扩张组织稳定器的大体上平面的接触部分在最宽尺寸处的扩张尺寸在5.0mm至18.0mm之间。在一些实施例中,可扩张组织切割器的切割尺寸可调节。在一些实施例中,可扩张组织稳定器的接触部分的尺寸可调节。在一些实施例中,可扩张组织切割器和可扩张组织稳定器包括一种或多种导电材料。
在一些实施例中,本文公开了一种操作装置组件以在哺乳动物的心脏的右心房和左心房之间的间隔中产生确定尺寸的孔,以用于治疗充血性心力衰竭的方法,该方法包括:a)将装置组件靠近房间隔的中心输送至心脏的右心房,该装置组件包括:输送导管,该输送导管具有输送腔;具有远端扩张器末端的远端扩张器导管;到射频(rf)发生器的第一连接器和第二连接器;该rf发生器定位成远离输送导管;封装在输送腔内的可扩张组织切割器,该可扩张组织切割器附装至组织切割器导管,其中,可扩张组织切割器包括电联接至用于rf发生器的第一连接器的阴极,组织切割器导管与输送导管同轴,并且可以在其中滑动;和封装在输送腔内的可扩张组织稳定器,该可扩张组织稳定器附装至组织稳定器导管,并且与组织切割器导管相邻,组织稳定器导管与输送导管同轴,并且可以在其中滑动,其中,组织切割器导管在输送导管中位于组织稳定器导管的远侧;b)将组件的远端扩张器末端推进穿过房间隔,使得远端扩张器导管位于左心房中,而输送导管的剩下的一半位于右心房中;c)相对于所有其他部件推进远端扩张器导管,以使可扩张组织切割器、支撑支柱和组织切割器阴极脱鞘和展开、完全扩张和锁定就位;d)向近侧抽回组织切割器导管,使得可扩张组织切割器的组织切割器阴极与间隔的左心房表面接触;e)相对于所有其他装置部件收回组织稳定器导管,以使组织稳定器、支撑支柱和组织稳定器的稳定部分在右心房中脱鞘、展开、完全扩张和锁定就位;f)向近侧推进展开的组织稳定器,使得组织稳定器的稳定部分与间隔的右心房表面(与可扩张组织切割器的组织切割器阴极相对)接触;g)在哺乳动物的表面上设置阳极,该阳极包括连接器以电联接至用于rf发生器的第二连接器;h)将阴极联接至用于rf发生器的第一连接器;i)将阳极联接至用于rf发生器的第二连接器;j)使用rf发生器向阴极通电,使得组织切割器切下一块组织以在房间隔中形成吻合部;k)将切除的组织块、组织切割器、组织稳定器和一部分远端扩张器导管向近侧收回到右心房中;l)向远侧推进组织切割器导管和远端扩张器导管,使得切除的组织块在组织切割器的支柱内收缩;m)将切除的组织块和组织切割器的端部捕获在由组织稳定器支柱和组织稳定器的稳定部分构成的笼中,并且向近侧首先抽回到所述组织稳定器导管中,然后抽回到所述输送导管中;和n)将装置从间隔和心房完全抽出。
在一些实施例中,本文公开了使用经导管装置组件切除哺乳动物的房间隔,以治疗充血性心力衰竭的方法,该方法包括:使可扩张组织切割器在导丝上前进并穿过房间隔到达左心房,该可扩张组织切割器处于压缩状态;扩张并移动组织切割器,以在左心房中向房间隔提供张力;将组织切割器平移至与房间隔接触;在rf阴极和rf阳极之间将rf功率传输穿过房间隔,从而产生孔,其中,rf阴极或rf阳极位于可扩张组织切割器上,而rf阴极或rf阳极中的另一个位于输送导管上或与哺乳动物的组织接触;以及使可扩张组织切割器与切下的房间隔一起重新入鞘到输送导管中。在一些实施例中,可扩张组织稳定器在房间隔的相对侧上展开,以在将rf功率传输穿过房间隔从而产生一个孔之前提供组织稳定。
在一些实施例中,本文公开了使用经导管装置组件切除房间隔以治疗充血性心力衰竭的方法,该方法包括:穿刺房间隔的卵圆窝,并将导丝推进至左心房;在导丝上推进可扩张组织稳定器并使其穿过房间隔,该可扩张组织稳定器处于压缩状态;展开和移动组织稳定器,以在左心房中向房间隔提供张力;将可扩张组织切割器输送至右心房,该可扩张组织切割器处于容纳在装置组件的输送导管中的第二压缩状态;使可扩张组织切割器在右心房中扩张;使切割器向前平移,以与房间隔接触,从而将房间隔夹在可扩张组织切割器和可扩张组织稳定器之间;在rf阴极和rf阳极之间将rf功率传输穿过房间隔,从而产生孔,其中,rf阴极或rf阳极位于可扩张组织稳定器上;以及使可扩张组织切割器和可扩张组织稳定器与切下的房间隔一起重新入鞘到输送导管中。
附图说明
特别地在随附权利要求书中阐述了本文的装置组件的新颖性特征。通过参考下文阐述说明性实施例的详细说明和附图,可以更好地理解本公开的特征和优点,在这些说明性实施例中利用了本文的装置组件的原理,并且图中:
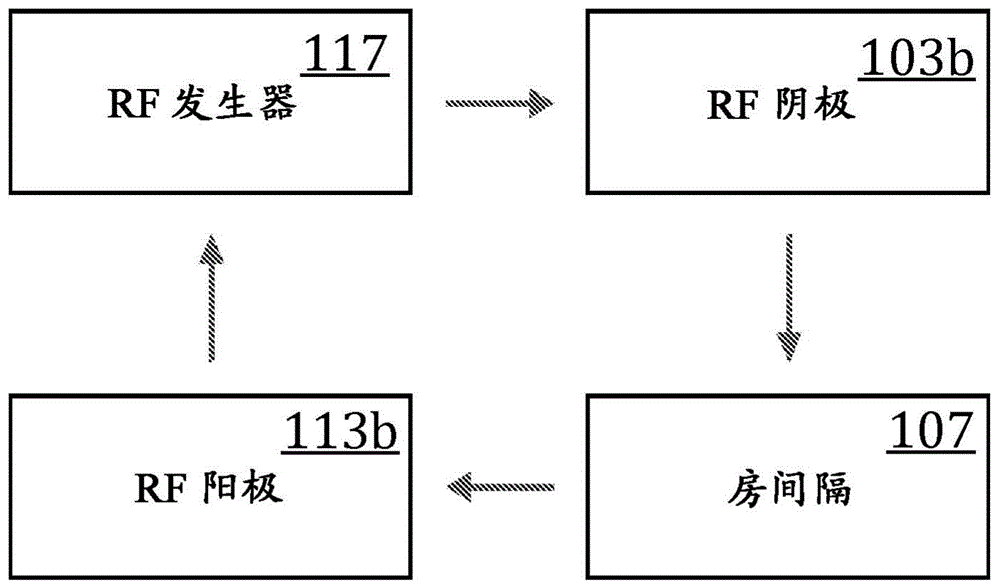
图1是用于心房间吻合的基于rf能量的装置组件的示例性实施例的示意图;在这种情况下,是装置组件的rf发生器、阴极和阳极;
图2是用于心房间吻合的基于rf能量的装置组件的示例性实施例的图示;
图3a-3c示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图4a-4d示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图5a-5d示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图6a-6b示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图7a-7b示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;装置组件的组织稳定器;组织切割器的细网筛,以便于在切割后将切除的组织保持在装置组件中;组织稳定器的细网筛,以便于在切割后将切除的组织保持在装置组件中;扩张器末端,以便于装置组件穿过房间隔;
图8示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图9a-9c示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图10a-10d示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图11示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图12a-12b示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图13a-13b示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图14a-14b示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图15a-15d示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的rf阴极和阳极;
图16a-16b示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图17a-17d示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;
图18a-18c示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图19a-19b示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图20a-20d示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图21示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图22示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;和
图23a-23c示出了用于心房间吻合的基于rf能量的装置组件的示例性实施例;在这种情况下,是装置组件的组织切割器;
图24a-24b示出了用于心房间吻合的另一基于rf能量的装置组件的实施例的示例性侧视图和透视图;
图24c示出了图24a的用于心房间吻合的基于rf能量的装置组件的实施例的示例性端视图;
图25a示出了图24a的rf烧灼电极元件的示例性实施例;
图25b示出了图24a的rf烧灼电极元件的示例性实施例,其中,电极具有次级网格结构,以在其扩张状态下增加结构刚度;
图26示出了图24a的组织稳定器元件的示例性实施例;
图27a-27f示出了图24a的基于rf能量的装置组件的示例性实施例,以及用于心房间吻合的顺序展开方法和操作;
图28a-28k示出了图24a的基于rf能量的装置组件的示例性实施例,以及用于心房间吻合的顺序展开方法、手术方法、切除组织捕获和装置收回。
具体实施方式
chf的特征是心肌功能下降,这是由于其泵送能力减弱,称为射血分数降低的心力衰竭(hfref),或者由于肌肉在射血之前充血能力降低的僵硬,称为射血分数保留的心力衰竭(hfpef)。心脏无法喷血或充血会导致呼吸急促、疲劳和明显的功能受限症状。尽管hfpef的上升速度比hfref更快,但是hfref和hfpef的患病率大致相等。当从心脏到重要器官的血液流动不畅时,肾素-血管紧张素-醛固酮系统(raas)被激活,向身体发出信号以保持流体,从而增加心室中的压力。特别地,随着左心房压力(lap)升高,液体回流到肺循环中,导致肺水肿和严重的呼吸急促。虽然正常成年人的lap在10-15mmhg的范围内,但是心力衰竭的患者的lap经常在30-40mmhg的范围内,在一些实施例中,该lap在心脏需求增加时达到峰值。
现有的心力衰竭药物治疗试图通过肾脏排泄(利尿剂)、神经激素阻滞或外周血管扩张来清除体内多余的液体,以减轻衰竭心脏的压力负荷。这些药物治疗缓解了一些症状,并且在治疗hfref方面显示出微小的死亡率优势,但重要的是,尚未显示出改善hfpef患者的生存率。
心力衰竭的基于装置的疗法有限。在机械辅助循环中,电动泵被通过外科手术植入并承担衰竭心脏的功能,该机械辅助循环具有高度侵入性,并且保留在疾病的晚期进行。经皮机械泵用于急性治疗,但是仅允许短期使用。同样,减少心脏后负荷并改善冠状动脉灌注的主动脉内球囊泵仅用于急性住院治疗。最后,在心脏再同步治疗中,植入式起搏器改善了衰竭心室的协调收缩,该心脏再同步治疗在改善心力衰竭且并发有电传导异常的患者的死亡率方面显示出良好的效果。
实验疗法试图通过在房间隔内植入金属支架来降低升高的左心房压力,支架在高压左心房与低压右心房之间产生分流。由于右心房和静脉贮存器是高度顺应性的,因此在一些实施例中,从左向右的血液分流有效地降低左心房压力,而不会显著升高右心房压力,从而缓解症状并改善心脏力学。这些心房间分流的早期人类数据显示出有改善功能状态和血液动力学参数的前景。
这些心房间分流的最佳尺寸尚不清楚,尽管已使用模拟数据和早期动物研究对其进行了估算。重要的是,心房间孔的尺寸必须足够大,以允许有效的左心房卸载,同时不允许过多的血液流向右侧从而在右心房和心室上施加过大的压力。临床上广泛接受的是,如果先天性房间隔缺陷的个体的缺陷尺寸导致分流分数大于50%,则应当封闭。因此,确定心房间分流器的大小,使得不超过50%的左心房血液被分流,这对于减小长期不良影响很重要。
植入式心房间分流器有许多缺点。由于异物留在心室内并与血液接触,因此存在凝结和形成血栓的风险,这长期地或直到装置表面内发生皮化之前,都可能需要药物抗凝治疗。植入物还存在装置破裂、移位或栓塞的风险。在一些实施例中,植入的支架还使得随后的经房间隔手术变得困难,因为它可能限制导管在左心房中移动的自由度。最后,如果需要闭合,则在一些实施例中,笨重的支架增加了密封心房间分流器的难度。
球囊房间隔造口术是一种使用相关联的医疗装置的手术,该医疗装置试图产生一个心房间孔,以允许血液在心脏左侧和右侧之间混合。该装置用于儿科人群,以在最终手术矫正之前治疗先天性心脏病。带有或不带有叶片的放气球囊经由静脉系统穿过房间隔并进入左心房。随后将球囊充气并向近端拉动,从而撕开间隔并打开心房间孔。该装置产生的心房间孔在患者之间不可复制。由于间隔已撕裂,因此产生的组织瓣会保持原位,并最终融合在一起。由这些装置组件产生的孔在几个月内会均匀闭合。这些心房间孔的暂时性质使其适合于先天性出生缺陷的短期治疗,但不适用于需要更持久治疗的成年心力衰竭人群。
因此,能够在无需植入物的情况下,以确保“长期”通畅的方式产生确定尺寸的心房孔来减轻心房压力的装置是有利的。使用这种装置将获得与可植入支架等同的生理功能,而没有遗留装置的负面后遗症。希望产生一种尺寸精确的孔,该孔在期望的治疗益处的持续时间内可以保持成形。由于这种疗法对高并发症负担的患者人群最可能有益,因此通过微创手术产生这种孔也是有利的。因此,该装置的目的是使得能够通过小的(<18fr、<6.0mm、<0.236英寸)经皮穿刺来产生尺寸精确的孔。
在一些实施例中,本文中的“远端/远侧”是指例如本文中的装置组件的定位成远离装置组件的操作者的位置、部分或元件,本文中的“近端/近侧”是指定位成更靠近装置组件的操作者的位置、部分或元件。例如,图4d中的导丝的末端远离输送导管或输送导管的远侧末端。
除非另有定义,否则本文中使用的所有技术术语的含义与本公开所属领域的普通技术人员通常所理解的含义相同。如本说明书和随附权利要求书中所使用的单数形式“一个”、“一种”和“该/所述”包括复数引用,除非上下文另外明确指出。除非另有说明,否则本文中对“或”的任何引用旨在涵盖“和/或”。除非另有说明,否则根据实施例,本说明书和权利要求书中使用的术语“约”和“大约/大致”是指小于或等于数值的+/-1%、+/-2%、+/-3%、+/-4%、+/-5%、+/-6%、+/-7%、+/-8%、+/-9%、+/-10%、+/-11%、+/-12%、+/-14%、+/-15%或+/-20%的变化。作为非限制性示例,根据实施例,约100米表示95米至105米(100米的+/-5%)、90米至110米(100米的+/-10%),或85米至115米(100米的+/-15%)的范围。
除非另有说明,否则如本说明书和随附权利要求书中所使用的术语“接合”是指将两件物品配对或放在一起的行为。
本公开涉及用于通过降低哺乳动物心脏的左心房中升高的血压来治疗心力衰竭的基于rf能量的装置组件和方法。在一些实施例中,本文公开了经导管的房间隔切除装置组件,其构造成在心脏的右心房和左心房之间产生确定尺寸的心房孔,以减轻左心房高压,从而允许不超过50%的左心房血液分流至心脏的右心房。代替使用机械组织切割器,在一些实施例中,本文公开了利用基于rf能量的组织切割器的经导管的房间隔切除装置组件。在一些实施例中,这种基于rf能量的组织切割器有利地便于比传统的机械组织更有效、准确、可控的组织切割。在一些实施例中,本文公开了用于哺乳动物的心房间吻合以治疗充血性心力衰竭的装置组件,该装置组件包括:输送导管,该输送导管具有输送腔,并且可转向或可弯曲;射频(rf)发生器,该rf发生器定位成远离输送导管;和封装在输送腔内的可扩张组织切割器,该可扩张组织切割器附装至组织切割器导管,并且构造成在处于输送腔外部时扩张,其中,可扩张组织切割器电连接至rf发生器,组织切割器导管与输送导管同轴,并且可以在输送导管内滑动,组织切割器导管包括第一腔。在一些实施例中,可扩张组织切割器包括一种或多种导电材料。在一些实施例中,可扩张组织切割器通过导线连接至rf发生器。在一些实施例中,导线至少部分地在组织切割器导管的壁部中,或者至少部分地沿着组织切割器导管。
在一些实施例中,可扩张组织切割器包括rf阳极,并且rf发生器构造成产生rf能量,该rf能量从rf阴极穿过哺乳动物的组织到达rf阳极。在一些实施例中,rf阴极与哺乳动物的身体接触。在一些实施例中,rf阳极与rf阴极之间的距离在约1毫米至约2米的范围内。在一些实施例中,可扩张组织切割器包括rf阴极,并且rf发生器构造成产生rf能量,该rf能量从rf阴极穿过哺乳动物的组织到达rf阳极。在一些实施例中,rf阳极与rf阴极之间的距离在约1毫米至约2米的范围内。在一些实施例中,rf阳极与哺乳动物的身体接触。在一些实施例中,rf阴极是单点电极、贴片电极或环形电极。在一些实施例中,装置组件包括rf阳极,其中,rf阳极位于导丝、引导导管或输送导管上。在一些实施例中,rf阳极是单点电极、贴片电极或环形电极。在一些实施例中,rf发生器构造成产生交流频率在约300khz至约3mhz的范围内或者功率在约1瓦至约500瓦的第二范围内的交流电。在一些实施例中,rf发生器构造成在装置组件的至少一部分操作期间输出恒定的电压、功率或电流。在一些实施例中,rf发生器构造成输出具有至少一部分正弦波的电流、电压或功率。在一些实施例中,rf发生器包括监视器,该监视器构造成监测组织切割器处的参数。在一些实施例中,rf发生器包括调节器,该调节器构造成基于监测到的参数来调节rf发生器的输出。在一些实施例中,rf发生器包括泵,该泵构造成使冷却剂循环到组织切割器,从而调节组织切割器的温度。在一些实施例中,可扩张组织切割器至少部分地绝缘或至少部分地不导电。在一些实施例中,组织切割器的至少一部分远侧切割边缘不是绝缘或不导电的。在一些实施例中,装置组件包括扶正器/定心装置,该扶正器安装在组织切割器导管的外部,并且与输送导管可滑动地接合。在一些实施例中,所述扶正器构造成在组织切割器和输送导管之间提供扶正。在一些实施例中,组织切割器构造成在哺乳动物的左心房中展开,并且被拉向哺乳动物的右心房,从而在装置组件操作期间为组织提供稳定和保持。在一些实施例中,装置组件包括导丝。在一些实施例中,导丝构造成从输送腔的远端延伸出,并且大约在卵圆窝处穿过哺乳动物的右心房和左心房之间的房间隔中的初始穿刺部位,从而为装置组件提供进入左心房的工作轨道。在一些实施例中,导丝与第一腔同轴地定位,并且与第一腔可滑动地接合。在一些实施例中,装置组件包括引导导管,其中,引导导管同轴地定位在第一腔中,并且其中,引导导管包括第二腔,导丝构造成在该第二腔中滑动。在一些实施例中,组织切割器从房间隔切除的组织至少被组织切割器捕获和保持。在一些实施例中,组织切割器构造成缩回到收缩的输送腔中,其中,组织稳定器同时在组织切割器内完全收缩,将切除的组织捕获在其中。在一些实施例中,可扩张组织切割器的切割尺寸可调节。在一些实施例中,本文公开了用于哺乳动物的心房间吻合以治疗充血性心力衰竭的装置组件,该装置组件包括:输送导管,该输送导管具有输送腔,并且可转向或可弯曲;射频(rf)发生器,该rf发生器定位成远离输送导管;封装在输送腔内的可扩张组织切割器,该可扩张组织切割器附装至组织切割器导管,并且构造成在处于输送腔外部时扩张,其中,可扩张的切割器电连接至rf发生器,组织切割器导管与输送导管同轴,并且可以在输送导管内滑动,组织切割器导管包括第一腔;和封装在输送腔内的可扩张组织稳定器,该可扩张组织稳定器在远端处或附近附装至组织稳定器导管,并且构造成在处于输送导管或组织切割器导管外部时扩张,组织稳定器导管与输送腔或第一腔同轴,并且可以在输送腔或第一腔内滑动;组织稳定器导管包括第二腔,该第二腔可滑动地接合至组织切割器导管或扩张器末端导管并与之同轴。在一些实施例中,可扩张组织切割器包括一种或多种导电材料。在一些实施例中,可扩张组织切割器通过导线连接至rf发生器。在一些实施例中,导线至少部分地在组织切割器导管的壁部中,或者至少部分地沿着组织切割器导管。
在一些实施例中,可扩张组织切割器包括rf阳极,并且rf发生器构造成产生rf能量,该rf能量从rf阴极穿过哺乳动物的组织到达rf阳极。在一些实施例中,rf阴极与哺乳动物的身体接触。在一些实施例中,rf阳极与rf阴极之间的距离在约1毫米至约2米的范围内。在一些实施例中,可扩张组织切割器包括rf阴极,并且rf发生器构造成产生rf能量,该rf能量从rf阴极穿过哺乳动物的组织到达rf阳极。在一些实施例中,rf阳极与rf阴极之间的距离在约1毫米至约2米的范围内。在一些实施例中,rf阳极与哺乳动物的身体接触。在一些实施例中,装置组件包括rf阳极,其中,rf阳极位于导丝、引导导管、组织稳定器导管、组织稳定器或输送导管上。在一些实施例中,rf发生器构造成产生交流频率在约300khz至约3mhz的范围内或者功率在约1瓦至约500瓦的第二范围内的交流电。在一些实施例中,rf发生器构造成在装置组件的至少一部分操作期间输出恒定的电压、功率或电流。在一些实施例中,rf发生器构造成输出具有至少一部分正弦波的电流、电压或功率。在一些实施例中,rf发生器包括监视器,该监视器构造成监测组织切割器处的参数。在一些实施例中,rf发生器包括调节器,该调节器构造成基于监测到的参数来调节rf发生器的输出。在一些实施例中,rf发生器包括泵,该泵构造成使冷却剂循环到组织切割器,从而调节组织切割器的温度。在一些实施例中,组织切割器至少部分地绝缘或至少部分地不导电。在一些实施例中,组织切割器的至少一部分远侧切割边缘不是绝缘或不导电的。在一些实施例中,装置组件包括扶正器,该扶正器安装在组织切割器导管的外部,并且与输送导管可滑动地接合。在一些实施例中,所述扶正器构造成在组织切割器和输送导管之间提供扶正。在一些实施例中,组织切割器构造成在哺乳动物的左心房中展开,并且被拉向哺乳动物的右心房,从而在装置组件操作期间提供组织稳定和保持。在一些实施例中,装置组件包括导丝。在一些实施例中,导丝构造成从输送腔的远端延伸出,并且大约在卵圆窝处穿过哺乳动物的右心房和左心房之间的房间隔中的初始穿刺部位,以便为装置组件提供进入左心房的工作轨道。在一些实施例中,导丝同轴地定位在第一腔内,并且与第一腔可滑动地接合。在一些实施例中,装置组件包括引导导管,其中,引导导管同轴地定位在第一腔中,并且其中,引导导管包括第二腔,导丝构造成在该第二腔中滑动。在一些实施例中,组织切割器从房间隔切除的组织至少被组织切割器捕获和保持。在一些实施例中,组织切割器包括自扩张支架,该自扩张支架具有钝的、圆形、正方形或六边形的远端边缘,使得在将任何rf能量施加到房间隔之前,该远端边缘不会刺穿房间隔。在一些实施例中,组织切割器包括自扩张支架和附装在支架远端处或附近的柔性金属环。在一些实施例中,组织切割器包括以下一项或多项:柔性金属环;自扩张线圈;自扩张支架;自扩张金属线;卷状薄片;一个或多个自扩张撑杆;铰链支柱;球囊;自扩张网筛;机械致动式钳口;或其组合。在一些实施例中,可扩张组织切割器构造成通过一个或多个能量偏置元件扩张。在一些实施例中,可扩张组织切割器构造成通过机械致动(例如经由伞状机构)扩张。在一些实施例中,可扩张组织切割器构造成自扩张,使得在组织切割器脱鞘/释放时,它从其收缩状态呈现完全扩张。在一些实施例中,组织切割器包括网筛,所述网筛构造成便于将切除的组织保持在所述组织切割器内。在一些实施例中,组织切割器构造成被收回到收缩的输送腔中,其中,组织稳定器同时在组织切割器内完全收缩,将切除的组织捕获在其中。在一些实施例中,可扩张组织切割器的切割尺寸可调节,并且其中,可扩张组织稳定器的尺寸可调节。在一些实施例中,组织稳定器导管的远端构造成沿着导丝的轨道延伸,并且穿过初始穿刺部位,使得组织稳定器也延伸穿过房间隔进入左心房中。在一些实施例中,组织稳定器在左心房中同轴地扩张,使得其尺寸足够大,以防止通过初始穿刺部位将组织稳定器拉回,并且使得组织稳定器在初始穿刺部位周围的房间隔上提供支撑、张紧作用。在一些实施例中,可扩张切割器构造成可滑动地前进,并且同轴地扩张至比组织稳定器的扩张尺寸大的切割尺寸。在一些实施例中,组织切割器导管构造成向远侧延伸,直到完全扩张的组织切割器在卵圆窝处或附近与房间隔的右心房侧接合,使得组织切割器刺穿并完全切穿房间隔,从而在房间隔中产生房压释放孔,其中,房压释放孔足够大,以允许血液通过房压释放孔从左心房流到右心房,使得不超过50%的左心房血液分流至右心房,并且其中,房压释放孔足够大和/或具有这种形状,使得减缓组织的自然愈合过程,以保持房间隔中的房压释放孔通畅,而不需要在其中植入支架或瓣膜。在一些实施例中,组织稳定器构造成部分收缩,组织稳定器导管构造成被缩回,直到捕获切除的组织,并且将部分收缩的组织稳定器的至少一部分拉入组织切割器的开口中,该组织切割器至少部分地扩张。在一些实施例中,组织稳定器或组织切割器包括:可充气球囊;扩张齿;扩张网筛;至少一根弯曲的导线;扩张板;扩张盘;扩张叶片;弹簧线圈;至少一个支柱;至少一个铰接臂;伞状延伸器;或其组合。在一些实施例中,用于除了可充气球囊之外的任何元件的组织稳定器材料包括形状记忆合金,该形状记忆合金包括:镍钛诺;镍钛;铜铝镍;或锌金铜。在一些实施例中,组织切割器材料包括形状记忆合金,该形状记忆合金包含:镍钛诺;镍钛;不锈钢;铜铝镍;锌金铜;或其组合。在一些实施例中,组织切割器包括:丝网;连接锐齿的导线;可收缩的孔锯结构;可收缩的开放式柱形结构;可收缩的开放式桶形结构;可收缩的开放式锥形结构;或其组合。在一些实施例中,组织稳定器的扩张尺寸比组织切割器的扩张尺寸大。在一些实施例中,组织切割器的扩张尺寸比组织稳定器的扩张尺寸小约1%至约50%。在一些实施例中,组织切割器构造成切割以下形状的孔或洞:圆形;椭圆形;三角形;正方形;矩形;或多边形;或其组合。在一些实施例中,组织稳定器的扩张尺寸比组织切割器的扩张尺寸小。在一些实施例中,组织切割器的扩张尺寸比组织稳定器的扩张尺寸大约1%至约50%。在一些实施例中,组织稳定器的扩张尺寸比组织切割器的扩张尺寸大。在一些实施例中,组织稳定器的扩张尺寸比组织切割器的扩张尺寸大约1%至约50%。在一些实施例中,装置组件在导丝上包括亲水涂层。在一些实施例中,装置组件在导丝上包括疏水涂层。在一些实施例中,装置组件包括结合到导丝的远侧末端中的力/压力传感器。在一些实施例中,装置组件包括结合到导丝中的氧饱和度检测传感器。在一些实施例中,一个或多个传感器结合到装置的导管中的任何一个或多个中。在一些实施例中,一个或多个传感器结合到组织切割器中。在一些实施例中,一个或多个传感器结合到组织稳定器中。在一些实施例中,装置组件包括结合到导丝的远侧末端中的切割点或边缘。在一些实施例中,装置组件包括结合到导丝的远侧末端中的弯曲或成形的端部。在一些实施例中,组织稳定器在关键位置处包括不透射线的标记带,以便:确定装置在体内的位置、确定其与其他系统部件的关系,和允许可见性并确认其展开状态。在一些实施例中,组织稳定器和/或组织切割器通过确保将任何切除的组织捕获并保留在装置组件内来提供栓塞保护。在一些实施例中,包括可充气球囊的组织稳定器包括保护裙部,该保护裙部保护充气球囊的近端边缘。在一些实施例中,保护裙部相对于球囊的状态扩张和收缩。在一些实施例中,组织稳定器和/或组织切割器包括:扩张网;扩张板;扩张盘;扩张叶片;扩张撑杆或尖齿;或扩张线圈;其中,组织稳定器和/或组织切割器由形状记忆合金制成,该形状记忆合金在完全穿过房间隔后沿着向外方向扩张,以相对于房间隔呈大约90°角的取向,并且构造成被向后拉动以接合该间隔,从而在与组织稳定器或组织切割器接合之前和之后使其稳定,并且其中,在组织切割器接合之后,组织稳定器沿着与其打开方向相同的方向收缩,从而在组织切割器重新入鞘时,捕获从间隔切下的组织的切除部分,使得切除组织和组织稳定器收缩到输送导管中。在一些实施例中,组织稳定器和/或组织切割器包括:至少一个支柱;至少一个铰接臂;或伞状延伸器;其中,组织稳定器在完全穿过房间隔后沿着向外方向扩张,以相对于房间隔呈大约90°角的取向,并且构造成被向后拉动以接合该间隔,从而在与组织稳定器或组织切割器接合之前或之后使其稳定;并且其中,在组织切割器激活之后,组织稳定器沿着与其打开方向相同的方向收缩,从而在组织切割器重新入鞘时,捕获从间隔切下的切除组织,使得切除的组织和组织稳定器收缩到输送导管中。在一些实施例中,组织稳定器包括:至少一根弯曲的导线;或弹簧线圈;其中,组织稳定器由形状记忆合金制成,该形状记忆合金构造成在完全穿过间隔之后沿着横向于近侧-远侧轴线的向外方向扩张,且具有比组织切割器尺寸大或小的径向尺寸,并且构造成被向后拉动以接合该间隔,以在与组织切割器接合之前和之后使其稳定;并且其中,在组织切割器激活之后,组织稳定器沿着与其打开方向相同的方向收缩,从而在组织切割器重新入鞘时,捕获从间隔切下的组织的切除部分,使得切除的组织和组织稳定器适配到输送导管中。在一些实施例中,可扩张组织稳定器在脱鞘时是自扩张的。在一些实施例中,可扩张组织切割器在脱鞘时是自扩张的。在一些实施例中,输送导管是线增强的或编织的。在一些实施例中,输送导管包括增强的远侧末端。在一些实施例中,输送导管包括约0.5英寸至约4英寸的弯曲半径。在一些实施例中,引导导管构造成以预定的方式朝向房间隔弯曲。在一些实施例中,可扩张切割器构造成在扩张之后在房间隔中产生多个穿孔。在一些实施例中,可扩张组织切割器构造成平移穿过房间隔,从而在扩张之后在房间隔处产生一个完整的切口。在一些实施例中,组织切割器包括近端边缘和远端边缘。在一些实施例中,当组织切割器完全扩张时,近端边缘不扩张。在一些实施例中,组织稳定器包括多于一个的可扩张网状盘,当靠近房间隔并且在右心房中时,该多于一个的可扩张网状盘中的至少一个扩张。在一些实施例中,当扩张时,多个可扩张网状盘中的两个将房间隔夹在盘之间。在一些实施例中,当扩张时,多个可扩张网状盘中的两个接触,并且将房间隔夹在盘之间。在一些实施例中,组织稳定器包括多于一个的可扩张网状盘,多个可扩张网状盘中的一个构造成当组织稳定器重新入鞘时堵塞组织切割器的远端开口或输送导管的远端开口。在一些实施例中,多个可扩张网状盘中的一个构造成在组织稳定器重新入鞘时捕获组织切割器的远端。在一些实施例中,多个可扩张网状盘中的一个的宽度比组织切割器的远端的宽度大。在一些实施例中,多个可扩张网状盘包括形状记忆合金或金属。在一些实施例中,组织切割器包括支架。在一些实施例中,组织切割器包括以下一项或多项:由支柱构成的多个支架网格、可选地在远端连接的多个支柱、金属环、和细网筛。在一些实施例中,金属环是柔性的,多个支柱径向分布,并且连接到组织切割器导管。在一些实施例中,金属环至少部分导电或至少部分不导电。在一些实施例中,金属环包括形状记忆材料或非形状记忆材料。在一些实施例中,多个支柱包括形状记忆材料、刚性材料、能量偏置材料或其组合。在一些实施例中,多个支柱至少部分导电或至少部分不导电。在一些实施例中,细网筛构造成便于在切割后将切除的组织保持在装置组件内。在一些实施例中,组织切割器包括形状记忆材料、能量偏置材料或两者。在一些实施例中,输送导管还包括分裂鞘管(splitsheathcatheter),该分裂鞘管构造成使组织切割器能够入鞘和脱鞘。在一些实施例中,输送导管也是分裂鞘管,该分裂鞘管构造成使组织切割器能够入鞘和脱鞘。在一些实施例中,组织稳定器包括细网筛,该细网筛构造成便于在切割后将切除的组织保持在装置组件内。在一些实施例中,装置组件还包括扩张器末端,该扩张器末端构造成便于该装置组件在导丝上通过和/或穿过房间隔。
在一些实施例中,本文公开了使用经导管装置组件切除哺乳动物的房间隔,以治疗充血性心力衰竭的方法,该方法包括:使可扩张组织切割器在导丝上前进并穿过房间隔到达左心房,该可扩张组织切割器处于压缩状态;扩张并移动组织切割器,以在左心房中向房间隔提供张力;将组织切割器平移至与房间隔接触;在rf阴极和rf阳极之间将rf功率传输穿过房间隔,从而产生孔,其中,rf阴极或rf阳极位于可扩张组织切割器上,而rf阴极或rf阳极中的另一个位于输送导管上或与哺乳动物的组织接触;以及使可扩张组织切割器与切下的房间隔一起重新入鞘到输送导管中。在一些实施例中,可扩张组织稳定器在房间隔的相对侧上展开,以在将rf功率传输穿过房间隔从而产生一个孔之前提供组织稳定。
在一些实施例中,本文公开了使用经导管装置组件切除房间隔,以治疗充血性心力衰竭的方法,该方法包括:将可扩张组织稳定器推进穿过房间隔,该可扩张组织稳定器处于压缩状态;展开和移动组织稳定器,以在左心房中向房间隔提供张力;将可扩张组织切割器输送至右心房,该可扩张组织切割器处于容纳在装置组件的输送导管中的第二压缩状态;使可扩张组织切割器在右心房中扩张;使组织切割器向前平移,以与房间隔接触,从而将房间隔夹在可扩张组织切割器和可扩张组织稳定器之间;在rf阴极和rf阳极之间将rf功率传输穿过房间隔,从而产生孔,其中,rf阴极或rf阳极位于可扩张组织稳定器上;以及使可扩张组织切割器和可扩张组织稳定器与切除的组织一起重新入鞘到输送导管中。在一些实施例中,该方法包括允许装置组件通过股静脉进入血管。在一些实施例中,该方法包括穿刺房间隔的卵圆窝,并将导丝推进至左心房。在一些实施例中,组织稳定器和/或组织切割器在导丝上前进。在一些实施例中,不需要导丝,在没有通过导丝预穿刺并且没有通过导丝引导的情况下将装置(本文描述的任何装置)推进穿过间隔。在一些实施例中,使可扩张切割器在右心房中扩张包括使输送导管相对于组织切割器平移。在一些实施例中,在经房间隔穿刺之后,导丝保留在左心房中。在一些实施例中,切除的组织包括至少一部分房间隔。在一些实施例中,展开组织稳定器包括同时或在不同的时间点展开多于一个的组织稳定盘。在一些实施例中,一个所述组织稳定盘在左心房中展开。在一些实施例中,一个所述组织稳定盘在右心房中展开。在一些实施例中,该方法包括从受试者移除重新入鞘的装置组件。在一些实施例中,将引导导管在导丝上推进至房间隔包括将引导导管推进出输送导管。在一些实施例中,使用现成的经房间隔套件进行穿刺房间隔的卵圆窝。在一些实施例中,组织切割器和组织稳定器的重新入鞘包括用组织稳定器堵塞输送导管的远端开口。在一些实施例中,组织切割器和组织稳定器的重新入鞘包括在重新入鞘期间用组织稳定器堵塞组织切割器的远端开口。在一些实施例中,该方法包括从受试者移除重新入鞘的装置组件。
在一些实施例中,现成的经房间隔穿刺套件构造成与本文的经导管房间隔切除装置组件一起使用,从而通过从主装置组件上移除穿刺末端和导丝来简化经导管房间隔切除装置的设计,从而降低复杂性和成本。这种现成的经房间隔穿刺套件的一个示例是型号为407366的swartztmbraidedtransseptalguidingintroducers(编织型经房间隔导引器)lamptm系列,长度为180cm,直径为0.035英寸。在一些实施例中,现成的血管通路护套用于将装置组件展开到股静脉中。
导丝
在一些实施例中,使用标准的经房间隔穿刺技术将导丝放置穿过房间隔,并且提供沿着其推进装置组件的工作轨道。在一些实施例中,装置的各个部件沿着导丝相对于彼此和房间隔平移。在一些实施例中,导丝包括在装置组件中。在一些实施例中,导丝不包括在装置组件中。在一些实施例中,导丝在其远端处具有可扩张元件,以用作组织稳定器和组织保持元件。
引导导管
在一些实施例中,在本文的装置组件中包括刚性引导导管,其具有预弯曲形状,以将组织切割器以大致垂直的取向引导向房间隔。在一些实施例中,也使用可转向或可偏转的导管来实现该对准。在一些实施例中,引导导管具有中心腔,导丝穿过该中心腔。在一些实施例中,根本不需要引导导管;在这些实施例中,作为导丝、导管1、导管2、导管3、导管4或其组合的特征,结合了预弯曲的形状、可转向性或可偏转性。
(可扩张)组织稳定器/组织保持元件
在一些实施例中,组织稳定器在组织切割器的激活期间向房间隔提供反张力,以使由于不平衡力引起的任何意外的组织变形、旋转或移位最小化。在一些实施例中,组织稳定器还向房间隔提供张力,以使壁部随着心跳的运动最小化。在一些实施例中,组织稳定器还兼用作组织保持元件,以防止切除的组织意外地脱离装置组件,并且允许在将装置组件从体内移除之前将切除的组织平移并包装到输送导管中。在一些实施例中,组织稳定器包括以下一个或多个:球囊、自扩张网、线圈和手动致动的柔性支柱。在一些实施例中,组织稳定器连接至导管2(例如组织稳定器导管),该导管2具有中心腔,其允许导丝和/或引导导管在内部平移/通过。在一些实施例中,组织稳定器连接至导丝,并且由自扩张网制成,该自扩张网在输送至左心房之前被约束在单独的导管内。在一些实施例中,该自扩张网在展开之前以收缩状态驻留在引导导管(导管1)内。在一些实施例中,rf阳极结合在组织稳定器中。在一些实施例中,不需要单独的组织稳定器,因为通过组织切割器执行这些功能。在一些实施例中,组织切割器在左心房中展开,并且被向后拉动,从而用于组织稳定和保持的双重目的。
(可扩张)组织切割器/切割元件
在一些实施例中,rf电外科组织切割器(或者本文中等同的rf电外科组织切割器)包括具有暴露的导电表面积的扩张结构。在一些实施例中,组织切割器被输送至间隔,并且在展开/扩张、通电和致动时,切除一部分组织,以产生规定的孔。在一些实施例中,组织切割器通过沿着导管3(组织切割器导管)的长度延伸的导线连接至rf发生器,并且用作将能量引导到组织中的rf阴极。在一些实施例中,该导线嵌入导管3的壁中,或者可替代地在装置组件中的其他导管中或沿着其长度延伸。在一些实施例中,组织切割器有利地具有非常小的暴露的导电材料的表面积,使得紧邻组织切割器的能量密度足够高地集中,以实现期望的组织效果。在一些实施例中,非常小的暴露的导电材料的表面积在组织切割器的总表面积的约0.01%至约50%的范围内。在一些实施例中,非常小的暴露的导电材料的表面积在组织切割器的总表面积的约0.01%至约1%的范围内。在一些实施例中,非常小的暴露的导电材料的表面积在组织切割器的总表面积的约0.1%至约1%的范围内。在一些实施例中,非常小的暴露的导电材料的表面积在组织切割器的总表面积的约0.1%至约5%的范围内。在一些实施例中,非常小的暴露的导电材料的表面积在组织切割器的总表面积的约0.1%至约10%的范围内。在一些实施例中,非常小的暴露的导电材料的表面积在组织切割器的总表面积的约1%至约15%的范围内。在一些实施例中,希望快速连续地选择性地为组织切割器的离散部分通电,以在组织切割器的通电部分周围维持高能量密度,而不需要立即为整个组织切割器通电。在一些实施例中,在施加能量期间,还有利地在组织切割器与房间隔之间保持小的限定间隙,以允许电弧放电,并且使对组织的任何不期望的热效应最小化。在一些实施例中,通过装置使用方法或通过为了确保维持间隙而结合的装置特征来维持这种间隙。在一些实施例中,有利地在组织切除期间或之后旋转或振荡/振动组织切割器,以防止、最小化或破坏成焦/炭形成。
在一些实施例中,rf是电磁频谱中与无线电波相关的任何频率或频率的组合。当从rf阴极提供rf电流、电压和/或功率时,电流然后通过组织和/或rf阴极与rf阳极之间的任何其他rf传导介质传播。
在一些实施例中,rf阴极是rf电流从中离开的电极;这种电流沿着正电荷移动的方向。在一些实施例中,rf阳极是rf电流流入其中的电极。在一些实施例中,rf阴极或阳极是单点电极、环形电极、板状电极、尖头电极、叶片形电极、贴片电极或任何其他类型的电极。
在一些实施例中,本文的装置(例如组织切割器)构造成用于电外科手术,其中,向组织施加射频交流极性电流作为切割手段。在电外科手术中,组织被rf电流加热。在一些实施例中,仅加热待切割的组织,而不加热其附近的其他组织。在一些实施例中,仅加热待切割的组织的一部分。在一些实施例中,组织的这种加热受组织切割器的导电区域的大小、形状和/或几何形状控制。在一些实施例中,将组织加热到预定温度或预定的温度范围。在一些实施例中,将待切割的组织加热至不低于60℃、70℃、80℃、90℃、100℃或甚至更高的温度。在一些实施例中,将待切割的组织加热到50℃至100℃的范围内。
rf能量阱(rf阳极或rf回路)
在一些实施例中,rf阳极用作rf阴极的rf电流阱,以限定rf能量在哺乳动物体内传输的场。在一些实施例中,本文公开的装置组件包括rf能量阱(rf阳极或rf回路),以将来自rf阴极的rf能量吸出体外,从而限定rf能量传输的场。参考图1,在一些实施例中,rf发生器117产生rf电流,该rf电流经由导线(例如直丝、同轴电缆)传输到rf阴极103b。在一些实施例中,rf阴极经由rf电流/电压将rf能量穿过组织107传输至rf阳极113b,rf阳极接收rf能量,然后经由导电连接将能量回传至rf发生器。在一些实施例中,rf阳极就位成紧邻rf阴极,或者在身体外部但是与身体接触(例如皮肤贴片电极)。在一些实施例中,rf阳极被结合成组织稳定器的特征。在一些实施例中,rf阳极在导丝、组织稳定器导管、组织切割器导管或输送导管上。
输送导管
在一些实施例中,输送导管是用于装置组件的所有其他部件(不包括rf发生器和在一些实施例中的rf能量阱)的主壳体导管。在一些实施例中,组织切割器容纳至输送导管的远端,并且确保组织切割器在展开之前保持收缩。在一些实施例中,输送导管还允许切除的组织堆积在其腔中。在一些实施例中,输送导管具有预弯曲的形状、可转向性或可偏转性,以便于相对于房间隔定向。
rf发生器
在一些实施例中,一种产生在约300khz至约3mhz的范围内的射频频谱中的功率水平在约5w至约300w的范围内的交流电流、电压和/或功率的装置。在一些实施例中,产生在约9khz至约300mhz范围内的射频频谱中的交流电流、电压和/或功率的装置。在一些实施例中,位于无菌场外部的rf发生器通过无菌连接器连接至rf阳极和阴极,该无菌连接器进入无菌场,并且通过连接至rf阳极和阴极的导线输送rf能量。在一些实施例中,rf发生器通过输出恒定电压、恒定功率和/或恒定电流来操作。在一些实施例中,rf发生器在组织切割的整个过程中输出恒定的正弦波。在一些实施例中,rf信号输出被中断和衰减,使得在装置组件的固定百分比的操作时间(在操作时间的0.01%至99.9%的范围内)内施加rf能量。在一些实施例中,这些不同的rf能量输出模式产生不同的组织效应。在一些实施例中,预期恒定的正弦波将产生期望的组织汽化,而不会热损伤或成焦。在一些实施例中,rf发生器包括电池,从而不需要进入/离开无菌场的导线。在一些实施例中,rf发生器在无菌场之内或之外。在一些实施例中,rf发生器监测组织切割器的远端处或附近的温度或阻抗,并且调节功率、电压或电流输出,以确保连续的组织切割。在一些实施例中,rf发生器包括泵,以使诸如盐水的冷的冷却剂循环通过组织切割器导管,以调节其温度和最小化/防止成焦。
在一些实施例中,rf发生器包括电源、接通/断开开关、处理器、计算机存储器、通信元件、到rf阴极的电连接装置以及到rf阳极的电连接装置。在一些实施例中,手动控制rf发生器。在一些实施例中,使用诸如温度反馈的反馈系统来自动控制rf发生器。
在一些实施例中,rf发生器包括构造成执行可执行指令的操作系统。操作系统例如是包含程序和数据的软件,该软件管理装置的硬件,并且提供执行应用程序的服务。在一些实施例中,rf发生器包括存储和/或内存装置。该存储和/或内存装置是一个或多个用于临时或永久地存储数据或程序的物理装置。在一些实施例中,rf发生器包括显示器,以向使用者发送视觉信息。在一些实施例中,rf发生器包括输入装置,以从使用者接收信息。在一些实施例中,本文的rf发生器包括一个或多个用程序编码的非暂时性计算机可读存储介质,该程序包括可由可选地联网的数字处理装置的操作系统执行的指令。在一些实施例中,本文的rf发生器包括至少一个计算机程序或使用该计算机程序。在一些实施例中,计算机程序包括可在数字处理装置的cpu中执行的一系列指令,该指令被编写成执行指定任务。
参考图2,在一些实施例中,装置组件包括输送导管201、组织切割器导管202、组织稳定球囊204e和导丝206,包含有组织切割器阴极203b的组织切割球囊203e附装至该组织切割器导管202,该组织稳定球囊204e附装在组织稳定器导管205的远端,该导丝206可滑动地接合在组织稳定器导管的腔内。在一些实施例中,rf阴极203b位于组织切割器的远端上或远端附近,rf阳极213b位于组织稳定器的近端上或近端附近。组织切割器和组织稳定器都包括至少一个可扩张或可充气的球囊。
在一些实施例中,本文公开的使用装置组件的方法包括一个或多个过程步骤,该过程步骤从以下步骤中选取,但不一定按照确切的顺序:
-使用标准技术(例如seldinger方法)通过股静脉实现进入血管;
-使用标准介入技术进行穿过房间隔的卵圆窝的房间隔穿刺,将导丝留在原位;
-例如通过腹股沟将装置组件引入,并且在导丝上输送至右心房;
-将组织稳定器在导丝上引入,并且穿过房间隔到达左心房;在左心房中,该组织稳定器通过充气(在球囊的情况下)、机械致动或自扩张材料的脱鞘来扩大直径(可替代地,将组织切割器在导丝上引入,并且穿过房间隔到达左心房;在左心房中,通过相对于组织切割器向后拉动其约束导管使组织切割器脱鞘);
-将组织切割器(经由输送导管)输送至右心房;在右心房中,通过向后拉动该组织切割器的约束导管使其在右心房中脱鞘(可替代地,将组织稳定器(经由输送导管)输送至右心房;在右心房中,该组织稳定器通过充气(在球囊的情况下)、机械致动或自扩张材料的脱鞘来扩大直径;
-在脱鞘之后(或者在脱鞘过程中),组织切割器完全扩张;
-组织切割器在导丝上平移,直到其接触房间隔,从而将组织夹在组织切割器和组织稳定器之间;
-对组织切割器通电,将rf电流发送穿过(在rf阴极和阳极之间的)间隔,以产生一个孔,该孔的形状由组织切割器的几何形状确定;并且
根据实施例,以任何顺序执行以下步骤:
-组织切割器收缩;
-相对于输送导管向后拉动组织稳定器,从而将切除的组织包装在输送导管中;
-组织稳定器收缩;和
-从身体移除装置。
支架
在一些实施例中,本文公开的组织切割器包括支架。在一些实施例中,组织切割器采用自扩张(例如形状记忆材料)支架的形式,该支架沿着其远端边缘的整个长度变尖,并且在从右心房中的输送导管(导管4,未示出)展开时自扩张。组织切割器除了其远端边缘之外完全绝缘;其近端附装至组织切割器导管,并且通过在组织切割器导管内或沿着组织切割器导管延伸的导线联接至rf发生器。在一些实施例中,组织切割器导管具有中心腔,该中心腔包含导丝、引导导管和组织稳定器。
在一些实施例中,该装置在导丝上前进,其中,组织稳定器附装至其相应的导管(导管2),并且被输送穿过房间隔,在该房间隔处,致动该组织稳定器以使其完全扩张。在一些实施例中,相对于组织切割器导管向后拉动输送导管(导管4),从而使支架和组织切割器暴露和扩张。在一些实施例中,将rf阳极结合到组织稳定器中,该组织稳定器例如是组织稳定器导管(在左心房中)上的环形电极,或者是放置在哺乳动物身体表面上的垫片。在适当就位时,在一些实施例中,组织切割器由rf发生器通电,导致组织破裂和切除。在一些实施例中,组织切割器、切除的组织和组织稳定器在输送导管(导管4)中收缩,并且将装置从身体移除。
在一些实施例中,本文公开的组织切割器包括支架。在一些实施例中,如图3a-3c所示,组织切割器采用自扩张(例如形状记忆材料)支架的形式。在一些实施例中,将支架图案激光切割到形状记忆材料的柱形管上。在一些实施例中,支架303具有近似菱形图案形状的网格。在一些实施例中,支架网格具有其他形状,例如圆形、三角形、矩形等。在一些实施例中,如图3c所示,支架303具有至少三个轴对称的支柱303m,该支柱303m在其扩张直径处通过环303b在远端连接。在一些实施例中,作为图3b所示的环303b的替代方案,环303b在图3a的支架303中(同轴地更靠近图3a的导管302的纵轴线)。可替代地,图3c的实施例环在图3a的实施例外部同轴地用作稳定器(距图3a的导管302的纵轴线更远)。可替代地,图3c的实施例用作组织切割器,其中,环303b被锐化以切割间隔,或者被通电以使用rf能量(作为阴极)切割房间隔。在一些实施例中,如图3a-3b所示,支架末端303j在其远端边缘被锐化,并且能够穿透房间隔和用作锚固机构,以使支架基本上垂直于房间隔定位。在一些实施例中,除了其远侧末端303j、支柱的冠部303k、支柱的谷部303l和/或环303b之外,支架303完全绝缘303h。在一些实施例中,支架的近端附装至组织切割器导管302,并且通过在组织切割器导管内或沿着组织切割器导管延伸的导线(未示出)联接到rf发生器。在一些实施例中,支架(部分地)是绝缘的或由诸如聚对二甲苯、ptfe的非导电材料构成。在一些实施例中,支架在从右心房或左心房中的导管(输送导管或组织稳定器导管,未示出)展开时自扩张,其中,扩张的直径朝向房间隔。在一些实施例中,组织切割器在适当就位时由rf发生器通电,并且平移穿过房间隔,导致组织破裂和切除。在一些实施例中,支架除了其远侧末端和锐化的边缘之外完全绝缘,组织切割器在适当就位时(远侧末端已经穿透房间隔)由rf发生器通电,并且使组织切割器旋转,导致组织破裂和切除。在一些实施例中,使用具有锥形的穿透末端的分裂鞘管使自扩张支架在左心房中展开,以便于穿过房间隔。在一些实施例中,分裂鞘向远侧移动,以使远端边缘朝向房间隔的支架303脱鞘。在特定实施例中,图3b示出了金属导线环303b,该金属导线环303b在支柱的冠部303k上的多个位置处通过小孔303n拴系,从而在环和支架的远端边缘之间维持间隙。在该实施例中,支架303除了其远侧末端303j和支柱的冠部303k之外完全绝缘。在一些实施例中,环303b被缝合、焊接、钎焊、铜焊、胶粘、螺纹连接或缠绕穿过支架的远端边缘、在支架的远端边缘上或周围。在一些实施例中,当支架完全扩张时,环303b采用圆形、多边形、套索或任何其他几何形状的形式。在一些实施例中,支架仅用作自扩张支架,以将金属环扩张至期望的几何形状。在一些实施例中,自扩张支架是管状网筛构型的编织支架。在一些实施例中,组织切割器导管302具有中心腔,该中心腔包含导丝、引导导管和组织稳定器。
在一些实施例中,支架组织切割器在导丝上在左心房中展开,其非绝缘/切割边缘朝向房间隔。在一些实施例中,组织稳定器从经导管房间隔切除装置中排除。如图4a-4d所示,支架组织切割器403收缩并容纳在分裂鞘管408中。在一些实施例中,导管408包括盖408a和轴408e。导管轴具有中心腔408f,该中心腔408f与导丝406可滑动地接合。盖408a具有锥形的穿透末端408d,以便于导管408穿过房间隔(在导丝上)从右心房到达左心房。导管的盖408a具有第二腔408b,该第二腔408b容纳收缩的支架组织切割器403。图4d示出了图4c的详细视图。在一些实施例中,支架组织切割器通过绝缘体403h部分地绝缘,使其切割边缘403b暴露(定向成朝向间隔),并且其后端通过导线(未示出)联接至rf发生器。在一些实施例中,支架组织切割器403附装至组织切割器导管402,该组织切割器导管402具有中心腔,与导管408的轴408e可滑动地接合。在一些实施例中,结合了扶正器411,该扶正器411具有安装至组织切割器导管402的外径和支架组织切割器408e的内径的中心腔。在一些实施例中,支架组织切割器403通过在组织切割器导管402中或沿着该组织切割器导管402延伸的导线联接至rf发生器。在一些实施例中,电极放置在身体外部但与其接触(例如皮肤贴片电极),以用作rf阳极。在一些实施例中,环形电极在右心房中驻留在组织切割器导管402上,并且用作rf阳极,从而不需要放置在外部的rf阳极。
在一些实施例中,装置组件400向前推进至左心房,使得导管408的盖408a穿过间隔407。组织切割器导管402和输送导管401在导管408向前推进时保持静止,以使支架组织切割器403脱鞘并展开其切割边缘。在一些实施例中,通过向后拉动组织切割器导管402,使得支架组织切割器的切割边缘与间隔407接触,从而输送rf能量。在一些实施例中,在组织切割之后,通过使导管408相对于组织切割器导管402向后(向近侧)滑动来使支架组织切割器403收缩,该组织切割器导管402是静止的,或者向远侧移动以支撑支架在盖408a中收缩。在一些实施例中,切除的组织被包装在支架403本身内,随后是导管408的盖408a的第二腔408b。在一些实施例中,在组织切除之后,鉴于切除的组织保持在组织切割器中,组织切割器兼作组织保持元件。
在一些实施例中,组织切割器保持在右心房中。该装置在导丝上推进,组织稳定器附装至其相应的导管(导管2),并且被输送穿过间隔,在该处被致动成完全扩张。在一些实施例中,相对于组织切割器导管向后拉动输送导管(导管4),从而使支架组织切割器暴露和扩张。在一些实施例中,将rf阳极结合到组织稳定器中,该组织稳定器例如是组织稳定器导管(在左心房中)上的环形电极,或者是放置在哺乳动物身体表面上的垫片。在适当就位时,在一些实施例中,组织切割器由rf发生器通电,导致组织破裂和切除。在一些实施例中,组织切割器、切除的组织和组织稳定器在输送导管中收缩,并且将装置从身体移除。
在一些实施例中,支架组织切割器具有钝的、圆形、正方形或六边形的远端边缘,使得在将rf能量施加到间隔之前,该远端边缘不会刺穿组织;在施加能量之前,它仅沿着其远端边缘的长度接合组织。
在一些实施例中,支架组织切割器包括形状记忆材料,例如:镍钛;铜铝镍;锌金铜;或其组合。
在一些实施例中,支架完全绝缘或包括非导电材料。在一些实施例中,组织切割器包括在一个或多个位置固定到支架的远端的柔性金属环,例如303b。在一些实施例中,在柔性金属环与组织之间产生电弧,由此有利于组织切割,例如图3a-3b。在一些实施例中,支架仅用作自扩张支架,以将金属环扩张至期望的几何形状。在一些实施例中,支架具有尖锐的末端,例如305,其穿透组织并用作锚固机构,以使支架定位成基本上垂直于间隔。在一些实施例中,金属环被缝合、焊接、钎焊、铜焊、胶粘、螺纹连接或缠绕穿过支架的远端边缘、在支架的远端边缘上或周围。在一些实施例中,当支架完全扩张时,金属环采用圆形、多边形或套索的形式。
在一些实施例中,金属环遵循在支架的远端边缘处的齿的轮廓。在一些实施例中,金属环在离散位置锚固,从而在锚固位置之间的金属环与支架之间维持间隙。在一些实施例中,金属环被锚固至支架的远端边缘。
在一些实施例中,经导管房间隔切除装置包括分裂导管。在图4和图5所示的实施例中,分裂鞘管408与导管401一起构成输送导管,其腔408b与导管401的腔一起构成输送腔;分裂鞘管508与导管501一起构成输送导管,其腔508b与腔501a一起构成输送腔。
在一些实施例中,组织切割器和组织稳定器都是自扩张支架,每个支架上的非绝缘边缘分别用作rf阴极503b和阳极513b。参考图5a-5d,导管508包括盖508a和轴508e,导管轴具有中心腔(未示出),该中心腔与导丝(未示出)可滑动地接合;盖具有锥形的末端508d,以便于导管穿过间隔507(在导丝上)从右心房到达左心房;导管的盖508a具有第二腔508b,该第二腔508b容纳收缩的组织稳定器504。在一些实施例中,组织稳定器504部分地绝缘504h,使其非绝缘的边缘暴露,并且安装在组织稳定器导管505的远端。在一些实施例中,导线将组织稳定器连接至rf发生器,在组织稳定器导管505的壁内延伸。在一些实施例中,支架组织切割器503至少部分地绝缘503h,使其非绝缘的边缘暴露,并且安装在组织切割器导管502的远端。在一些实施例中,导线将组织切割器连接至rf发生器,至少部分地在组织切割器导管502的壁内延伸。在一些实施例中,组织切割器导管502具有与组织稳定器导管505可滑动地接合的中心腔。在一些实施例中,输送导管501具有中心腔,该中心腔与组织切割器导管502可滑动地接合。在一些实施例中,结合了扶正器511,该扶正器511具有安装至组织稳定器导管505的外径和组织稳定器504的内径的中心腔。
在一些实施例中,如图5a所示,在导丝上(未示出)将装置组件推进到体内,直到将组织稳定器导管505的整个盖508a推进到左心房中。在一些实施例中,通过相对于其他装置部件向前推进导管508,使组织稳定器脱鞘并在左心房中展开。在一些实施例中,相对于其他装置部件向后拉动组织稳定器导管505,以使组织稳定器与间隔接触,如图5b所示。在一些实施例中,向后拉动输送导管501,同时装置组件500的其他装置部件保持静止,以使支架组织切割器503在右心房中脱鞘并展开。在一些实施例中,将组织切割器导管502相对于其他装置部件向前推进,直到支架组织切割器与间隔接触,如5c-5d所示。在一些实施例中,组织稳定器和支架组织切割器在间隔的两侧“配合/接合”,以产生夹持效果。在一些实施例中,然后通过rf发生器施加能量,以切除组织并产生孔。在一些实施例中,推动输送导管,以使支架组织切割器重新入鞘,而向后拉动导管508,以使组织稳定器支架504重新入鞘。在一些实施例中,切除的组织被组织稳定器导管505刺穿和保持。在一些实施例中,在施加rf能量之前,使组织稳定器在右心房中展开,并且向远侧推动组织稳定器导管以与间隔接触,而使组织切割器在左心房中展开,并且向近侧拉动组织切割器导管以实现与间隔并置。
具有金属/导线环的支柱
在一些实施例中,如图7a-7b所示,组织切割器包括柔性金属环703,其通过连接至组织切割器导管702的远端的多个径向分布的支柱703d展开成其扩张状态;这些支柱相对于组织切割器导管提供结构刚度和同轴对准。在一些实施例中,金属环在其收缩/初始状态预展开中折叠成标准的褶皱、线圈、多个环/翼瓣、手风琴状、卷曲或直形构型。在一些实施例中,金属环包括导线。在一些实施例中,金属环从柱形管切下。在一些实施例中,金属环包括导电的形状记忆金属。在一些实施例中,金属环包括导电的非形状记忆金属。在一些实施例中,金属环从支柱的末端向后缩进(凹入)固定距离(例如约0.1mm至约10.0mm)。在一些实施例中,金属环具有缠绕在单个支柱周围的较小的环/翼瓣703g。在一些实施例中,金属环的弧长是固定的。在一些实施例中,金属环的端部聚集在一起,并且沿着组织切割器导管的长度延伸,使得金属环作为圈套被致动。
在一些实施例中,组织切割器的支柱包括导电的形状记忆材料,使得它们在释放时(通过其约束导管712/701相对于组织切割器导管702的可滑动平移)张开,从而将金属环扩张到期望的构型,如图7b所示。在一些实施例中,支柱确保金属环与组织切割器导管702之间同轴对准,并且通过延伸确保与装置组件中的所有其他导管(除了导丝706之外)同轴对准。在一些实施例中,支柱预弯曲以在完全扩张时成u形弯曲构型,从而允许支柱向后弯曲大约180°,以使金属环定向成朝向房间隔(当输送至左心房并在其中展开时)。在一些实施例中,支柱是预弯曲的,并且构造成在由径向方向和近端-远端方向确定的平面上扩张为张开的横截面(扩张至比其约束直径大的直径)。在一些实施例中,该横截面具有不同的形状,例如钟形、圆锥形、u形或任何其他几何形状。在一些实施例中,朝向支柱的末端的几何形状的宽度递增,以便于金属环就位。在一些实施例中,朝向支柱的末端的几何形状的宽度递增,它们之间的宽度变窄,以便于金属环就位。在一些实施例中,朝向支柱的末端的几何形状的宽度变窄,且宽度没有递增,以便于金属环就位。在一些实施例中,组织切割器的支柱不包括形状记忆材料,而是通过能量偏置元件(例如弹簧)彼此连接,该能量偏置元件在收缩/受约束时被压缩,而在释放时径向向外张开(通过向后平移其约束导管),从而扩张非形状记忆金属环。在一些实施例中,支柱通过伞状机构机械致动,其中,两个支柱(致动支柱和扩张支柱)通过铰接点连接,并且通过另一铰接点分别连接到致动导管和组织切割器导管,使得当致动导管相对于组织切割器导管向前平移时,致动支柱使扩张支柱通过其铰接点在扩张导管上径向向外旋转。在一些实施例中,该径向扩张将金属环扩张到期望的直径,达到使致动导管平移的程度。另外,在一些实施例中,用致动线滑轮系统代替致动导管,其中,致动线的平移使扩张支柱扩张。在一些实施例中,扩张机构由金属环驱动,而不是由金属环附装到其上的支柱驱动。在一些实施例中,支柱和金属环完全绝缘,或者可替代地,支柱和金属环由非导电材料组成,并且一单独的(导电)金属环固定至绝缘(或非导电)金属环,以用作组织切割器。在一些实施例中,支柱是绝缘的,而金属环是非绝缘的。在一些实施例中,支柱和金属环都部分绝缘。在一些实施例中,包括纺织品、聚合物或金属的细网筛或膜703f结合在组织切割器的支柱之间和/或周围,并且连接至金属环703b,如图7a所示,或者可替代地连接在支柱之间和/或周围但不连接至金属环,或者可替代地在金属环的平面内,或者可替代地在金属环的平面中,但是设置为凹入/缩回,以帮助确保在切割之后将所有切除的组织保持在装置组件中。在一些实施例中,金属环固定至支柱的远侧末端;可替代地,金属环从末端缩回(凹入)固定的距离(例如约0.1mm至约10.0mm)。在一些实施例中,组织切割器在左心房中展开,并且被向近端拉动以接合和切割组织。在一些实施例中,分裂鞘管用于允许组织切割器在左心房中入鞘和脱鞘。在一些实施例中,组织切割器在右心房中展开,并且被向远端推进以接合和切割组织。
在一些实施例中,如图7a-7b所示,组织稳定器704包括一个或多个自扩张(形状记忆)支柱。在一些实施例中,组织稳定器支柱704a的末端被锐化,以允许穿透房间隔。在一些实施例中,组织稳定器支柱的末端是钝的,以防止穿透房间隔。在一些实施例中,组织稳定器704扩张以具有比组织切割器703在完全展开时的扩张直径大的直径。在一些实施例中,组织稳定器扩张以具有比组织切割器在完全展开时的扩张直径小的直径。在一些实施例中,包括纺织品、聚合物或金属的细网筛或膜704f结合在组织稳定器的支柱之间和/或周围,如图7a所示,以帮助确保在切割之后将所有切除的组织保持在装置组件中。在一些实施例中,组织稳定器完全绝缘。在一些实施例中,组织稳定器部分绝缘,使得组织稳定器的(远侧)末端非绝缘以允许rf通电。在一些实施例中,组织稳定器采用球囊、形状记忆网筛、形状记忆线圈和自扩张(例如形状记忆)笼的形式。在一些实施例中,rf阳极放置在患者皮肤上的身体外部的垫片上。在一些实施例中,rf阳极位于房间隔707的近侧,但是在组织稳定器704的远侧。在一些实施例中,rf阳极位于房间隔的远侧,但是在组织稳定器的近侧。在一些实施例中,组织稳定器在右心房中展开,并且被向远侧前进以接触和稳定组织。在一些实施例中,组织稳定器在左心房中展开,并且被向近侧拉动以接触和稳定组织。在一些实施例中,使用分裂鞘管来允许组织稳定器在左心房中入鞘和脱鞘,其中,扩张器末端715连接至扩张器末端导管716。
在一些实施例中,如图20a-20d所示,组织切割器包括柔性金属环2003b,该柔性金属环2003b在扩张导管2009的远端通过一系列锚固点2009b安装至一个或多个支柱2009a,扩张导管2009在其中点及每个支柱的近端和远端处具有铰接点,以在相对于致动导管2010(在其远端处附装至扩张导管2009)平移而轴向压缩时,允许它们向外(径向)弯曲。在一些实施例中,金属环2003b随着支柱的扩张而扩张(图20b-20d)。在一些实施例中,组织切割器在右心房中展开,并且向远侧前进以接合和切割组织,或者可替代地,组织切割器在左心房中展开,并且被向近侧拉动以接合和切割组织。在一些实施例中,支柱和/或导管包括自扩张金属、非自扩张金属、聚合物、或聚合物/金属混合物。在一些实施例中,支柱是绝缘的,而金属环是非绝缘的。在一些实施例中,支柱和金属环都是部分地绝缘。在一些实施例中,当组织切割器在左心房中展开时,不需要单独的组织稳定器或组织稳定器导管。在一些实施例中,当组织切割器在左心房中展开时,使用单独的组织稳定器或组织稳定器导管。
在一些实施例中,如图7a-7b所示,装置组件包括扩张器末端715,以便于装置在导丝上通过并穿过房间隔。
支柱
在一些实施例中,组织切割器包括柔性的金属环,该金属环通过连接至组织切割器导管的远端的一系列支柱展开成其扩张状态。在一些实施例中,金属环在其收缩/初始状态预展开中折叠成标准的褶皱、线圈、环、手风琴状、卷曲或直形构型。在一些实施例中,金属环包括导线。在一些实施例中,金属环从柱形管切下。在一些实施例中,金属环是形状记忆金属。在一些实施例中,金属环从支柱的末端向后缩进(凹入)固定距离(例如约0.1mm至约10.0mm)。在一些实施例中,金属环具有缠绕在支柱周围的较小的环/翼瓣。在一些实施例中,金属环的端部与组织切割器导管相交并沿着该组织切割器导管的长度延伸,使得该环作为圈套被致动。在一些实施例中,这些支柱包括形状记忆材料,使得它们在释放时(通过输送导管相对于组织切割器导管的可滑动平移)张开,从而将金属环打开至期望的(扩张)构型。在一些实施例中,支柱确保金属环与组织切割器导管之间同轴对准,并且通过延伸确保与装置中的所有其他导管(除了导丝之外)同轴对准。在一些实施例中,支柱预弯曲以在完全扩张时成u形弯曲,从而允许支柱向后弯曲大约180°,并且使金属环在输送至左心房并在其中展开时定向成朝向房间隔。
在一些实施例中,支柱不是由形状记忆材料制成,而是通过诸如弹簧的能量偏置元件彼此连接,该能量偏置元件在收缩/受约束时被压缩,而在释放时径向向外张开支柱(通过向后拉动输送导管),从而扩张非形状记忆金属环。
在一些实施例中,这些支柱通过伞状机构机械致动,其中,两个支柱(致动支柱和扩张支柱)通过铰接点连接,并且通过另一铰接点分别连接到致动导管和组织切割器导管,使得当致动导管相对于组织切割器导管向前平移时,致动支柱使扩张支柱通过其铰接点在扩张导管上径向向外旋转。在一些实施例中,该径向扩张将金属环扩张到期望的直径,达到使致动导管平移的程度。另外,在一些实施例中,用致动线滑轮系统代替致动导管,其中,致动线的平移使扩张支柱扩张。
在一些实施例中,金属环包括导电的形状记忆材料,并且通过一系列径向分布的支柱连接至组织切割器导管,该支柱提供结构刚性和相对于组织切割器导管的同轴对准。在一些实施例中,扩张机构由金属环驱动,而不是由金属环附装于其上的支柱驱动。在一些实施例中,支柱和金属环都由导电的形状记忆材料组成,其中,支柱是绝缘的,而金属环是非绝缘的。在一些实施例中,支柱和金属环部分绝缘。在一些实施例中,支柱和金属环完全绝缘,或者由非导电材料制成,并且将一单独的(导电)金属环固定至绝缘(或非导电)金属环,以用作组织切割器。
在一些实施例中,包括纺织品、聚合物或金属的细网筛结合在支柱之间,并且连接至金属环,或者在金属环的平面内,或者平行于组织平面和/或金属环,但是缩回,以帮助确保在切割之后将所有切除的组织保持在装置组件中。在一些实施例中,金属环固定至支柱的远侧末端;可替代地,金属环从末端缩回(凹入)固定的距离(例如约0.1mm至约10.0mm),以在支柱末端与组织接合时在金属环与组织之间确保小的限定间隙。
具有金属环的笼
在一些实施例中,如图19a-19b所示,组织切割器在自扩张(形状记忆)笼1903p的表面(例如远侧表面或远端表面)上包括柔性金属环1903b,该自扩张(形状记忆)笼1903p在右心房中展开,从而使金属环扩张。在一些实施例中,金属环安装在笼的远侧表面上,使其与房间隔1907接触。在一些实施例中,笼支柱的近端连接至组织切割器导管1902的远端,导管1902具有中心腔,致动导管1914可滑动地接合在该中心腔中。在一些实施例中,包括笼表面的支柱的中心端连接到致动导管1914。在一些实施例中,输送导管1901具有中心腔,并且与组织切割器导管可滑动地接合。在一些实施例中,通过向近侧拉动输送导管并允许自扩张笼展开,或者通过使致动导管相对于组织切割器导管向近侧滑动的机械致动来展开笼。在一些实施例中,rf阳极放置在组织保持元件1904上、组织保持元件导管1905上、或者在患者皮肤上的身体外部的垫片上。在一些实施例中,金属环包括形状记忆材料,并且在从输送导管释放时驱动笼完全扩张。在一些实施例中,将多个柔性的电绝缘的金属环安装至笼的近侧或远侧表面,每个金属环在笼扩张时具有特有的扩张尺寸,其范围从约2mm至约5mm,使得通过选择性地将rf能量引导到与期望的孔尺寸相对应的金属环上来切除组织。
在一些实施例中,组织切割器在自扩张(形状记忆)笼的近侧表面(如果在右心房中展开)或远侧表面(如果在左心房中展开)上包括柔性金属环,在导丝上将该自扩张笼放置成穿过间隔。在一些实施例中,导管包括盖和轴。在一些实施例中,导管轴具有中心腔,该中心腔与导丝可滑动地接合。在一些实施例中,导管盖具有锥形的末端,以便于导管从右心房穿过间隔(在导丝上)到达左心房。在一些实施例中,导管盖具有容纳收缩的笼的第二腔。在一些实施例中,笼在左心房中扩张,从而使金属环扩张,使其被rf通电以切割组织。在一些实施例中,金属环放置在笼的近侧表面上,使其与间隔接触,或者放置在笼的弯曲表面周围,使得当近侧表面与间隔接触时,在金属环与组织之间保持小的限定间隙。在一些实施例中,rf阳极采用环形电极的形式,并且沿着组织切割器导管靠近间隔放置,或者放置在位于右心房中的其他装置部件上。在一些实施例中,不需要单独的组织稳定器或组织稳定器导管,因为这些功能由安装有金属环的笼执行。在一些实施例中,当组织切割器在左心房中展开时,不需要单独的组织稳定器或组织稳定器导管。
线圈和卷
在一些实施例中,如6a-6b所示,组织切割器采用自扩张线圈603a的形式,该自扩张线圈603a在右心房内从输送导管601展开时直径扩大并且缩短(例如沿着近侧-远侧轴线)。在一些实施例中,当组织切割器导管602保持静止时,线圈603a随着输送导管601被向后拉动而自扩张。在一些实施例中,输送导管601具有与组织切割器导管602可滑动地接合的腔。在一些实施例中,组织切割器导管602具有为导丝606提供通道的腔,线圈安装至组织切割器导管602。在一些实施例中,线圈的环的尺寸确定成校正其在组织切割器导管602中的偏心定位。在一些实施例中,除了远端的圆形线圈之外,线圈通过绝缘体603h绝缘,使得在线圈完全展开时构成闭合的电极环(rf阴极)603b。在一些实施例中,线圈通过在组织切割器导管(未示出)的壁内延伸的导线在其近端连接至rf发生器。在一些实施例中,线圈具有两个磁体603c,该磁体603c在线圈充分暴露时联接,以构成闭合的多边形或圆形环。在一些实施例中,电极603b在展开时被朝向房间隔607推进并被通电,切除的组织栓塞保持穿在导丝上。在一些实施例中,自扩张线圈的弹簧状形状为切割器603提供了提高的推动能力,以在电极和间隔之间实现并置。
在一些实施例中,组织稳定器(未示出)将在左心房中展开。在一些实施例中,组织稳定器导管与组织切割器导管602的腔可滑动地接合。在一些实施例中,组织稳定器导管具有腔,该腔为导丝606提供了通道。当导丝位于左心房中时,组织稳定器导管可以穿过房间隔,并且在左心房中展开;组织稳定器导管可以缩回到组织切割器导管中。在一些实施例中,组织切割器603可以在右心房中展开;组织切割器和组织稳定器都与房间隔接触,将该间隔夹在中间。
在一些实施例中,如图8所示,组织切割器是自扩张线圈(形状记忆)803a,当将其从组织切割器导管802(其第一腔802a)向前推出时,该自扩张线圈803a最初径向向外弯曲,最终构成与间隔接触的闭环电极803b。在一些实施例中,仅电极环暴露且非绝缘,绝缘体803h沿着线圈可滑动地接合在组织切割器导管的第一腔中的长度覆盖连接到环的线圈。在一些实施例中,两个磁体(未示出)位于暴露的非绝缘线圈的始端和末端,其联接以构成闭环电极。在一些实施例中,组织切割器导管802具有如图8所示的双级腔;其第二腔802b与组织保持元件导管805可滑动地接合,其第一腔802a容纳自扩张线圈。在一些实施例中,环的直径足够大,使得尽管其偏心定位,环也可以在组织保持元件上行进。在一些实施例中,组织保持元件的直径比电极环的直径小。在一些实施例中,组织切割器导管的两个腔的尺寸/直径彼此相似。在一些实施例中,第一腔比第二腔小或大。在一些实施例中,自扩张线圈的尺寸确定成校正其在组织切割器导管802中的偏心定位。在一些实施例中,在线圈展开之前,任何上述组织保持元件804在左心房中展开。在一些实施例中,组织保持导管具有与导丝806可滑动地接合的腔。
在一些实施例中,自扩张线圈在右心房中展开。在一些实施例中,组织切割器导管802将在导丝806上穿过间隔,以使组织保持元件在左心房中展开。在组织保持元件展开之后,在一些实施例中,组织切割器导管在右心房中缩回,并且通过向远侧推动线圈来展开自扩张线圈803a。在一些实施例中,在施加rf能量之前,使组织保持元件和组织切割器都与间隔接触以实现并置。在通电之后,在一些实施例中,在自扩张线圈缩回到组织切割器导管的第一腔802a中之后,组织栓塞保持穿在组织保持导管805上,并且被包装在输送导管801中。
在一些实施例中,自扩张线圈在左心房中展开。在一些实施例中,组织切割器导管802在导丝806上穿过间隔,以使组织保持元件在左心房中展开。在组织保持元件展开之后,在一些实施例中,通过向远侧推动线圈使自扩张线圈803a在左心房中展开。在一些实施例中,在环形电极803b展开之后,组织切割器导管缩回右心房中。在一些实施例中,在施加rf能量之前,使电极环与间隔接触以实现并置,组织保持元件保持远离电极环。在一些实施例中,在通电之后,在自扩张线圈缩回到组织切割器导管的第一腔802a中之后,组织栓塞保持穿在组织保持导管805上,并且被包装在输送导管801中。
在一些实施例中,如图21所示,组织切割器采用卷状薄片2103q的形式,该卷状薄片2103q除了其至少一部分远端之外完全绝缘2103h。在一些实施例中,在从输送导管2101展开时,薄片展开,并且远端扩张,以具有更大的直径。在一些实施例中,薄片的近端附装至组织切割器导管2102。在一些实施例中,薄片包括自扩张(形状记忆)金属。在一些实施例中,结合有本文所述的任一种组织保持元件2104,以捕获和保持切除的组织。
在一些实施例中,组织切割器采用连接至一个或多个自扩张支柱的一个或多个单点电极的形式,该自扩张支柱在展开时从组织切割器导管向外(径向)扩张,使得在rf通电和组织切割器旋转时,产生尺寸精确的心房间孔。在一些实施例中,通过向近侧拉动输送导管以使组织切割器导管脱鞘,从而展开自扩张支柱。在一些实施例中,组织切割器导管具有中心腔,并且与穿过间隔的组织保持元件导管可滑动地接合,以使组织保持元件2104在左心房中展开。
在一些实施例中,如图22所示,组织切割器采用安装在一个或多个扩张支柱2203r上的一个或多个单点电极2203b的形式,该扩张支柱2203r通过伞状机构机械致动,并且由扩张导管2209锚固或支撑。在一些实施例中,两个支柱——致动支柱2203s和扩张支柱——用作单臂,并且通过铰接点2203t连接;支柱分别通过铰接点连接到致动导管2214和扩张导管。在一些实施例中,致动导管相对于扩张导管平移,以通过致动支柱使扩张支柱从其在扩张导管上的铰接点向外(径向)旋转。在一些实施例中,扩张支柱是自扩张式,使得当脱鞘时,支柱从扩张导管向外(径向)扩张,从而不需要致动导管和致动支柱。在一些实施例中,通过向近侧拉动输送导管2201以使扩张导管脱鞘,从而展开自扩张支柱。在一些实施例中,扩张导管具有中心腔,并且与穿过房间隔的组织保持元件导管2205可滑动地接合,以使组织保持元件2204在左心房中展开。在扩张之后,在rf通电和组织切割器旋转时,产生尺寸精确的心房间孔。
在一些实施例中,如23a-23c所示,组织切割器2303采用一个或多个支柱2309a的形式,该支柱2309a扩张成在扩张导管2309的远端处的一系列铰接点2309b处具有弯曲构型。在一些实施例中,一个或多个电极2303b固定或以其他方式附装在支柱的铰接点处。在一些实施例中,支柱朝向扩张导管2309的远端定位。在一些实施例中,铰接点位于每个支柱的中点和/或近端和远端处;当致动导管2314相对于扩张导管平移时,这些铰接点允许支柱径向向外弯曲。在一些实施例中,在扩张之后,电极与房间隔接触;随后在rf通电和组织切割器旋转时,产生尺寸精确的心房间孔。在一些实施例中,组织切割器定位于右心房中,组织保持元件(未示出,位于左心房中)捕获并保持切除的组织。在一些实施例中,组织切割器位于左心房中,并且定向成使得电极面对房间隔;在组织切割之后,组织切割器捕获并保持切除的组织,从而兼作组织保持元件。在这些实施例中,支柱包括自扩张金属、非自扩张金属、聚合物或聚合物/金属混合物。
在其他实施例中,现在参考图24a-24b,该装置组件包括输送导管2401、电极导管2402、组织稳定器导管2405和远端扩张器导管(未示出),部分绝缘的电极2403附装至该电极导管2402,该电极2403具有阴极2403b,并且包括电极支柱部分2403d1、d2、d3,绝缘的组织稳定器2404附装至该组织稳定器导管2405,该组织稳定器2404具有稳定环2404b,并且包括组织稳定器支柱部分2404d1、d2、d3、d4,包括扩张器末端2408d和扩张器轴2408e的远端扩张器2408附装至该远端扩张器导管。远端扩张器导管的内腔与尺寸在0.014英寸至0.035英寸之间的任何现成的导丝2406可滑动地接合并且可以在该导丝2406上平移。在诸如图24a-28k所示的实施例中,装置的阳极被包括为与rf发生器以及由此与组织切割器的rf阴极电连通的后贴片。可替代地,组织稳定器可以包括阳极部分,例如环2404b,或者稳定器或装置的另一部分。
如图24c所示,当在横截面中从装置的近端向远端看时,远端装置组件包括:1)远端扩张器腔2408f,以允许利用扩张器导管2408g在导丝上平移,2)远端扩张器导管2408;3)电极导管2402,4)与电极导管邻接的电极附装部分2403t,5)嵌入式绝缘电源线2402c,6)组织稳定器附装部分2404t,7)远端扩张器轴2408e,8)输送导管腔2401a中的输送导管2401,9)电极支柱部分2403d1,10)电极切割部分2403b,11)组织稳定器支柱部分2404d1,12)组织稳定器稳定部分或环2404b,和13)组织稳定器导管腔2405b内的组织稳定器导管2405。
在一些实施例中,电极用作rf阴极。放置在身体表面的接地垫片用作rf阳极。在一些实施例中,rf阳极以非绝缘区段或者非绝缘的基于金属的不透射线的标记环或带(例如铂、铂铱合金、金、镍钛合金(镍钛诺)和/或钯)的形式在组织稳定器的附装部分处结合在组织稳定器中。在一些实施例中,rf阳极可替代地以基于金属的不透射线的标记环、带或油墨(例如铂、铂铱合金、金、镍钛诺和/或钯)的形式结合在输送导管的远侧末端中。
电极组件
电极-设计
如图25a-25b所示,电极2503采用单部件支架的形式,该单部件支架由超弹性形状记忆合金(也称为伪弹性行为材料)组成,例如镍钛合金/镍钛诺(替代合金包括铜铝合金、铜铝镍合金、铜铝铍合金和铜锌铝合金);电极是从壁厚在0.05mm至0.30mm之间、直径在1.0mm至1.8mm之间的管激光切割而成,具有特定的激光切割图案(图25a),并且热定型为特定的扩张形式(如图24a和24b所示,参考2403),其允许部件的一端在释放时扩张成直径介于4.0mm至12.0mm之间的更大尺寸,而另一端保持从其被切割下来的管的尺寸,以提供附装其相应的导管(例如2808z)的刚性主体。电极主要从单个管上激光切割而成,通常没有离散的部分;然而,以三个主要部分(图25a所示)描述了电极的主网格结构:(1)切割部分2503b、(2)支柱部分2503d、和(3)附装部分2503t。
(1)切割部分2503b在释放时具有平坦/平面的环状构型,其具有直径在4.0mm至12.0mm之间的扩张尺寸。切割部分与间隔的左心房表面接触,并且在通过射频(rf)能量通电时在其近侧表面上产生等离子体。在一些实施例中,当通过rf能量传导支柱通电时,切割部分在其近侧表面(与间隔2407接触的表面)上产生一层等离子体。切割部分的尺寸小导致这种效果;将在下文和本文其他地方描述这种尺寸,即宽度和直径(在相乘时得到表面积)。在一些实施例中,切割部分具有到支柱的一系列附装点和应力释放区段,该应力释放区段的形状确定成允许电极以可预测的方式折叠和展开,而不会塑性屈服、变形或破裂。切割部分到支柱的附装点具有厚度从0.140mm可变地减小到0.065mm的圆形交叉点,并且以90°角连接到支柱,以确保切割部分和支柱之间的持久连接,从而防止在电极的扩张和收缩期间断裂。切割部分的应力释放区段的尺寸确定成使其在受约束时的弯曲半径最大(0.02mm至1.40mm),以使扩张过程中的挠曲最小。切割部分的宽度在0.05mm至0.25mm之间,以在rf通电和切割期间抵抗热损伤,使得电极保持结构完整性以允许在切割之后收缩。在一些实施例中,切割部分替代地扩张成非圆形的横截面轮廓,例如椭圆形、三角形、正方形、六边形、八边形或其他多边形。然而,在本文的实施例中,切割部分在电极收缩时沿着径向和周向向内折叠,从而将切除的组织牢固地抓在其腔内。在一些实施例中,切割部分非电绝缘,或者替代地,仅在其远端表面上电绝缘。
(2)支柱部分2503d允许电极扩张和收缩,在释放时以及在rf通电和切割期间提供轴向和周向强度,并且将rf能量从附装部分传递至切割部分。通过借助远端扩张器的平移和/或旋转来释放或约束电极,支柱允许电极扩张和收缩,使得支柱当其在远端扩张器中收缩时使切割部分收缩。在一些实施例中,多个支柱在2mm至20mm之间径向分布,每个支柱的宽度在0.2mm至2.5mm之间,厚度相似地在0.2mm至2.5mm之间。支柱是刚性的,以在rf通电和切割过程中,当支柱与间隔的左心房表面接触并且受到张力时抵抗电极的意外收缩。本文提到的厚度和宽度与材料选择(在该示例中为镍钛诺)相结合,产生了足够的刚度。本文中提到的尺寸相似的其他材料替代地具有足够的刚性。支柱具有足够的柔性,以允许通过远端扩张器相对于电极的有意平移和/或旋转来有意收缩。类似地,厚度和宽度与材料选择(在该示例中为镍钛诺)相结合,产生了足够的柔性。替代地,本文中提到的尺寸相似的其他材料具有足够的柔性。支柱通过一个或多个可扩张的周向环连接,以在电极的展开状态下增加电极的刚度。在本文提供的一些实施例中,切割器是基于能量的而非基于机械的(锋利的刀片),支柱是电绝缘的,以防止电流泄漏,使得将传输到附装部分的所有rf能量传导至切割部分,除了支柱的近端边缘,以便于在rf通电和切割期间产生等离子体。
(3)附装部分2503t允许将电极联接到其相应的导管(例如2408g)和电源线(例如2402c),并且使电极与所有其他装置/系统部件同轴对准。图25的实施例中的附装部分至少在电极的远端处包括凹入的切口2503v,以便于电源线的薄型附装。电源线通过焊接、与激光或焊机的热链接、钎焊或机械锻造而电联接到电极的附装部分,以在电极和电源线之间提供持久且一致的电连接,以确保通过电源线传输的所有rf能量相应地传导至附装部分和电极的其余部分。在一些实施例中,附装部分在其远端处具有一个或多个切口2503u,其具有直径在0.5mm至2.0mm之间的扩张尺寸,以便于胶水或塑料回流(reflow),从而允许将电极持久地附装至其相应的导管上。附装部分的刚性特性允许电极与其相应的导管中心对准,使电极组件与所有其他装置/系统部件有效对准,从而确保电极与组织稳定器和输送导管同轴对准。电联接有电源线的附装部分是电绝缘的,以防止电流泄漏,使得将所有rf能量传输到电极的切割部分。电源线由铜基导线(例如铜、铜包钢)组成,并且可能具有绝缘涂层(例如聚酰亚胺、聚酰胺-酰亚胺)。包括电源线的导线规格在40awg至20awg之间。
如图25b所示,电极可以具有次级网格结构,以在其扩张状态下增加结构刚性。虽然电极主要从单个管激光切割而成,并且通常没有离散的部分,但是认为该次级网格结构包括交织在主网格结构中的u形部分(2503w)、y形部分(2503x)和r形部分(2503y)的连接阵列。r形部分连接到主网格结构的支柱。u形部分不直接连接到主网格结构。y形部分在其基部或顶点处具有伸出的臂部。在一些实施例中,完整的阵列包括或包含串联连接的部分r、u^n、y、u^n和r,其中n是任何整数。其他实施例在支柱之间可以具有重复m次的(r、u^n、y、u^n、r)^m完整阵列部分。与电极的远端处的切口2503v柱形对准的y形部分可以在其远端处具有附加的u形区段,该u形区段将y形部分桥接到附装部分处的凹入切口2503v的任一侧。u形、y形和r形部分的连接阵列可以沿着支柱的长度在任何位置连接到支柱,以调整在电极上增加结构刚度的位置。在一些实施例中,次级网格结构在支柱部分的长度上包括多个u形、y形和r形部分的连接阵列。另外,在这些实施例中,y形部分可以连接到另一y形部分,或一直连接到电极的附装部分。重要的是,在每个可能的阵列排列中,每个y形部分的连接臂部分是阵列中最靠近电极附装部分的部分。这种设计确保了当电极与扩张器导管收缩时,次级结构也关闭,以防止扩张器导管沿着电极平移时它们被扩张器导管卡住。在可替代的实施例中,次级结构的阵列没有y形部分,但是该阵列被热定型成在完全打开时进一步径向向内倾斜,以确保次级阵列在组织稳定器通过输送导管收缩时完全收缩。次级网格结构旨在增加部件对在致动期间因剪切力、压缩力和张力而变形的抵抗力,而不影响通过电极启动等离子体切割的功率需求,因为次级网格结构旨在完全绝缘。次级网格结构的每个连接阵列的弧长的长度并不在物理上限制电极可以扩张和收缩的程度。在一些实施例中,阵列的弧长具有不同的长度,越接近电极切割部分,其长度越短或更长,以确保阵列的弧长允许支架完全打开,同时还提供了附加的稳定性。由于电极从相同的起始图案及其热定型激光切割而成,因此,次级网格结构的折叠和打开设计成不会在其扩张和收缩时以任何方式撞击主网格结构。次级网格结构改善了电极的机械性能,并且用作栓塞保护机构——网格有效地减小了电极支柱之间的孔径,栓塞流过该孔并流入全身血管。
电极-电绝缘体
施加到电极上的电绝缘体包括厚度在5μm至30μm之间的电介质涂层,并且提供了介电强度以在rf通电和切割期间抵抗电介质击穿。电极上的绝缘体是柔性的,以免损害电极的柔性。
在一些实施例中,施加到电极的电绝缘体包括或包含化学气相沉积的聚对二甲苯聚合物(例如聚对二甲苯c、聚对二甲苯n)、聚氨酯(pu)、聚四氟乙烯(ptfe)、膨体聚四氟乙烯(eptfe)、聚酰亚胺(pi)、聚酯、聚对苯二甲酸乙二醇酯(pet)、硅树脂、或上述任何材料的共聚物。
电极-导管
附装至电极的导管2402是双腔导管。主腔可以具有ptfe衬里,以便于相对于远端扩张器导管的润滑平移和/或旋转。在一些实施例中,主腔的增强可以包括或包含具有硬度更高的机织或编织材料,例如尼龙或不锈钢,以提高导管的可推动性和柔性。次级腔可以具有pi衬里,电源线被限制在其中,以使电源线与所有其他装置/系统部件和身体电隔离。在一些实施例中,结合有聚合物护套以覆盖两个腔,该护套具有从10d到90d(肖氏值)的高硬度,以在保持柔性的同时使导管的可推动性最大化,并且回流以使电极导管具有圆形的横截面轮廓。
通过使外部聚合物护套经过电极的附装部分的切口回流到内部聚合物衬里,将电极牢固地附装至电极导管,从而封装和电隔离电源线。
电极导管可以替代地是单腔导管。
电极导管在其远侧末端处具有基于金属的不透射线的标记,该标记可以采用环、带或油墨(例如铂、铂铱合金、金、镍钛诺、钯)的形式,以允许荧光透视可见。
电极-栓塞保护
电极在其支柱之间或周围可以具有过滤器或膜,以捕获在rf通电和切割期间或之后可能产生的微粒和栓塞。在一些实施例中,过滤器或膜可以包括或包含孔径在0.001mm至1.000mm之间的浸涂pu,以允许捕获颗粒,同时允许血液流经膜。在一些实施例中,过滤器或膜可替代地包括或包含“蛤壳式夹合(clamshelled)”在支柱周围的机织或编织的pet、ptfe、eptfe或eptfe膜,其孔径在0.001mm至1.000mm之间。过滤器或膜可替代地包括孔径在0.001mm至1.000mm之间的机织或编织的镍钛诺网。
组织稳定器组件
组织稳定器-设计
组织稳定器2604采用由诸如镍钛诺(替代合金包括铜铝合金、铜铝镍合金、铜铝铍合金和铜锌铝合金)的超弹性形状记忆合金组成的单部件支架的形式;组织稳定器是从壁厚在0.05mm至0.30mm之间、直径在1.5mm至2.5mm之间的管激光切割而成,具有特定的激光切割图案(图26),并且热定型为特定的扩张形式(如图24a-24b所示,参考2404),它允许部件的一端在释放时扩张成直径介于5.0mm至18.0mm之间的更大尺寸,而另一端保持从其被切割下来的管的尺寸,以提供附装其相应的导管的刚性主体。
组织稳定器从单个管上激光切割而成,通常没有离散的部分;然而,在一些实施例中,组织稳定器的主网格结构由三个部分组成(如图26所示):(1)稳定部分或环2604b、(2)支柱部分2604d、和(3)附装部分2604t。
(1)稳定部分或环2604b在释放时具有平坦/平面的环状构型,其具有直径在5.0mm至18.0mm之间的扩张尺寸。稳定部分与间隔的右心房表面接触,以在rf通电和切割过程中使间隔张紧。在一些实施例中,稳定部分具有到支柱的一系列附装点和应力释放区段,该应力释放区段的形状确定成允许组织稳定器以可预测的方式折叠和展开,而不会塑性屈服、变形或破裂。在图26的实施例中,稳定部分到支柱的附装点至少具有厚度从0.140mm可变地减小至0.065mm的圆形交叉点,并且以90°角连接到支柱,以确保稳定部分和支柱之间的持久连接,从而防止在组织稳定器的扩张和收缩期间断裂。稳定部分的应力释放区段的尺寸确定成使其在受约束时的弯曲半径最大(0.02mm至1.40mm),以使扩张过程中的挠曲最小。稳定部分的宽度和/或厚度在0.05mm至0.25mm之间,以便当其在通过电极进行rf通电和切割期间使间隔张紧时抵抗热损伤,使得组织稳定器保持结构完整性以允许在切割之后收缩。在一些实施例中,稳定部分替代地扩张成非圆形的横截面轮廓,例如椭圆形、三角形、正方形、六边形、八边形或其他多边形。稳定部分在组织稳定器收缩时向内和周向地折叠,从而将电极和切除的组织牢固地抓在其腔中。稳定部分完全非电绝缘。
(2)支柱部分2604d允许组织稳定器扩张和收缩,在释放时以及在rf通电和切割期间提供轴向和周向强度,并且在切割之后封装电极和切除的组织,从而防止电极接触任何意外的心内结构。通过相对于输送导管平移和/或旋转来释放或约束组织稳定器,支柱允许组织稳定器扩张和收缩,使得支柱当其在输送导管中收缩时使稳定部分收缩。多个支柱在2-20mm之间径向分布,每个支柱的宽度在0.2mm至2.5mm之间,厚度在0.2mm至2.5mm之间。支柱具有足够的刚性,以在rf通电和切割期间,当组织稳定器与间隔的右心房表面接触并处于张力下时,抵抗组织稳定器的意外收缩。本文提到的厚度和宽度与材料选择(在该示例中为镍钛诺)相结合,产生了足够的刚度。本文中提到的尺寸相似的其他材料替代地具有足够的刚性。支柱具有足够的柔性,以允许通过输送导管在相对于组织稳定器平移和/或旋转时收缩。本文提到的厚度和宽度与材料选择(在该示例中为镍钛诺)相结合,产生了足够的柔性。本文提到的尺寸相似的其他材料替代地具有足够的柔性。当稳定器不用作阳极或阴极时,支柱完全电绝缘,以在rf通电和切割过程中以及在切割之后在电极上收缩期间防止电弧。在这种实施例中,外部贴片附装至患者,例如附装至其皮肤(例如其背部),并且电联接至rf发生器,如本文中所描述的那样。
(3)在一些实施例中,附装部分2604t允许组织稳定器与其相应的导管和所有其他装置/系统部件同轴对准。在一些实施例中,附装部分在其近端处具有一个或多个切口2604u,其具有直径在0.5mm至2.0mm之间的扩张尺寸,以便于胶水或塑料回流,从而允许将组织稳定器持久地附装至其相应的导管上。在一些实施例中,附装部分的刚性特性允许组织稳定器与其相应的导管中心对准,这使组织稳定器组件与所有其他装置/系统部件有效对准,从而确保组织稳定器与电极和输送导管同轴对准。在一些实施例中,附装部分完全电绝缘,以在rf通电和切割期间防止从电极产生电弧。
在一些实施例中,组织稳定器具有次级网格结构,以在其扩张状态下增加结构刚性。虽然组织稳定器通常从单个管激光切割而成,并且通常没有离散的部分,但是认为这种次级网格结构包括交织在主网格结构中的u形、y形和r形部分的连接阵列。r形部分连接到主网格结构的支柱。u形部分不直接连接到主网格结构。y形部分在其基部或顶点处具有伸出的臂部。在一些实施例中,完整的阵列可以包括或包含串联连接的部分r、u^n、y、u^n和r,其中n是任何整数。其他实施例在支柱之间可以具有重复m次的(r、u^n、y、u^n、r)^m完整阵列部分。u形、y形和r形部分的连接阵列可以沿着支柱的长度在任何位置连接到支柱,以调整在组织稳定器上增加结构刚度的位置。在不同的实施例中,在一些实施例中,次级网格结构在支柱部分的长度上可以包括或包含多个u形、y形和r形部分的连接阵列。在这些实施例中,y形部分可以连接到另一y形部分,或一直连接到主网格结构的附装部分。重要的是,在每个阵列中,每个y形部分的连接臂部分是阵列中最靠近组织稳定器附装部分的部分。这种设计确保了当组织稳定器与输送导管收缩时,次级结构也关闭,以防止输送导管沿着组织稳定器平移时它们被输送导管卡住。在可替代的实施例中,次级结构的阵列没有y形部分,但是该阵列被热定型成在完全打开时进一步径向向内倾斜,以确保次级阵列在组织稳定器通过输送导管收缩时完全收缩。次级网格结构旨在增加对在致动期间因剪切力、压缩力和拉力而变形的抵抗力。次级网格结构的每个连接阵列的弧长足够长,使得其不在物理上限制组织稳定器可以完全打开和关闭的程度。在一些实施例中,阵列的弧长具有不同的长度,越接近组织稳定器稳定部分开口端,其长度越短或更长,以确保阵列具有足够的弧长来允许部件完全打开,同时还增加了部件的稳定性。由于它们都从相同的起始图案切割而成,因此,次级网格结构的折叠和打开旨在不会在其扩张和收缩时以任何方式撞击主网格结构。
次级网格结构改善了组织稳定器的机械性能,并且用作小栓塞保护机构——它有效地减小了组织稳定器支柱之间的孔径,栓塞流过该孔并流入全身血管。
在一些实施例中,组织稳定器用于通过将装置的远端平移到输送导管中来吞没切除的组织和电极,使得输送导管最初使组织稳定器收缩,这继而引起组织稳定器的支柱和次级网格结构在电极上施加径向压缩,继而在切除的组织上施加径向压缩,从而允许在一个运动中通过输送导管吞没所有三个部件。
在一些实施例中,电极和组织稳定器在切割之后通过一系列钩或突片的接合而“相配合”。这些钩或突片可以沿着组织稳定器的支柱部分周向结合,使得当电极平移到组织稳定器的口部中时,钩/突片通过电极切割部分接合。在接合之后,切下的组织保持在相配合的笼中。通过机械地联接电极和组织稳定器,可以通过推进输送导管使整个系统有效收缩。在该实施例的替代方案中,将突片结合到电极中,并且与组织稳定器上的结构配合,以实现相似的联接。在一些实施例中,通过远端扩张器导管的平移使相联接的系统收缩。
组织稳定器-电绝缘体
在一些实施例中,施加到组织稳定器上的电绝缘体包括厚度在5μm至30μm之间的电介质涂层,并且提供了介电强度以在rf通电和切割期间抵抗电介质击穿。电极上的绝缘体是柔性的,以免损害电极的柔性。
在一些实施例中,施加到组织稳定器的电绝缘体可以包括或包含化学气相沉积的聚对二甲苯聚合物(例如聚对二甲苯c、聚对二甲苯n)、pu、ptfe、eptfe、pi、聚酯、pet、硅树脂、或上述任何材料的共聚物。
组织稳定器-导管
在一些实施例中,附装至组织稳定器的导管2405是单腔导管。其腔可以具有ptfe衬里,以便于相对于电极导管的润滑平移和/或旋转。结合有聚醚嵌段酰胺(peba)护套以增强腔,该护套具有从10d到90d(肖氏值)的高硬度,以使导管的可推动性和柔性最大化,并且回流以使组织稳定器导管具有圆形的横截面轮廓。
在一些实施例中,通过使外部聚合物护套通过组织稳定器的附装部分的切口回流到组织稳定器导管的内部聚合物衬里,将组织稳定器牢固地附装到组织稳定器导管,从而封装组织稳定器的附装部分。
组织稳定器导管可以替代地采用双腔导管的形式。在这种实施例中,第二腔将容纳导线,以用作将rf能量传输到位于组织稳定器上的rf阳极的回路路径。该导线由铜基导线(例如铜、铜包钢)组成,并且可能具有绝缘涂层(例如pi、聚酰胺-酰亚胺)。导线规格在40awg至20awg之间。
在一些实施例中,组织稳定器导管在其远侧末端处具有基于金属的不透射线的标记,该标记可以采用环、带或油墨(例如铂、铂铱合金、金、镍钛诺、钯)的形式,以允许荧光透视可见。
组织稳定器-栓塞保护
在一些实施例中,组织稳定器在其支柱之间或周围具有过滤器或膜,以捕获在rf通电和切割期间或之后可能产生的微粒和栓塞。在一些实施例中,过滤器或膜包括或包含孔径在0.001mm至1.000mm之间的浸涂pu,以允许捕获颗粒,同时允许血液流经膜。过滤器或膜可替代地包括蛤壳式夹合在支柱周围的机织或编织的pet、ptfe、eptfe或eptfe膜,其孔径在0.001mm至1.000mm之间。过滤器或膜可替代地包括孔径在0.001mm至1.000mm之间的机织或编织的镍钛诺网。
远端扩张器组件
远端扩张器-设计
远端扩张器2408由两个部分组成:(1)扩张器轴2408e和(2)扩张器末端2408d。
(1)扩张器轴2408e由具有高硬度(肖氏值为10d至90d)的聚合物组成,以便于电极收缩。在一些实施例中,扩张器轴是透明的,以允许在装置/系统插入体内之前在其收缩状态下观察电极。在一些实施例中,扩张器轴由pet、peba、聚醚醚酮(peek)、ptfe、硅树脂、聚苯乙烯(ps)、pu、乳胶或其共聚物组成。扩张器轴替代地可以具有朝向其近端径向分布的切口,从而允许过渡到更大的尺寸,以适应切割之后电极和切除组织的收缩和堆积。扩张器轴替代地可以具有朝向其近端的由合金(例如镍钛诺、不锈钢)构成的嵌入式重叠的不协调的环,从而允许过渡到更大的尺寸,以适应切割之后电极和切除的组织的收缩和堆积。扩张器轴替代地可以在其近端具有一定长度的柔性材料(例如硅氧烷、聚氨酯或pebax),从而允许过渡到更大的尺寸,以允许在切割之后电极与切除的组织一起收缩和堆积。在一些实施例中,扩张器掺杂有不透射线的聚合物,或者具有嵌入式不透射线的金属带,以允许在荧光透视成像下可视化。
(2)扩张器末端2408d附装至扩张器轴,并且轮廓无创伤,以使左心房中的任何意外损坏或刺穿最小化。在一些实施例中,扩张器末端的锥度在1°至45°之间,以便于装置穿过间隔到达左心房。在一些实施例中,扩张器轴包括pet、peba、peek、ptfe、硅酮、ps、pu、乳胶、或者其共聚物或组合。在一些实施例中,扩张器末端在其远侧末端处具有基于金属的不透射线的标记,该标记可以采用环、带或油墨(例如铂、铂铱合金、金、镍钛诺、钯)的形式,以允许荧光透视可见。扩张器轴和末端可以替代地制造成单个部件,并且包括聚丙烯、pet、peba、peek、ptfe、硅树脂、ps、pu、乳胶、硫酸钡(或硫酸盐)或者其共聚物或组合。在一些实施例中,远端扩张器与输送导管的远端配合。远端扩张器可以替代地位于输送导管之内和之外,并且可以自由平移。
远端扩张器-导管
在一些实施例中,附装到远端扩张器的导管是单腔的薄壁pi导管。远端扩张器导管可以具有ptfe衬里,以便于相对于导丝2406的润滑平移和/或旋转。在一些实施例中,远端扩张器通过塑料回流、包塑或胶水牢固地附装至远端扩张器导管。
装置/系统输送导管
输送导管-设计
在一些实施例中,输送导管2401是可转向导管,其具有单个主腔和用于牵引线的通道。其腔2401a具有ptfe衬里,以便于相对于组织稳定器导管的润滑平移和/或旋转。在一些实施例中,分别使用具有高硬度和每英寸交叉(pic)数量的机织或编织不锈钢来增强该腔,并且使导管的可推动性和柔性最大化。输送导管可以具有预定的远端弯曲形状。在一些实施例中,输送导管可以经由沿着其轴的长度嵌入的一根或多根牵引线来转向或偏转(单向、双向、四向或全向地)。输送导管的弯曲半径可以在45°至270°之间。在一些实施例中,输送导管在远侧末端处具有基于金属的不透射线的标记环或带(例如铂、铂铱合金、金、镍钛诺和/或钯),以允许荧光透视可见。不透射线的标记环或带附加地提供了箍紧强度,以在切割之后便于组织稳定器收缩。在一些实施例中,输送导管在其远侧末端处具有不透射线的标记油墨,以允许荧光透视可见。
在rf阳极结合到输送导管的远侧末端中或结合到组织稳定器的一部分(例如稳定环2404b)中的实施例中,输送导管包括导线,以用作将rf能量传输到rf阳极的返回路径。该导线由铜基导线(例如铜、铜包钢)组成,并且可能具有绝缘涂层(例如聚酰亚胺、聚酰胺-酰亚胺)。导线的规格在40awg至20awg之间。
装置/系统手柄
部件展开和定位
装置的手柄具有致动器,以除了操纵输送导管之外,还允许远端扩张器导管、电极导管和组织稳定器导管的平移和/或旋转。在一些实施例中,远端扩张器导管和电极导管超过输送导管的远侧末端平移的最大距离是60mm。在一些实施例中,在远端扩张器导管和电极导管之间的最大可平移距离受展开电极所需的最小平移限制。在一些实施例中,组织稳定器导管相对于输送导管的末端在向近侧约20mm至向远侧约20mm之间平移。在一些实施例中,通过使远端扩张器导管向前平移和/或旋转,或者使电极导管向后平移和/或旋转来使电极展开。在一些实施例中,通过致动螺纹/旋转机构或简单的平移机构来实现电极的展开和收缩。在一些实施例中,装置手柄具有安全止动件,该安全止动件在电极导管相对于远端扩张器导管平移和/或旋转之前必须脱开;止动件结构的目的是在rf通电和切割之前防止电极不希望地或过早地展开。可替代地,在一些实施例中,手柄用于致动电极展开的机构同时将电源线与rf发生器联接,从而抑制电极的rf通电,直到电极已经展开。
rf通电和切割
在一些实施例中,rf通电和切割是完全手动的,以向最终使用者提供对rf通电的开始、持续时间和停止的控制,并且在切割之前和之后提供与电极的平移有关以及在切割之前提供与用组织稳定器张紧间隔有关的触觉输入和反馈。在一些实施例中,使用erbe250drf发生器单元以1秒的脉冲输送150w的单极rf能量。在一些实施例中,将接地垫片放置在患者的外皮肤表面上。
在一些实施例中,通过将按钮、旋钮或致动器结合到手柄中来实现一个或多个过程步骤的自动化。
在一些实施例中,当输送rf能量时,射频发生器构造成测量和检测阻抗、温度、电流输出或固定持续时间的变化,以向最终使用者提供切割完成的指示。
装置致动
在一些实施例中,如图27a-f所示,该装置在导丝2706上插入和推进,使用标准的经房间隔穿刺方法穿过股静脉就位,并且被输送至右心房。在导管的输送可转向或可偏转的实施例中,装置定向成具有近似垂直于间隔的位置,以使组织变形最小化,使装置相对于导丝定位的中心化最大化,并且改善装置的并置,使得远端扩张器导管2708的远端扩张器末端2708d相对于房间隔2707处于适当的附近处(a)。将导丝2706以及然后远端扩张器末端2708d推进穿过房间隔,使得远端扩张器导管2708定位在左心房中(b),而剩下的一半输送导管2701位于右心房中。远端扩张器导管2708相对于所有其他装置/系统部件向远侧移动,以使电极2703、支撑支柱、电极阴极2703b脱鞘和展开,并且暴露电极导管2702(c)。可替代地,还可以通过相对于远端扩张器导管2708向近侧拉动电极导管2702来使电极2703展开。将电极导管2702向近侧抽回,使得电极2703b的切割部分与间隔2707的左心房表面接触(d)。相对于所有其他装置/系统部件向远侧推进组织稳定器导管2705,以使组织稳定器2704、支撑支柱和稳定部分/稳定器环2704b在右心房中脱鞘和展开;在展开之后,进一步推进稳定器导管2705,使得组织稳定器的稳定部分与间隔的右心房表面(与电极相对)接触(e)。可替代地,相对于组织稳定器2704将输送腔向近侧抽回,以使组织稳定器2704、支撑支柱和稳定部分/稳定器环2704b在右心房中脱鞘和展开;在展开之后,向远侧推进组织稳定器,使得组织稳定器的稳定部分与间隔的右心房表面(与电极相对)接触(e)。因此,还可以通过相对于组织稳定器导管2705收回输送导管2701来使组织稳定器2704展开。一旦电极和组织稳定器已经定位在间隔的相对表面上,同时使用rf发生器向电极通电和将其向近侧抽回,以从间隔切除一块组织(f)。
在组织切割之后,电极2703和组织稳定器2704以交叠的状态保持配合,并且电极2703与切除的组织块嵌在组织稳定器2704的稳定器接触环2704b和支柱中,从而构成封装切除的组织的笼。包含捕获的电极和切除的组织的笼随后被向近侧抽回右心房中,并且与切除的组织一起收缩到输送导管2701中。
在一些实施例中,在组织稳定器2704和电极2703收缩之前,朝向组织稳定器在组织稳定器导管2705中的附装部分抽回切除的组织。
在可替代的实施例中,组织稳定器2704和电极2703在切割之后不配合;它们分别收缩到输送导管2701和远端扩张器2708中。
切除的组织可以起初保留在电极2703中,并且首先通过相对于电极收回远端扩张器导管2708来固定,以便使电极收缩在切除的组织周围。随后,推进输送导管2701(或者相对于输送导管收回所有其他装置/系统部件),以在将该装置从身体移除之前,“吞没”收缩的电极和切除的组织。
在一些实施例中,如图28a-k所示,在导丝2806上插入和推进该装置,并且输送至右心房。在导管的输送可转向或可偏转的实施例中,装置定向成具有近似垂直于间隔的位置,以使组织变形最小,使装置相对于导丝的定位的中心化最大,并且改善装置的并置,使得远端扩张器导管2808的远端扩张器末端2808d相对于房间隔2807处于适当的附近处。将导丝2806以及然后远端扩张器末端2808d和远端扩张器2808(包括切割元件固定器2808z和远端扩张器导管2808g)推进穿过房间隔,使得远端扩张器位于左心房(a)中。相对于所有其他装置/系统部件向远侧推进远端扩张器导管2808,以使电极2803和支撑支柱脱鞘和展开,并且暴露电极导管2802(b)。可替代地,还可以通过相对于远端扩张器导管2708向近侧拉动电极导管2802来使电极2803展开。电极2803、支撑支柱(例如2803d3)和电极阴极2803b完全扩张并锁定就位(c)。向近侧抽回电极导管2802、切割元件固定器2808z和远端扩张器导管2808g,使得电极2803的切割部分2803b与间隔2807的左心房表面接触(d)。使组织稳定器导管2805相对于所有其他装置/系统部件向近侧运动,以使组织稳定器2804、支撑支柱和组织稳定器的稳定部分在右心房中脱鞘和展开(e);组织稳定器2804、支撑支柱(例如2804d2)和组织稳定器的稳定环2804b(根据实施例,其可以是或可以不是阳极)完全扩张并锁定就位(f)。在展开之后,组织稳定器导管2805被(向远侧)推进成推动组织稳定器2804,使得组织稳定器的稳定环2804b与间隔2807的右心房表面(与电极相对)接触(g)。可替代地,相对于组织稳定器2804向近侧抽出输送腔,以使组织稳定器2704、支撑支柱和稳定部分/稳定器环2804b在右心房中脱鞘和展开;在展开之后,向远侧推进组织稳定器,使得组织稳定器的稳定部分与间隔的右心房表面(与电极相对)接触。因此,还可以通过相对于组织稳定器导管2805收回输送导管2801来使组织稳定器2804展开。一旦电极2803和组织稳定器2804已经定位在间隔2807的相对表面上,同时使用rf发生器向电极通电,使得电极2803切下一块组织,在房间隔中形成吻合部(h)。将切除的组织块、电极2803、组织稳定器2804和一部分远端导管2808向近侧收回到右心房中(i)。向远侧推进电极导管2802、切割元件固定器2808z和远端扩张器导管2808g,使得切除的组织块在电极2803的支柱内收缩(j)。切除的组织块和电极2803的端部然后被捕获在由组织稳定器支柱(例如2804d1、d2、d3、d4)和组织稳定器的稳定部分(例如2804b)构成的笼中,并且向近侧首先被抽回到组织稳定器导管2805中,然后被抽回到输送导管2801中,然后将装置从间隔和心房完全抽出(k)。然后,最终将重新组装的装置从身体移除。
在可替代的实施例中,组织稳定器2804和电极2803在切割之后不配合;它们分别收缩到输送导管2801和远端扩张器2808中。
切除的组织可以起初保留在电极2803中,并且首先通过相对于电极收回远端扩张器导管2808来固定,以便使电极收缩在切除的组织周围。随后,推进输送导管2801(或者相对于输送导管收回所有其他装置/系统部件),以在将该装置从身体移除之前,“吞没”收缩的电极和切除的组织。
球囊
在一些实施例中,如图10a-10d所示,组织切割器包括在组织切割器导管1002的远端处或远端附近安装至球囊1003e的柔性金属环1003b。在一些实施例中,金属环固定到在右心房中扩张的圆柱形球囊的远端处或附近。在一些实施例中,金属环定位在球囊的远端表面上(图10a),或者可替代地沿着球囊的弯曲表面定位(图10b),使得当球囊的远端表面与间隔1007接触时,在组织与金属环之间保持小的限定间隙。在一些实施例中,组织切割器和组织切割器导管1002具有中心腔1002a,以允许组织稳定器导管1005和组织稳定器1004平移。在一些实施例中,组织稳定器导管1005具有与导丝1006可滑动地接合的中心腔。在一些实施例中,组织稳定器1004是采用本文所述的任何形式的球囊。在一些实施例中,将rf阳极结合到组织稳定器、组织稳定器导管或外部电极(例如皮肤贴片)中。在一些实施例中,在组织切割器展开之前和在组织切除之后,组织切割器导管1002和组织切割器1003容纳在输送导管1001中。
在一些实施例中,如图11所示,组织切割器在圆柱形球囊1103e的近端表面上包括柔性金属环1103b,圆柱形球囊1103e在导丝1106上穿过间隔被放置在左心房中。在一些实施例中,球囊在左心房中扩张,从而使金属环扩张,使其rf通电以切割组织。在一些实施例中,金属环1103b放置在球囊的近端表面上,使其与间隔1107接触,或者放置在圆柱形球囊的弯曲表面周围(未示出),使得当近端表面与间隔接触时,在金属环与组织之间保持小的限定间隙。在一些实施例中,rf阳极1113b沿着组织切割器导管1102或者在位于右心房中的其他装置部件上被放置在间隔的附近。在一些实施例中,不需要单独的组织稳定器或组织稳定器导管,因为这些功能由安装有金属环1103b的球囊1103e实现。在这些实施例中,向近侧拉动球囊,以在金属环和间隔之间实现并置。
在一些实施例中,通过使球囊1103e扩张到相应的直径,使金属环1103b扩张到最大直径从约2mm至约15mm的任何尺寸。在一些实施例中,最大直径在横向于远端-近端轴线的平面上。
在一些实施例中,球囊包括圆柱形、圆锥形、反圆锥形、金字塔形的至少一部分、哑铃形、球形、圆顶形、足球形的至少一部分和纺锤形的至少一部分中的一个或多个。
在一些实施例中,多个柔性金属环安装至球囊的近端或远端表面或附近(这取决于组织切割器展开的位置),当球囊扩张到相应的直径时,每个柔性金属环具有从约2mm至约15mm的唯一的扩张尺寸,使得通过选择性地将rf能量引导至与所期望的孔尺寸相对应的金属环来切除组织。
在一些实施例中,rf阴极和阳极安装在相同的球囊上,如图12a-12b所示。在一些实施例中,球囊1203e的形状是哑铃形(通过狭窄的“颈部”连接的两个圆柱形“盘”),并且被推进穿过间隔1207(放气,在输送导管中),使其颈部位于间隔中的平面上。在一些实施例中,rf阴极1203b和阳极1213b采用安装在每个盘的内表面(朝向间隔侧)上的柔性金属环的形式;当球囊被完全充气后,金属环与间隔接触。在一些实施例中,金属环沿着每个盘的弯曲表面安装,使得在金属环与间隔之间保持小的限定间隙。在一些实施例中,不需要单独的组织稳定器,因为哑铃形的球囊就足够了。在一些实施例中,不需要引导导管,因为充气的哑铃形状将与间隔相互作用,以确保金属环平行于间隔1207定位。在一些实施例中,rf阴极位于右心房中的近侧盘上,rf阳极位于左心房中的远侧盘上。在其他实施例中,rf阴极位于左心房中的远侧盘上,rf阳极位于右心房中的近侧盘上。
在一些实施例中,如图13a-13b所示,组织切割器是安装在圆柱形球囊1303e的弯曲表面的中点周围的柔性金属环1303b。在一些实施例中,球囊1303e安装至组织切割器导管1302,该组织切割器导管1302具有中心腔并且与导丝1306可滑动地接合。在一些实施例中,球囊1303e(图13a)被推进(被放气,在输送导管1301之外)穿过间隔1307,使得金属环1303b位于间隔中的平面上。在一些实施例中,将输送导管1301拉回,以使球囊1303e脱鞘;使气囊1303e充气,以使组织扩张,并且向金属环1303brf通电,从而使组织径向汽化以产生孔。在一些实施例中,在球囊充气之前向金属环1303brf通电;rf通电和球囊充气逐步交替,直到球囊1303e完全充气。在一些实施例中,当球囊1303e从其放气状态转变为完全充气状态时,向金属环1303brf通电。在一些实施例中,球囊1303e的外边缘在扩张时向外张开并具有更大的直径,以便于和确保球囊1303e穿过间隔并在间隔的每一侧定位。
形状记忆网筛
在一些实施例中,组织切割器是导电的金属环,该金属环固定在自扩张(具有形状记忆材料,例如镍钛诺)圆柱形网筛上,并且安装至网筛的远端表面(朝向间隔侧),或圆柱形网筛的弯曲表面周围并且从远端表面缩进(凹入)介于约0.1mm至约10.0mm的范围内的固定距离。在一些实施例中,网筛具有与组织稳定器导管可滑动地接合的中心腔。网筛安装至组织切割器导管,并且以收缩状态容纳在输送导管中。在一些实施例中,本文所述的任何组织稳定器可以与这些实施例一起使用。在一些实施例中,rf阳极位于组织稳定器、组织稳定器导管(以环形电极的形式)上,或者在身体外部但与身体接触(例如皮肤贴片电极)。
在一些实施例中,在经房间隔穿刺和组织稳定器的输送/展开之后,通过向后拉动输送导管使圆柱形网筛在右心房中展开,从而暴露金属环。在一些实施例中,在rf通电之前,使网筛与间隔接触。
在一些实施例中,如图9a-9c所示,组织切割器是导电的金属环903b,该金属环903b固定至自扩张(形状记忆)圆柱形网筛903o上,并且安装至其近端表面(朝向间隔侧),或网筛的弯曲表面周围并且从近端表面缩进(凹入)固定距离(0.1-10.0mm)。在一些实施例中,网筛安装至组织切割器导管902;二者均具有与导丝906可滑动地接合的中心腔。在一些实施例中,网筛903o以收缩状态容纳在输送导管901内。为了使网筛903o在左心房中展开,在一些实施例中,输送导管穿过间隔907到达左心房。在一些实施例中,向后拉动输送导管901,以使网筛903o展开。在一些实施例中,在右心房中进一步向后拉动输送导管,以暴露位于组织导管902上的环形电极rf阳极913b。在一些实施例中,向后拉动组织切割器导管902,以使网筛903c与间隔907接触。在一些实施例中,在组织切割之后,将切除的组织和网筛903o包装在输送导管901内。在一些实施例中,rf阳极在身体外部但与身体接触(例如皮肤贴片电极)。
在一些实施例中,网筛包括圆柱形、圆锥形、反圆锥形、金字塔形的至少一部分、哑铃形、球形、圆顶形、足球形的至少一部分和纺锤形的至少一部分中的一个或多个。
在一些实施例中,如图18a-18c所示,哑铃形的自扩张(形状记忆)网筛1803o包括两个电绝缘的盘(或球),并且附装至导线的末端。在一些实施例中,柔性金属环安装在每个网筛盘的向内表面(朝向间隔侧)上,或者可替代地安装在每个盘的弯曲表面周围(相对于接触间隔的表面缩进)。在一些实施例中,盘被约束在输送导管中,并且被释放以允许在间隔1807的任一侧扩张。在一些实施例中,金属环用作rf阴极1803b和阳极1813b。在一些实施例中,rf阴极位于远侧盘上,而rf阳极位于近侧盘上;在其他实施例中,rf阴极位于近侧盘上,而rf阳极位于远侧盘上。在一些实施例中,盘用于确保和保持金属环与间隔的平行对准以及在切割期间和切割之后牢固地接合组织。在一些实施例中,将盘安装在导管(未示出)上,该导管具有与导丝可滑动地接合的中心腔;一单独的输送导管容纳收缩的盘及其相应的导管。在一些实施例中,仅一个金属环(rf阴极)安装在任一盘上,其中,rf阳极位于输送导管上,或者在身体外部但与身体接触(例如皮肤贴片电极)。
在一些实施例中,用平移、向前拧紧运动、移除固定销、马达控制或结合磁体约束壳体导管中的网,从而致动自扩张(形状记忆)网筛的扩张。
在一些实施例中,通过使网筛扩张到相应的直径,使金属环扩张到最大直径从约2mm至约15mm的任何尺寸。在一些实施例中,最大直径在横向于近端-远端轴线的平面上。
在一些实施例中,多个柔性的、电绝缘的金属环安装至自扩张(形状记忆)网筛的近端或远端表面,当网筛扩张到相应的直径时,每个金属环具有从约2mm至约15mm的唯一的扩张尺寸,使得通过选择性地将rf能量引导至与所期望的孔尺寸相对应的金属环来切除组织。
在一些实施例中,除了小的暴露的圆形表面积之外,自扩张(形状记忆)网筛完全绝缘。在一些实施例中,该暴露的圆形表面积用作电导体,并且通过用作rf电流的源或回路来实现金属环的功能。在一些实施例中,具有部分导电的自扩张网筛的组织切割器不需要任何金属环。
切断器
在一些实施例中,如图14a-14b所示,组织切割器采用机械致动式钳口的形式,通过致动线滑轮系统来打开和闭合钳口,该线滑轮系统在拉紧时闭合钳口1403i,而在释放(不拉动)时打开钳口1403i。在该实施例中,每个钳口通过导线连接至rf发生器,其中一个钳口用作rf阴极,另一个钳口用作rf阳极。在该实施例中,钳口1403i在导丝1406上被推进至间隔1407,并且被致动以咬合和与间隔接合;随后rf通电以产生孔。在一些实施例中,切除的组织被保持在组织切割器的钳口1403i中,该钳口被输送导管重新收回,由此用作组织保持元件。在一些实施例中,第二组织稳定器1404被引入左心房中,以使组织进入钳口1403i的口部中。
在一些实施例中,如图15a-15d所示,rf阴极1503b和阳极1513b采用半圆形导电金属条的形式,该金属条沿输送导管1501或组织切割器导管1502的远端边缘排列,使得当组织稳定器1504将间隔1507拉入输送导管1501或组织切割器导管1502中时,金属条1503b和1513b被rf通电,并且在间隔1507中产生孔;通过组织稳定器1504将切除的组织包装到输送导管1501或组织切割器导管1502中。在一些实施例中,金属条从输送导管1501或组织切割器导管1502的远端边缘缩进(凹入),以在金属条1503b和1513b与间隔1507之间确保小的限定间隙。在一些实施例中,组织稳定器1504扩张的直径小于输送导管1501或组织切割器导管1502的内径。
在一些实施例中,如图16a-16b所示,组织切割器采用沿着输送导管1601或组织切割器导管1602的边缘的不可扩张的环1603b的形式。在一些实施例中,组织稳定器1604用作rf阳极。在一些实施例中,当组织稳定器1604被定位在左心房中时,将组织稳定器向近侧拉入输送导管1601或组织切割器导管1602中;然后施加rf能量以在间隔1607中产生孔。
其他切割元件扩张机构
在一些实施例中,组织切割器包括柔性导电环,该柔性导电环在展开时扩张以采用马蹄形构型。如图17a-17d所示,输送导管1701具有两个偏心腔1701a和1701b以及在其远端处的凹入区域1701c。在一些实施例中,导丝1706位于第一腔1701a中。在一些实施例中,第二腔1701b以其收缩状态容纳金属环1703b的一端,并且允许金属环向前平移以完全扩张(图17d)。在一些实施例中,金属环的另一侧固定在输送导管1701的凹入区域中。在一些实施例中,完全扩张的金属环保持与导丝同轴。在一些实施例中,金属环在其未扩张状态中缠绕在第二腔的挤出管1701d周围,使得导丝位于金属环的圆周内部。通过在导丝上使一单独的组织保持元件导管穿过腔1701a进入左心房中,使组织保持元件展开。
在一些实施例中,组织切割器包括环形或支架状结构形式的不锈钢、钴铬合金或其他类型的可塑性变形的导电材料,其直径通过球囊扩张而增大。
其他装置结构
在一些实施例中,本文的装置组件包括结合使用马达或压电电路来振荡/振动或致动。在一些实施例中,类似地,结合了旋转以在组织切割器通电并切割组织时最小化或防止组织粘连。
在一些实施例中,导丝用作阳极,这消除了具有包括电极形环的附加导管的必要性。
在一些实施例中,可扩张组织稳定器具有单独的铁磁条的阵列,该铁磁条径向分布以构成阵列(朝向间隔)。在一些实施例中,组织切割器导管具有位于组织切割器与房间隔之间的盘状磁体,其尺寸小于输送导管的内径,并且在组织切割器导管的远侧末端同轴地布置在其周围。在一些实施例中,盘状磁体同轴地布置在一单独的导管周围,该单独的导管可滑动地接合在组织切割器导管中,并且具有内腔,组织稳定器导管与该单独的导管同轴,并且可以在其中滑动。在一些实施例中,当组织稳定器穿过间隔在左心房中展开时,盘状磁体向前推进以与间隔接触,使得间隔锁定在磁性盘和铁磁阵列之间(从而固定和稳定间隔)。向组织切割器施加rf能量以切出孔,并且将切除的组织包装在输送导管内,同时将其锁定在磁性盘和组织稳定器之间。在一些实施例中,组织切割器和磁性盘在左心房中展开,而组织稳定器在右心房中展开,并且磁性盘和铁磁阵列都朝向间隔。
在一些实施例中,在组织切割和切除期间,通过一单独的抽吸导管和抽吸杯向间隔的近端侧(在右心房中)施加抽吸以稳定组织。在一些实施例中,抽吸导管可滑动地接合在组织切割器导管内,并且具有中心腔,组织稳定器导管穿过该中心腔。在一些实施例中,施加抽吸以使杯和间隔接合。在一些实施例中,在组织切割之后,施加的抽吸将切除的组织抽到组织切割器导管内,从而确保对组织的捕获和保留。在一些实施例中,在组织切割和切除期间,在间隔的远端侧(在左心房中)使用组织稳定器,以在施加抽吸时稳定组织。在一些实施例中,杯包括诸如橡胶、硅树脂或其他聚合物的材料。
在一些实施例中,本文公开的各种导管包括聚合物、金属、或金属/聚合物编织/卷绕加强的一种或多种材料,以允许装置用于插入/引入体内的可推动性。
在一些实施例中,本文公开的各种导管具有孔口,以在将装置插入/引入体内期间允许快速的导线交换。在一些实施例中,输送导管包含一个或多个不透射线的标记,以便于导引和输送至心脏(右心房、左心房、房间隔)。在一些实施例中,输送导管的远侧末端用刚性或形状记忆材料加强,以便于组织切割器的脱鞘/重新入鞘。在一些实施例中,输送导管的范围是5-24fr。在一些实施例中,在组织切割器导管的远端处包括温度传感器,以监测进行组织切割的区域的温度,从而确保温度保持在预定范围内。在一些实施例中,将音频或视觉反馈/警告系统结合到导管手柄中,以通知使用者/操作者与预定范围的偏差。
在一些实施例中,包括阻抗传感器,以监测rf阴极与阳极之间的阻抗,从而确认组织切除完成,或者基于测量到的增大的组织阻抗,向rf发生器提供直接反馈,以调制电压。在一些实施例中,阻抗传感器包括本文公开的装置组件的一个或多个部件。
在一些实施例中,组织稳定器用于将超声能量径向向外引导,然后轴向引导至间隔,以允许间隔的超声介导切割。在一些实施例中,组织稳定器用于使反射条对准和将激光能量径向向外引导,然后轴向引导至间隔,以允许间隔的激光介导切割。
在一些实施例中,组织切割器导管在rf发生器和组织切割器之间具有内部电路,该内部电路允许将传输到组织切割器的电流量限制到预定的阈值;在一些实施例中,将音频或视觉反馈/警告系统结合在导管手柄中,以通知使用者使用的输入能量过量。在一些实施例中,如果输入能量低于期望阈值,则组织切割器导管或组件的其他部件上的内部电路阻止电流传输;将音频或视觉反馈/警告系统结合在导管手柄或rf发生器中,以警告使用者使用的输入能量不足。
在一些实施例中,组织切割器导管具有盐水冲洗通道,以冲洗整个导管中的盐水;盐水或其他溶液循环通过远侧末端并流出近端,或者可替代地循环通过远端。在一些实施例中,盐水冲洗系统是独立单元,其用注射器手动操作,或者集成到rf发生器中。
在一些实施例中,本文公开的一个或多个电极或导电元件涂覆有聚四氟乙烯(ptfe),以最小化成焦。
基于等离子体的方法
在一些实施例中,除了1-100μm的边缘之外,组织切割器是绝缘的,该边缘以1-60hz的脉冲从rf发生器传输0.5k-4.0kv下的15-200μj的电流,以使组织切割器的导电边缘周围的组织电离,从而产生用于组织切除的等离子体薄层。
实现/数据汇总
本文公开的本发明的实施例在一系列台式试验、当日死亡的急性动物研究和慢性动物研究中制造和测试,通过该慢性动物研究,可以允许猪存活多达5个月以评估使用该装置产生的心房间孔的持久性。一个这种实施例用于在两只活的约克夏杂交公猪中产生大约8mm直径的心房间孔。该手术在荧光镜和心脏内回声引导下成功进行。没有遇到并发症。30天的荧光透视检查和心内回声证实心房间孔持续通畅,没有再生长的迹象。
对于这些测试,电极包括单部件镍钛诺支架,该支架具有圆形切割部分和4个支柱,该圆形切割部分具有8mm的扩张外径、0.0635mm的宽度。电极在除了切割部分之外的所有表面上涂有一层11μm厚的聚对二甲苯c膜。电极联接至32awg的铜线,并且附装至5fr的不锈钢增强型聚酰亚胺导管。在展开之前,电极以收缩状态位于8fr的远端扩张器轴内。组织稳定器包括单部件镍钛诺支架,该支架具有稳定部分、4个支柱、和附装至6fr的导管的附装部分,该稳定部分具有11mm的扩张直径。组织稳定器以收缩状态容纳在具有8.5-9.0fr的内径和12fr的外径的可转向输送导管中。将该装置在0.024英寸的经房间隔导丝上通过14fr的血管通路护套插入股静脉中。使用erbe250drf发生器单元以1秒的脉冲输送150w的单极rf能量。在猪的背面放置了接地垫片。
尽管本文已经示出和描述了本文公开的优选实施例,但是本领域的技术人员显而易见的是,这些实施例仅通过示例提供。在不背离本文公开的情况下,本领域的技术人员现在将想到多种变型、改变和替代方案。应当理解,在实践本文的装置组件时,可以采用本文描述的装置组件的实施例的各种替代方案。随附权利要求旨在限定本文的装置组件的范围,并且由此涵盖这些权利要求的范围内的方法和结构及其等同物。
- 还没有人留言评论。精彩留言会获得点赞!