一种异种生物羊膜产品的制备方法与流程
本项目涉及动物源性医疗器械材料技术领域,具体涉及一种异种生物羊膜产品的制备方法。
背景技术:
羊膜作为一种免疫豁免生物移植物,天然羊膜具有大量不同的胶原、纤维粘连蛋白、层粘连蛋白和蛋白多糖等成份。此外,天然羊膜含有多种营养因子,比如转化生长因子-β(tgf-β)、转化生长因子-α(tgf-α)、碱性生长因子(bfgf)、表皮生长因子(egf)、神经生长因子(ngf)、脑源性神经营养因子(bdnf)、肝细胞生长因子(hgf)和角化细胞生长因子(kgf)等,可以促进细胞生长、增殖和分化。羊膜可以充当“基底膜”而有利于细胞粘附和生长促进上皮化,具有抗炎、抗粘连,减轻疼痛等生物学特性,早在1910年开始就被应用于烧伤患者及其他外科手术用于促进表皮化、减轻疼痛和预防感染。羊膜与人眼结膜组织结构相似,含有眼表上皮细胞生长所需要的物质,其光滑、无血管、神经及淋巴,具有一定的弹性。羊膜的生物学特点使其作为一种新型、可靠的供体材料而广泛应用于眼科临床。此外,羊膜在深度烧创伤、糖尿病足、脏器、骨科肌腱的修复等临床领域的应用也进一步开发。
然而,目前国内外上市的产品均为产妇自愿捐献的羊膜,同种异体来源羊膜缺乏统一的供体筛选获取标准,存在潜在的hiv、梅毒螺旋体、hbv、hcv感染可能,以及获取和使用的伦理等问题,导致原材料来源不足。羊膜处理相关的专利较多涉及冷冻干燥技术(如中国专利zl03150838.3)、去细胞技术(如中国专利cn105194735a)、酸碱消毒(如中国专利cn104083803a)。而这些处理会对羊膜所含有的生物活性成分有较大的损失。此外,羊膜的机械强度也因处理会变差,临床使用会导致更容易撕裂。
综上所述,寻求可以符合伦理要求且可规模化获得羊膜的途径是羊膜在临床规模使用的必要前提。同时,采用怎样的羊膜处理工艺,将直接关系到羊膜产品的生物功能和机械强度,从而直接影响临床使用效果。合理的工艺处理是获得临床使用效果佳的羊膜产品前提及急需解决的关键之一。
技术实现要素:
为了解决现有技术中原材料的来源、加工工艺及羊膜特性保护方法存在的问题,本发明提供一种异种生物羊膜产品的制备方法,可规模化获得大量羊膜,能保持天然羊膜特性。
本发明异种生物羊膜产品的制备方法的技术方案包括:
获取动物胎盘后清洗,手工剥离并保留羊膜基膜;
将步骤a中所得的羊膜基膜清洗灭菌后平铺固定,并裁剪;
将步骤b中裁剪的羊膜基膜置于含有保存液的内包装并密封,经辐照灭菌得到异种生物羊膜产品。
优选的,在上述异种生物羊膜产品的制备方法中,动物选自猪、牛、羊、马、兔中任一种。
优选的,在上述异种生物羊膜产品的制备方法中,所述步骤a具体操作方法为:动物自然顺产或剖腹产后,第一时间搜集动物胎盘,使用水或含有双抗的无菌水清洗动物胎盘残留的血液,清洗后的动物胎盘在预设时间内转于gmp厂房,将羊膜从动物胎盘上手工钝性剥离,剥离后的羊膜去除血管、血管节丰富组织、绒毛膜及羊膜的纤维细胞层和海绵层,保留具有一定力学强度上皮细胞层、基底膜层和致密层部分,形成羊膜基膜。
优选的,在上述异种生物羊膜产品的制备方法中,清洗后的动物胎盘在室温下在4小时内转于gmp厂房,或在6℃-0℃的冷藏条件下12小时内转于gmp厂房;或在低于0℃的冷冻条件下10天内转于gmp厂房。
优选的,在上述异种生物羊膜产品的制备方法中,所述步骤b具体操作方法为:使用普通无菌pbs或含有双抗的无菌pbs清洗羊膜基膜,采用羊膜固定环固定对羊膜基膜夹合铺展,沿羊膜固定环环边裁剪。
优选的,在上述异种生物羊膜产品的制备方法中,所述双抗为青霉素和链霉素,其中,青霉素的浓度为20-200μg/ml,链霉素的浓度为20-200μg/ml。
优选的,在上述异种生物羊膜产品的制备方法中,所述羊膜固定环由两部分可相互嵌合的外环和内环组成,羊膜固定环的形状是圆形或方形,材质是高分子材料或无机陶瓷材料或金属材料。
优选的,在上述异种生物羊膜产品的制备方法中,所述步骤c具体操作方法为:裁剪的羊膜基膜置于含有保存液的内包装并密封,置于-20℃到20℃内容器后转移至电离辐射灭菌设备内处理,使用带有明确产品标识的外包装,得到异种生物羊膜产品。
优选的,在上述异种生物羊膜产品的制备方法中,所述保存液由dmem培养基与甘油组成,两者的质量比范围在20:80-80:20范围内,保存液中可选择性的添加0-10mg/ml的半胱氨酸、0-10mg/ml的维生素c、0-1mg/ml的原花青素中任一种或多种。
优选的,在上述异种生物羊膜产品的制备方法中,所述电离辐射是伽马射线或高能电子束辐照,辐照量为10-30kgy,辐照的温度控制在-20℃到20℃之间。
本发明相对于现有技术的优点和有益效果是:
(1)本发明的异种生物羊膜来源广泛,可实现原材料的规模化获取及标准化筛选。
(2)本发明的异种生物羊膜制备方法简洁,不使用酸碱、有机溶剂或物理手段对组织进行处理,尽量保留天然羊膜的致密结构及生物特性。
(3)本发明的异种生物羊膜为保存液存在下的湿态保存,保存液具有降低辐照对羊膜的影响,冷冻状态下维持羊膜的结构和活性的作用。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图
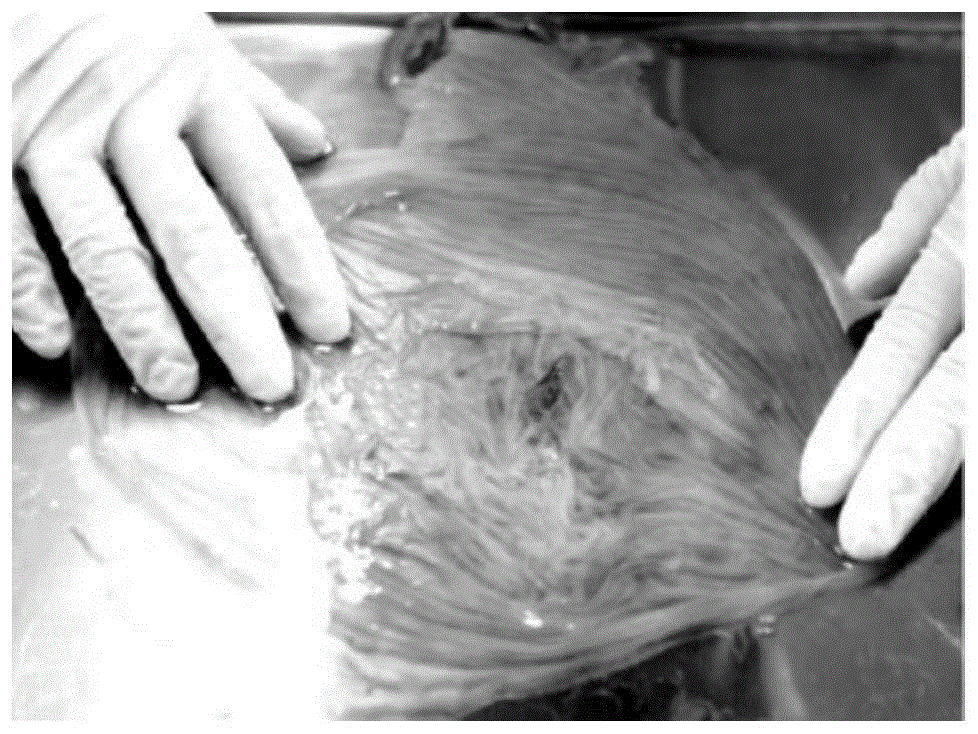
图1为本发明中使用无菌pbs冲洗清理后的新鲜羊膜;
图2为本发明中钝性剥离,保留羊膜上皮层,基底膜及致密层;
图3为本发明得到透明/半透明的生物羊膜;
图4为新鲜羊膜he染色(40倍)的示意图;
图5为本发明制得的生物羊膜he染色(40倍)的示意图。
具体实施方式
本发明提供一种异种生物羊膜产品的制备方法,主要包括胎盘获取与剥离;清洗灭菌与固定;辐照灭活及包装。
在胎盘获取与剥离阶段,动物(动物的来源是符合动物源性医疗器械材料来源监管要求的饲养场,种类是猪、牛、羊、马、兔中一种)生产(自然顺产或剖腹产)后,第一时间搜集胎盘,使用水或含有双抗的无菌水清洗胎盘残留的血液,然后将清洗后的动物胎盘转移到处理间,清洗后的动物胎盘在室温下转移时间要求在4个小时内,在冷藏条件下(6℃-0℃)转移时间要求在12小时内,在冷冻条件下(低于0℃)转移时间要求在10天内。处理间力求洁净,标准化生产要求在百万级或十万级或万级或百级gmp厂房内。最后将羊膜从动物胎盘上手工钝性剥离,剥离后的羊膜去除血管、血管节丰富组织、绒毛膜及羊膜的纤维细胞层和海绵层,保留具有一定力学强度上皮细胞层、基底膜层和致密层部分,形成透明的羊膜基膜。
在清洗灭菌与固定阶段,普通无菌pbs或含有双抗的无菌pbs清洗羊膜基膜,双抗为青霉素和链霉素,其中,青霉素的浓度为20-200μg/ml,链霉素的浓度为20-200μg/ml。采用羊膜固定环将羊膜基膜固定夹合铺展,对羊膜基膜保护的同时便于使用者分辨上皮层面,羊膜固定环是由两部分可以相互嵌合的外环和内环组成。羊膜固定环的形状是圆形或方形,材质是高分子材料或无机陶瓷材料或金属材料。外环一侧有向内突出的固定长度的封堵,以固定内环。外环的封堵长度为半径的0-1倍。内环的环界面是圆形或长方形设计。
在辐照灭活及包装阶段,将裁剪的羊膜基膜置于含有保存液的内包装并密封,保存液由dmem培养基与甘油组成,两者的质量比范围在20:80-80:20范围内。保存液中可添加0-10mg/ml的半胱氨酸、0-10mg/ml的维生素c、0-1mg/ml的原花青素种的一种或多种,用以降低辐照对羊膜性能的影响。置于-20℃到20℃内容器转移电离辐射灭菌设备内处理,电离辐射是伽马射线或高能电子束辐照,辐照量为10-30kgy,辐照的温度控制在-20℃到20℃之间,使用带有明确产品标识的外包装,得到异种生物羊膜产品。
本发明所使用原材料为动物来源,具体的,是动物源性(猪、牛、羊、马、兔)的羊膜,动物羊膜可以实现原材料的规模化获取及标准化筛选。
动物的来源是符合国家有关动物源性医疗器械及原材料的相关法规,部分条例举例如下:动物源性医疗器械注册技术审查指导原则(2017年修订版),《yy/t0771.1-2009动物源医疗器械第1部分风险管理应用》,《yy/t0771.2-2009动物源医疗器械第2部分:来源、收集与处置的控制》,《yy/t0771.3-2009动物源医疗器械第3部分:病毒和传播性海绵状脑病(tse)因子去除与灭活的确认》,《yy/t0771.4-2015动物源医疗器械第4部分:传播性海绵状脑病(tse)因子的去除和或灭活及其过程确认分析的原则》。
动物的来源除了满足法规要求外,还满足监管要求,其主要内容如下:动物来源监管(动物养殖场或育种厂建立完善的动物种属来源,做到按头溯源);饲养过程监管(根据动物饲养国标及规范,定期检验检疫做好溯源记录,排查致病源);动物生产取材监管(动物洁净产房中生产,取得生产废弃物胎盘,使用含有双抗的无菌pbs冲洗后,迅速置于冷冻条件下冷冻,通过冷链运输至生产车间)。
下文以三个实施例对上文进行展开说明。
实施例1
严格按照国家相关标准,筛选畜禽饲养及屠宰符合卫生检疫规范的养殖场的种属来源明确的波尔山羊。
在胎盘获取与剥离阶段,选择符合兽医检测标准及可溯源的健康的待产母羊于动物产房生产,所得新鲜胎盘室温下使用无菌pbs冲洗净血液、组织液等,4℃下1小时内转移至万级gmp厂房中,进行后处理。在gmp厂房的洁净操作台内,将胎盘平铺于聚四氟乙烯的平板上,钝性剥离血管/血管节丰富的组织、绒毛膜及羊膜的纤维细胞层和海绵层等,保留具有一定力学强度上皮细胞层、基底膜层和致密层部分,形成羊膜基膜。
在清洗灭菌与固定阶段,将得到的羊膜基膜用无菌pbs冲洗3次,随后浸泡于双抗的无菌pbs约15min(其中,青霉素的浓度为100μg/ml,链霉素的浓度为100μg/ml)。无菌pbs冲洗3次后,铺展羊膜于1cm×1cm的方形聚乙烯固定环底环模具上,缓慢盖上上环,分辨内皮层背向底环,并沿着环边对羊膜基膜进行裁剪。
在辐照灭活及包装阶段,配置保存液,保存液配方为dmem培养基与甘油质量比50:50。保存液中添加1mg/ml的原花青素,用以降低辐照对羊膜性能的影响。随后,每片羊膜基膜添加2ml保护液并密封包装。内包装表面帖服辐照指示贴后,转移到0℃保温器皿中,置于辐照灭菌箱中。0℃环境下,采用20kgy的辐照量辐照。使用带有明确产品标识的外包装,得到异种生物羊膜产品。产品使用前保存于-20℃。
实施例2
严格按照国家相关标准,筛选畜禽饲养及屠宰符合卫生检疫规范的养殖场的种属来源明确的波尔山羊。选择符合兽医检测标准及可溯源的健康的待产母羊于动物产房生产,所得新鲜胎盘室温下使用无菌pbs冲洗净血液、组织液等。-20℃下保存,每2天转移一批次胎盘原材料至万级gmp厂房中,进行后处理。在gmp厂房的洁净操作台内,将胎盘平铺于带有有一定弧度的玻璃平面上,钝性剥离血管/血管节丰富的组织、绒毛膜及羊膜的纤维细胞层和海绵层等,保留具有一定力学强度上皮细胞层、基底膜层和致密层部分,形成羊膜基膜。
将得到的羊膜基膜用无菌pbs冲洗3次,随后浸泡于双抗的无菌pbs约25min(其中,青霉素的浓度为50μg/ml,链霉素的浓度为50μg/ml)。无菌pbs冲洗3次后,铺展羊膜基膜于半径为1.5cm圆形聚四氟乙烯固定环底环模具上,缓慢盖上上环,分辨内皮层背向底环,并沿着环边对羊膜进行裁剪。
配置保存液,保存液配方为dmem培养基与甘油质量比70:30。保存液中添加5mg/ml的半胱氨酸,用以降低辐照对羊膜性能的影响。随后,每片羊膜基膜添加2ml保护液并密封包装。内包装表面帖服辐照指示贴后,转移到-10℃保温器皿中,置于辐照灭菌箱中。-10℃环境下,采用25kgy的辐照量辐照。使用带有明确产品标识的外包装,得到异种生物羊膜产品。产品使用前保存于-20℃。
实施例3
严格按照国家相关标准,筛选畜禽饲养及屠宰符合卫生检疫规范的养殖场的种属来源明确的波尔山羊。选择符合兽医检测标准及可溯源的健康的待产母羊于动物产房生产,所得新鲜胎盘室温下使用无菌pbs冲洗净血液、组织液等。4℃下1小时内转移至万级gmp厂房中,进行后处理。在gmp厂房的洁净操作台内,将胎盘平铺于聚四氟乙烯的平板上,钝性剥离血管/血管节丰富的组织、绒毛膜及羊膜的纤维细胞层和海绵层等,保留具有一定力学强度上皮细胞层、基底膜层和致密层部分,形成羊膜基膜。
将得到的羊膜基膜用无菌pbs冲洗3次,随后使用含有双抗的无菌pbs冲洗3次(其中,青霉素的浓度为20-200μg/ml,链霉素的浓度为20-200μg/ml)。然后无菌pbs冲洗3次,铺展羊膜于10个×10个排列的聚乙烯保存环模具组,单个环尺寸为1cm×1cm,环间距为1cm,分别缓慢盖上上环,分辨内皮层背向底环,并沿着环之间中间位置对羊膜和模具组进行切割,得到100个羊膜样品。
配置保存液,保存液配方为dmem培养基与甘油质量比50:50。保存液中添加5mg/ml的维生素c和1mg/ml的原花青素,用以降低辐照对羊膜性能的影响。随后,每片羊膜基膜添加2ml保护液并密封包装。内包装表面帖服辐照指示贴后,置于辐照灭菌箱中,保持灭菌箱在0℃环境,采用20kgy的辐照量辐照。使用带有明确产品标识的外包装,得到生物羊膜产品。产品使用前保存于-20℃。
通过上述方法制得的生物羊膜,如图5所示,生物羊膜he染色(40倍)的情况下,生物羊膜保留单层的上皮细胞,膜厚度均匀,而图4中所示的新鲜羊膜he染色(40倍)的情况下,新鲜羊膜原材料上皮层保留可见的柱状的细胞。
以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!