使用远红外线放射陶瓷组合物和低强度超声波的改善及治疗因关节炎损伤的骨组织的装置的制作方法
[0001]
本发明涉及使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置,其是用放射大量远红外线的陶瓷组合物来温热刺激炎症部位,通过照射使细胞的运动或生长因子的合成增加并使诱导型一氧化氮合酶蛋白的表达减少的低强度超声波,来显示出从根本上缓解及改善炎症的效果的装置。
[0002]
并且,本发明涉及使用远红外线放射陶瓷组合物和低强度超声波的用于改善及治疗由关节炎损坏的骨组织的装置,更详细地,涉及通过用放射大量远红外线的陶瓷组合物温热刺激由关节炎损坏的骨组织部位来增加骨体积、增加骨截面厚度以及减少平均截面片段数量,通过照射低强度超声波来改善及治疗由关节炎损坏的骨组织的装置。
背景技术:
[0003]
日常生活中发生的免疫反应是在人体内部发生的生理保护活动,而炎症是可以通过我们的肉眼确认的免疫反应之一。炎症会引起发烧症状、血管舒张及肿胀等多种可见的生理现象,当炎症被炎症反应介质促进时,使血管的舒张及血管通透性增加,并且收集具有吞噬作用的颗粒细胞、树突细胞及b细胞等并激活它们。当炎症反应开始时,细胞因子(cytokine)会过量分泌,从而引起与炎症相关的疾病,并且由炎症性细胞因子表达的诱导型一氧化氮合酶(inos)促进氧化一氮(no,nitric oxide)的生成。
[0004]
氧化一氮在我们身体中在病例上其到重要作用,其杀死细菌以参与免疫反应,但已知若其分泌量过多会导致宿主内更深的炎症反应,从而导致负面后果。
[0005]
炎症性疾病是全世界主要的死亡原因之一。炎症性疾病影响各种器官及组织,例如,血管、心脏、大脑、神经、关节、皮肤、肺、眼睛、胃肠道、肾脏、甲状腺、肾上腺、胰腺、肝及肌肉。炎症性疾病的治疗成为制药公司和研究人员的关注对象。尽管最近在该领域进行了许多研究,且当前用于炎症性疾病的疗法包括用非特异性药物缓解症状以及减少炎症、延缓疾病的发展等,但这些疗法具有药物副作用及耐性等的严重问题。
[0006]
据报告,关节炎与其他肌肉骨骼系统疾病是成年人残疾的最常见原因。关节炎是如下的难治性疾病:初期,由关节软骨的变形开始,但逐渐导致由关节软骨及软骨下骨组织的破坏而引起的疼痛及僵硬症。正在使用的作为现有关节炎治疗方法有减少炎症的药物治疗法、作为诱导软骨再生的手术方法的微穿孔、在损伤部位大的情况下用人工关节代替的人工关节置换术等。它们主要被用作关节的治疗方法,而对因关节炎而损坏的骨组织的治疗疗法仍然不足。
[0007]
远红外线不像可见光或近红外线,不被活体吸收并被反射,而是被活体吸收且借助渗透力渗透到活体内以产生自发热,从而不仅带来温热效果及出汗效果,吸收到活体内的远红外线还促进新陈代谢,改善血液循环,恢复酶的生成并激活衰老细胞,从而促进废物和多余脂肪的排泄,抑制导致疲劳或衰老的乳酸、游离脂肪酸、脂肪酸脂、胆固醇、过量的盐及尿酸的生成,保持健康年轻。
[0008]
当显示出如上所述的效果的远红外线与温热治疗结合使用时,作为缓解肌肉痛、关节炎、及由此产生的疼痛的方案公开了房屋形状或带状产品。
[0009]
另一方面,已知低强度超声波改变相邻细胞的细胞膜通透性,并将ca
2+
离子诱导至细胞内,从而增加了细胞内的ca
2+
浓度,这种细胞内的变化通过增加细胞的运动或生长因子来对伤口愈合产生有益影响。另外,具有引起继发性生理反应的效果,例如,增加血流量、增加新陈代谢、增加胶原蛋白组织的伸张力、增加疼痛阈值、缓解肌肉痉挛、增加酶活性、改变骨骼肌的收缩力等。近年来,已知当对关节部位施加超声波时,超声波震动传递到软骨组织内的软骨细胞,直接影响软骨细胞的活化,因此可以治疗因软骨细胞的活性能力降低而产生的退行性关节炎,正在开发用于治疗关节炎的组合物或超声波治疗仪。
[0010]
现有技术文献
[0011]
专利文献
[0012]
韩国专利公开:第10-2003-0079902号(2003.10.10)
[0013]
韩国专利授权:第10-0537343号(2005.12.12)
技术实现要素:
[0014]
技术问题
[0015]
本发明的目的在于,提供用放射大量远红外线的陶瓷组合物来温热刺激炎症部位,通过照射使细胞的运动或生长因子的合成增加并使诱导型一氧化氮合酶(inos)蛋白的表达减少的低强度超声波,来从根本上缓解及改善炎症的装置。
[0016]
并且,炎症部位可以是由关节炎损坏的骨组织部位,从而提供用于改善及治疗由关节炎损坏的骨组织的装置。
[0017]
解决问题的手段
[0018]
本发明的目的是通过提供包括:超声波照射部,通过生成低强度超声波来照射炎症的产生部位;温热刺激部,将通过加热陶瓷组合物来产生的远红外线适用于炎症的产生部位;以及控制部,用于控制上述低强度超声波的频带、强度及照射时间中的至少一种和上述温热刺激部的温度的使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置来实现。
[0019]
在本发明的一实施方式中,炎症部位可以是由关节炎损坏的骨组织部位,可由此改善及治疗由关节炎损坏的骨组织部位。
[0020]
根据本发明的优选特征,上述控制部用于控制上述低强度超声波使其具有0.5mhz至1.5mhz的频带及100mw/cm2至150mw/cm2的强度。
[0021]
根据本发明的更优选特征,上述控制部用于控制上述低强度超声波使其具有1.1mhz的频带、120mw/cm2的强度、1:9的脉冲持续时间(pulse duration)、50%的工作周期(duty cycle)的条件。
[0022]
根据本发明的进一步优选特征,上述控制部用于控制上述低强度超声波使其每次具有15分钟至25分钟的照射时间。
[0023]
根据本发明的更进一步优选特征,上述控制部用于控制上述低强度超声波使其每次具有20分钟的照射时间。
[0024]
根据本发明的更进一步优选特征,上述控制部用于控制上述温热刺激部使其加热
至35℃至40℃的温度。
[0025]
根据本发明的更进一步优选特征,上述控制部用于控制上述温热刺激部使其加热至38℃的温度。
[0026]
根据本发明的更进一步优选特征,上述陶瓷组合物由麦饭石、火山石、碳、火山灰及黑云母组成。
[0027]
根据本发明的更进一步优选特征,上述陶瓷组合物由100重量份的麦饭石、0.5重量份至1.5重量份的火山石、0.05重量份至0.15重量份的碳、1重量份至3重量份的火山灰及0.5重量份至1.5重量份的黑云母组成。
[0028]
根据本发明的更进一步优选特征,上述陶瓷组合物由如下的步骤制备而成:原料粉碎步骤,分别粉碎麦饭石、火山石、碳、火山灰及黑云母;微粉碎步骤,将分别通过上述原料粉碎步骤粉碎的粉碎物混合,并加入水后进行微粉碎;空气注入步骤,注入空气,以使通过上述微粉碎步骤的微粉碎的粉碎物具有颗粒形状;成型步骤,将通过上述空气注入步骤具有颗粒形状的微粉碎物放入模具并进行加压成型;烧成步骤,对通过上述成型步骤成型的成型物进行烧成;以及研磨步骤,对通过上述烧成步骤烧成的成型物的表面进行研磨。
[0029]
根据本发明的更进一步优选特征,在上述微粉碎步骤与上述空气注入步骤之间还进行用银纳米微粒子对通过上述微粉碎步骤微粉碎的粉碎物进行涂敷的步骤。
[0030]
根据本发明的更进一步优选特征,在上述微粉碎步骤中,将分别通过上述原料粉碎步骤粉碎的粉碎物混合来制备混合物,在100重量份的上述混合物中加入60重量份至80重量份的水后,粉碎成1000目至3000目的大小。
[0031]
根据本发明的更进一步优选特征,在上述烧成步骤中,将通过上述成型步骤成型的成型物在900℃至1200℃的温度下烧成10小时至24小时。
[0032]
并且,本发明的目的还可以通过提供用于改善及缓解炎症部位的装置的操作方法来实现,上述用于改善及缓解炎症部位的装置的操作方法包括:通过生成上述低强度超声波来照射炎症部位的步骤;将通过加热陶瓷组合物来产生的远红外线适用于炎症部位的步骤;以及控制所照射的上述低强度超声波的频带、强度及照射时间中的至少一种和上述陶瓷组合物的加热温度的步骤。
[0033]
在本发明的一实施方式中,上述炎症的产生部位可以是由关节炎损坏的骨组织部位。
[0034]
根据本发明的优选特征,上述控制步骤用于控制上述低强度超声波使其以0.5mhz至1.5mhz的频带及100mw/cm2至150mw/cm2的强度照射。
[0035]
根据本发明的更优选特征,上述控制步骤用于控制上述低强度超声波使其具有1.1mhz的频带、120mw/cm2的强度、1:9的脉冲持续时间(pulse duration)、50%的工作周期(duty cycle)的条件。
[0036]
根据本发明的进一步优选特征,将通过上述控制步骤控制的超声波以每周2次至4次的频率照射3周至5周,每次照射15分钟至25分钟。
[0037]
根据本发明的更进一步优选特征,将通过上述控制步骤控制的超声波以每周3次的频率照射4周,每次照射20分钟。
[0038]
根据本发明的更进一步优选特征,在上述控制步骤中,将上述陶瓷组合物的加热温度控制为35℃至40℃。
[0039]
根据本发明的更进一步优选特征,在上述控制步骤中,将上述陶瓷组合物的加热温度控制为38℃。
[0040]
根据本发明的更进一步优选特征,将通过上述控制步骤加热的陶瓷组合物以每次40分钟至80分钟、每周4次至6次的频率适用于炎症部位,持续3周至5周。
[0041]
根据本发明的更进一步优选特征,将通过上述控制步骤加热的陶瓷组合物以每次60分钟、每周5次的频率适用于炎症部位,持续4周。
[0042]
发明的效果
[0043]
根据本发明使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置通过放射大量远红外线的陶瓷组合物来温热刺激炎症部位,通过照射使细胞的运动或生长因子的合成增加并使诱导型一氧化氮合酶蛋白的表达减少的低强度超声波,来显示出从根本上缓解及改善炎症的卓越效果。
[0044]
并且,根据本发明的使用远红外线放射陶瓷组合物和低强度超声波的用于改善及治疗由关节炎损坏的骨组织的装置通过用放射大量远红外线的陶瓷温热刺激由关节炎损坏的骨组织部位来增加骨体积、增加骨截面厚度以及减少平均截面片段数量,通过照射低强度超声波来显示出改善及治疗由关节炎损坏的骨组织的卓越效果。
附图说明
[0045]
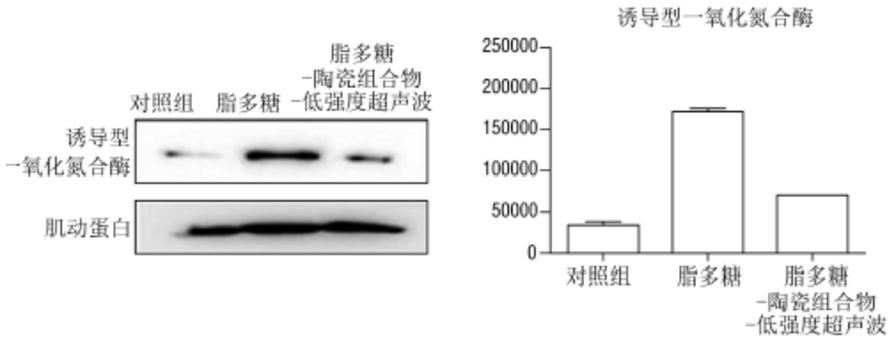
图1为示出通过蛋白质印迹(western blot)分析由本发明的实验例1处理的巨噬细胞(raw 264.7cell)的诱导型一氧化氮合酶蛋白的图表。
[0046]
图2为示出通过一氧化氮测定方法分析由本发明的实验例1处理的巨噬细胞(raw 264.7cell)的一氧化氮的合成量的图表。
[0047]
图3为示出测量由本发明的实验例2处理的实验组1、关节炎诱导组及对照组的血液中白细胞介素-6(il-6)的浓度的图表。
[0048]
图4为示出通过拍摄本发明的实验例2的实验组1至实验组3、关节炎诱导组及对照组的足部来测量骨体积的图表。
[0049]
图5为示出通过拍摄本发明的实验例2的实验组1至实验组3、关节炎诱导组及对照组的足部来测量骨截面厚度的图表。
[0050]
图6为示出通过拍摄本发明的实验例2的实验组1至实验组3、关节炎诱导组及对照组的足部来测量平均截面片段数量的图表。
[0051]
图7为示出根据本发明的使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置的照片。
[0052]
图8为示出应用了根据本发明的远红外线放射陶瓷组合物的温热刺激装置的照片。
[0053]
图9为示出使用在本发明的实验例2中使用的远红外线放射陶瓷组合物的温热刺激过程的示意图。(ndc:陶瓷组合物)
具体实施方式
[0054]
以下,将详细说明本发明的优选实施例和各成分的物理性质,其旨在充分详细地解释以使本领域普通技术人员能够容易地实施本发明,这并不意味着限制本发明的技术思
想及范围。
[0055]
根据本发明的使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置包括:超声波照射部,通过生成低强度超声波来照射炎症的产生部位;温热刺激部,将通过加热陶瓷组合物来产生的远红外线适用于炎症的产生部位;以及控制部,用于控制上述低强度超声波的频带、强度及照射时间中的至少一种和上述温热刺激部的温度。
[0056]
并且,上述炎症部位可以是由关节炎损坏的骨组织部位,可由此改善及治疗由关节炎损坏的骨组织部位。
[0057]
在上述超声波照射部投射到人体组织的情况下,可以生成用于增加血流量、增加新陈代谢、增加胶原蛋白组织的伸张力、增加疼痛阈值、缓解肌肉痉挛、增加酶活性、改变骨骼肌的收缩力等的生理反应的低强度超声波,并照射到炎症部位。
[0058]
上述温热刺激部经加热过程后形成显示出增加骨体积、增加骨截面厚度以及减少平均截面片段数量的放射大量远红外线的陶瓷组合物,上述陶瓷组合物由麦饭石、火山石、碳、火山灰及黑云母组成,优选地,由100重量份的麦饭石、0.5重量份至1.5重量份的火山石、0.05重量份至0.15重量份的碳、1重量份至3重量份的火山灰及0.5重量份至1.5重量份的黑云母组成。
[0059]
上述麦饭石是由每立方厘米(cm3)约有3万个至15万个孔形成的超多孔质原石,具有非常强的吸附力,作为包含约25000多种无机盐类的矿物,并且显示出加热时会发出大量的远红外线的特征。
[0060]
并且,上述火山灰(pozzolan)由火山灰组成,其作为一种蜡石,在5μm至20μm波长中放射出90%至97%远红外线。
[0061]
并且,与黄土、麦饭石相比,上述黑云母是具有约3倍以上的远红外线放射率且含有大量锗的矿物。上述火山石仅由纯无机物组成,因此不仅包含各种必需的矿物成分,而且还显示出放射高远红外线的特征。
[0062]
由上述成分组成的陶瓷组合物由如下的步骤制备而成:原料粉碎步骤,分别粉碎麦饭石、火山石、碳、火山灰及黑云母;微粉碎步骤,将分别通过上述原料粉碎步骤粉碎的粉碎物混合,并加入水后进行微粉碎;空气注入步骤,注入空气,以使通过上述微粉碎步骤的微粉碎的粉碎物具有颗粒形状;成型步骤,将通过上述空气注入步骤具有颗粒形状的微粉碎物放入模具并进行加压成型;烧成步骤,对上述成型步骤成型的成型物进行烧成;以及研磨步骤,对通过上述烧成步骤烧成的成型物的表面进行研磨。
[0063]
上述原料粉碎步骤是将麦饭石、火山石、碳、火山灰及黑云母分别以350目至700目的大小粉碎的步骤,若通过上述原料粉碎步骤粉碎的原料的粒子大小小于350目,则因粒子大小过大而使通过上述微粉碎步骤微粉碎的过程难以进行,若通过上述原料粉碎步骤粉碎的原料的粒子大小大于700目,则通过上述微粉碎步骤微粉碎的过程的效率会有所提高,但因粉碎工程的时间过长而有可能导致生产性降低。
[0064]
上述微粉碎步骤由如下的过程组成:以如上所述的含量范围混合分别通过上述原料粉碎步骤粉碎的粉碎物,相对于100重量份的上述混合物混合60重量份至80重量份的水后,使用球磨机将其微粉碎至1000目至3000目的粒子大小。
[0065]
在此情况下,若通过上述过程微粉碎的粉碎物的粒子大小小于1000目,则因成型后产品的表面粗糙而不美观,若粉碎物的粒子大小大于3000目,则会降低生产性。
[0066]
上述空气注入步骤是注入空气以使通过上述微粉碎步骤微粉碎的粉碎物呈颗粒形状的步骤,并且是使用喷雾干燥机注入空气以使通过上述微粉碎步骤微粉碎的粉碎物呈颗粒形状的步骤。
[0067]
在上述过程中,使用喷雾干燥机注入空气以具有颗粒形状是为了防止在上述成型步骤中所进行的加压过程中对产品产生裂纹及裂缝。
[0068]
上述成型步骤是将通过上述空气注入步骤具有颗粒形状的微粉碎物放入模具并进行加压成型的步骤,其由将通过上述空气注入步骤具有颗粒形状的微粉碎物放入模具并进行加压成型的过程实现,上述加压成型是制造所要制造的形状的模具并将呈颗粒形状的粉末填充到油空压机后,按照产品的种类施加响应压力来成型的过程。在此情况下,如果可以原样使用上述颗粒形状的微粉碎物,则也可以重新粉化使用。
[0069]
上述烧成步骤是对通过上述成型步骤成型的成型物进行烧成的步骤,其由对通过上述成型步骤成型的成型物以900℃至1200℃的温度进行10小时至24小时的烧成的过程实现。
[0070]
在上述烧成步骤中,若烧成温度低于900℃,则因烧成不能完全进行而降低成型物的外观品质,若上述烧成温度高于1200℃,则会降低成型品的机械物性。并且,在上述烧成步骤中,若烧成时间小于10小时,则不能完全烧成,若在上述烧成步骤中,烧成时间大于24小时,则降低生产性。
[0071]
上述研磨步骤是对通过上述烧成步骤烧成的成型物的表面进行研磨的步骤,其由如下的过程实现:当完成由如上所述的温度及时间进行的烧成步骤时,自然冷却所烧成的成型物,并对自然冷却的成型物的表面进行研磨。
[0072]
上述研磨步骤由通过将切割石放入震动抛光机或离心抛光机来切割上述成型物的表面后进行研磨的过程实现,在此情况下,切割时间平均为20小时至30小时左右。
[0073]
并且,在经如上所述的时间的切割过程后,将其表面被切割的成型物放入抛光研磨机,并放入抛光石及抛光用化合物进行抛光研磨。
[0074]
在如上所述地以两个步骤进行切割及研磨的情况下,当将陶瓷组合物用作项链、手链等的医疗设备时,因其外观美观而商品性得到提高。在制造出通过如上所述的过程放射远红外线的陶瓷组合物,将其以适当的大小和重量牢固包装并销售,其可应用于电热垫、热疗设备、腰带、坐垫、枕头、手链及项链等的医疗设备。
[0075]
并且,在上述微粉碎步骤与上述空气注入步骤之间还可以进行用银纳米微粒子对通过上述微粉碎步骤微粉碎的粉碎物进行涂敷的步骤。若用银纳米微粒子涂敷上述微粉碎的粉碎物,则远红外线陶瓷组合物的抗菌性大大提高。
[0076]
在此情况下,在对上述微粉碎的粉碎物涂敷银纳米微粒子的过程中,通过混合表面活性剂和硝酸银来制备混合溶液。在此情况下,阳离子、阴离子、非离子表面活性剂均可用作上述表面活性剂。而且,当将溶解有硼酸钠的水溶液作为还原剂加入到上述混合溶液时,在溶解的银粒子还原的过程中,上述混合溶液的颜色从无色渐渐变为深棕色并生成银微粒子。在此情况下,所加入的表面活性剂阻碍银微粒子的生长,从而获得银纳米粒子分散在水溶液中的胶体。而且,为了去除如上所述的银微粒子的生成后未反应的物质及杂质,以5000rpm至8000rpm的速度离心分离,则所生成的银纳米微粒子分离为银纳米微粒子及溶液,弃去上清液并重复洗涤三次,来最终制备借助表面活性剂稳定的银胶体。为了获得如此
制备的银纳米微粒子均匀分散的粉末,向上述微粉碎的粉碎物加入0.5%的盐酸(hcl)或氢氟酸(hf)溶液并进行酸处理,将其与稳定的银胶体混合并搅拌,则生成涂敷有纳米微粒子的微粉碎物,可以通过使用喷雾干燥机注入空气以使其呈颗粒形状的方式进行干燥来使用。
[0077]
在此情况下,上述酸处理是因为若进行酸处理,则在上述微粉碎的粉碎物的表面生成多个硅烷醇基(sioh),并且去除了杂质,因此可以使银纳米微粒子容易地固定。在此情况下,优选地,上述微粉碎的粉碎物与银胶体的混合比例为100:0.1重量份至100:0.4重量份,但不限于此。
[0078]
上述控制部控制上述低强度超声波使其具有0.5mhz至1.5mhz的频带及100mw/cm2至150mw/cm2的强度以显示出炎症缓解及改善效果,优选地,控制上述低强度超声波使其具有1.1mhz的频带、120mw/cm2的强度、1:9的脉冲持续时间(pulse duration)、50%的工作周期(duty cycle)的条件。
[0079]
并且,上述控制部控制上述低强度超声波使其每次具有15分钟至25分钟的照射时间,优选地,控制上述低强度超声波使其每次具有20分钟的照射时间。
[0080]
并且,上述控制部控制上述温热刺激部使其加热至35℃至40℃的温度,以便从构成上述温热刺激部的陶瓷组合物大量放射远红外线,最优选地,控制上述温热刺激部使其加热至38℃的温度。
[0081]
并且,根据本发明的用于缓解及改善炎症的装置的操作方法包括:通过生成上述低强度超声波来照射炎症部位的步骤;将通过加热陶瓷组合物来产生的远红外线适用于炎症部位的步骤;以及控制所照射的上述低强度超声波的频带、强度及照射时间中的至少一种和上述陶瓷组合物的加热温度的步骤。
[0082]
上述炎症部位可以由关节炎损坏的骨组织部位,由此可以改善及治疗由关节炎损坏的骨组织部位。
[0083]
在此情况下,上述陶瓷组合物在成分、含量、制备方法及作用上与在上述使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置中所记载的内容相同,因此将省略其说明。
[0084]
上述控制步骤控制上述低强度超声波使其以0.5mhz至1.5mhz的频带及100mw/cm2至150mw/cm2的强度照射,优选地,控制上述低强度超声波使其具有1.1mhz的频带、120mw/cm2的强度、1:9的脉冲持续时间(pulse duration)、50%的工作周期(duty cycle)的条件。
[0085]
并且,将通过上述控制步骤控制的超声波以每周2次至4次的频率照射3周至5周,每次照射15分钟至25分钟,优选地,以每周3次的频率照射4周,每次照射20分钟。
[0086]
并且,在上述控制步骤中,将上述陶瓷组合物的加热温度控制为35℃至40℃,优选地,控制为38℃。
[0087]
并且,将通过上述控制步骤加热的陶瓷组合物以每次40分钟至80分钟、每周4次至6次的频率适用于炎症部位,持续3周至5周,优选地,以每次60分钟、每周5次的频率适用于炎症部位,持续4周。
[0088]
以下,将参照实验例说明根据本发明的使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置的操作方法及通过其操作方法所产生的效果。
[0089]
制备例1:放射远红外线的陶瓷组合物的制备
[0090]
以350目至700目的大小分别粉碎麦饭石、火山石、碳、火山灰及黑云母,通过混合分别粉碎的95.9kg的麦饭石、1kg的火山石、0.1kg的碳、2kg的火山灰及1kg的黑云母来制备混合物,将70kg的水与100kg的上述混合物混合,使用球磨机粉碎成1000目至3000目的粒子大小后,用喷雾干燥机向通过上述过程粉碎的粉碎物注入空气来制粒,将制粒的粉碎物放入模具并压缩成型,将烧成压缩成形的成型物在1050℃的温度下烧成17小时,切割烧成的成型物后,放入抛光研磨机,加入抛光石及抛光用化合物并通过抛光研磨过程制备了放射远红外线的陶瓷组合物。
[0091]
实验例1:在raw 264.7细胞(cell)中的ndc刺激的抗炎作用的评估
[0092]
raw 264.7细胞的培养及lps处理
[0093]
为了观察免疫反应,在培养箱(incubator)中培养了raw 264.7细胞(37℃、5%的co2)。细胞培养分为对照组、炎症诱导组、放射远红外线的陶瓷组合物及低强度超声波刺激组。为了诱导炎症,以1μg/ml的浓度处理了脂多糖(lps,lipopolysaccharide)。放射远红外线的陶瓷组合物是在培养箱内相应细胞培养皿(cell culture dish)上、下放置通过上述制备例1制备的方式远红外线的陶瓷组合物来进行培养,而低强度超声波刺激则通过使产生1.1mhz、120mw/cm2的低强度超声波的换能器接触到相应细胞培养皿下部来进行刺激,为了超声波刺激,在皿与换能器之间涂敷了超声波刺激用凝胶。
[0094]
将通过蛋白质印迹(western blot)分析由本发明的实验例1处理的巨噬细胞(raw 264.7cell)的诱导型一氧化氮合酶蛋白示于图1。
[0095]
如图1所示,可知,与炎症诱导组(lps)相比,由通过本发明的装置放射远红外线的陶瓷组合物及强度超声波刺激的实验组(lps-ndc-u)的诱导型一氧化氮合酶蛋白的表达明显减少。
[0096]
并且,将通过一氧化氮测定方法分析由本发明的实验例1处理的巨噬细胞(raw 264.7cell)的一氧化氮的合成量示于图2。
[0097]
(但是,一氧化氮的测量使用了一氧化氮测定方法,上述一氧化氮测定方法使用格里斯试剂(griess reagent),该测定方法是如下的方法:将样品(sample)离心后,分别分离100μl的上清液,并在常温下,将100μl的格里斯试剂(griess reagent)在96孔板(well plate)上反应10分钟后,以595nm的波长测定吸光度。)
[0098]
如以下图2所示,可知,与炎症诱导组(lps)或对照组(con)相比,由通过本发明的装置发射远红外线的陶瓷组合物及低强度超声波刺激的实验组(lps-ndc-u)的一氧化氮的合成量明显降低。
[0099]
实验例2:在诱导类风湿性关节炎的小动物中观察血液中白细胞介素-6浓度(ra+ndc+u)
[0100]
给实验大鼠(c57bl6、雄性、8周龄)提供基本饮食(固体饲料,cargill agri purina股份有限公司,群山,韩国/自由饮水)一星期和适应环境后,每组配置10只,以使各组具有类似的平均体重。
[0101]
实验组1:向10只8周龄雄性大鼠(c57bl6)的足底分别注射0.05ml的关节炎诱导物质以诱导关节炎,上述关节炎诱导物质是通过将弗氏完全佐剂(cfa,complete freund's adjuvant)与生理盐水以1:1的重量比混合而成,在从诱导关节炎的时间经过一周后,将诱导关节炎的骨组织部位介于具有由通过上述制备例1制备的陶瓷组合物组成的温热刺激部
的根据本发明的用于改善及治疗由关节炎损坏的骨组织的装置,以38℃的温度进行温热刺激,每次1小时,以每周5次的频率进行4周,同时通过超声波照射部向诱导关节炎的骨组织部位施用低强度超声波(1.1mhz的频率(frequency)、120mw/cm2的强度(intensity)、1:9的脉冲持续时间(pulse duration)、50%的工作周期(duty cycle))4周,每周3天,每次20分钟。
[0102]
实验组2:向10只8周龄雄性大鼠(c57bl6)的足底分别注射0.05ml的关节炎诱导物质以诱导关节炎,上述关节炎诱导物质是通过将弗氏完全佐剂(cfa,complete freund's adjuvant)与生理盐水以1:1的重量比混合而成,在从诱导关节炎的时间经过一周后,将关节炎产生部位介于通过上述制备例1制备的陶瓷组合物的上部,以38℃的温度进行温热刺激,每次1小时,以每周5次的频率进行4周。
[0103]
实验组3:向10只8周龄雄性大鼠(c57bl6)的足底分别注射0.05ml的关节炎诱导物质以诱导关节炎,上述关节炎诱导物质是通过将弗氏完全佐剂(cfa,complete freund's adjuvant)与生理盐水以1:1的重量比混合而成,在从诱导关节炎的时间经过一周后,向诱导关节炎的部位照射低强度超声波(1.1mhz的频率(frequency)、120mw/cm2的强度(intensity)、1:9的脉冲持续时间(pulse duration)、50%的工作周期(duty cycle))4周,每周3天,每次20分钟。
[0104]
关节炎诱导组:向10只8周龄雄性大鼠(c57bl6)的足底分别注射0.05ml的关节炎诱导物质以诱导关节炎,上述关节炎诱导物质是通过将弗氏完全佐剂(cfa,complete freund's adjuvant)与生理盐水以1:1的重量比混合而成,从诱导关节炎的时间开始放置5周。
[0105]
对照组:10只8周龄雄性大鼠(c57bl6)。
[0106]
通过测量由本发明的实验例2处理的实验组1、关节炎诱导组及对照组的血液中白细胞介素-6的浓度来以平均值示于图3。
[0107]
实验组1:关节炎诱导组及对照组的血液中白细胞介素-6的浓度是从实验组和对照组的心脏采血,用乙二胺四乙酸微型容器(edta micro-tainer)(bd biosciences,美国)仅分离血清以用作样品,使用小鼠白细胞介素-6elisa试剂盒(mouse il-6elisa kit)通过酶免疫法(mouse enzyme-linked immunosorbent assay[elisa]kits,ab100712,abcam,san francisco,ca,美国)定量小鼠血清内白细胞介素-6。
[0108]
实验方法是根据制造商(abcam)的elisa说明书进行,其结果如以下图3所示,可知,与关节炎诱导组(ra)相比,实验组(ra+ndc+u)与对照组(con)相同地,未测量到白细胞介素-6的浓度。
[0109]
通过拍摄上述实验例2的实验组1至实验组3、关节炎诱导组及对照组的足部来测量骨体积并示于图4。
[0110]
{但是,足部拍摄是使用体内微计算机断层扫描技术(in-vivo micro ct)(skyscan 1176,bruker,德国)进行,并且在第0天(day 0)和第28天(day 28)(关节炎诱导前、刺激4周后)通过呼吸麻醉拍摄足部。}
[0111]
如以下图4所示,可知,与关节炎诱导组(ra)或对照组(con)相比,本发明的实验组1(ra+ndc+u)、实验组2(ra+ndc)及实验组3(ra+u)的骨体积明显增加。
[0112]
并且,通过拍摄上述实验例2的实验组1至实验组3、关节炎诱导组及对照组的足部
来测量骨截面厚度并示于图5。
[0113]
{但是,足部拍摄是使用体内微计算机断层扫描技术(in-vivo micro ct)(skyscan 1176,bruker,德国)进行,并且在第0天(day 0)和第28天(day 28)(关节炎诱导前、刺激4周后)通过呼吸麻醉拍摄足部。}
[0114]
如以下图5所示,可知,与关节炎诱导组(ra)或对照组(con)相比,本发明的实验组1(ra+ndc+u)的骨截面厚度明显增加。
[0115]
并且,通过拍摄上述实验例2的实验组1至实验组3、关节炎诱导组及对照组的足部来测量平均截面片段数量并示于图6。
[0116]
{但是,足部拍摄是使用体内微计算机断层扫描技术(in-vivo micro ct)(skyscan 1176,bruker,德国)进行,并且在第0天(day 0)和第28天(day 28)(关节炎诱导前、刺激4周后)通过呼吸麻醉拍摄足部。}
[0117]
如以下图6所示,可知,与关节炎诱导组(ra)相比,本发明的实验组(ra+ndc+u)的平均截面片段数量明显减少,与对照组(con)相当。
[0118]
因此,根据本发明的使用远红外线放射陶瓷组合物和低强度超声波的用于缓解及改善炎症的装置用放射大量远红外线的陶瓷来温热刺激炎症部位,通过照射使细胞的运动或生长因子的合成增加并使诱导型一氧化氮合酶蛋白的表达减少的低强度超声波,来显示出从根本上缓解及改善炎症的效果。
[0119]
并且,根据本发明的使用远红外线放射陶瓷组合物和低强度超声波的用于改善及治疗由关节炎损坏的骨组织的装置用由放射大量远红外线的陶瓷组合物组成的温热刺激部来温热刺激由关节炎损坏的骨组织部位,以增加骨体积、增加骨截面厚度以及减少平均截面片段数量,并且通过照射低强度超声波来显示出改善及治疗由关节炎损坏的骨组织的效果。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1