用于在动脉闭塞远侧灌注组织的系统和方法与流程
背景技术:
本申请涉及用于在闭塞动脉远侧灌注组织的系统和对应方法,并且更具体地讲,涉及基于导管的系统,这些系统基于此类系统包括的传感器、效应器、控制器和过程来提供诊断信息,其中特别要注意被灌注的组织和灌注流体的特定特性。
本申请涉及用于在闭塞动脉远侧灌注组织的系统和对应方法,并且更具体地讲,涉及基于导管的系统,这些系统基于此类系统包括的传感器、效应器、控制器和过程来提供诊断信息,其中特别要注意被灌注的组织和灌注流体的特定特性。
存在用于评估血管闭塞后的组织状况的方法。例如,血管造影评估、关于临时测试闭塞和全身性低血压的激发试验、残端压力和放射性核素成像已用于评估在治疗结束前的侧支流量的充足性。灌注部分闭塞的血管以及测量生理参数也已经完成。压力梯度、流量梯度(血流储备分数,ffr)也已用于确定对狭窄的未闭塞血管进行选择性血管重建的需要。ffr通常指冠状动脉狭窄时最大可实现血液流量的整个心动周期压力衍生指数,其被表示为该动脉正常时的最大可实现血液流量的比率。
然而,以上所有评估都是基于静态测量值的指数,该静态测量值具有对压力、流量、阻力相互作用的线性期望,而没有对粘度、[o2]、组织体积或自动调节状态的调整。另外,通常用于获得这些测量值的药理操作超出了生理反应的范围(腺苷、二氢吡啶等)。这些前提不适用于具有自动调节的组织(诸如脑部、肾脏和心脏)-恰好是其中信息最关键的组织。另外,在这些组织中的每个组织内,诸如年龄、慢性高血压或组织压力、氧化应激的变化具有深远的影响。然而,以上方法仅提供粗略估计并且仅用于在最佳临床状况下预测结果。
因此,需要用于在闭塞远侧灌注组织的系统,该系统实时获取或以其他方式导出信息以用于例如组织抢救(包括血管区域中的正常、受损和死亡组织),而不会增加额外的创伤。此类可操作生理信息有益地使输注和/或再灌注更安全和更有效,并且/或者提供诱导缺血耐受性,以使组织更好地承受缺血性损伤以及与缺血和再灌注相关的继发性损伤。
技术实现要素:
该申请公开了允许在动脉闭塞远侧进行安全且有效的灌注的系统和对应方法。这些系统解决了该规程的许多当前确定的限制。灌注可以通过各种系统来实现,包括在标题为“systemandmethodforintravascularcooling(用于血管内冷却的系统和方法)”的美国专利8,343,097以及标题为“devicesforestimatingregionalmetabolicrateoforgansbasedonheatgenerationandforestimatingregionalbloodflow(s)forthevolume(s)oftissueperfused(用于基于热量生成来估计器官局部代谢率以及用于估计被灌注的组织体积的局部血液流量的设备)”的美国专利公布20160206816中公开的系统,上述专利均据此以引用方式并入本文。根据至少一个实施方案的本发明的系统包括流体导管(诸如其上附接有传感器或具有与其相关联的传感器的导管)、控制器、泵和流体源,其被通信地互连并且被编程以执行方法和/或执行算法,从而基于从传感器收集的数据以及来自操作员或查找表的输入来控制泵。设备通过确定被灌注组织的灌注液和组织灌注参数,并且在这些参数内进行灌注来完成这一点。这些参数可包括:a.灌注液参数:1)粘度、2)温度、3)[o2]、4)[co2]和5)其他血管活性物质,以及b.组织参数:1)灌注体积/压力/组织体积曲线,以及2)估计的自动调节形状或不良自动调节曲线。
可由这些系统和方法获得或以其他方式导出临床可操作的信息和治疗操作。此类信息可包括:1)组织自动调节的功能状态,2)被灌注的组织的量,3)避免突破缺血性或气压性创伤阈值所需的血压参数,4)所需的o2和流量要求。另外,可估计血管顺应性和侧支循环状态。
附图说明
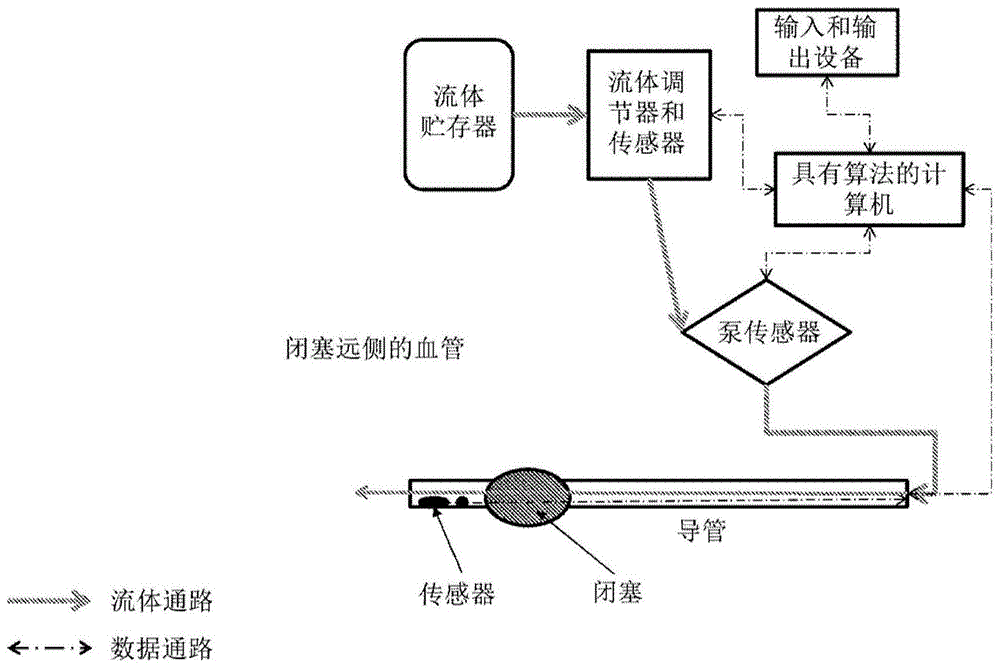
图1是根据本文公开的系统的至少一个实施方案的用于在闭塞远侧灌注组织的系统的示意图。
图2是根据本文公开的方法的至少一个实施方案的通过系统操作执行的用于在闭塞远侧灌注组织的方法的流程图。
图3是总结不同状况下的cbf(脑部组织的压力/灌注(针对100cc脑部体积)曲线)的自动调节的图。
图4是描绘肾脏实验数据,即在不同实验状况下的肾脏的自动压力灌注曲线的图。
图5a1至图5e3是示出在各种情况和状况下的针对脑部曲线的灌注压力(p,mmhg)与流量(q,cc/min)关系的理想化曲线的图。
图6是描绘恒定流速下的随时间推移的安全流量和压力的图。
图7是描绘整体流量压力/时间的图;示出了隐藏阈值。
图8是描绘整体流量:压力/时间的图;如果突破危险边界状况时的一些预期结果。
图9是描绘整体流量:压力/时间的图;安全恒定流量;类似于图6,具有使用所公开的设备时适当的生理阈值。
图10是描绘整体流量:压力/时间的图;安全脉动流量;具有使用所公开的设备时适当的生理阈值。
图11是描绘整体流量:压力/时间的图;危险初始流量。表明了即使流体的单个短脉冲也可超过极限值并且引起血管破裂。这就是在临床文献中不建议在闭塞远侧进行注射的原因。
图12是描绘整体流量:压力/时间的图;危险恒定流量。即使血管没有立即破裂,但随时间推移,仍可能随时间超过流量并且突破危险阈值
图13是描绘整体流量:压力/时间的图;危险脉动流量。即使血管没有立即破裂,但随时间推移,仍可能随时间超过流量并且突破危险阈值
图14至图18是描绘流量压力/时间的图;示出了阈值。
具体实施方式
当在闭塞血管远侧灌注组织时或者在故意闭塞血管的情况下,可操作信息受到限制。对于患有闭塞的患者,在闭塞远侧进行的灌注将提供大量潜在强大的治疗干预,诸如局部降低体温、脱细胞再灌注以及超选择性药物和溶解气体治疗。灌注远侧闭塞由于有关此类操纵的安全性和有效性的不确定性而受到限制。在操作上,在闭塞远侧进行的选择性灌注将需要关键的实时信息,诸如适当的压力、流速、被灌注的组织量、流体的粘度。[o2]、组织温度和组织的自动调节状态。需要此类信息来避免诸如血管灾难性破裂、恶性水肿、灌注不足和/或过度灌注的问题。
正常组织具有自恃自动调节,从而保护其免受气压性创伤并且确保足够的血液流量。另一方面,死亡组织可能对气压或流量相关的创伤发展为出血和细胞毒性水肿高度敏感,而缺血性受损组织的压力极大地取决于曲线的两端-得不到足够血液或损坏性充血。另外,缺血后充血和缺血再灌注损伤可能正在进行中。血液灌注液特性(诸如粘度和po2、co2)以及有效组织体积、组织代谢状态和温度都对于有效且安全灌注所需的体积和压力具有深远影响。迄今为止,在这方面几乎没有信息可用于指导专业人员。因此,本文公开的系统通常优选实时地提供此类信息以用于在血管闭塞远侧灌注组织。
另外,可以调节组织以更好地承受缺血。调节可以是具有内源特性的强大组织保护方法,类似于经由降低体温进行的组织保护。调节可在缺血性事件之前(预调节)、期间(内部或每次调节)和之后(后调节)执行。仅内部/每次调节和后调节是临床实用方法,而内部/每次调节比后调节更有效。可以通过在有害刺激之间定期灌注将组织反复暴露于缺血来执行调节。迄今为止,尚无设备或系统用于有效地和实用地对处于缺血/再灌注及相关损伤的急性风险中的组织进行调节。因此,本文公开的发明系统可进一步操作以优选地基于由系统获得或导出的实时信息来自动或半自动地提供组织调节。
有效地接管器官灌注的灌注组织的类似问题也面临着有关器官移植运输和心肺旁通回路的问题,并已通过动物和临床试验的指南得到解决。因此,尽管可结合脑部和脑部损伤来讨论本申请的实施方案,但应当理解,系统可结合其他器官使用并且因此在这方面不受限制。
参照图1,示出了根据至少一个实施方案的用于在闭塞远侧灌注组织的系统的示意图。将导管101放置在血管中,然后将导管101的尖端导航到闭塞102的远侧。导管100具有数据通路和流体通路。该数据通路的传感器104可以在导管的远侧端部中,或者在泵/泵传感器106/108的近侧。传感器104/108可以包括压力、流速,并且可以包括[o2]、温度和用于优选实时地原位捕获组织和/或灌注液的其他特性的传感器。系统还可以包括用软件编程的控制器100,该控制器可操作以执行算法,该算法使系统可操作以收集灌注所期望的数据(如本文所述)并且操作控制泵106的致动器以优选实时地执行期望的功能(也如本文所述)。控制器可根据查找表或根据来自系统操作员的输入来计算某些输入参数。系统还包括输入设备112(诸如开关、旋转拨号盘、小键盘或键盘、触摸屏等),以及用于显示信息的输出设备114(诸如lcd监视器、打印机等)。
系统还可在计算机存储器设备中存储关于温度、流速、时间等的一个或多个预定义指令集,其可由系统在用户进行选择时实现。如本文所讨论,指令集可包括针对系统的操作参数的序列和定时,例如,用于逐渐冷却和加热输注液和/或感兴趣部位,维持输注液和/或感兴趣部位的温度,控制压力和流速以及本文讨论的任何其他变量或参数。存储器可进一步将例如由系统收集和/或估计的数据存储在数据库中。还可以看出,系统包括用于储存输注液的贮存器116,以及优选地包括通过相关联传感器120获得的流体状况118。
图2是描绘关于确定用于灌注的输注流体的参数的系统操作的操作的流程图。可计算对流量特性的预期影响,并且可由系统确定阈值/警报限值。通常,一旦将导管放置在闭塞的远侧,然后便可确定残端压力,并且输注可开始并基于来自系统传感器的反馈而逐渐增加。然后可确定输注液体积/压力/分钟曲线,如本文所讨论的,其通过嵌入式过程用于计算生理上有意义的输注液体积/压力/分钟/组织体积曲线。然后,在考虑进行任何操作时,控制器可控制泵供应安全灌注。
该过程通常从来自用户的输入开始,或者基于系统经由传感器获得的信息,诸如输注液粘度(其可在原位或使用查找表来确定)、输注液温度和输注液的[o2]。此后,可在闭塞远侧引入导管,然后系统可测量参数(诸如残端压力)。然后,输注可以从所计算的流量和压力开始并且自残端压力以5%的增量进行施加。基于传感器反馈,然后可计算组织体积并且可估计自动调节拐点。顺应性和q/p可周期性地进行测试并且在整个治疗过程中根据需要进行调整。
图3是总结不同状况下的cbf(脑部组织的压力/灌注(针对100cc脑部体积)曲线)的自动调节的图。曲线针对全血输注液,其中[o2]、[co2]、有功能和无功能的自动调节改变,但未探索粘度或温度的影响,并且针对已灌注的100cc的脑部组织进行标准化。
图4描绘了来自肾脏实验的数据,并且更具体地描绘了在不同实验状况下的肾脏的自动压力灌注曲线。应当注意形状、斜率和截距与组织和输注液状况相关地变化。更具体地,该图示出了高血压中肾血管床中压力流量关系的频谱。模式a表示在无并发症的高血压中观察到的正常肾脏自动调节反应,并且示出了肾脏血液流量(rbf)的恒定性,尽管bp在自动调节范围内变化。模式b表明周围肾脏血管舒张,但在进行单肾切除术后却仍保持自动调节。模式c示出了在5/6肾脏消融模型中观察到的受损rbf自动调节反应。模式d示出了在用二氢吡啶ccb治疗的5/6肾脏消融的大鼠中的肾脏自动调节的完全丧失。尽管将rbf描绘为因变量,但考虑到自动调节阻力变化仅限于肾小球前脉管系统,因此预计pgc也会获得相同的关系。
图5a1至图5e3示出了在各种情况和状况下的针对脑部曲线的灌注压力(p,mmhg)与流量(q,cc/min)关系的理想化曲线。所探索的状况包括a)脑部体积的改变,b)脑部温度,c)具有完整自动调节和缺乏自动调节的脑部,以及灌注液充足,d)含氧血液或盐水,以及e)脱氧盐水。立即认识到组织灌注是复杂的。血管阻力用于确保足够的即时组织[o2]并且保护其免受气压性/充血性创伤。
图5a1至图5a3相对于具有完整自动调节并且在正常血细胞比容和正常温度下用正常含氧血液灌注的组织示出了在给定压力下的不同组织质量对流量的影响。
图5a1的曲线图针对100cc的脑部进行归一化。
图5a2的曲线针对50cc的脑部进行归一化。
图5a3的曲线针对200cc的脑部进行归一化。
图5b1至图5b3是理想化曲线,其相对于具有完整自动调节并且用充分含氧盐水灌注的组织示出了在给定压力下的不同体积对流量的影响。充分含氧盐水通常指的是携带足够的o2以进行组织代谢(或约4cc/100cc)的盐水。应当注意,对于灌注相同量的流体,低粘度盐水所需的压力要小得多。
图5b1的曲线图针对100cc的脑部进行归一化。
图5b2的曲线针对50cc的脑部进行归一化。
图5b3的曲线针对200cc的脑部进行归一化。
图5c1至图5c3是理想化曲线,其相对于具有完整自动调节并且用脱氧盐水灌注的组织示出了在给定压力下的不同体积对流量的影响。应当注意,对于灌注相同量的流体,低粘度盐水所需的压力要小得多,并且在使用脱氧流体的情况下,组织的行为类似于无自动调节的情况。
图5c1的曲线图针对100cc的脑部进行归一化。
图5c2的曲线针对50cc的脑部进行归一化。
图5c3的曲线针对200cc的脑部进行归一化。
图5d1至图5d3是理想化曲线,其示出了具有完整自动调节的组织以及在完整自动调节下的脑部/灌注液温度的影响(各自具有100cc的脑部体积)。应当注意,随着温度下降,脑代谢率(cmr)下降,这继而导致血液流量的下降。
图5d1的脑部/灌注液温度为33℃,被灌注有充分含氧血液。
图5d2的脑部/灌注液温度为26℃,被灌注有充分含氧血液。
图5d3的脑部/灌注液温度为33℃,被灌注有充分含氧盐水。
图5e1至图5e3与图5a1至图5a3类似,但添加了理想化的缺血阈值和充血阈值。曲线图相对于具有完整自动调节并且在正常血细胞比容和正常温度下用正常含氧血液灌注的组织示出了在给定压力下的不同组织质量对流量的影响。缺血阈值被理想化为等于20cc的充分含氧血液/100cc的脑部/min。充血阈值具有两种类型:压力>1.5倍正常值时为高血压,流量为高雷诺数时为高流量血管病。
如图5b1至图5b3所示,有可能向具有完整自动调节的组织递送足够的氧气并且向其灌注充分含氧盐水。缺血阈值被理想化为等于20cc的充分含氧血液/100cc的脑部/min。曲线图将类似于图5e1至图5e3中描绘的曲线图。实际提取的氧气量仅为4cc,并且也可使用高压方法以溶解氧的形式输送。充血阈值似乎具有两种类型:压力>1.5倍正常值时为高血压,流量为高雷诺数时为高流量血管病。
图6至图18示出了整体流量与压力关系,以及每单位体积组织的流量与曲线的使用场景关系。应当注意,这些整体流量图中的单位是以cc为单位的流量/min,其与临界生理指标、脑血液流量等中使用的单位不同,后者是以cc为单位的流量/min/100cc的组织。
图6示出了恒定流速下的随时间推移的安全流量和压力。
图7示出了整体流量压力/时间;示出了隐藏阈值。阈值的具体值取决于被灌注的组织的量、[o2]等。
图8示出了整体流量:压力/时间;如果突破危险边界状况时的一些预期结果。
图9示出了整体流量:压力/时间;安全恒定流量;类似于图6,具有使用所公开的设备时适当的生理阈值。
图10示出了整体流量:压力/时间;安全脉动流量;具有使用所公开的设备时适当的生理阈值。
图11示出了整体流量:压力/时间;危险初始流量。表明了即使流体的单个短脉冲也可超过极限值并且引起血管破裂。这解释了在临床文献中不建议在闭塞远侧进行注射的原因。
图12示出了整体流量:压力/时间;危险恒定流量。即使血管没有立即破裂,但随时间推移,仍可能随时间超过流量并且突破危险阈值
图13示出了整体流量:压力/时间;危险脉动流量。即使血管没有立即破裂,但随时间推移,仍可能随时间超过流量并且突破危险阈值
图14至图15示出了流量压力/时间;示出了阈值。应当注意,尽管可估计导管和营养血管的总阈值(图14),但很有可能在受损的营养血管中,阈值可能会完全不同。
重新参见图1,根据本文公开的至少一个实施方案的系统由多个部件以及使用该设备的方法组成。系统部件通常包括:
1)医用导管,其可放置或导航到动脉中,从而以由系统控制的流量、压力和其他变量向目标组织供给灌注液。血管已经被闭塞,在这种情况下,导管放置在闭塞的远侧。在血管不闭塞的情况下,设想足以闭塞目标血管的远侧尖端的扩大。在要施用冷流体的情况下,将并入绝缘传感器和温度测量传感器。在一个实施方案中,导管为5french、140cc长、空气绝缘的单个耐高压内腔导管,其中柔软锥形尖端的、单轨引导的导管从股动脉途径通过引导导管放置到脑循环中。在另一个实施方案中,导管为5french、100cc长、空气绝缘、双腔、远侧的球囊导管,其中柔软锥形尖端的、单轨引导的导管从股动脉途径通过引导导管放置到冠状循环中。在另一个实施方案中,导管为7french、115cc长、空气绝缘、双腔、远侧的球囊导管,其中柔软锥形尖端的、单轨引导的导管从股动脉途径通过引导导管放置到颈内动脉循环中并且用于测试闭塞以及在血栓提取期间使用。
2)传感器包括接近实时的压力和流量测量设备,其优选位于导管的远侧端部处。这些设备可位于导管的远侧尖端处,或者例如更近侧地位于导管柄部中。如果放置在更近侧,则必须将导管阻力和顺应性的校正合并到由系统执行的计算中。附加的传感器可包括导管和/或流体贮存器中的温度传感器、[o2]等,以及气泡检测器。在一个实施方案中,温度传感器将位于流体通路中的远侧尖端处,并且第二传感器位于流体贮存器中,其中压力传感器位于与导管相接的泵注射器中,用于校正导管和连接管的阻力,并且伺服机构监测注入的流体量。在另一个实施方案中,压力传感器、流体速率传感器和温度传感器将在远侧嵌入导管。成本、尺寸和传感器技术将决定优选实施方案。
3)泵优选是高精度、数字控制的体积或压力相关泵。据设想,当输注冷盐水时,该泵将为高压泵,以克服所需的小直径流体导管的高阻力,以便减少通过时间的热量损失或增加对额外绝缘的需求。在这种情况下,将需要对导管和/或远侧压力传感器的阻力进行高度准确的校正。泵要求将取决于特定的临床应用。一个泵可能无法以合理的成本覆盖所需的全部范围。然而,对这种泵的描述将是精确控制到1mmhg压力的递送,要求向远侧递送0-60mmhg的范围,其中流速为0-150cc/min以及精确控制的+/-5%cc/min流速。另外,设想将安全阀或分流器安装到位以作为泵故障的备用。
4)输入和输出设备是必需的以允许操作员输入和访问有关规程的信息。可以用计算机gui来显示由系统确定或以其他方式计算的相关变量,如本文所讨论的,包括位于远侧或在泵和/或贮存器处或介于两者之间的任何点的温度、压力、流量、[o2]等。另外,可分别合并音频警报和视觉警报。
5)具有传感器的流体贮存器和流体调节器;流体贮存器足以存储和/或维护/调节输注液的特性/参数(诸如温度、压力、[o2]等)。
6)计算机控制器:控制器足以处理由用户捕获和输入和/或查找的数据,以计算本文讨论的用于控制泵的变量,并且基于这种输入和计算/确定来控制泵。
7)算法:系统优选地通过允许对闭塞远侧的灌注进行计算和控制的过程来编程。具体地,通过确定:
输注液的参数:
1.粘度,
2.[o2]、[co2],
3.温度,以及
4.导管的顺应性、阻力,以及
5.所输注的体积与压力关系的曲线。
可基于输注液参数使用算法来计算以下关键参数中的一个或多个:
1.被灌注的组织量。
2.自动调节曲线的形状。
3.具有完整自动调节与功能失调的自动调节的组织量。
4.组织血管顺应性。
5.临界阈值的估计。
系统然后可以:
1.控制组织的灌注参数,
2.在安全临界阈值内;以及
3.监测所有临界变化并且相应地调整。
正常血液流量:到组织的血液流量取决于局部血管阻力。当组织需要更多血液时,组织血管扩张,从而导致局部血管阻力的下降,并且更多的血液流向组织。堵塞动脉导致中风和心脏病发作。堵塞血管导致堵塞远侧的组织血压的大幅下降。当这种情况发生时,远侧组织的局部血管严重扩张,从而导致组织血管阻力的大幅下降,但不足以维持活组织血液流量。存在这种渐变。血管床是网络,并且这些血管(位于闭塞远侧,来自未闭塞的其他血管)的血液流量,即“侧支流量”是关键的。血管所服务的组织的时间和量也很重要。组织血液流量受到的限制越多,血液流量受到限制的时间越长,组织将死亡的可能性就越大。
自动调节:包括脑部、心脏和肾脏在内的组织自动调节流量。这种现象被称为自动调节,在大血压范围内保持血液流量恒定。这是通过响应于血液流量而改变血管阻力来进行的。曲线的特征在于初始斜率、平台和最终斜率。第一斜率终止于自动调节的下限lla。第二斜率开始于自动调节的上限ula。自动调节曲线的斜率(斜率下和斜率上)类型分别为每mmhg/组织体积的cbf变化1.7%和2.0%。斜率下与平均实验数据类似;斜率上较小。该曲线可从图3中看出,显示了自动调节曲线的形状被许多代谢成分(包括[o2]、[co2])改变。其也可由高血压、创伤和中风所引起的血管床的变化改变。尽管此处未显示,但也存在与温度和血液粘度有关的显著变化。根据大量实验数据很好地表征这些效应。在具有衰竭的自动调节的组织床中,流量将取决于灌注压力(图16)。众所周知,在较高压力下,损坏血管和引起出血的风险增加(流量破坏阈值)(图14至图18)。取决于血管床的完整性(损伤的类型、强度和持续时间),破坏阈值可能变化,例如,健康(高阈值)、缺血性损伤(低阈值)、创伤性损伤(低阈值)。因此,由于具有完整自动调节的组织床中看到的压力耐受性的宽范围的减小或完全消失,因此在具有衰竭的自动调节的受损组织床中达到流量破坏阈值的风险增加(图17、图18)。
对自动调节曲线进行建模:自动调节曲线的许多数学模型可用,所有这些都可以用作预期血液流量/分钟/组织体积的基础。基于流动物理学的两个模型是固定的或可变的最大血管反应性。高于自动调节上限ula的可变最大流量-压力关系与低于自动调节下限lla的该关系具有相同的斜率,并且因此与其平行。这是基于以下事实:在实验文献中最经常描述的cbf自动调节曲线示出了可以通过拟合到cbf-压力曲线的报告数据来计算和使用该平行模式a的三阶多项式,例如,
cbf=4.79×10-5p3-1.74×10-2p2+2.51p-38.8-1.74×10-2p2+2.51p-38.8。
这被限制为不解释、不直观并且在较低的流量水平下不准确。
当在闭塞远侧灌注时,组织的体积未知。如果要确定生理测量流量/分钟/组织体积,则必须计算该组织体积。另外,除非灌注液是血液或具有类似粘度的物质,否则将成比例地改变流速。同样有问题的是温度、[o2]、[co2]的影响以及自动调节的运行。
因此,问题是给定测量的输注体积/压力曲线和输注液粘度、[o2]、[co2]、温度和设备顺应性、阻力时计算组织的流量/分钟/体积,给定灌注情况时识别新阈值,以及最终将灌注保持在这些阈值内。
在这方面,本申请公开了一种系统,其执行以下中的一者或多者。1)输入或查找正常情况下的血液的正常、已知和预期的自动调节曲线。2)输入或查找当血液作为输注液时的斜率、平台和临界阈值。3)输入或测量影响灌注物料流量的因素,诸如粘度和导管特性。4)确定影响对灌注物料流量(诸如[o2]、[co2])的组织反应和组织自动调节状态的因素。5)给定#3和#4,计算出新预期压力-体积/组织灌注单位曲线。6)将这些值(#3、#4和#5)加载到计算机中,从而以每单位流量/压力的预期斜率、平台和阈值控制泵。6)放置设备,并且开始输注,以及使用输注液体积压力信息来计算组织的流量/分钟/体积。
在至少一个实施方案中,用于将正常生理血脑自动调节曲线映射到输注液的体积/压力曲线的方法可以是微分、线性代数或串行一阶校正。优选的实施方案是串行一阶校正,因为它是说明性的、直观的、最容易执行的,并且在此进行了教导。
在以下附图中可以看到这些想法的图形表示。图5a1至图5a3示出了用含氧血液灌注的组织量将如何改变体积/压力曲线。图5b1至图5b3示出了充分含氧的低粘度流体(诸如盐水)将如何改变在不同灌注组织量下的体积压力曲线。图5c1至图5c3类似地示出了不含氧盐水以及没有调节的组织的影响。图5d1至图5d3示出了温度对代谢进而对自动调节曲线的影响。图5e1至图5e3示出了可如何确定缺血的明显阈值和高压-充血阈值。图6示出了在输注安全、有效的恒定体积的流体时的压力时间曲线。图7示出了所遵守的阈值。图8示出了系统可以防止交叉的各种阈值。图9和图10示出了在恒定和脉动模式下在阈值内工作的设备和方法。图11、图12、图13示出了突破阈值的可能故障模式。图14至图15示出了总血管和营养血管的阈值可能不相同,并且图16至图18的实例具有完整的自动调节并且已衰竭。
算法的导出
计算:
·确定被灌注的脑部的cc,cbf,
·当在37.8℃的温度下用盐水灌注时,[o2]不变
·对于来自q/p曲线初始部分的数据,
·给定q/p曲线,
假定:
a)qbulk=p*lπ(r)4/8η灌注液由所公开的设备测量
b)
c)l、π(r)4/8在两个等式中都是相同的。
i.l、r在自动p/v曲线的两端都相同,其中血管的半径和长度被最大地扩张。
ii.qcbf/p曲线的形状在正常情况下是已知的[针对η=3.6的血液,[o2]>4cc/100cc的脑部,温度=37.8,具有完整的自动调节等]。
(1)针对具有自动调节的组织;初始(p=1-75mmhg)斜率和最终(p>175mmhg)斜率与最大扩张一致。
(2)针对具有自动调节的组织;曲线中间部分(175>p>75mmhg)的斜率为零。
(3)对于没有自动调节或没有o2的组织,斜率在整个p范围内与最大扩张类似。
d)初始和最终qcbf/p斜率近似=55cc/min/75mmhg/100cc的脑部。
e)每一个单位压力和脑部体积的血液流量/分钟的复合斜率:=0.0074cc/min/1mmhg/1cc的脑部应当注意,这表示系统的最大斜率。
f)灌注液的η是已知的,并且对于盐水而言是0.9cp,或者是血液的η的1/4。
在粘度为1/4的情况下校正流动盐水将使被灌注的脑部的流量或量在相同压力下增加4倍。
但是由于血管被最大地扩张,因此被灌注的脑部量在相同压力下必须增加,或者压力在相同灌注下必须减少。
由于4*0.0074cc/min/1mmhg/1cc的脑部≠0.0296cc/min/1mmhg/1cc的脑部
g)然后4*0.0074cc/min/1mmhg/1cc的脑部必须
1.(0.0074cc/min/0.25mmhg/1cc的脑部)=
2.0.0074cc/min/1mmhg/4cc的脑部
h)使用这一点,可以确定用输注液灌注的脑部的体积,在给定压力梯度下该输注液的粘度为血液的粘度的1/4:
(qbulk/p)/(0.0074cc/min/0.25mmhg/1cc的脑部)=灌注的以cc为单位的脑部
i)示例;如果用37.8℃盐水输注血管并且给出以下公式:
qbulk/p=(20cc/min)/(10mmhg)
则脑部的体积
=(20cc/min)/(10mmhg)/((0.0074cc/min)/(0.25mmhg/1cc的脑部))
=67.6cc的脑部
则以cc/min/100cc为单位的脑部的cbf为
=(20cc/min)/(67.6cc/100cc的脑部)
=29.6cc/min/100cc的脑部/
鉴于以上所述,可以探索预期的缺血阈值、预期的高压阈值、预期的充血阈值、自动调节曲线的拐点以及温度对代谢率进而对cbf的影响。
用于确定预期的缺血阈值的示例性计算:
假定脑部需要4cc的o2/100cc的脑部/分钟的在37.8℃下的可用o2。应当注意,这假设所有溶解的o2可用,这是对盐水的简化,但并非对于血液(其是粗略的近似值)。o2含量可通过溶解时间分压来计算。因此,缺血阈值为0.04cc的o2/1cc的脑部/分钟,则67.6cc的脑部需要(67.6cc的脑部)×(0.04cc的o2/1cc的脑部/分钟)或此组织在该流量下的缺血阈值要求输注盐水具有[o2]=2.7cc。假设存在约0.034cc的[o2]/100cc的盐水,因此在输注盐水中为0.0034cc的[o2]/1cc的盐水×67.6cc的脑部=0.23cc。因此,通过输注0.23cc的o2/min/1cc的脑部无法满足2.7cc的缺血阈值。如果未达到缺血阈值,则q/v曲线的斜率保持不变。
缺血阈值可通过以下方式来满足:1)通过增加压力来增加流量,2)通过降低代谢率cmro2来降低阈值,或3)增加溶解的o2。从理论上讲,这些中的每一者可以独立地增加12倍(2.7/0.23)。将压力增加12倍或增加到120mmhg(12×10mmhg)将达到缺血阈值。但这将在超过充血阈值时损坏组织。充血阈值很难(如果不是不可能的话)与高压阈值分开,并且在组织水平下可能几乎是同义词。为了我们的目的,我们将流量和/或压力视为独立的破坏阈值。尚不清楚在高于其时损坏组织毛细血管等的流速的确切流动性质,然而估计将其置于约100-120cc/min/100cc的脑部或1-1.2cc/min/1cc的脑部。
假设在此示例中,进入脑部的流量为29.6cc/min/100cc的脑部/,并且将在100-120cc/min/100cc的脑部下满足预期充血阈值,压力只能在可预期充血性损坏之前增加3-4倍或者增加到30-40mmhg的压力。应当注意,高压阈值似乎在200-220mmhg的范围内,但在慢性高血压中较高,而在未执行自动调节的组织中较低。从而:新缺血阈值为0.04cc的o2/1cc的脑部/min的1/2或0.02cc的o2/min/1cc的脑部;67.6cc的脑部需要(67.6cc的脑部)×(0.02cc的o2/1cc的脑部/min);或在此流量下的该组织量的缺血阈值要求输注盐水具有[o2]=1.35cc的o2/min。假设存在约0.34cc的[o2]/100cc的盐水,因此在输注盐水中为0.0034cc的[o2]/1cc的盐水/min×67.6cc的脑部=0.23cc的o2/min。
通过使用高压可达到缺血阈值,从而增加o2的分压。在正常生理状况下室内空气中的o2的分压约为100mmhg。没有血红蛋白的惊人有效的o2承载能力时,[o2]只能来源于流体(并且在该示例中是盐水)中的溶解氧。在3atp时,o2的分压增加约20倍。在此示例中,可以通过将o2在盐水中的分压增加到大约2atp来达到缺血阈值。这种过饱和流体会自发起泡。
通过采用降低体温,也可在较低流速下达到缺血阈值。降低体温,在冷却盐水中具有三种影响;1)将cmr减少约10%/1℃,2)将o2的溶解度增加约1.5%/1℃,并且3)将粘度增加1.5%/1℃。(对于此示例,冷却对粘度和溶解度的影响可以忽略,因为它们较小,尺寸类似,并且可对o2的递送具有相反的影响)。
实施例:使用上面的实施例给出,假设我们将流体的温度冷却到25℃,并且假设脑部很快达到该较低温度。这将使cmro2减少约75%,从而将减少a所需的[o2]并且由此将缺血阈值降低50%。
组织调节:在上述参数的监测下,可通过控制和反复降低动脉闭塞远侧的组织温度来调节处于缺血性损伤和与缺血相关的继发性损伤风险中的组织。因此,动脉闭塞可以是病理状况(例如,缺血性中风/梗塞),或人为造成的(例如,球囊闭塞)。在降温阶段之间暂停,以允许组织温度恢复到较高的温度。通过这样做,可使得处于危险中的组织准备好更好地承受由缺血和再灌注引起的后果。
尽管出于清楚和理解的目的已经对上述发明进行了详细描述,但本领域的技术人员通过阅读本公开内容将理解,可以在形式和细节上进行各种改变而不背离本发明的真实范围。
- 还没有人留言评论。精彩留言会获得点赞!