多糖的乙酰化的制作方法
通过引用并入任何优先权申请
根据37cfr1.57,在与本申请一起提交的申请数据表中标识的其外国或国内优先权要求的任何和所有申请据此通过引用并入本文中。
公开的领域
本文所述的实施方案涉及增加多糖中乙酰化的量的方法、乙酰化的多糖和治疗方法。特别地,多糖衍生自植物或其植物部分。当对植物部分实施制备工艺以提取其多糖时,这种纯化工艺导致天然植物多糖的脱乙酰化。本文描述了在加工制备方法之后增加植物多糖中乙酰化的量的方法,使得乙酰化的水平超过天然植物多糖中最初发现的多糖中的乙酰化量。
相关技术的描述
多糖是多年来受到越来越多关注的用于补充剂和药物的天然资源。已经显示出天然多糖具有较少的副作用,但是由于其固有的物理化学性质,它们的生物活性难以与合成药物的生物活性相比。因此,研究人员已经基于构效关系改变了天然多糖的结构和性质,并且已经获得了更好的功能改进的多糖。然而,多糖的主要修饰方法可能是必需的,因为它们可以影响它们的物理化学性质和生物活性。分子修饰方法主要包括化学、物理和生物改变。化学修饰是最广泛使用的方法;通过接枝到其他基团上,可显著提高多糖的水溶性和生物活性。物理和生物修饰仅改变多糖的分子量,从而改变其物理化学性质和生物活性。大多数的分子修饰导致多糖的抗氧化活性增加,并且在这些修饰中,硫酸化和乙酰化修饰是非常常见的。此外,修饰是如本文所讨论的增加抗炎活性的最常见的应用。
背景
该领域涉及用于开发用于治疗应用的乙酰化的糖或碳水化合物的植物和植物部分的加工。本文还描述了获得高度乙酰化的糖或碳水化合物的有效方法,所述糖或碳水化合物已经从植物和/或植物部分提取出。
芦荟是芦荟属的肉质植物物种。它在世界各地的热带气候中野生生长并栽培用于农业和医药用途。芦荟由于其保湿和愈合特性而在化妆品和替代医药工业中得到广泛认可。
芦荟已经使用了数十年以缓解刺激例如干燥的皮肤或晒伤引起的疼痛。芦荟凝胶的提取和表征已经揭示了该凝胶包含许多类型的粘多糖。
在医学实践中,多糖已知为可解释其治疗性质的信号传导分子。已知形成凝胶的复合碳水化合物用作缓和剂或润肤剂。在一些情况下,已经认识到几种类型是抗炎和免疫调节剂。
多糖,乙酰化甘露聚糖,是由β-(1→4)-连接的d-甘露糖残基的主要主链组成的多糖,所述β-(1→4)-连接的d-甘露糖残基被少量葡萄糖残基点缀,在o-2、o-3、o-2/o-3或o-6处乙酰化,其含有由o-6-连接的单个α-d-半乳糖和α-l-阿拉伯糖残基构成的侧链。芦荟乙酰化甘露聚糖可具有免疫刺激活性。对多糖的结构细节的研究已经表明乙酰化甘露聚糖呈现复杂的乙酰化模式。然而,在多糖的提取和加工过程中,多糖可以被脱乙酰化。乙酰化的多糖已被归因于促进免疫调节活性。因此,需要以高含量有效地乙酰化该多糖的羟基的方法以保持其免疫调节活性。
概述
在第一方面,提供了制备乙酰化的多糖的方法。该方法包括a)提供多糖;b)将所述多糖纯化至90重量%的纯度;c)提供乙酰化试剂;d)提供催化剂;e)将所述乙酰化试剂和催化剂与所述多糖混合,从而制备乙酰化的多糖,其中乙酰化超过步骤a)中多糖的乙酰化;以及f)纯化所述乙酰化的多糖。在一些实施方案中,所得多糖的特征在于乙酰化超过天然存在的多糖的乙酰化。在一些实施方案中,多糖来自植物或其植物部分。在一些实施方案中,多糖为粉末制剂。在一些实施方案中,多糖来自植物或其植物部分的提取过程。在一些实施方案中,植物或其部分包含全叶粉末状提取物或植物内部透明凝胶粉末状提取物。在一些实施方案中,所述植物是芦荟属的肉质植物。在一些实施方案中,其植物部分包含外部绿皮和/或植物内部透明凝胶。在一些实施方案中,多糖包括葡甘露聚糖、葡半乳甘露聚糖、半乳甘露聚糖、甘露聚糖及它们的乙酰化形式。在一些实施方案中,多糖包含羟基,其中羟基能够被乙酰基取代。在一些实施方案中,多糖包含甘露糖部分。在一些实施方案中,甘露糖部分包含羟基,其中所述羟基能够被乙酰化。在一些实施方案中,乙酰化的多糖在甘露糖部分上在甘露糖位点2、3和/或6处包含乙酰基。在一些实施方案中,将多糖纯化至1-90重量%纯度。在一些实施方案中,将多糖纯化至90重量%纯度。在一些实施方案中,乙酰化的多糖被纯化至90重量%纯度。在一些实施方案中,所述方法还包括测定乙酰化的多糖的含量和乙酰化的多糖上乙酰基的位置。在一些实施方案中,通过红外光谱法(ir)和/或核磁共振(nmr)光谱法进行测定。在一些实施方案中,乙酰化试剂是乙酸酐(ch3co)2o、乙酰氯或乙酸。在一些实施方案中,催化剂是吡啶、氢氧化钠、氢氧化钾、碳酸钠或碳酸钾和/或溶剂。在一些实施方案中,步骤b)的纯化步骤通过乙醇沉淀进行。在一些实施方案中,步骤d)的纯化步骤通过透析进行。
在第二方面,提供了由本文任一实施方案中的方法制备的乙酰化的多糖。在一些实施方案中,所述方法包括a)提供多糖;b)纯化多糖至90重量%纯度;c)提供乙酰化试剂;d)提供催化剂;e)将乙酰化试剂和催化剂与多糖混合,从而制备乙酰化的多糖,其中乙酰化超过步骤a)中多糖的乙酰化;以及f)纯化所述乙酰化的多糖。在一些实施方案中,所得多糖的特征在于乙酰化超过天然存在的多糖的乙酰化。在一些实施方案中,多糖来自植物或其植物部分。在一些实施方案中,多糖为粉末制剂。在一些实施方案中,多糖来自植物或其植物部分的提取过程。在一些实施方案中,植物或其部分包含全叶粉末状提取物或植物内部透明凝胶粉末状提取物。在一些实施方案中,所述植物是芦荟属的肉质植物。在一些实施方案中,其植物部分包含外部绿皮和/或植物内部透明凝胶。在一些实施方案中,多糖包括葡甘露聚糖、葡半乳甘露聚糖、半乳甘露聚糖、甘露聚糖和/或它们的乙酰化形式。在一些实施方案中,多糖包含羟基,其中羟基能够被乙酰基取代。在一些实施方案中,多糖包含甘露糖部分。在一些实施方案中,甘露糖部分包含羟基,其中所述羟基能够被乙酰化。在一些实施方案中,乙酰化的多糖在甘露糖部分上在甘露糖位点2、3和/或6处包含乙酰基。在一些实施方案中,将多糖纯化至1-90重量%纯度。在一些实施方案中,将多糖纯化至90重量%纯度。在一些实施方案中,乙酰化的多糖纯化至90重量%纯度。在一些实施方案中,所述方法还包括测定乙酰化的多糖的含量和乙酰化的多糖上乙酰基的位置。在一些实施方案中,通过红外光谱法(ir)和/或核磁共振(nmr)光谱法进行测定。在一些实施方案中,乙酰化试剂是乙酸酐(ch3co)2o、乙酰氯或乙酸。在一些实施方案中,催化剂是吡啶、氢氧化钠、氢氧化钾、碳酸钠或碳酸钾和溶剂。在一些实施方案中,步骤b)的纯化步骤通过乙醇沉淀进行。在一些实施方案中,步骤d)的纯化步骤通过透析进行。在一些实施方案中,乙酰化的多糖包含至少一个、至少两个或至少三个乙酰基。在一些实施方案中,乙酰化的多糖包含甘露糖基团。在一些实施方案中,多糖包括葡甘露聚糖、葡半乳甘露聚糖、半乳甘露聚糖、甘露聚糖和/或它们的乙酰化形式。
在第三方面,提供了药物制剂,其包含本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖和药学上可接受的赋形剂。在一些实施方案中,制剂是丸剂。在一些实施方案中,制剂是液体。在一些实施方案中,制剂是片剂、胶(gummy)、胶囊或锭剂。在一些实施方案中,制剂还包含无毒辅助物质,例如润湿剂、ph缓冲剂和吸收增强制剂。
在第四方面,提供了治疗、改善或预防有需要的个体的炎性反应的方法。所述方法包括向有需要的患者施用本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖或本文提供的任一实施方案的药物制剂。在一些实施方案中,乙酰化的多糖每天至少三次、每天两次、每天一次、每周一次或每月一次施用。在一些实施方案中,患者患有免疫病症。在一些实施方案中,所述免疫病症是系统性狼疮、硬皮病、溶血性贫血、血管炎、i型糖尿病、格雷夫斯病、类风湿性关节炎、多发性硬化、goodpasture’s综合征、肌病、重症联合免疫缺陷、digeorge综合征、超免疫球蛋白e综合征、常见变异型免疫缺陷、慢性肉芽肿病、wiskott-aldrich综合征、自身免疫淋巴细胞增生性综合征,高igm综合征、白细胞粘附缺陷、nf-κb必需调节蛋白(nemo)突变、选择性免疫球蛋白a缺陷、x-连锁无丙种球蛋白血症、x-连锁淋巴增生性疾病或共济失调-毛细血管扩张。在一些实施方案中,患者被鉴定为接受用于炎症的治疗。在一些实施方案中,患者被鉴定为接受用于免疫病症的治疗。在一些实施方案中,所述方法还包括测量或评价炎症反应的抑制。在一些实施方案中,所述方法还包括在施用本文任一实施方案的乙酰化的多糖或通过本文实施方案的方法制备的乙酰化的多糖或本文实施方案的药物制剂之前、期间或之后,向所述个体提供另外的治疗。在一些实施方案中,个体是患者。在一些实施方案中,患者是个体。在一些实施方案中,个体是哺乳动物。在一些实施方案中,个体是人、马、狗、猫。
在第五方面,提供了治疗有需要的个体的免疫病症的方法。所述方法包括向有需要的患者施用本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖或本文提供的任一实施方案的药物制剂。在一些实施方案中,乙酰化的多糖每天至少三次、每天两次、每天一次、每周一次或每月一次施用。在一些实施方案中,所述免疫病症是系统性狼疮、硬皮病、溶血性贫血、血管炎、i型糖尿病、格雷夫斯病、类风湿性关节炎、多发性硬化、goodpasture’s综合征、肌病、重症联合免疫缺陷、digeorge综合征、超免疫球蛋白e综合征、常见变异型免疫缺陷、慢性肉芽肿病、wiskott-aldrich综合征、自身免疫淋巴细胞增生性综合征,高igm综合征、白细胞粘附缺陷、nf-κb必需调节蛋白(nemo)突变、选择性免疫球蛋白a缺陷、x-连锁无丙种球蛋白血症、x-连锁淋巴增生性疾病或共济失调-毛细血管扩张。
在第六方面,提供了增加有需要的个体的抗炎il-10(白介素10)的表达的方法。所述方法包括向有需要的患者施用本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖或本文提供的任一实施方案的药物制剂。在一些实施方案中,乙酰化的多糖每天至少三次、每天两次、每天一次、每周一次或每月一次施用。在一些实施方案中,患者患有免疫病症。在一些实施方案中,所述方法还包括监测抗炎il-10(白介素10)的表达。在一些实施方案中,有需要的个体是哺乳动物。在一些实施方案中,个体是人、马、狗、猫。
在第七方面,提供了提高有需要的个体的抗炎性细胞因子的表达的方法。所述方法包括向有需要的患者施用本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖或本文提供的任一实施方案的药物制剂。在一些实施方案中,乙酰化的多糖每天至少三次、每天两次、每天一次、每周一次或每月一次施用。在一些实施方案中,患者患有免疫病症。在一些实施方案中,所述方法还包括监测抗炎的表达。在一些实施方案中,有需要的个体是哺乳动物。在一些实施方案中,个体是人、马、狗、猫。在一些实施方案中,抗炎性细胞因子选自白介素(il)-1受体拮抗剂、il-4、il-6、il-10、il-11和il-13。
在第八方面,提供了治疗有需要的个体的肿瘤的方法。所述方法包括向有需要的患者施用本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖或本文提供的任一实施方案的药物制剂。在一些实施方案中,乙酰化的多糖每天至少三次、每天两次、每天一次、每周一次或每月一次施用。在一些实施方案中,患者患有癌症。在一些实施方案中,所述肿瘤选自肺癌、皮肤癌、肝癌、脑癌、肾癌、子宫癌。在一些实施方案中,患者被鉴定为接受用于癌症的治疗。在一些实施方案中,所述方法还包括测量或评价肿瘤生长。在一些实施方案中,所述方法还包括在施用本文任一实施方案的乙酰化的多糖或通过本文任一实施方案的方法制备的乙酰化的多糖或本文任一实施方案的药物制剂之前、期间或之后,向所述个体提供另外的治疗。在一些实施方案中,个体是哺乳动物。在一些实施方案中,个体是人、马、狗、猫。
在第九方面,提供了治疗有需要的个体的病毒或细菌感染的方法。所述方法包括向有需要的患者施用本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖或本文提供的任一实施方案的药物制剂。在一些实施方案中,所述方法还包括监测在病毒或细菌感染期间释放的细胞因子的水平。所述方法包括向有需要的患者施用本文提供的任一实施方案的乙酰化的多糖或通过本文提供的任一实施方案的方法制备的乙酰化的多糖或本文提供的任一实施方案的药物制剂。在一些实施方案中,细胞因子选自il-1β、il-6、il-7、il-8、il-10,肿瘤坏死因子(tnf)-α、干扰素(ifn)-γ和ifn-α/β。
在一些实施方案中,乙酰化的多糖具有约1千道尔顿至约70千道尔顿的分子量。在一些实施方案中,乙酰化的多糖具有约5千道尔顿至约50千道尔顿的分子量。在一些实施方案中,乙酰化的多糖具有约10千道尔顿至约40千道尔顿的分子量。在一些实施方案中,乙酰化的多糖具有约15千道尔顿至约30千道尔顿的分子量。在一些实施方案中,乙酰化的多糖具有约18千道尔顿的分子量。在一些实施方案中,乙酰化的多糖具有约29千道尔顿的分子量。在一些实施方案中,乙酰化的多糖具有小于、大于或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69或70千道尔顿或在它们之间的任何数或任何范围的分子量。
附图的简要说明
本文所述的组合物、系统、装置和方法的特征和优点将从以下描述中并结合附图变得显而易见。这些附图仅描述了根据本公开内容的几个实施方案,而不应被认为是对其范围的限制。在附图中,除非上下文另有规定,否则类似的附图标记或符号通常标识类似的组件。附图可能不按比例绘制。
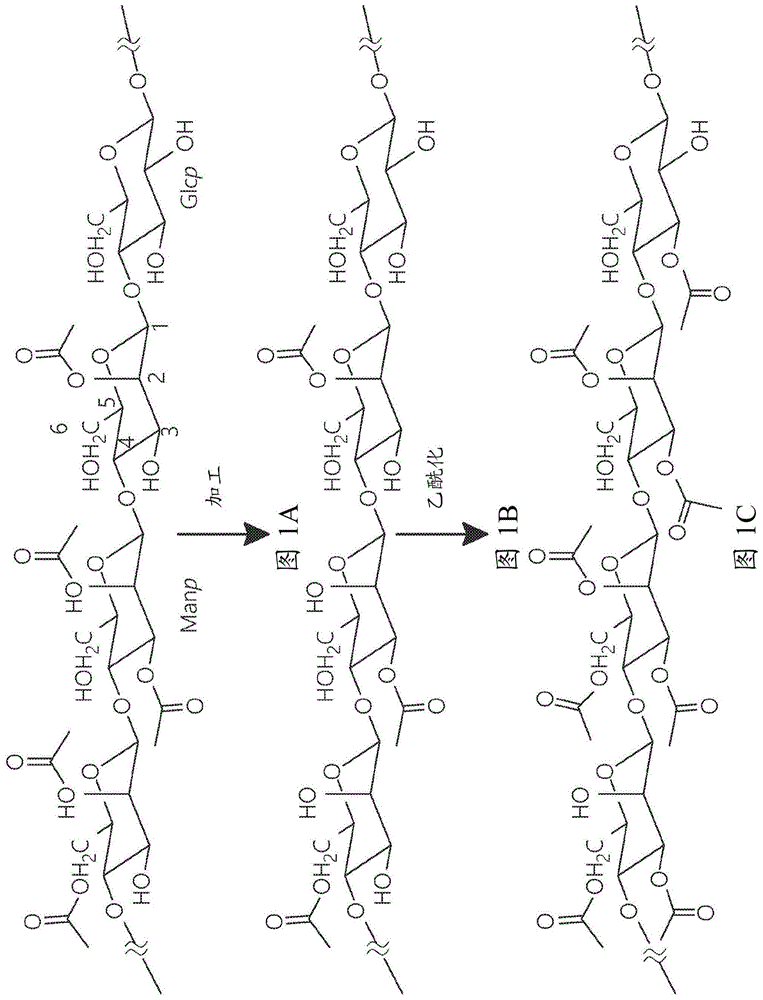
图1a-1c显示了乙酰化天然芦荟葡甘露聚糖的方法。图1a)插入有葡糖基的天然芦荟葡甘露聚糖的一般结构,其具有1,4-β-连接的主链并且在2、3或6位乙酰化;图1b)加工后具有较少乙酰基的多糖;图1c)乙酰化后高度乙酰化的多糖。manp:吡喃甘露糖基;glcp:吡喃葡萄糖基。
图2a显示粗多糖83008-175-15(1)的ir光谱。
图2b显示来自粗多糖83008-175-15(1)的乙酰化产物83018-3-3(2)的ir光谱。
图3显示a)粗多糖83008-175-15(1)的1hnmr光谱;b)来自该粗多糖的乙酰化产物83018-3-3(2)的1hnmr光谱。
图4a显示富集的多糖83018-7-11(3)的ir光谱。
图4b显示来自富集的多糖83018-7-11(3)的乙酰化产物83018-9-21(4)的ir光谱。
图5显示a)富集的多糖83018-7-11(3)的1hnmr光谱;b)来自该富集的多糖的乙酰化产物83018-9-21(4)的1hnmr光谱。
图6显示a)富集的多糖83018-7-11(3)的碳-13光谱;b)来自该富集的多糖的乙酰化产物83018-9-21(4)的碳-13光谱。6m:吡喃甘露糖基的c-6;6m6:6-乙酰基吡喃甘露糖基的c-6;3m23:2,3-二乙酰基吡喃甘露糖基的c-3。
图7显示富集的多糖83018-7-11(3)的hsqc谱;hsqc用于直接关联c-h耦合的核。在等高线图中,水平轴和垂直轴分别是质子化学位移和碳化学位移。当质子与碳键合时,在来自碳信号的水平线和来自质子信号的垂直线的交点处可以发现交叉峰。
图8显示富集的多糖83018-9-21(4)的hsqc谱。
图9a显示乙酰化的多糖降低抗炎活性。该图显示1-4对细胞因子il-1β、il-6、il-8、il-10、mip-1α和tnfα的作用。
图9b显示1-4对细胞因子il-10的作用。
定义
如本文所述,“多糖”是由通过糖苷键结合在一起的单糖单元的长链组成的聚合的碳水化合物分子。在水解过程中,这些多糖裂解成组分单糖或寡糖。多糖在结构上可以从直链多糖到高度支化的多糖。有几种类型的多糖。在没有限制的情况下,多糖可以包括结构多糖、中性多糖、酸性多糖、细菌荚膜多糖和储存多糖。多糖在有生命的有机体如植物中的功能可以是结构相关的或储存相关的。淀粉(葡萄糖的聚合物)在植物中用作储存多糖,其以直链淀粉和支化的支链淀粉的形式存在。
“纯化”是本领域技术人员已知的技术,其中化合物、化学物质、蛋白质或dna作为外来物质或污染物质。不受限制,纯化可以通过亲和纯化、过滤、蒸发、液-液萃取、结晶、重结晶和分馏进行。在一些实施方案中,将粗多糖纯化至1-90重量%纯度。在本文的一些实施方案中,将粗多糖纯化至90重量%纯度。在本文的一些实施方案中,乙酰化产物被纯化至90重量%纯度。在一些实施方案中,通过本文所述的方法产生的产物通过乙醇沉淀来纯化。在一些实施方案中,通过透析进行纯化。
如本文所述的“葡甘露聚糖”是芦荟中的主要多糖,其由具有1,4-β-连接的主链的甘露糖和葡萄糖组成,其中甘露糖是主要的。
如本文所述的“乙酰化”是指将乙酰基官能团引入化合物中的反应。乙酰化是指将乙酰基(导致乙酰氧基)引入化合物的过程,即,乙酰基取代活性氢原子。在本文的一些实施方案中,多糖在羟基处被乙酰化。术语“乙酰基”是指“-c(=o)ch3”基团。
如本文所述的“乙酰化试剂”是用于化合物的乙酰化的化学物质。不受限制,可以在酸催化剂或碱催化剂的存在下用酸酐进行乙酰化。各种金属盐如cocl2、ticl4-agclo4、tacl和tacl5-sio2、ce(iii)三氟甲磺酸盐、sn(iv)卟啉和一些金属三氟甲磺酸盐如sc(otf)3、mesiotf、in(otf)3、cu(otf)2和bi(otf)3、双(环戊二烯基)二氯化锆、i2、1,3-二溴-5,5-二甲基乙内酰脲(hydentoin)或三氯异氰尿酸也可用于反应中以提高效率。
如本文所述的“催化”是指在称为“催化剂”的另外物质的存在下化学反应速率的增加。如本文所述,用于乙酰化的方法也可与催化剂一起提供。在本文的一些实施方案中,催化剂是吡啶、氢氧化钠、氢氧化钾、碳酸钠或碳酸钾和溶剂。
如本文所述,“红外光谱法”(ir光谱法或振动光谱法)是涉及电磁光谱的红外区域的光谱法,即,具有比可见光更长的波长和更低的频率的光。其涵盖主要基于吸收光谱法的一系列技术。ir光谱法是本领域技术人员已知的,并且可以用于化合物和化学品的鉴定和表征。在本文的一些实施方案中,ir光谱法用于测定多糖的含量或用于表征多糖。
如本文所述,“核磁共振光谱法”或“nmr光谱法”是利用某些原子核的磁性的研究技术。可以使用它来确定原子或包含该原子的分子的物理性质和化学性质。1d、2d或3dnmr光谱的分析可使用分子的化学位移的研究来用于测定所关注的分子的性质、特征和结构。该技术是本领域技术人员已知的,并且可以使用例如200、300、400、500、600、800、900mhznmr仪器来应用。在本文的一些实施方案中,使用nmr光谱技术分析多糖的乙酰化含量。
本文所述的“药物赋形剂”是指与药物的活性成分一起配制的物质。可以包含它以为了长期稳定的目的、填充(bulkingup)含有有效活性成分的固体制剂(因此通常称为“填充剂(bulkingagent)”、“填充剂(filler)”或“稀释剂”),或赋予最终剂型中的活性成分治疗增强,例如促进药物吸收、降低粘度或增强溶解度。赋形剂也可用于制备过程中,以帮助处理所涉及的活性物质,例如通过促进粉末流动性或不粘特性,以及帮助体外稳定性,例如防止在预期的储存期内变性或聚集。合适的赋形剂的选择还取决于给药途径和剂型,以及活性成分和其它因素。
本文所述的“免疫病症”是指免疫系统的功能障碍。免疫病症可以是“原发性免疫缺陷疾病”,其是由遗传性基因突变引起的疾病。免疫病症也可以是“继发性或获得性免疫缺陷”,其由身体外的某物如病毒或免疫抑制药物引起。不受限制,实例是系统性狼疮、硬皮病、溶血性贫血、血管炎、i型糖尿病、格雷夫斯病、类风湿性关节炎、多发性硬化、goodpasture’s综合征、肌病、重症联合免疫缺陷、digeorge综合征、超免疫球蛋白e综合征、常见变异型免疫缺陷、慢性肉芽肿病、wiskott-aldrich综合征、自身免疫淋巴细胞增生性综合征,高igm综合征、白细胞粘附缺陷、nf-κb必需调节蛋白(nemo)突变、选择性免疫球蛋白a缺陷、x-连锁无丙种球蛋白血症、x-连锁淋巴增生性疾病或共济失调-毛细血管扩张。例如,当在患者的血清或脑脊液中检测时,可以通过检查神经特异性自身抗体或其它生物标记的特征谱来分析免疫病症。
本文所述的“细胞因子”是指在细胞信号传导中重要的小蛋白。细胞因子释放对在它们周围的细胞的行为有影响。细胞因子作为免疫调节剂参与例如自分泌信号传导、旁分泌信号传导和内分泌信号传导。抗炎性细胞因子的实例可包括但不限于白介素(il)-1受体拮抗剂、il-4、il-6、il-10、il-11和il-13。
详细说明
多糖是芦荟中的主要成分之一。芦荟中的主要的多糖是葡甘露聚糖,其由具有1,4-β-连接的主链的甘露糖和葡萄糖组成,其中甘露糖是主要的。甘露糖部分的羟基可以被乙酰基取代,并且芦荟多糖被称为乙酰化的葡甘露聚糖或可互换地称为乙酰化甘露聚糖(acemannan)。乙酰化甘露聚糖是文献中常用的商品名。据报道,乙酰化的葡甘露聚糖负责芦荟的多种生物活性,包括免疫刺激、抗炎、降血糖、降血脂、抗菌、抗病毒和抗肿瘤作用。
在甘露糖部分上发现的乙酰化的基团的位置是2-、3-或6-乙酰基,2,3-;2,6-;或3,6-二乙酰基和2,3,6-三乙酰基取代。在天然的乙酰化的葡甘露聚糖中发现的所报道的乙酰基含量在芦荟中是15-26%乙酰化。
芦荟叶包括外部绿皮和内部透明凝胶。外部绿皮和内部凝胶都含有多糖。在芦荟制备方法中,基于待使用的植物部分,可使用外部绿皮和凝胶(称为100x)由整个叶提取物制备芦荟叶产物,或由仅使用内部凝胶(称为200x)的提取物制备芦荟叶产物。在芦荟产品制备过程中,将酶和/或热施加到植物部分上。酶和热都可以使多糖脱乙酰化,导致多糖上的乙酰基减少。因此,当多糖经历制备过程时,乙酰基的含量通常小于它们的天然前体。为了恢复或增加在制备过程中损失的乙酰基的含量,在与葡甘露聚糖的反应中使用乙酰化试剂来合成高度乙酰化的多糖。
在本文的实施方案中描述了芦荟粉末,其用作反应起始材料,其首先通过乙醇沉淀纯化。过滤乙醇未溶解的多糖并与乙醇可溶性分子分离,得到粗芦荟多糖。然后将粗多糖溶于水中,并在装有纯化水的容器中透析。经常用新鲜水替换水,直到透析过程完成。离心透析液,然后冷冻干燥,得到纯度为70重量%-90重量%的富集的乙酰化的葡甘露聚糖。
乙酰化试剂乙酸酐(ch3co)2o用于制备高度乙酰化的葡甘露聚糖。乙酰氯和乙酸也可以用作乙酰化剂。用乙酸酐处理粗多糖或富集的多糖,并通过透析来纯化反应产物,以去除未反应的乙酰化剂、催化剂(例如吡啶、氢氧化钠、氢氧化钾、碳酸钠或碳酸钾和溶剂)。对纯化的反应产物进行光谱分析和化学分析以测定多糖含量和乙酰基含量。
红外光谱法(ir)和核磁共振(nmr)光谱法用于反应起始材料和产物的鉴定和定量。
在一些实施方案中,患者被鉴定为在被医师诊断患有炎症后接受用于炎症的治疗。在一些实施方案中,炎症表现为皮肤或内部器官的发热、疼痛、发红、肿胀和功能丧失中的一种或多种。在一些实施方案中,患者被鉴定为在被医师诊断患有免疫病症后接受用于免疫病症的治疗。在一些实施方案中,通过监测患者中的抗炎性细胞因子来测量炎症反应的抑制,所述抗炎性细胞因子选自白介素(il)-1受体拮抗剂、il-4、il-6、il-10、il-11和il-13。在一些实施方案中,患者被鉴定为在被医师诊断患有癌症后接受用于癌症的治疗。在一些实施方案中,通过用一种或多种以下技术监测肿瘤的大小来测量和评估肿瘤生长:计算机断层成像、磁共振成像(mri)、x-射线、乳房x线照相术、超声和正电子发射断层成像(pet)。
材料和方法
芦荟叶汁粉末(200x或100x)购自海南南洋芦荟生物工程(美国)有限公司(hainanaloecorpco.,ltd.)(中国海南)或pharmachemlaboratories,inc.,improveusa(anaheim,ca,usa)。无水乙醇和二甲亚砜(dmso)购自国药集团化学试剂有限公司(sinopharmchemicalreagentco.,ltd)(中国上海)。透析膜购自上海源叶生物科技有限公司(shanghaiyuanyebiologicaltechnologyco.,ltd)(中国上海)。乙酸酐购自成都科隆化学品有限公司(chengdukelongchemicalreagentinc.)(中国成都)。吡啶购自中国上海试剂工厂(中国上海)。所有试剂和化学品不经进一步纯化即使用。傅立叶变换红外光谱法在perkinelmerfrontierft-ir光谱仪(perkinelmerinstruments,norwalk,ct,usa)上进行。1hnmr(400mhz)和13cnmr(100mhz)光谱在brukerultrashield400plus或bruker400avanceiii仪器(fremont,ca,usa)上记录,用d2o作为溶剂(sigma-aldrich,st.louis,mo,usa)。化学位移以百万分率(ppm,δ)报告。通过称量约2-10mg样品和5mg内标物烟酰胺(sigma-aldrich,st.louis,mo,usa)进行通过1hnmr对乙酰基的定量。将样品和烟酰胺都溶解在1ml的d2o中,并在4℃下培育24h,然后进行nmr分析。使用brukertopspin软件的标准梯度脉冲序列,通过异核单量子相干(hsqc)光谱获得1h-13c相关光谱,并在pabbobb-1h/dz-grd探针上进行。使用配备有tskgelpwxl保护柱(40x6mm)(sigma-aldrich)的polysep-gfc-p-linear柱(300x7.5mm)(phenomenex,inc.,torrance,ca,usa),在尺寸排阻色谱法(sec)上测定多糖的分子量。流动相是0.1mnacl,其在使用前通过0.22μmgswp膜(merckmillipore,darmstadtgermany)预过滤。在分析期间,使流动相进一步通过在线过滤器(0.10μmx25mmdurapore膜过滤器,milliporeco.,bedford,ma),然后到达sec柱。流速为0.7ml/min,注射体积为100μl,并且在35℃下实施柱色谱法。样品最初以0.25-2mg/ml的浓度溶解在0.1mnacl中,使其在4℃下溶胀20-24小时,然后在注射前通过0.45μmmce过滤器过滤。光散射测量使用dawnenhancedopticalsystem(dawnheleosii)mals检测器,其配备有100mw662nmga/as激光器和18°研究级光散射光度计(wyatttechnologyco,santabarbara,ca,usa)。色谱系统由具有waters2410差示折射计(waterscorp,milford,ma,usa)的2690分离模块组成。该仪器由制造商使用用于mals检测器的在甲苯中的200kda聚苯乙烯和用于mals/ri检测器的66,000da牛血清白蛋白(bsa)进行验证。所述sec/mals/ri检测器串联连接。使用bsa测定检测器间延迟为255.6μl。使用wyattastra6.1.5.22软件分析来自光散射和差示折射计的数据。在整个实验期间使用0.14ml/g的折射率增量(dn/dc)。使用zimm外推法处理得自mals测量的数据。对于通过用普鲁兰多糖或葡聚糖标准物校准的sec/ri系统进行的样品mw和mwd分析,通过绘制分子量对保留时间的对数来获得校准曲线,并且使用empower3gpc/sec软件(waterscorp,milford,ma,usa),对窄多分散性普鲁兰多糖进行线性回归,并对宽多分散性葡聚糖进行三阶多项式拟合。对于普鲁兰多糖校准结合宽多分散性芦荟多糖,使用三阶多项式拟合。
实施方案1:由粗芦荟多糖制备乙酰化的多糖
将总共100克的200x芦荟叶汁粉末溶解在900毫升水中以制备10%芦荟溶液。在搅拌下向10%芦荟溶液缓慢加入3,600毫升乙醇,并将乙醇溶液在4℃下放置18小时。在乙醇溶液中形成白色沉淀,通过过滤系统获得沉淀。沉淀用250ml乙醇漂洗两次并冷冻干燥,得到39g粗多糖,83008-175-15(1)。
将总共500毫克的83008-175-15(1)置于100-ml圆底烧瓶中并加入40毫升dmso。将dmso溶液在室温下搅拌24小时后,依次将3毫升吡啶和2.5毫升乙酸酐引入dmso溶液中。下面所示的反应在冰水浴中搅拌30分钟的条件下进行。然后将反应溶液升温至室温,持续1.5小时。2小时后,向反应产物中加入水,并将溶液转移到具有截留分子量(mwco)为8,000-14,000da的透析膜管中。将反应产物透析直至除去吡啶的气味。冷冻干燥透析液,得到白色的乙酰化的多糖83018-3-3,产物的总重量为47毫克,纯度为86重量%(2)。
通过红外光谱法(ir)分析乙酰化产物(2),其中在~1741cm-1处的羰基(=o)和在~1247cm-1处的酯基(-o-)的拉伸键(stretchbond)显示出在乙酰化产物(2)中比在粗多糖(1)中更强(图2a和2b),表明在乙酰化产物(2)中存在更多的乙酰基,并且表明已经发生了乙酰化。与通过该反应的乙酰化的设备方法相比,该反应导致获得更高的乙酰化的令人惊讶的结果。
在1hnmr光谱中,乙酰基出现在2.0-2.2ppm处并进行定量。通过1hnmr表明,多糖分别在粗多糖(1)中产生7.5%的乙酰化,在乙酰化产物(2)中产生17.8%的乙酰化,这进一步证实了2的乙酰化(图3)。整个样品显示糖的多个乙酰化的羟基。
实施方案2:由富集的多糖制备乙酰化的多糖
将乙醇未溶解的粗多糖83008-175-15(1)在具有mwco8,000-14,000da的膜管中透析以产生富集的多糖83018-7-11(3)。然后如在实施方案1中所用的相同条件用乙酸酐-吡啶处理多糖3,得到乙酰化产物83018-9-21,(4)。使用截留分子量(mwco)为8,000-14,000da的膜,通过透析纯化产物4,冷冻干燥得到白色粉末。
多糖4在ir光谱中显示出比多糖3更强的约1742cm-1的羰基信号和约1244cm-1的酯信号(图4a和4b)。在1hnmr光谱(图5)的分析中,多糖3和多糖4的乙酰基的含量分别为17.2%和24.5%,表明如多糖产物4中所示的成功乙酰化。因此,与粗多糖相比,乙酰化反应令人惊讶地产生高百分比的乙酰化产物。
比较多糖3和多糖4的13cnmr,对应于乙酰基的信号增加(参见图6)。例如,在60.3ppm处的信号来自c-6,并且当6-o被乙酰基取代时向低场移动至63.5ppm。在3中在60.3ppm处的信号强度高于在63.5ppm处的信号强度,表明在3的6-oh处更少的乙酰基。然而,在多糖4中,来自乙酰化物c-6的强度显著高于其未乙酰化的c-6。类似地,由于在约72-74ppm的o-2和o-3的乙酰化,由c-2和c-3产生的信号也增加(图6)。
尽管13cnmr光谱清楚地显示了乙酰化前和乙酰化后多糖的差异,但由于其在这里的低灵敏度和低分辨率,在多糖3和多糖4上获得2dhsqc(异核单量子相干)光谱。在多糖3的hsqc光谱中,显示了在5.35,5.42/69.7处的来自质子-碳相干性的特征性交叉峰,其对应于c-2的信号,这是由于在o-2和o-3位两者上的乙酰基的取代,并且命名为2m23(m代表吡喃甘露糖基部分)。在5.10/71.7、5.34,5.40/71.6和4.78/73.1处的交叉峰分别起因于由于2,3-o-二乙酰基(3m23)取代引起的c-3的信号、由于2-o-乙酰基(2m2)取代引起的c-2的信号和由于3-o-乙酰基(3m3)取代引起的c-3的信号。在3.55,3.78/60.3处的交叉峰被指定为c-6(6m)的信号,即未乙酰基取代的6-o位置,而在4.19,4.28/63.5(6m6)处发现6-乙酰化的质子-碳交叉峰。在图7中示出了其它交叉峰的分配。
将多糖4的hsqc光谱(图8)与多糖3的hsqc光谱进行比较,由来自2-o-乙酰基(2m2)的c-2和3-o-乙酰基(3m3)的c-3取代的信号引起的交叉峰变成弱交叉峰或交叉峰消失,而2,3-o-二乙酰基取代的分别在5.34,5.41/69.5处的起因于c2(2m23)信号的交叉峰和在5.10/71.8处的由于c-3(3m23)信号的交叉峰变得占优势。类似地,在4中在4.16,4.37/62.6(6m6)处的6-乙酰化交叉峰的信号强度比在3.69,3.79/60.1(6m)处的未乙酰化信号强,而多糖3中在6m6和6m观察到相反的信号强度。所有这些结果表明,多糖4中存在比多糖3更多的乙酰基,证实多糖4是多糖3的乙酰化产物。
以与上述相同的方式对加工的芦荟多糖100x(033694-3500ps,6)、内部凝胶200x(030604-3500ps,9)和100x(032889-3500ps,12)进行乙酰化,分别得到三种乙酰化的多糖7(83018-51-22)、10(83018-51-20)和13(83018-16-16)。nmr分析证实了多糖7、10和13分别是其前体多糖6、9和12的乙酰化多糖。在乙酰化之前和乙酰化之后通过质子nmr测定的乙酰化基团的含量显示于表1中。
表1.乙酰化之前和之后多糖的乙酰化基团的含量
多糖分子量的分析
发现乙酰化后分子量降低(表2)。理论上,乙酰化的多糖的分子量应增加,因为增加了更多的乙酰基。降低的原因可能是乙酰化破坏了归因于氢键的多糖间的网络。乙酰基键的形成使得羟基的数目对于氢键较少可用。
表2.乙酰化之前和之后多糖的分子量
实施方案5:乙酰化的多糖的免疫调节活性
如表3所示,内部凝胶030604-3500ps,9的未乙酰化的芦荟制剂显示出免疫调节活性,因为其在lps存在下对pbmc的处理导致促炎性细胞因子(il-1β和il-6)的显著降低和抗炎性il-10的显著增加,这与它们被lps刺激的表达水平相比。有趣的是,该制剂的乙酰化83018-51-20,10,其乙酰化的多糖从13.5%增加到19.7%(增量为46%),导致促炎性il-1β和tnf-α的显著降低,这表明该特定芦荟制剂的乙酰化的增加引起其免疫调节活性的变化。另一方面,未乙酰化的芦荟凝胶粉末(200x)3显示出免疫调节活性,因为其在lps存在下对pbmc的处理导致il-6、tnf-α和ifn-γ的显著降低,并且导致il-10的显著增加,这与它们被lps刺激的表达水平相比。该制剂的乙酰化4,其乙酰化的多糖从14.2%增加到24.5%(增量为42%),导致il-10的显著增加,但导致促炎性细胞因子的不显著变化,表明该特定芦荟制剂的乙酰化的增加引起其免疫调节活性的变化。结果表明测试的芦荟制剂的乙酰化增加引起其免疫调节活性的显著改变。
表3.多糖的乙酰化基团的含量和对来自人pbmc的细胞因子表达的作用
实施方案6:粗多糖83018-3-3(2)的乙酰化
将500毫克的粗多糖83008-175-15(1)样品精确称量到50毫升圆底烧瓶中并加入40毫升dmso。将溶液在环境温度下搅拌24小时后,在冰水浴中相继加入3毫升吡啶和2.5ml乙酸酐,同时搅拌30分钟,然后升温至室温,并持续1.5小时。2小时后,通过添加20ml水淬灭反应。将反应产物转移到具有mwco8,000-14,000da的透析膜管中,直到没有闻到吡啶的气味。将透析液冻干,产生47mg白色的乙酰化的多糖83018-3-3(2)。ir(kbr)νmax.:3437,1741,1638,1376,1247,1037cm–1.1hnmr(400mhz,d2o)δ(ppm):2.01–2.20(br.,m,-coch3);13cnmr(100mhz,d2o)δ(ppm)100.2(c-1m),99.6(c-1m3),98.7(c-1m2),98.4(c-1m23),76.9(c-4m),75.0(c-5m),73.3(c-3m3),71.8(c-3m23),71.4(c-3m,c-2m2),69.8(c-2m),69.5(c-2m23),68.4(c-2m3),62.8(c-6m6)和60.3(c-6m)。乙酰基基团的含量为17.8%。
实施方案7:富集的多糖83018-9-21(4)的乙酰化
将500毫克的富集的多糖83018-7-11(3)精确称量到50毫升圆底烧瓶中并加入24毫升dmso。将溶液在环境温度下静置24小时,在冰水浴中相继加入1.8毫升吡啶和1.5毫升乙酸酐,同时搅拌30分钟,然后升温至室温,持续1.5小时。2小时后,加入水以淬灭反应,并将溶液转移到具有8,000-14,000da的mwco的透析膜管中。将反应产物透析,直到没有闻到吡啶的气味,并将透析液冻干,产生白色的富集的乙酰化的多糖产物83018-9-21(4),362毫克。ir(kbr)νmax.:3474,1742,1638,1375,1244,1043cm–1.1hnmr(400mhz,d2o)δ(ppm):1.98-2.22(br.,m,-coch3);13cnmr(100mhz,d2o)δ(ppm):100.2(c-1m),99.5(c-1m3),99.8(c-1m2),98.3(c-1m23),77.0(c-4m),75.0(c-5m),73.4(c-4m2),73.3(c-3m,c-3m3),71.8(c-3m23),69.7(c-3m),69.5(c-2m23),68.6(),62.6(c-6m6)和60.0(c-6m)。乙酰基基团的含量为24.5%。
实施方案8:用于制备粗多糖033694airs(5)的一般方法
将总共50克的芦荟叶汁粉末(100x,033694)精确称量到1l玻璃粉碎器中并加入450毫升水。将溶液超声处理直至芦荟粉末完全溶解,然后在搅拌下将其缓慢倒入1800毫升无水乙醇中。将醇溶液置于冰箱中在4℃过夜。在真空下通过滤纸过滤获得白色沉淀,并用25毫升80%乙醇洗涤。在除去25毫升80%乙醇洗涤溶液后,通过再加入25毫升80%乙醇重复洗涤。在真空中干燥沉淀,获得总共27克粗多糖033694airs(5)。ir(kbr)νmax:3376,1591,1420,1259,and1093cm–1.1hnmr(400mhz,d2o)δ(ppm):2.03-2.17(br.,m,-coch3)。乙酰基基团的含量为2.6%。
实施方案9:富集的多糖100x-airs-3500daps(6)的制备
称量总共2克的粗多糖033694airs(5)并溶解在约100毫升水中,并在具有mwco3500da的膜管中透析2天。在透析过程中,经常用新鲜水替换溶液,直到完成该过程。将透析液冻干,产生202毫克白色的富集的多糖100x-airs-3500daps(6)。ir(kbr)νmax.:3412,1737,1629,1376,1248,and1034cm–1.1hnmr(400mhz,d2o):δ(ppm):2.00-2.20(br.,m,-coch3)。乙酰基基团的含量为12.1%。
实施方案10:富集的多糖的乙酰化83018-51-22(7)
将500mg富集的多糖100x-airs-3500daps(6)精确称量到50ml圆底烧瓶中并加入40ml的dmso。将溶液在环境温度下静置24小时,在冰水浴中相继加入3ml吡啶和2.5ml乙酸酐,同时搅拌30分钟,然后使其升温至室温,持续1.5小时。2小时后,加入水以淬灭反应,并将溶液转移到具有3500da的透析膜管中。将反应产物透析,直到没有闻到吡啶的气味,并将透析液冻干,产生白色的富集的乙酰化的多糖产物,83018-51-22(7)430mg。ir(kbr)νmax.:3329,1740,1641,1376,1247,and1042cm–1.1hnmr(400mhz,d2o)δ(ppm):1.99-2.24(br.,m,-coch3)。乙酰基基团的含量为20.3%。
实施方案11:用于制备粗多糖030604airs(8)的一般方法
将总共100克的芦荟凝胶粉末(200:1,030604)精确称量到1-l玻璃烧杯中并加入900ml水。将溶液超声处理直至芦荟粉末完全溶解,然后在搅拌下将其缓慢倒入3600ml无水乙醇中。将醇溶液置于冰箱中在4℃过夜。通过滤纸过滤获得白色沉淀,并用50ml的80%乙醇洗涤两次。在真空中干燥沉淀,获得总共41g的粗多糖030604airs(8)。ir(kbr)νmax:3385,1735,1591,1413,1250,and1091cm–1.1hnmr(400mhz,d2o):δ(ppm):2.01-2.17(br.,m,-coch3)。乙酰基基团的含量为3.6%。
实施方案12:富集的多糖100x-030604-3500daps(9)的制备
称量总共2g的粗多糖030604airs(8)并溶解在约100ml水中,然后在具有mwco3500da的膜管中透析2天。在透析过程中,经常用新鲜水替换溶液,直到完成该过程。将透析液冻干,产生405mg白色的富集的多糖100x-030604-3500daps(9)。ir(kbr)νmax.:3420,1740,1644,1376,1246,and1068cm–1.1hnmr(400mhz,d2o)δ(ppm):2.02-2.20(br.,m,-coch3)。乙酰基基团的含量为13.5%。
实施方案13:富基的多糖的乙酰化,83018-51-20(10)
将300毫克的富集的多糖100x-030604-3500daps(9)样品精确称量到50毫升圆底烧瓶中并加入24ml的dmso。将溶液在环境温度下静置24小时,在冰水浴中相继加入1.8毫升吡啶和1.5ml乙酸酐,同时搅拌30分钟,然后使其升温至室温,持续1.5小时。2小时后,加入水以淬灭反应,并将溶液转移到具有3500da的透析膜管中。将反应产物透析直到没有闻到吡啶的气味,并且将透析液冻干,产生白色的富集的乙酰化的多糖产物83018-51-20(10)191mg。ir(kbr)νmax.:3440,1741,1638,1376,1246,and1042cm-1.1hnmr(400mhz,d2o)δ(ppm):1.97-2.24(br.,m,-coch3)。乙酰基基团的含量为19.7%。
实施方案14:制备粗多糖032889airs(11)的一般方法
将总共100g的芦荟叶汁粉末(100x,032889)精确称量到1l玻璃粉碎器中并加入900ml水。将溶液超声处理直至芦荟粉末完全溶解,然后在搅拌下将其缓慢倒入3600ml无水乙醇中。将醇溶液置于冰箱中在4℃过夜。通过过滤获得白色沉淀并用50ml的80%乙醇洗涤两次。将沉淀真空干燥,得到总共50g粗多糖032889airs(11)。ir(kbr)νmax:3374,1591,1418,1254,and1088cm–1;1hnmr(400mhz,d2o)δ(ppm):2.02-2.17(br.,m,-coch3)。乙酰基基团的含量为3.3%。
实施方案15:富集的多糖100x-032889-3500daps(12)的制备
称量总共1g的粗多糖032889airs(11)并溶解在100ml水中,然后在具有mwco3500da的膜管中透析2天。在透析过程中,经常用新鲜水替换溶液,直到完成该过程。冻干透析液,产生126mg白色的富集的多糖100x-030604-3500daps(12)。ir(kbr)νmax.:3401,1739,1634,1376,1248,and1067cm–1.1hnmr(400mhz,d2o)δ(ppm):2.01-2.20(br.,m,-coch3)。乙酰基含量为11.6%。ν
实施方案16:富集的多糖的乙酰化,83018-16-16(13)
将总共300mg富集的多糖100x-032889-3500daps(12)精确称量到50ml圆底烧瓶中并加入24ml的dmso。将溶液在环境温度下静置24小时,在冰水浴中相继加入1.8ml吡啶和1.5ml乙酸酐,同时搅拌30分钟,然后升温至室温,持续1.5小时。2小时后,加入水以淬灭反应,并将溶液转移到具有3500da的透析膜管中。将反应产物透析,直到没有闻到吡啶的气味,并将透析液冻干,产生白色的富集的乙酰化的多糖产物,83018-16-16(13)。ir(kbr)νmax.:3428,1738,1639,1375,1246,and1042cm–1.1hnmr(400mhz,d2o)δ(ppm):2.00-2.19(br.m,-coch3)。乙酰基基团的含量为20.2%。
另外的实施方案
药物制剂
在一些实施方案中,活性成分和活性成分的混合物可用于例如包含药学上可接受的载体的药物制剂中,以制备用于储存和随后给药。此外,一些实施方案包括使用上述活性成分与药学上可接受的载体或稀释剂。用于治疗用途的可接受的载体或稀释剂是制药领域熟知的,并且描述于例如remington’spharmaceuticalsciences,18thed.,mackpublishingco.,easton,pa.(1990),其通过引用以其整体并入本文中。可以在药物制剂中提供防腐剂、稳定剂、染料和甚至矫味剂。例如,可以加入苯甲酸钠、抗坏血酸和对羟基苯甲酸的酯作为防腐剂。此外,可以使用抗氧化剂和助悬剂。
可以配制活性成分的药物制剂,并用作片剂、胶囊或酏剂用于口服给药。注射剂可以常规形式制备,以液体溶液或悬浮液形式、在注射前适于在液体中溶解或悬浮的固体形式、或乳液形式。合适的赋形剂是,例如,水、盐水、右旋糖、甘露糖醇、乳糖、卵磷脂、白蛋白、谷氨酸钠、半胱氨酸盐酸盐等。此外,如果需要,可注射的药物制剂可以含有少量的无毒的辅助物质,例如润湿剂、ph缓冲剂等。如果需要,可以使用吸收增强制剂(例如脂质体)。
对于注射,本发明的药剂可以配制在水溶液中,优选地配制在生理上相容的缓冲液中,例如hanks溶液、ringer溶液或生理盐水缓冲液。对于这种经粘膜给药,在制剂中使用适合于要渗透的屏障的渗透剂。这种渗透剂在本领域中通常是已知的。使用药学上可接受的载体将本文公开的用于实践本发明的成分配制成适于全身给药的剂型,这在本发明的范围内。通过适当选择载体和合适的生产质量管理规范,本文公开的药物制剂,特别是配制为溶液的那些药物制剂,可以肠胃外给药,例如通过静脉内注射。可以使用本领域熟知的药学上可接受的载体将活性成分容易地配制成适于口服给药的剂型。这种载体能够将本发明的化合物配制成片剂、丸剂、胶囊剂、液体、凝胶剂、糖浆剂、浆液、混悬剂等,用于待治疗的患者的口服摄取。
用于肠胃外给药的药物制剂包括水溶性形式的活性成分的水溶液。另外,活性成分的悬浮液可以制备成适当的油性注射悬浮液。合适的亲脂性溶剂或媒介物包括脂肪油如芝麻油,或其他有机油如大豆油、葡萄籽油或杏仁油,或合成的脂肪酸酯如油酸乙酯或甘油三酯,或脂质体。水性注射悬浮液可含有增加悬浮液粘度的物质,例如羧甲基纤维素钠、山梨糖醇或右旋糖酐。任选地,悬浮液还可以含有合适的稳定剂或增加成分的溶解度的试剂以允许制备高浓度的溶液。在药物制剂的一些实施方案中,媒介物是亲脂性溶剂、脂肪油、有机油或脂质体。在一些实施方案中,媒介物是芝麻油、大豆油、葡萄籽油或杏仁油,或合成的脂肪酸酯,例如油酸乙酯或甘油三酯,或脂质体。
用于口服使用的药物制剂可以通过将活性成分与固体赋形剂混合,任选地研磨所得混合物,并且在添加合适的助剂(如果需要的话)之后加工颗粒的混合物以获得片剂或糖衣丸芯来获得。合适的赋形剂特别是填充剂,例如糖,包括乳糖、蔗糖、甘露糖醇或山梨糖醇;纤维素制剂,例如玉米淀粉、小麦淀粉、大米淀粉、马铃薯淀粉,明胶,黄蓍胶、甲基纤维素、羟丙基甲基纤维素、羧甲基纤维素钠和/或聚乙烯吡咯烷酮(pvp)。如果需要,可以加入崩解剂,例如交联聚乙烯吡咯烷酮、琼脂或藻酸或其盐,例如藻酸钠。糖衣丸芯被提供有合适的包衣。为此目的,可以使用浓缩的糖溶液,其可以任选地含有阿拉伯树胶、滑石、聚乙烯吡咯烷酮、卡波姆凝胶、聚乙二醇和/或二氧化钛、漆溶液和合适的有机溶剂或溶剂混合物。可将染料或颜料添加到片剂或糖衣丸包衣中以用于鉴定或表征活性成分剂量的不同组合。为此目的,可以使用浓缩的糖溶液,其可以任选地含有阿拉伯树胶、滑石、聚乙烯吡咯烷酮、卡波姆凝胶、聚乙二醇和/或二氧化钛、漆溶液和合适的有机溶剂或溶剂混合物。可将染料或颜料添加到片剂或糖衣丸包衣中以用于鉴定或表征活性成分剂量的不同组合。这样的制剂可以使用本领域已知的方法制备。参见,例如,美国专利号5,733,888(可注射的药物制剂);5,726,181(水溶性差的化合物);5,707,641(治疗活性蛋白或肽);5,667,809(亲脂剂);5,576,012(增溶性聚合剂);5,707,615(抗病毒制剂);5,683,676(颗粒药物);5,654,286(局部制剂);5,688,529(口服混悬剂);5,445,829(延长释放制剂);5,653,987(液体制剂);5,641,515(控释制剂)和5,601,845(球体制剂);所有这些文献的全部内容通过引用并入本文。药物制剂可以以其本身已知的方式制备,例如通过常规的混合、溶解、制粒、制糖衣丸、水飞(levitating)、乳化、包封、包埋或冻干方法。在一些实施方案中,药物制剂还包含赋形剂。在一些实施方案中,制备用于口服使用的药物制剂。在一些实施方案中,赋形剂是糖,包括乳糖、蔗糖、甘露糖醇或山梨糖醇;纤维素制剂,例如玉米淀粉、小麦淀粉、大米淀粉、马铃薯淀粉、明胶、黄蓍胶、甲基纤维素、羟丙基甲基纤维素、羧甲基纤维素钠和/或聚乙烯吡咯烷酮(pvp)。
为了配制包含一种或多种本文公开的活性成分的剂量,可以使用已知的表面活性剂、赋形剂、平滑剂、悬浮剂和药学上可接受的成膜物质和包衣助剂等和药学上可接受的成膜物质和包衣助剂等。优选地,醇、酯、硫酸化的脂肪族醇等可以用作表面活性剂;蔗糖、葡萄糖、乳糖、淀粉、结晶纤维素、甘露糖醇、轻质无水硅酸盐、铝酸镁、偏硅酸铝酸镁(magnesiummethasilicatealuminate)、合成硅酸铝、碳酸钙、酸式碳酸钠、磷酸氢钙、羧甲基纤维素钙等可用作赋形剂;硬脂酸镁、滑石、硬化油等可作为平滑剂;椰子油、橄榄油、芝麻油、花生油、大豆油可用作悬浮剂或润滑剂;邻苯二甲酸乙酸纤维素作为碳水化合物如纤维素或糖的衍生物,或乙酸甲酯-甲基丙烯酸酯共聚物作为聚乙烯的衍生物可以用作悬浮剂;增塑剂如邻苯二甲酸酯等可用作悬浮剂。除了上述成分之外,还可以将甜味剂、香料、着色剂、防腐剂等加入到本发明化合物的给药制剂中,特别是当该化合物口服给药时。
本文还公开了医药学领域熟知的用于包括眼内、鼻内和耳内递送的各种药物制剂。药物制剂包括水溶性形式的活性成分的眼用水溶液,例如滴眼剂,或结冷胶(sheddenetal.,clin.ther.,23(3):440-50(2001))或水凝胶(mayeretal.,ophthalmologica,210(2):101-3(1996));眼用软膏;眼用混悬液,例如微粒、含有药物的小聚合物颗粒,其悬浮在液体载体介质中(joshi,a.,j.ocul.pharmacol.,10(l):29-45(1994)),脂溶性制剂(almetal.,prog.clin.biol.res.,312:447-58(1989)),和微球(mordenti,toxicol.sci.,52(1):101-6(1999));和眼用嵌入剂。例如,这些制剂可用作用于眼睛的抗炎药。所有上述参考文献的全部内容通过引用并入到本文中。为了稳定性和舒适性,这类合适的药物制剂最经常且优选地配制成无菌、等渗和缓冲的制剂。如remington’spharmaceuticalsciences,18thed.,mackpublishingco.,easton,pa.(1990)(其通过引用全文并入本文中)中所公开的那样,以及本领域技术人员所熟知的,合适的制剂最经常且优选地是等渗的、轻微缓冲的以维持5.5至6.5的ph,并且最经常且优选地包括抗微生物防腐剂和合适的药物稳定剂。
本文所述的药物制剂可以通过口服或非口服途径给药。当口服给药时,药物制剂可以以胶囊、片剂、颗粒、喷雾、糖浆或其它这样的形式给药。药物制剂也可以用茶调制,或通过将粉末状的药物制剂溶解在流体中来形成,所述流体通常是水、水果汁或蔬菜汁或牛奶。当非口服给药时,其可以作为水性悬浮液、油性制剂等或作为滴剂、栓剂、膏剂、软膏剂等给药,当通过注射、皮下、腹膜内、静脉内、肌内等给药时。类似地,可以如本领域技术人员认为合适的那样局部给药,以使本发明的成分与活组织最佳接触。
旨在细胞内给药的药剂可以使用本领域普通技术人员熟知的技术施用。例如,可以将这样的药剂封装到脂质体中,然后通过本文所述的任何方法给药。在脂质体形成时存在于水溶液中的所有分子被并入水性内部。脂质体内容物都被保护免受外部微环境的影响,并且因为脂质体与细胞膜融合,所以被有效地递送到细胞质中。另外,由于它们的疏水性,可以直接在细胞内施用小的有机分子。
在一些实施方案中,本文所述的药物制剂被配制成单一丸剂或片剂或胶状剂或胶囊剂或锭剂。在一些实施方案中,丸剂或片剂具有10mg至2000mg的质量。在一些实施方案中,丸剂或片剂具有100mg至1500mg的质量。在一些实施方案中,丸剂或片剂具有500mg至1200mg的质量。在一些实施方案中,丸剂或片剂具有800mg至1100mg的质量。
关于本文中基本上任何的复数和/或单数术语的使用,本领域技术人员可以根据上下文和/或应用将复数转换成单数和/或将单数转换成复数。为了清楚起见,本文可以清楚地阐述各种单数/复数排列置换。
本领域技术人员将理解,通常,本文使用的术语,特别是在所附权利要求(例如,所附权利要求的主体)中使用的术语,通常旨在为“开放式”术语(例如,术语“包括(including)”应被解释为“包括但不限于”,术语“具有”应被解释为“至少具有”,术语“包括(includes)”应被解释为“包括但不限于”,等)。本领域的技术人员还将理解,如果打算引用特定数量的引入的权利要求,则在权利要求中明确地叙述这种意图,并且在没有这种叙述的情况下,不存在这种意图。例如,为了帮助理解,以下所附的权利要求可以含有介绍性短语“至少一个/一种”和“一个/一种或多个/多种”的使用以引入权利要求叙述。然而,这种短语的使用不应该被解释为暗示由不定冠词“一个”或“一种”引入的权利要求叙述将含有这种引入的权利要求叙述的任何具体权利要求限制为仅含有一种这种叙述的实施方案,甚至当相同的权利要求包括介绍性短语“一个/一种或多个/多种”或“至少一个/一种”以及诸如“一个”或“一种”的不定冠词(例如,“一个”和/或“一种”应解释为意指“至少一个/一种”或“一个/一种或多个/多种”;对于用于引入权利要求叙述的定冠词的使用也是如此。此外,即使明确叙述了具体数量的引入的权利要求叙述,本领域技术人员将认识到这种叙述通常应该被解释为意指至少所叙述的数量(例如,直接叙述“两种叙述”,而没有其它修饰语,意指至少两种叙述,或者两种或更多种叙述)。此外,在使用类似于“a、b和c等中的至少一个/一种”的惯例的那些情况下,通常这样的构造旨在表示本领域技术人员将理解该惯例的含义(例如,“具有a、b和c中的至少一个/一种的系统”将包括但不限于仅具有a、仅具有b、仅具有c、具有a和b在一起、具有a和c在一起、具有b和c在一起和/或具有a、b和c在一起等的体系)。在使用类似于“a、b或c等中的至少一个/一种”的惯例的那些情况下,通常这种构造旨在本领域技术人员将理解该惯例的含义(例如,“具有a、b和c中的至少一个/一种的系统”将包括但不限于仅具有a、仅具有b、仅具有c、具有a和b在一起、具有a和c在一起、具有b和c在一起和/或具有a、b和c在一起等的体系)。本领域技术人员将会进一步理解,无论是在说明书、权利要求书还是附图中,实际上任何呈现两个或更多个可替代的术语的分离的词语和/或短语都应该被理解为考虑包括术语中的一个、术语中的任一个或两个术语的可能性。例如,短语“a或b”将被理解为包括“a”或“b”或“a和b”的可能性。
此外,在本公开的特征或方面是根据马库什组来描述的情况下,本领域技术人员将认识到,本公开也由此根据马库什组的任何单个成员或成员亚组来描述。
如本领域技术人员将理解的,出于任何目的和所有目的,例如就提供书面描述而言,本文公开的所有范围还涵盖其任何和所有可能的子范围及其子范围的组合。任何列出的范围可以容易地被认为充分地描述并且使得相同的范围能够被分解为至少相等的一半、三分之一、四分之一、五分之一、十分之一等。作为非限制性实例,本文讨论的每个范围可以容易地分解成下三分之一、中三分之一和上三分之一等。如本领域技术人员还将理解的,所有语言如“至多”、“至少”、“大于”、“小于”等包括所列举的数字,并且是指随后可被分解成如上所述的子范围的范围。最后,如本领域技术人员将理解的,范围包括每个单独的成员。因此,例如,具有1-3个物品的组是指具有1、2或3个物品的组。类似地,具有1-5个物品的组是指具有1、2、3、4或5个物品的组,等等。
虽然本文已经公开了多个方面和实施方案,但是其它方面和实施方案对于本领域技术人员来说是显而易见的。本文公开的多个方面和实施方案是为了示例性说明的目的,而不是旨在限制,真正的范围和精神由所附权利要求来表示。
- 还没有人留言评论。精彩留言会获得点赞!