抑制方法
本申请要求于2018年9月13日提交的题为“methodsofinhibition”的澳大利亚临时申请第2018903445号的优先权,该澳大利亚临时申请的全部内容据此通过引用并入本文。
发明领域
本发明大体上涉及多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐用于抑制视觉障碍诸如近视(myopia)的发展或进展的用途。
发明背景
在本说明书中对任何之前的出版物(或来源于其的信息)或对任何已知的事物的引用不是并且不应当被视为承认或确认或以任何形式暗示该之前的出版物(或来源于其的信息)或已知的事物形成本说明书涉及的所致力于的领域中的普通的一般知识的一部分。
近视(myopia),通常被称为近视(short-sightedness),是由在发育期间眼睛的过度伸长(轴向长度)引起的视觉障碍。近视是低视力的主要原因,并且是世界上最常见的眼病,一些人估计,到2020年底,近视可能会影响多达三分之一的世界人口。流行率最高的是东亚城市,那里的很多地方,约80%-90%的离校生(schoolleaver)近视。
近视的流行似乎与在户外在强光下度过的时间量密切相关。具体地,流行病学研究已经报告,户外度过的时间是针对儿童近视发展的有效保护因素。动物研究已经表明,这种保护作用似乎与光诱导的眼睛内多巴胺水平的增加相关。
人们正在努力减少近视的发病和进展,包括增加儿童在户外在强光下度过的时间量。然而,在世界的许多地方,地理位置和当地气候限制可能阻止亮度级足够强或者阻止暴露时间足够长而不能防止近视。此外,社会和文化障碍可能阻止增加儿童在户外度过的时间,因为这被认为阻碍了教育和学术的进展。
目前减少近视进展的治疗选项包括光学方法,诸如单光镜片(singlevisionlenses)、多焦点镜片、周边镜片(peripherallenses)和角膜矫正术;以及药剂,诸如阿托品和哌仑西平(pirenzepine)。关于光学方法,来自临床试验的发现是混合的,其中大多数光学方法对近视进展速率示出有限的作用至非长期的作用。光学方法也不是针对预防近视的发病,仅是针对近视的进展。传统上,用诸如阿托品的药剂的治疗在降低近视进展速率方面最有效。然而,由于担心治疗后反弹效应以及严重的短期和长期的副作用,阿托品的广泛使用受到了抑制。
由于眼睛中存在大量屏障,将药物递送至眼睛的后段具有重大挑战。这对于局部递送的治疗剂特别重要,据估计,少于5%的局部施用的药物到达眼内组织(janoria等人(2007)expertopindrugdeliv,4(4):371-88;mantelli等人(2013)curropinallergydinimmunol,13(5):563-568)。用于将药物递送至眼睛后段的局部施用的问题包括由高泪液周转率(tearfluidturnover)、非生产性吸收、通过鼻泪管的引流、角膜上皮的不渗透性、短暂的角膜前停留时间和前段酶对药物的代谢引起的广泛的角膜前药物损失(janoria等人(2007)expertopindrugdeliv,4(4):371-88)。药物穿透至眼睛中的主要屏障中的一个是角膜上皮。角膜上皮在结构上类似于血脑屏障,顶端表面以下的细胞周围有紧密的连接(mantelli等人(2013)curropinallergyclinimmunol,13(5):563-568)。与血脑屏障类似,角膜上皮中的紧密连接是病原体和局部施用的药物的进入的屏障的主要原因(mantelli等人(2013)curropinallergyclinimmunol,13(5):563-568)。能够克服这些屏障的药物作为眼部障碍的疗法是有利的。
需要用于抑制诸如近视的视觉障碍的发展或进展的新疗法。
发明概述
本发明部分地基于这样的发现:多巴胺[2-(3,4-二羟基苯基)乙胺]或氘代多巴胺或其衍生物可以穿透眼部组织并且影响眼睛后段的结构,包括视网膜。鉴于多巴胺不能穿过血脑屏障,认为多巴胺或其氘代衍生物将不能穿过角膜上皮,这是由于与血脑屏障的结构相似性。令人惊讶的是,本发明人已经发现,多巴胺及其氘代衍生物能够穿透角膜上皮并且影响眼睛后段的结构。因此,本发明人认为,多巴胺或氘代多巴胺或其衍生物可以被局部地施用至受试者的眼睛,以抑制受试者的视觉障碍的发展或进展,特别是抑制涉及多巴胺水平降低的眼睛后段的视觉障碍诸如近视、与糖尿病视网膜病变相关的视觉障碍或与帕金森病相关的视觉障碍的发展或进展。
在本发明的一个方面中,提供了用于抑制受试者的视觉障碍的进展或发展的方法,该方法包括向受试者的眼睛局部地施用包含多巴胺或其药学上可接受的盐的组合物。在一些实施方案中,将该组合物局部地施用至受试者的双眼。
在另外的方面中,提供了包含多巴胺或其药学上可接受的盐的组合物用于抑制受试者的视觉障碍的发展或进展的用途,其中该组合物被局部地施用至受试者的眼睛。
在本发明的又一个方面中,提供了用于抑制受试者的视觉障碍的发展或进展的包含多巴胺或其药学上可接受的盐的组合物,其中该组合物被配制用于向受试者的眼睛局部施用。
本发明还提供了包含多巴胺或其药学上可接受的盐的组合物在制造用于抑制受试者的视觉障碍的发展或进展的药物中的用途,其中该组合物被配制用于向受试者的眼睛局部施用。
在本发明的另一个方面中,提供了用于抑制受试者的视觉障碍的发展或进展的方法,该方法包括向受试者的眼睛局部地施用包含氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐的组合物。在一些实施方案中,将该组合物施用至受试者的双眼。
在另外的方面中,提供了包含氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐的组合物用于抑制受试者的视觉障碍的发展或进展的用途,其中该组合物被局部地施用至受试者的眼睛。
在另一个方面中,提供了用于抑制受试者的视觉障碍的发展或进展的包含氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐的组合物,其中该组合物被配制用于向受试者的眼睛局部施用。
在又另一个方面中,提供了包含氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐的组合物在制造用于抑制受试者的视觉障碍的发展或进展的药物中的用途,其中该组合物被配制用于向受试者的眼睛局部施用。
在上述方面中的任一个的特定实施方案中,氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐是式i的化合物:
或其药学上可接受的盐,其中
r1、r2、r3、r4、r5、r6、r7、r8、r10和r11各自独立地选自h和d;
r9选自h、d和c(o)or12;
r12选自h和d;并且
其中r1至r12中的至少一个是d。
附图简述
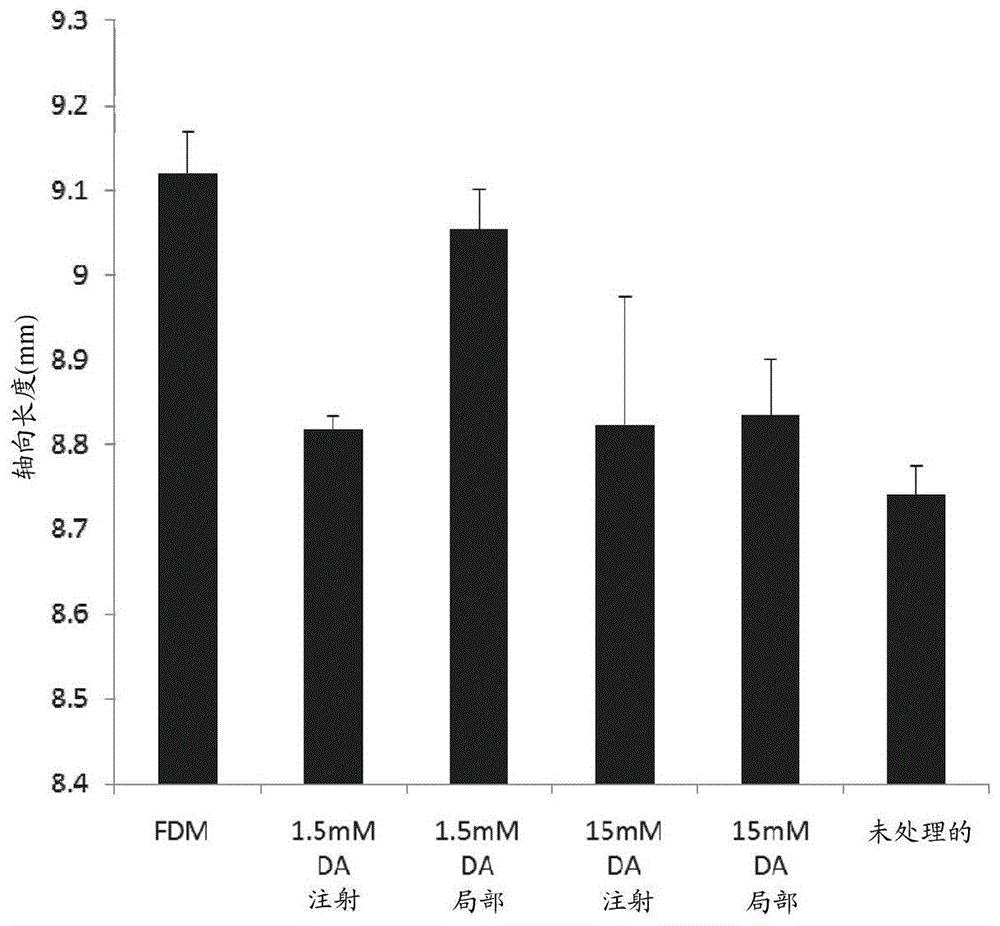
图1示出了与未处理、年龄匹配的对照相比,响应于漫射体磨损(fdm)、以及多巴胺(da)组合物的玻璃体内注射(注射)和局部施用(局部)的雏鸡眼睛的平均轴向长度(mm)。误差棒代表平均值的标准误差。
图2示出了与未处理、年龄匹配的对照相比,响应于漫射体磨损(fdm)、以及多巴胺(da)、阿托品、哌仑西平、tpmpa的玻璃体内注射以及与阿托品、哌仑西平或tpmpa组合的多巴胺的玻璃体内注射的雏鸡眼睛的平均轴向长度(mm)。误差棒代表平均值的标准误差。
图3示出了与未处理、年龄匹配的对照相比,响应于漫射体磨损(fdm)、以及多巴胺(da)、阿托品、tpmpa的局部施用以及与阿托品或tpmpa组合的多巴胺的局部施用的雏鸡眼睛的平均轴向长度(mm)。误差棒代表平均值的标准误差。
图4示出了与未处理、年龄匹配的对照相比,响应于漫射体磨损、以及多巴胺-1,1,2,2-d4(d4da)组合物的玻璃体内注射(注射)和局部施用(局部)的雏鸡眼睛的平均轴向长度(mm)。误差棒代表平均值的标准误差。
图5示出了与未处理、年龄匹配的对照相比,响应于漫射体磨损(fdm)、以及多巴胺-1,1,2,2-d4(d4da)、阿托品、tpmpa的玻璃体内注射以及与阿托品或tpmpa组合的多巴胺-1,1,2,2-d4的玻璃体内注射的雏鸡眼睛的平均轴向长度(mm)。误差棒代表平均值的标准误差。
图6示出了与未处理、年龄匹配的对照相比,响应于漫射体磨损(fdm)、以及多巴胺-1,1,2,2-d4(d4da)、阿托品、tpmpa的局部施用以及与阿托品或tpmpa组合的多巴胺-1,1,2,2-d4的局部施用的雏鸡眼睛的平均轴向长度(mm)。误差棒代表平均值的标准误差。
发明详述
1.定义
除非另外定义,否则本文使用的所有技术和科学术语都具有与本发明所属技术领域的普通技术人员通常理解的相同的含义。虽然与本文描述的那些方法和材料相似或等效的任何方法和材料都可以用于实践或测试本发明,但描述了优选的方法和材料。为了本发明的目的,下文中定义了以下术语。
冠词“一(a)”和“一(an)”在本文用于指一个/种或多于一个/种(即至少一个/种)该冠词的语法对象。举例来说,“一个要素(anelement)”意指一个要素或多于一个要素。
“约”意指变化多达参考的数量(quantity)、水平、值、数目、频率、百分比、尺寸、大小、量(amount)、重量或长度的15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%或1%的数量、水平、值、数目、频率、百分比、尺寸、大小、量、重量或长度。
如本文使用的,术语“和/或”指的是并且包括一个或更多个相关的列出项目的任何和所有可能的组合,以及当在替代方案(或)中解释时没有组合。
术语“载体”在本文中用于指液体稀释剂。“药学上可接受的载体”意指包含不是生物学上不合意的或不是其他方面不合意的材料(即,该材料可以与选定的活性剂一起被施用至受试者,而不引起任何不良反应或实质性的不良反应)的药物媒介物。载体可以包括赋形剂和其他添加剂,诸如稀释剂、洗涤剂、着色剂、润湿剂或乳化剂、ph缓冲剂、防腐剂和类似物。在特定实施方案中,载体是水性载体。术语“水性载体”在本文中用于指液体水性稀释剂,其中水性载体包括但不限于水、盐水、水性缓冲液以及包含水溶性或水混溶性添加剂诸如葡萄糖或甘油的水溶液。水性载体还可以呈水包油乳液的形式。
在整个本说明书和随后的权利要求中,除非上下文另外要求,否则词语“包含(comprise)”、以及变型诸如“包含(comprises)”和“包含(comprising)”,将被理解为意味着包括所陈述的整数或步骤或者整数或步骤的组但不排除任何其他的整数或步骤或者整数或步骤的组。因此,术语“包含(comprising)”及类似术语的使用指示所列出的整数是必需的或强制性的,但是其他整数是任选的并且可以存在或可以不存在。“由......组成(consistingof)”意指包括并且限于措辞“由......组成”后的任何内容。因此,措辞“由......组成”指示所列出的要素是必需的或强制性的,并且不可以存在其他要素。“基本上由......组成(consistingessentiallyof)”意指包括该措辞之后列出的任何要素,并且限于不干扰或不影响本公开内容中对于所列出的要素所指定的活性或作用的其他要素。因此,措辞“基本上由......组成”指示所列出的要素是必需的或强制性的,但是其他要素是任选的,并且可以存在或可以不存在,这取决于它们是否影响所列出的要素的活性或作用。
如本文使用的,术语“状况”指的是身体作为整体或其一部分的身体状态(physicalstate)的异常。
术语“氘代多巴胺”在本文中用于指包含至少一个替代氢原子的氘原子的多巴胺。例如,“氘代多巴胺”可以指的是包含至少1个、2个、3个、4个、5个、6个、7个、8个、9个、10个或11个氘原子的多巴胺。
“氘代多巴胺衍生物”意指包含至少一个替代氢原子的氘原子的多巴胺衍生物。例如,“氘代多巴胺衍生物”可以指的是包含至少1个、2个、3个、4个、5个、6个、7个、8个、9个、10个、11个或12个氘原子的多巴胺衍生物。“多巴胺衍生物”意指通过修饰例如通过与其他化学部分缀合或络合而从多巴胺衍生的分子。在优选的实施方案中,多巴胺衍生物是左旋多巴(levodopa)。
如本文使用的,术语“盐”和“前药”包括任何药学上可接受的盐、酯、水合物、溶剂化物或在施用至接受者之后能够(直接或间接)提供期望的化合物或其活性代谢物或残基的任何其他化合物。合适的药学上可接受的盐包括药学上可接受的无机酸的盐或药学上可接受的有机酸的盐,所述无机酸为诸如盐酸、硫酸、磷酸、硝酸、碳酸、硼酸、氨基磺酸和氢溴酸,所述有机酸为诸如乙酸、丙酸、丁酸、酒石酸、马来酸、羟基马来酸、富马酸、柠檬酸、乳酸、粘酸、葡糖酸、苯甲酸、琥珀酸、草酸、苯乙酸、甲磺酸、甲苯磺酸、苯磺酸、水杨酸、磺胺酸、天冬氨酸、谷氨酸、乙二胺四乙酸、硬脂酸、棕榈酸、油酸、月桂酸、泛酸、丹宁酸、抗坏血酸和戊酸。碱盐包括但不限于与药学上可接受的阳离子形成的那些盐,所述阳离子诸如钠、钾、锂、钙、镁、铵和烷基铵。此外,碱性含氮基团可以用诸如以下的剂来季铵化:低级烷基卤化物诸如甲基、乙基、丙基和丁基的氯化物、溴化物和碘化物;硫酸二烷基酯诸如硫酸二甲酯和硫酸二乙酯;以及其他的剂。然而,将理解的是,非药学上可接受的盐也落入本发明的范围内,因为这些盐可以用于制备药学上可接受的盐。盐和前药的制备可以通过本领域已知的方法进行。例如,金属盐可以通过期望的化合物与金属氢氧化物的反应来制备。酸盐可以通过使适当的酸与期望的化合物反应来制备。
如本文使用的,措辞“溶解形式”指的是这样的形式:其中化合物诸如多巴胺、氘代多巴胺或氘代多巴胺衍生物溶解在液体中,使得获得包含均匀分布的该化合物的溶液,该溶液大体上不含固体化合物。在一些实施方案中,液体是如本文描述的水性载体。
如本文使用的术语“受试者”指的是期望疗法或预防的脊椎动物受试者,特别是哺乳动物或鸟类受试者。合适的受试者包括但不限于灵长类动物;鸟类;牲畜动物,诸如绵羊、牛、马、鹿、驴和猪;实验室测试动物,诸如兔、小鼠、大鼠、豚鼠和仓鼠;伴侣动物,诸如猫和狗;以及圈养的野生动物,诸如狐狸、鹿和野狗。在特定实施方案中,受试者是人类。在一些实施方案中,受试者是例如从约2岁到20岁的年龄的人类儿童或年轻成人。然而,将理解的是,上述术语并不意味着存在症状。
如本文使用的,措辞“视觉障碍”指的是改变受试者的视觉的状况。在特定实施方案中,这样的状况与“视敏度(visualacuity)”的降低相关,所述“视敏度”的降低通常与视力的敏锐度或清晰度的降低或减弱相关。因此,“视敏度”的降低通常指的是形觉视力(formvision)的敏锐度或清晰度的任何可测量的降低或减弱,这取决于眼睛内视网膜焦点的锐度(sharpness)和脑解释能力的灵敏度。在某些实施方案中,视敏度指的是斯内伦敏度(snellenacuity)(例如20/20)。视觉障碍可以是疾病、障碍或状况。
除非另外具体说明,否则本文描述的每个实施方案将加以必要的修改被应用于所有的实施方案。
2.缩写
在整个申请中使用以下缩写:
d=氘
3.组合物
本发明部分地基于这样的发现:多巴胺[2-(3,4-二羟基苯基)乙胺]或氘代多巴胺衍生物或其类似物可以穿透眼部组织并且影响眼睛后段的结构,包括视网膜。因此,本发明人认为,包含多巴胺或氘代多巴胺或氘代多巴胺衍生物的组合物可以被局部地施用,以抑制受试者的视觉障碍的发展或进展,特别是抑制涉及多巴胺水平降低的眼睛后段的视觉障碍诸如近视、与糖尿病视网膜病变相关的视觉障碍或与帕金森病相关的视觉障碍的发展或进展。
在本发明的一个方面中,该组合物包含多巴胺或其药学上可接受的盐。在优选的实施方案中,这样的组合物被配制用于向眼睛局部施用,诸如以滴眼剂的形式向眼睛局部施用。在特定实施方案中,该组合物包含多巴胺或其药学上可接受的盐和药学上可接受的载体。在一些实施方案中,该组合物包含多巴胺或其药学上可接受的盐、药学上可接受的载体和抗氧化剂。
在本发明的另一个方面中,该组合物包含氘代多巴胺或氘代多巴胺衍生物,或其药学上可接受的盐。这样的组合物可以被配制用于向受试者的眼睛局部施用(localadministration),诸如向眼睛局部施用(topicaladministration),诸如以滴眼剂的形式或直接注射至眼睛中。在特定实施方案中,该组合物包含氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐,以及药学上可接受的载体。在一些实施方案中,该组合物包含氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐、药学上可接受的载体和抗氧化剂。
在一些实施方案中,该组合物包含氘代多巴胺或其药学上可接受的盐。氘代多巴胺可以包含一个或更多个替代氢的氘原子。例如,氘代多巴胺可以包含1个、2个、3个、4个、5个、6个、7个、8个、9个、10个或11个氘原子;特别地2个、3个或4个氘原子;最特别地4个氘原子。在特定实施方案中,氘代多巴胺是多巴胺-1,1,2,2-d4[2-(3,4-二羟基苯基)乙基-1,1,2,2,d4-胺];2-(3,4-二羟基苯基)乙基-1-氘-胺;2-(3,4-二羟基苯基)乙基-2,2-二氘-胺;或其药学上可接受的盐;特别地多巴胺-1,1,2,2-d4盐酸盐。
在一些实施方案中,该组合物包含氘代多巴胺衍生物或其药学上可接受的盐。氘代多巴胺衍生物可以包含一个或更多个替代氢的氘原子。
例如,氘代多巴胺衍生物可以包含1个、2个、3个、4个、5个、6个、7个、8个、9个、10个、11个或12个氘原子;特别地2个或3个氘原子;最特别地3个氘原子。在特定实施方案中,氘代多巴胺衍生物是氘代左旋多巴或其药学上可接受的盐。氘代左旋多巴可以是,但不限于,2-氨基-2-氘-3-(3,4-二羟基苯基)丙酸;2-氨基-2,3-二氘-3-(3,4-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(3,4-二羟基苯基)丙酸;2-氨基-3,3-二氘-3-(3,4-二羟基苯基)丙酸;2-氨基-3,3-二氘-3-(3,4-二氘氧基苯基)丙酸;2-氨基-2-氘-3-(2,3,6-三氘-4,5-二羟基苯基)丙酸;2-氨基-2,3-二氘-3-(2,3,6-三氘-4,5-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(2,3,6-三氘-4,5-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(2,3,6-三氘-4,5-二氘氧基苯基)丙酸;或其药学上可接受的盐;特别地2-氨基-2,3-二氘-3-(3,4-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(3,4-二羟基苯基)丙酸;或其药学上可接受的盐。在一些实施方案中,氘代多巴胺衍生物或其药学上可接受的盐选自wo2004/056724a1、wo2007/093450a1和wo2014/122184a1中公开的化合物,上述文献的全部内容通过引用并入本文。
在特定实施方案中,氘代多巴胺或氘代多巴胺衍生物或其药学上可接受的盐是式i的化合物:
或其药学上可接受的盐,其中
r1、r2、r3、r4、r5、r6、r7、r8、r10和r11各自独立地选自h和d;
r9选自h、d和c(o)or12;
r12选自h和d;并且
其中r1至r12中的至少一个是d。
在一些实施方案中,r6和r8是d。在一些实施方案中,r6、r7和r8是d。在一些实施方案中,r6、r7、r8和r9是d。
在一些实施方案中,r9是h或d;优选地d。在一些实施方案中,r6、r7、r8和r9是d。在一些实施方案中,r1、r2、r3、r4、r5、r10和r11是h。在优选的实施方案中,r6、r7、r8和r9是d;并且r1、r2、r3、r4、r5、r10和r11是h。
在可选择的实施方案中,r9是c(o)or12。在优选的实施方案中,r12是h。
在一些实施方案中,r9是c(o)or12;r6和r8是d;并且r1、r2、r3、r4、r5、r7、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r6、r7和r8是d;并且r1、r2、r3、r4、r5、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r8是d;并且r1、r2、r3、r4、r5、r6、r7、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r6和r8是d;并且r1、r2、r3、r4、r5、r7、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r6、r7和r8是d;并且r1、r2、r3、r4、r5、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r6和r7是d;并且r1、r2、r3、r4、r5、r8、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r2、r3、r6和r7是d;并且r1、r4、r5、r8、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r1、r4、r5和r8是d;并且r2、r3、r6、r7、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r1、r4、r5、r6和r8是d;并且r2、r3、r7、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r1、r4、r5、r6、r7和r8是d;并且r2、r3、r10、r11和r12是h。
在一些实施方案中,r9是c(o)or12;r1、r2、r3、r4、r5、r6、r7和r8是d;并且r10、r11和r12是h。
虽然本发明预期不同水平的氘富集,但由d占据的位置独立地具有不小于约80%、85%、90%、95%、98%或100%(以及其间的所有整数)的氘富集;特别地不小于约98%。氘富集水平可以使用本领域普通技术人员已知的常规分析方法来确定,包括质谱法和核磁共振光谱法。
在特定实施方案中,式i的化合物选自由以下组成的组:2-(3,4-二羟基苯基)乙基-1,1,2,2,d4-胺(多巴胺-1,1,2,2-d4);2-(3,4-二羟基苯基)乙基-1-氘-胺;2-(3,4-二羟基苯基)乙基-2,2-二氘-胺;2-氨基-2-氘-3-(3,4-二羟基苯基)丙酸;2-氨基-2,3-二氘-3-(3,4-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(3,4-二羟基苯基)丙酸;2-氨基-3,3-二氘-3-(3,4-二羟基苯基)丙酸;2-氨基-3,3-二氘-3-(3,4-二氘氧基苯基)丙酸;2-氨基-2-氘-3-(2,3,6-三氘-4,5-二羟基苯基)丙酸;2-氨基-2,3-二氘-3-(2,3,6-三氘-4,5-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(2,3,6-三氘-4,5-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(2,3,6-三氘-4,5-二氘氧基苯基)丙酸;和其药学上可接受的盐;特别地2-(3,4-二羟基苯基)乙基-1,1,2,2,d4-胺;2-氨基-2,3-二氘-3-(3,4-二羟基苯基)丙酸;2-氨基-2,3,3-三氘-3-(3,4-二羟基苯基)丙酸;和其药学上可接受的盐;最特别地2-(3,4-二羟基苯基)乙基-1,1,2,2,d4-胺及其药学上可接受的盐。
组合物中的多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐的量可以取决于正在治疗的视觉障碍、受试者的特性诸如体重和年龄以及施用途径。在一些实施方案中,组合物中的多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐处于在以下范围内的量:组合物的从0.0001%w/v至60%w/v、0.001%w/v至50%w/v、0.01%w/v至40%w/v、0.02%w/v至30%w/v、0.03%w/v至25%w/v、0.04%w/v至20%w/v、0.05%w/v至15%w/v、0.06%w/v至10%w/v、0.065%w/v至9%w/v、0.07%w/v至8%w/v、0.075%w/v至7%w/v、0.08%w/v至6%w/v、0.085%w/v至5%w/v、0.09%w/v至4%w/v、0.095%w/v至3%w/v、0.1%w/v至2%w/v或0.105%w/v至1%w/v(以及其间的所有整数);特别地组合物的约0.1%w/v、0.2%w/v、0.3%w/v、0.4%w/v、0.5%w/v、0.6%w/v、0.7%w/v、0.8%w/v、0.9%w/v或1%w/v。
在优选的实施方案中,多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐在组合物中呈溶解形式。技术人员将很清楚本领域中常规使用的确定化合物的溶解度的程序,例如在以下中描述的程序:goodwin(2006)drugdiscoverytoday:technologies,3(1):67-71;jouyban(2010)handbookofsolubilitydataforpharmaceuticals(crcpress);或者hefter和tomkins(2003)theexperimentaldeterminationofsolubilities(johnwiley8isons,ltd)。例如,可以使用uv光谱法或高效液相色谱法分析化合物的溶解度。
在一些实施方案中,多巴胺可以呈衍生物的形式,诸如其药学上可接受的盐和/或溶剂化物、或其前药。在一些实施方案中,多巴胺呈水合物的形式。在一些实施方案中,多巴胺的药学上可接受的盐是盐酸盐,诸如可得自sigma-aldrichco.llc的盐酸盐。在一些实施方案中,前药是酯和/或酰胺前药。在一些实施方案中,多巴胺的前药是多卡巴胺(n-(n-乙酰基-l-甲硫氨酰基)-3,4-双(乙氧基羰基)多巴胺,如yoshikawa等人(1995)hypertensres,18(增刊1):s211-s213中描述的);haddad等人(2018)molecules,23(1):40(doi:10.3390/molecules23010040)中描述的化合物,诸如酯前药,例如多巴胺的亲脂性3,4-o-二酯前药,如casagrande和ferrari(1973)farmacosci,28(2):143-148和borgman等人(1973)jmedchem,16(6):630-633中描述的;peura等人(2013)pharmres,30:2523-2537,tutone等人(2016)eurjmedchem,124:435-444或美国专利第4,064,235号中描述的酰胺前药;或美国专利第4,311,706号中描述的化合物;上述文献的全部内容通过引用并入本文。
在一些实施方案中,氘代多巴胺或氘代多巴胺衍生物可以呈衍生物的形式,诸如其药学上可接受的盐和/或溶剂化物、或其前药。在一些实施方案中,氘代多巴胺、氘代多巴胺衍生物或其类似物或药学上可接受的盐呈水合物的形式。在一些实施方案中,氘代多巴胺或氘代多巴胺衍生物的药学上可接受的盐是盐酸盐,诸如可得自sigma-aldrichco.llc的多巴胺-1,1,2,2-d4盐酸盐,或者在us2007/0027216a1中描述的盐的氘代衍生物,该文献的内容通过引用以其整体并入。在一些实施方案中,前药是酯和/或酰胺前药。在一些实施方案中,前药是氘代化合物的酯前药,诸如(2r)-2-苯基羰基氧基丙基(2s)-2-氨基-3-(3,4-二羟基苯基)丙酸酯甲磺酸盐的氘代衍生物,如us2009/0156679a1中描述的,左旋多巴甲酯或左旋多巴乙酯的氘代衍生物,如us2014/0088192a1中描述的,lewitt等人(2012)clinneuropharmacol,35:103-110中描述的xp21279的氘代衍生物,以及haddad等人(2018)molecules,23(1):40(doi:10.3390/molecules23010040)中描述的酯前药的氘代衍生物,包括多巴胺的亲脂性3,4-o-二酯前药的氘代衍生物,如casagrande和ferrari(1973)farmacosci,28(2):143-148和borgman等人(1973)jmedchem,16(6):630-633中描述的;多卡巴胺(n-(n-乙酰基-l-甲硫氨酰基)-3,4-双(乙氧基羰基)多巴胺,如yoshikawa等人(1995)hypertensres,18(增刊1):s211-s213中描述的);或氘代化合物的酰胺前药,诸如us2014/0088192a1中描述的左旋多巴酰胺、左旋多巴甲酰胺或左旋多巴磺酰胺的氘代衍生物,haddad等人(2018)molecules,23(1):40(doi:10.3390/molecules23010040)中描述的酰胺前药的氘代衍生物,wang等人(2013)jfooddruganal,21:136-141、zhou等人(2013)bioorganicmedchemlett,23:5279-5282和zhou等人(2010)eurjmedchem,45:4035-4042中描述的氨基酸前药的氘代衍生物,atlas等人(2016)cnsneuroscither,22:461-467中描述的酰胺前药的氘代衍生物,peura等人(2013)pharmres,30:2523-2537中描述的酰胺前药的氘代衍生物,tutone等人(2016)eurjmedchem,124:435-444中描述的酰胺前药的氘代衍生物,或美国专利第4,064,235号中描述的酰胺前药的衍生物;wo2016/065019中描述的磷酸酯前药的氘代衍生物;或者美国专利第4,311,706号中描述的化合物的氘代衍生物;上述文献的全部内容通过引用并入本文。
在一些实施方案中,组合物还包含抗氧化剂。抗氧化剂可以是减缓、抑制或防止本发明的组合物的任何组分,特别是多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐的氧化的任何化合物。合适的抗氧化剂可以包括但不限于抗坏血酸或维生素c、酚酸、山梨酸、亚硫酸氢钠、焦亚硫酸钠、硫代硫酸钠、乙酰半胱氨酸、乙二胺四乙酸(edta)、亚硝酸钠、抗坏血酸硬脂酸酯、抗坏血酸棕榈酸酯、α-硫代甘油、异抗坏血酸、盐酸半胱氨酸、柠檬酸、生育酚或维生素e、生育酚乙酸酯、二丁基羟基甲苯、大豆卵磷脂、硫代乙醇酸钠、丁基羟基茴香醚、没食子酸丙酯、尿酸、褪黑激素、硫脲、或其盐或组合。在一些实施方案中,抗氧化剂是抗坏血酸或其盐。
抗氧化剂可以以适合于显著地减缓、抑制或防止本发明的组合物的任何组分,特别是多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐的氧化的量存在。例如,抗氧化剂可以以在组合物的从0.01%w/v至10%w/v、0.01%w/v至5%w/v、0.03%w/v至4%w/v、0.05%w/v至3%w/v、0.07%w/v至2%w/v、0.09%w/v至1%w/v或0.1%w/v至0.5%w/v的范围内的量存在;特别地以组合物的约0.1%w/v的量存在。
在一些实施方案中,组合物还包含药学上可接受的载体。合适的药学上可接受的载体包括但不限于水性载体、油、脂肪酸、有机硅液体载体(siliconeliquidcarrier)诸如全氟化碳或氟化液体载体,例如如美国专利第6,458,376b1号中描述的,以及其组合。
在一些实施方案中,本发明的组合物包含油。合适的油包括但不限于杏仁油;蓖麻油;矿物油;橄榄油;花生油(peanutoil);椰子油;大豆油;玉米油(cornoil);茴香油;丁香油;桂皮油;肉桂油;花生油(arachisoil);玉米油(maizeoil);葛缕子油;迷迭香油;薄荷油;桉叶油;种子油诸如菜籽油、棉籽油、亚麻子油、红花油、芝麻油或葵花油;有机硅油;或其组合。在一些实施方案中,油可以以水包油乳液的形式与水性载体一起被包含在组合物中,任选地与表面活性剂一起。油可以以在组合物的从约0.1%w/v至20%w/v的范围内的量存在。
在一些实施方案中,载体是水性载体。水性载体优选地是药学上可接受的水性载体。可以使用本领域熟知的多种药学上可接受的水性载体。例如,水性载体可以选自但不限于盐水、水、水性缓冲液、包含水和可混溶溶剂的水溶液、及其组合。在一些实施方案中,水性载体是盐水。当使用盐水时,对于施用点,诸如眼睛,盐水优选地是等渗的。例如,在一些实施方案中,盐水包含0.15%w/v至8%w/v氯化钠;特别地0.18%w/v至7%w/v、0.22%w/v至5%w/v或0.45%w/v至3%w/v氯化钠;更特别地0.5%w/v至2%w/v或0.65%w/v至1.5%w/v氯化钠;最特别地约0.9%w/v氯化钠。
在水性载体不是等渗的(例如水)一些实施方案中,组合物可以包含张力剂(tonicityagent)。可以使用本领域熟知的任何药学上可接受的张力剂。合适的张力剂包括但不限于硼酸、酸式磷酸钠缓冲液、氯化钠、葡萄糖、海藻糖、氯化钾、氯化钙、氯化镁、聚丙二醇、甘油、甘露醇、或其盐或组合。张力剂可以以提供给施用点诸如眼睛等渗性的量存在于组合物中,例如在从0.02%w/v至15%w/v的范围内的量。
在一些实施方案中,载体是缓冲液,其中缓冲液将ph维持在从4至8、5至7、5.5至6.5的范围内或者约5.5、6.0或6.5。合适的缓冲剂包括但不限于乙酸、柠檬酸、焦亚硫酸钠、组氨酸、碳酸氢钠、氢氧化钠、硼酸、硼砂、碱金属磷酸盐、磷酸盐或柠檬酸盐缓冲液、或其组合。缓冲剂在组合物中可以以适合于维持期望的ph的量存在。
在一些实施方案中,组合物的ph在从4至8、5至7、5.5至6.5的范围内或者是约5.5、6.0或6.5。
在一些实施方案中,特别是当氘代多巴胺衍生物是氘代左旋多巴(即当式i的化合物中的r9是c(o)or12时)或其药学上可接受的盐时,该组合物还包含芳香族l-氨基酸脱羧酶的抑制剂。芳香族l-氨基酸脱羧酶的合适的抑制剂包括但不限于卡比多巴、苄丝肼、甲基多巴、或其盐或组合。在一些实施方案中,芳香族l-氨基酸脱羧酶的抑制剂是卡比多巴。
在本发明的组合物中芳香族l-氨基酸脱羧酶的抑制剂的量将取决于正在治疗的状况、组合物的施用途径和组合物中氘代左旋多巴的量。芳香族l-氨基酸脱羧酶的抑制剂应当以足以显著抑制氘代左旋多巴或其药学上可接受的盐的脱羧的量存在。在一些实施方案中,氘代左旋多巴或其药学上可接受的盐与芳香族l-氨基酸脱羧酶的抑制剂的比在以下范围内:从20:1至1:1、15:1至1:1、10:1至1:1、9:1至1:1、8:1至1:1、7:1至1:1、6:1至2:1或5:1至3:1。在一些实施方案中,氘代左旋多巴或其药学上可接受的盐与芳香族l-氨基酸脱羧酶的抑制剂的比是约4:1。
在一些实施方案中,组合物中芳香族l-氨基酸脱羧酶的抑制剂处于在以下的范围内的量:组合物的从0.0005%w/v至30%w/v、0.0025%w/v至15%w/v、0.005%w/v至12.5%w/v、0.0075%w/v至10%w/v、0.01%w/v至7.5%w/v、0.0125%w/v至5%w/v、0.015%w/v至2.5%w/v、0.0163%w/v至2.25%w/v、0.0175%w/v至2%w/v、0.0188%w/v至1.75%w/v、0.02%w/v至1.5%w/v、0.0213%w/v至1.25%w/v、0.0225%w/v至1%w/v、0.0238%w/v至0.75%w/v、0.025%w/v至0.5%w/v、0.0263%w/v至0.25%w/v(以及其间的所有整数);特别地组合物的约0.025%w/v、0.03%w/v、0.035%w/v、0.04%w/v、0.045%w/v、0.05%w/v、0.055%w/v、0.06%w/v、0.065%w/v、0.07%w/v、0.075%w/v、0.08%w/v、0.085%w/v、0.09%w/v、0.095%w/v、0.1%w/v、0.125%w/v、0.15%w/v、0.175%w/v、0.2%w/v、0.225%w/v或0.25%w/v。
该组合物还可以包含一种或更多种辅助药学活性剂或可以与一种或更多种辅助药学活性剂分开地、同时地或依次地施用。在一些实施方案中,辅助药学活性剂可以增加多巴胺能系统的活化。示例性的辅助药学活性剂包括,但不限于,多巴胺受体激动剂、γ-氨基丁酸(gaba)受体拮抗剂和/或毒蕈碱乙酰胆碱受体拮抗剂。在一些实施方案中,药学活性剂是用于抑制视觉障碍的发展或进展的剂,所述视觉障碍特别是涉及眼睛中降低的多巴胺水平的视觉障碍,诸如近视。
在一些实施方案中,本发明的组合物还包含多巴胺受体激动剂。多巴胺受体激动剂可以在任何多巴胺受体亚型具有激动剂活性,所述多巴胺受体亚型包括但不限于来自受体的d1样家族(d1和d5受体)和d2样家族(d2、d3和d4受体)的任何受体亚型,以及多巴胺受体异源二聚体。合适的多巴胺受体激动剂包括但不限于喹吡罗、阿扑吗啡、罗匹尼罗、普拉克索、右普拉克索(dexpramipexole)、吡贝地尔、罗替戈汀、溴隐亭、麦角乙脲、卡麦角林、2-氨基-6,7-二羟基-1,2,3,4-四氢萘(adtn)、培高利特、calidopa、dihydrexidine、doxathrine、丙基去甲阿扑吗啡、喹高利特、罗克吲哚、sumanirole、非诺多泮(fenoldopam)、麦角柯宁碱、1-苯基-2,3,4,5-四氢-(1h)-3-苯并氮杂
组合物中多巴胺受体激动剂的量可以取决于正在治疗的状况和施用途径。在一些实施方案中,组合物中多巴胺受体激动剂处于在以下的范围内的量:组合物的从0.01%w/v至20%w/v、0.01%w/v至10%w/v、0.01%w/v至5%w/v、0.03%w/v至3%w/v、0.033%w/v至2.7%w/v、0.038%w/v至2.4%w/v、0.043%w/v至2.1%w/v、0.05%w/v至1.8%w/v、0.06%w/v至1.5%w/v、0.075%w/v至1.2%w/v、0.1%w/v至0.9%w/v或0.15%w/v至0.6%w/v(以及其间的所有整数);特别地组合物的约0.2%w/v、0.21%w/v、0.22%w/v、0.23%w/v、0.24%w/v、0.25%w/v、0.26%w/v、0.27%w/v、0.28%w/v、0.29%w/v、0.3%w/v、0.31%w/v、0.32%w/v、0.33%w/v、0.34%w/v、0.35%w/v、0.36%w/v、0.37%w/v、0.38%w/v、0.39%w/v或0.4%w/v。
在一些实施方案中,本发明的组合物还包含gaba受体拮抗剂。gaba受体拮抗剂可以在任何gaba受体亚型具有拮抗剂活性,所述gaba受体亚型包括但不限于gabaa受体、gabab受体和/或gabaa-rho(以前为gabac)受体。合适的gaba受体拮抗剂包括但不限于荷包牡丹碱、氟马西尼、gabazine、戊四唑、(1,2,5,6-四氢吡啶-4-基)甲基次膦酸(tpmpa)、(3-氨基丙基)(环己基甲基)次膦酸(还被称为cgp-46381)、4-咪唑乙酸、木防己苦毒素、哌啶-4-基次膦酸(ppa)、哌啶-4-基亚硒酸(sepi)、3-氨基丙基-n-丁基次膦酸(还被称为cgp-36742)、(哌啶-4-基)甲基次磷酸(p4mpa)、或其盐或组合。在一些实施方案中,gaba受体拮抗剂选自tpmpa、荷包牡丹碱、及其盐和组合;特别地tpmpa及其盐。
组合物中gaba受体拮抗剂的量可以取决于正在治疗的状况和施用途径。在一些实施方案中,组合物中gaba受体拮抗剂处于在以下的范围内的量:组合物的从0.01%w/v至20%w/v、0.01%w/v至10%w/v、0.01%w/v至5%w/v、0.03%w/v至3%w/v、0.033%w/v至2.7%w/v、0.038%w/v至2.4%w/v、0.043%w/v至2.1%w/v、0.05%w/v至1.8%w/v、0.06%w/v至1.5%w/v、0.075%w/v至1.2%w/v、0.1%w/v至0.9%w/v或0.15%w/v至0.6%w/v(以及其间的所有整数);特别地组合物的约0.2%w/v、0.21%w/v、0.22%w/v、0.23%w/v、0.24%w/v、0.25%w/v、0.26%w/v、0.27%w/v、0.28%w/v、0.29%w/v、0.3%w/v、0.31%w/v、0.32%w/v、0.33%w/v、0.34%w/v、0.35%w/v、0.36%w/v、0.37%w/v、0.38%w/v、0.39%w/v或0.4%w/v。
在一些实施方案中,本发明的组合物还包含毒蕈碱乙酰胆碱受体拮抗剂。毒蕈碱乙酰胆碱受体拮抗剂可以在任何毒蕈碱乙酰胆碱受体亚型具有拮抗剂活性,所述毒蕈碱乙酰胆碱受体亚型包括但不限于m1受体、m2受体、m3受体、m4受体和m5受体。合适的毒蕈碱受体拮抗剂包括但不限于阿托品、哌仑西平、喜巴辛、东莨菪碱、环戊通、异丙托品、氧托品(oxitropium)、托吡卡胺、奥昔布宁、托特罗定、苯海拉明、双环维林、黄酮哌酯、噻托品、三己芬迪、索利那新、达非那新、苯扎托品、美贝维林、普环啶、阿地溴铵(aclidinium)、毒蕈碱毒素1(mt1)、毒蕈碱毒素2(mt2)、毒蕈碱毒素3(mt3)、毒蕈碱毒素4(mt4)、毒蕈碱毒素7(mt7)、或其盐或组合。在一些实施方案中,毒蕈碱乙酰胆碱受体拮抗剂选自阿托品、哌仑西平、喜巴辛、及其盐和组合;特别地阿托品和哌仑西平、及其盐和组合。
组合物中毒蕈碱乙酰胆碱受体拮抗剂的量可以取决于正在治疗的状况和施用途径。在一些实施方案中,组合物中毒蕈碱乙酰胆碱受体拮抗剂处于在以下范围内的量:组合物的从0.0001%w/v至30%w/v、0.0003%w/v至25%w/v、0.0005%w/v至20%w/v、0.0007%w/v至15%w/v、0.0009%w/v至10%w/v、0.001%w/v至5%w/v、0.003%w/v至1%w/v、0.005%w/v至0.5%w/v、0.007%w/v至0.2%w/v或0.009%w/v至0.1%w/v(以及其间的所有整数);特别地组合物的约0.009%w/v、0.01%w/v、0.02%w/v、0.03%w/v、0.04%w/v、0.05%w/vw/v、0.06%w/v、0.07%w/v、0.08%w/v、0.09%w/v或0.1%w/v。
本发明的组合物还可以包含表面活性剂。可以使用本领域熟知的多种药学上可接受的表面活性剂。示例性的表面活性剂包括但不限于以下类别的表面活性剂:醇;氧化胺;嵌段聚合物;羧基化的醇或烷基酚乙氧基化物;羧酸/脂肪酸;乙氧基化的芳基酚;乙氧基化的脂肪酯、油、脂肪胺或脂肪醇诸如鲸蜡醇;脂肪酯;脂肪酸甲酯乙氧基化物;甘油酯诸如单硬脂酸甘油酯;二醇酯;基于羊毛脂的衍生物;卵磷脂或其衍生物;木质素或其衍生物;甲酯;甘油单酯或其衍生物;聚乙二醇;聚丙二醇;烷基酚聚乙二醇;烷基硫醇聚乙二醇;聚丙二醇乙氧基化物;聚乙二醇醚,诸如cetomacrogol1000;聚合物表面活性剂;丙氧基化和/或乙氧基化的脂肪酸、醇或烷基酚;基于蛋白质的表面活性剂;肌氨酸衍生物;脱水山梨醇衍生物诸如聚山梨醇酯;山梨醇酯;山梨醇聚二醇醚的酯;脂肪酸烷醇酰胺;n-烷基多羟基脂肪酸酰胺;n-烷氧基多羟基脂肪酸酰胺;烷基多糖苷;季铵化合物诸如苯扎氯铵;环糊精诸如α-环糊精、β-环糊精或γ-环糊精;蔗糖酯或葡萄糖酯或其衍生物;磺基琥珀酸酯/盐(sulfosuccinate),诸如磺基琥珀酸钠二辛酯;或其组合。不希望受理论束缚,如果组合物中包含水性载体和油,则表面活性剂的存在可以用于与油一起乳化水性载体,并且可以增强活性成分诸如多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐穿透角膜上皮。表面活性剂可以以在组合物的从约0.1%w/v至30%w/v的范围内的量存在。
在一些实施方案中,本发明的组合物还包含流变改性剂。流变改性剂可以被用于改变组合物的表面张力和流动,并且当局部地应用时,还可以有助于组合物在眼睛表面上的停留时间。合适的流变改性剂在本领域中是熟知的。例如,流变改性剂可以选自但不限于透明质酸、壳聚糖、聚乙烯醇、聚乙二醇、聚乙烯吡咯烷酮、右旋糖酐、甲基纤维素、羟丙基甲基纤维素、羟乙基纤维素、羟丙基纤维素、羟丙基瓜尔胶、丙烯酸酯诸如卡波普聚合物(carbopolpolymer)、泊洛沙姆、阿拉伯树胶、黄原胶、瓜尔胶、刺槐豆胶、羧甲基纤维素、藻酸盐、淀粉(来自大米、玉米、马铃薯或小麦)、卡拉胶、魔芋、芦荟凝胶、琼脂糖、果胶、黄蓍胶、卡德兰胶(curdlangum)、结冷胶、硬葡聚糖、及其衍生物和组合。流变改性剂应当以足以获得期望的组合物粘度的量存在。流变改性剂可以以在组合物的从约0.5%w/v至5%w/v的范围内的量存在。
本发明的组合物还可以包含防腐剂。防腐剂可以特别地用于防止来自同一容器的经受多次使用的组合物中的微生物污染,例如,如果本发明的组合物被配制用于以多个单位剂型局部施用。合适的防腐剂包括本领域中常规地用于防止组合物中的微生物污染的任何药学上可接受的防腐剂。非限制性实例包括过硼酸钠、稳定化的氧氯络合物(stabilizedoxychlorocomplex)、聚季铵盐-1(polyquaternium-1)、苯基汞酸(phenylmercuricacid)、苯扎氯铵、氯丁醇、乙酸苯汞、硝酸苯汞、氯己定、苯度溴铵(benzododeciniumbromide)、西曲氯铵(cetrimoniumchloride)、硫柳汞、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、聚季铵盐氯化铵(polyquaterniumammoniumchloride)、聚氨基丙基双胍、过氧化氢、苯甲酸、酚酸、山梨酸、苄醇、或其盐或组合。防腐剂应当以提供足够的防腐活性的量存在。例如,防腐剂可以以在组合物的从约0.001%w/v至1%w/v的范围内的量存在。
增加组合物到眼睛中的渗透可以是合意的。因此,在一些实施方案中,本发明的组合物还可以包含渗透增强剂。合适的渗透增强剂包括但不限于二甲基亚砜(dmso);环糊精诸如α-环糊精、β-环糊精或γ-环糊精;edta;十烃季铵;甘氨胆酸盐;胆酸盐;皂苷;夫西地酸盐(fusidate);牛磺胆酸盐;聚乙二醇醚;聚山梨醇酯;或其盐、衍生物或组合。在一些实施方案中,渗透增强剂是二甲基亚砜。其他渗透增强剂包括纳米颗粒、微乳液、脂质体或胶束,在一些实施方案中,所述纳米颗粒、微乳液、脂质体或胶束包封组合物的一种或更多种组分,包括多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐。渗透增强剂应当以促进多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐渗透穿过角膜上皮的量存在。例如,渗透增强剂可以以在组合物的从约0.1%w/v至30%w/v的范围内的量存在。
在特定实施方案中,渗透增强剂是胶束。合适的胶束包括但不限于tritonx-100胶束,例如在jodko-piorecka和litwinienko(2015)freeradicalbiologyandmedicine,83:1-11中描述的胶束;表面活性剂纳米胶束,例如用十二烷基硫酸钠、十二烷基三甲基溴化铵、鲸蜡基三甲基溴化铵、正十二烷基四(环氧乙烷)、维生素etgps、辛基酚聚醚-40(octoxynol-40)和/或二辛酰基磷脂酰胆碱形成的纳米胶束;聚合物胶束,例如用聚(己内酯)、聚(d,l-丙交酯)、聚环氧丙烷、聚(β-苄基-1-天冬氨酸酯)、甲氧基聚(乙二醇)-己基取代的聚(丙交酯)、pluronicf127聚(氧乙烯)/聚(氧丙烯)/聚(氧乙烯)、f68、f127、聚(羟乙基天冬酰胺)-聚乙二醇-十六烷基胺、聚乙二醇40硬脂酸酯(polyoxyl40stearate)、n-异丙基丙烯酰胺和与n,n'-亚甲基双丙烯酰胺交联的乙烯吡咯烷酮和丙烯酸、pluronicf127和壳聚糖、聚(乳酸)、聚(乙醇酸)、聚(乙二醇)、聚(环氧乙烷)、n-邻苯二甲酰基羧甲基壳聚糖(n-phthaloylcarboxymethylchitosan)、聚(丙烯酸2-乙基己酯)-b-聚(丙烯酸)、聚(丙烯酸叔丁酯)-b-聚(2-乙烯基吡啶)、聚(环氧乙烷)-b-聚己内酯、聚(ε-己内酯)-b-聚(乙二醇)-b-聚(ε-己内酯)、聚(ε-己内酯)-b-聚(甲基丙烯酸)、聚(乙二醇)-b-聚(ε-己内酯-共-三亚甲基碳酸酯)、聚(天冬氨酸)-b-聚丙交酯、聚(乙二醇)-嵌段-聚(天冬氨酸-酰肼)、聚(n-异丙基丙烯酰胺-共-甲基丙烯酸)-g-聚(d,l-丙交酯)和/或硬脂酸接枝的壳聚糖寡糖形成的胶束;khuphe等人(2015)chem.commun.,51:1520-1523中描述的胶束;wo2005/076998a2中描述的胶束;或us2009/0092665a1中公开的胶束,上述文献的全部内容通过引用并入本文。在特定实施方案中,胶束将多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐包封在组合物中。在一些实施方案中,胶束包含多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐,诸如聚{(苯乙烯-alt-马来酸)-共-[苯乙烯-alt-(n-3,4-二羟基苯乙基-马来酰胺酸)]},如chenglin等人(2012)langmuir,28:9211-9222中描述的,该文献的全部内容通过引用并入本文。
在一些实施方案中,渗透增强剂是脂质体。合适的脂质体包括但不限于由二棕榈酰基磷脂酰胆碱诸如蛋磷脂酰胆碱(eggphosphatidylcholine)制备的脂质体;和在以下文献中描述的脂质体:zhigaltsev等人(2001)jliposomeres,11(1):55-71;jain等人(1998)drugdevindpharm,24(7):671-675;wo2014/076709a1;chonn等人(1995)curropinbiotechnol,6:698-708;lasic(1998)trendsbiotechnol,16:307-321;gregoriadis(1995)trendsbiotechnol,13:527-537;szoka和papahadjopoulos(1980)annrevbiophysbioeng,9:467-508;美国专利第4,235,871号;美国专利第4,837,028号;和美国专利公布第2004/0224010a1号。
本发明的组合物还可以另外包含螯合剂。合适的螯合剂包括但不限于氨基羧酸或其盐,诸如edta、氨三乙酸(nitrilotriaceticacid)、氨三丙酸(nitrilotripropionicacid)、二亚乙基三胺五乙酸、2-羟乙基-乙二胺三乙酸、1,6-二氨基-六亚甲基-四乙酸、1,2-二氨基-环己烷四乙酸、o,o'-双(2-氨基乙基)-乙二醇-四乙酸、1,3-二氨基丙烷-四乙酸、n,n-双(2-羟基苄基)乙二胺-n,n-二乙酸、乙二胺-n,n'-二乙酸、乙二胺-n,n'-二丙酸、三亚乙基四胺六乙酸、7,19,30-三氧杂-1,4,10,13,16,22,27,33-八氮杂双环[11,11,11]三十五烷(o-bis-tren)、乙二胺-n,n'-双(亚甲基膦酸)、亚氨基二乙酸、n,n-双(2-羟乙基)甘氨酸(dheg)、1,3-二氨基-2-羟基丙烷-四乙酸、1,2-二氨基丙烷-四乙酸、乙二胺-四(亚甲基膦酸)、n-(2-羟乙基)亚氨基二乙酸、或其组合或盐;特别地edta的药学上可接受的盐或混合盐,诸如二钠盐、三钠盐、四钠盐、二钾盐、三钾盐、锂盐、二锂盐、铵盐、二铵盐、钙盐或钙-二钠盐;最特别地edta二钠。螯合剂可以以在组合物的从约0.01%w/v至1%w/v的范围内的量存在。
本发明的组合物还可以包含通常存在于局部制剂或可注射眼用制剂中的任何其他药学上可接受的赋形剂。例如,组合物还可以包含醇诸如异丙醇、苄醇、鲸蜡硬脂醇或乙醇;润滑剂诸如葡萄糖、甘油、聚乙二醇、聚丙二醇或其衍生物;多糖诸如壳聚糖、壳多糖、皮肤素(dermatan)、透明质酸盐、肝素、软骨素、环糊精或其衍生物;或其组合。
在一些实施方案中,本发明的组合物被配制用于向眼睛局部施用。在这方面,本发明的组合物可以呈滴眼剂或凝胶的形式;特别是滴眼剂。不希望受理论束缚,将组合物配制用于向眼睛局部施用被认为增加使用者的依从性,特别是当组合物被用作预防措施或控制措施时。如果将组合物施用至儿童受试者,这可以是特别重要的。此外,这样的制剂可以降低多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐的脱靶效应(offtargeteffect)的发生率。
在一些实施方案中,本发明的组合物被配制用于多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐穿透角膜上皮。在优选的实施方案中,多于约10%、20%、30%、40%、50%、60%、70%或80%的剂量的多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐穿透角膜上皮。
当配制成滴眼剂或凝胶时,本发明的组合物可以呈单个单位剂型或多个单位剂型,优选地多个单位剂型。
在可选择的实施方案中,本发明的组合物被配制用于直接注射到眼睛中。在特定实施方案中,本发明的组合物被配制用于玻璃体内注射、结膜下注射、前房内注射、巩膜内注射、角膜内注射或视网膜下注射;特别地玻璃体内注射、巩膜内注射或角膜内注射。在一些实施方案中,本发明的组合物被配制用于脉络膜上腔注射(suprachoroidalinjection)。在一些实施方案中,本发明的组合物被配制用于经由微针注射,例如经由巩膜内施用或角膜内施用。
本领域技术人员可以容易地确定组合物的其他赋形剂和组分。用于配制和施用的技术可以在例如remington(1980)remington'spharmaceuticalsciences,mackpublishingco.,easton,pa.,最新版中找到;并且合适的赋形剂可以在例如katdare和chaubel(2006)excipientdevelopmentforpharmaceutical,biotechnologyanddrugdeliverysystems(crc出版社)中找到。
本领域技术人员将熟悉本发明的组合物的组分,并因此将能够容易地合成或获得这些组分,诸如从例如sigmaaldrichco.llc获得。例如,呈多巴胺盐酸盐形式的多巴胺可购自许多来源(诸如sigma-aldrichco.llc),并且合成路线在例如carter等人(1982)analyticalprofilesofdrugsubstances,11:257-272中可获得。
呈多巴胺-1,1,2,2-d4盐酸盐形式的氘代多巴胺可购自sigma-aldrichco.llc,并且氘代多巴胺或氘代多巴胺衍生物的合成路线在例如binns等人(1970)jchemsoc(c),8:1134-1138;wo2004/056724a1;wo2007/093450a1;wo2014/122184a1中可获得;所有上述文献通过引用以其整体并入本文。氘可以使用采用氘代试剂的合成技术和/或通过交换技术来引入到化合物中,这两种技术都是本领域的常规技术。
本发明的组合物可以通过以下来制备:在例如药学上可接受的载体或稀释剂中将组分混合,并且如果需要,将组合物的ph调节至在从4至8、5至7、5.5至6.5的范围内或约5.5、6.0或6.5的ph。可以使用本领域中常规地使用的任何药学上可接受的ph调节剂,诸如盐酸、氢氧化钠等来调节组合物的ph。本领域技术人员将很清楚合适的剂。
本发明的组合物还可以在使用前灭菌,例如通过过滤、高压灭菌法和/或γ辐照。
4.用于预防和治疗视觉障碍的方法
本发明的组合物可用于抑制受试者的视觉障碍的进展或发展,特别是抑制涉及眼睛中降低的多巴胺水平的视觉障碍,诸如与糖尿病视网膜病变或帕金森病相关的视觉障碍、或近视。因此,本发明的组合物可以在抑制受试者的视觉障碍的进展或发展的方法中使用。本发明的组合物还可以用于制造用于本文描述的用途的药物。
本发明的组合物可用于抑制受试者的视觉障碍的进展。在这方面,本发明的组合物可以被用于治疗视觉障碍。在一些实施方案中,本发明的组合物可以减缓受试者的视觉障碍的进展。
本发明的组合物还可用于抑制受试者的视觉障碍的发展。因此,本发明的组合物可用于预防受试者的视觉障碍。在一些实施方案中,本发明的组合物可以延迟受试者的视觉障碍的发病,即可以增加发展视觉障碍时受试者所处的年龄,并且因此延迟视觉障碍的可能的严重性。
视觉障碍可以是涉及眼睛中降低的多巴胺水平的任何视觉障碍,特别是涉及视网膜中降低的多巴胺水平的任何视觉障碍。因此,视觉障碍可以是任何视觉障碍,其中增加眼睛中、特别是视网膜中的多巴胺水平与视觉障碍的进展或发展的有效抑制相关。
存在许多涉及眼睛中降低的多巴胺水平的视觉障碍。例如,视觉障碍可以是,但不限于,与糖尿病视网膜病变或帕金森病相关的视觉障碍、近视、增加的眼睛生长(increasedoculargrowth)、降低的空间和时间对比灵敏度、弱视、视力模糊或复视、眼睛疲劳、主动睁开眼睛的问题(失用症)、眼睑痉挛(eyelidspasm)(睑痉挛(blepharospasm))、过度眨眼、改变的颜色知觉、降低的深度知觉或视幻觉。在一些实施方案中,视觉障碍选自与糖尿病视网膜病变或帕金森病相关的视觉障碍以及近视。在特定实施方案中,视觉障碍是近视。
在一些实施方案中,视觉障碍选自由以下组成的组:与糖尿病视网膜病变或帕金森病相关的视觉障碍、近视、增加的眼睛生长、降低的空间和时间对比灵敏度、弱视、视力模糊或复视、眼睛疲劳、主动睁开眼睛的问题(失用症)、眼睑痉挛(eyelidspasm)(睑痉挛(blepharospasm))、过度眨眼、改变的颜色知觉、降低的深度知觉、色素性视网膜炎、年龄相关性黄斑变性或视幻觉。在一些实施方案中,视觉障碍选自与糖尿病视网膜病变或帕金森病相关的视觉障碍、色素性视网膜炎、年龄相关性黄斑变性以及近视。在特定实施方案中,视觉障碍是近视。
在一些实施方案中,视觉障碍与帕金森病不相关。
在特定实施方案中,视觉障碍是眼睛后段的障碍。合适的障碍包括但不限于与糖尿病视网膜病变或帕金森病相关的视觉障碍、色素性视网膜炎、年龄相关性黄斑变性以及近视。
与帕金森病相关的视觉障碍包括但不限于降低的视敏度、降低的对比灵敏度和/或颜色辨别障碍。
与糖尿病视网膜病变相关的视觉障碍包括但不限于降低的视敏度、降低的对比灵敏度和降低的周边视野。
该方法包括向受试者施用本发明的组合物。本发明的组合物可以通过局部施用到眼睛表面或经由直接注射到眼睛中来局部地施用。
在一些实施方案中,组合物以例如滴眼剂或凝胶的形式局部地施用至眼睛。在优选的实施方案中,组合物作为滴眼剂被应用。本发明的组合物可以被应用于眼睛的任何表面,优选地角膜/巩膜,从而允许组合物中存在的组分,特别是多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐穿透到眼睛中。在一些实施方案中,组合物被配置成使得多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐穿透角膜上皮。
在其他实施方案中,组合物通过注射到眼睛中来施用。例如,组合物可以直接注射到巩膜、前房或玻璃体中,或者可以注射到结膜下的空间、球周的空间、球后的空间或脉络膜上腔的空间中。在特定实施方案中,本发明的组合物经由以下来施用:玻璃体内注射、结膜下注射、前房内注射、巩膜内注射、角膜内注射或视网膜下注射;特别是玻璃体内注射、巩膜内注射或角膜内注射。在一些实施方案中,本发明的组合物经由脉络膜上腔注射来施用。在一些实施方案中,本发明的组合物通过玻璃体内注射来施用。在其他实施方案中,本发明的组合物使用微针来注射,例如经由巩膜内施用或角膜内施用。为了经由这些途径施用,本发明的组合物可以呈无菌可注射溶液的形式。
本发明的组合物被优选地施用于其中或其上的眼睛的部分是允许组分,特别是多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐穿透到眼睛中,优选地穿透到视网膜中的部分。优选地在角膜/巩膜和结膜上进行施用以用于局部施用,或者可以将组合物注射到结膜下的空间、球周的空间、球后的空间或脉络膜上腔的空间中,或注射到巩膜、角膜、前房或玻璃体中。
当局部地应用时,本发明的组合物可以与硬性隐形眼镜和软性隐形眼镜两者一起使用。
根据本领域技术人员熟知的方法,可以为不同的适应症建立剂量方案。组合物的剂量将取决于待治疗的状况、受试者的年龄和施用途径。
本发明的组合物可以以合适的量局部地施用或通过注射施用,以便提供在从0.001mg/kg/天至12mg/kg/天、特别地从0.001mg/kg/天至4mg/kg/天、更特别地从0.001mg/kg/天至2mg/kg/天的范围内的多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐的剂量。在一些实施方案中,组合物以合适的量施用,以便提供在从0.001mg/kg/天至30mg/kg/天,特别地从0.001mg/kg/天至12mg/kg/天,更特别地从0.001mg/kg/天至4mg/kg/天,最特别地从0.001mg/kg/天至2mg/kg/天的范围内的多巴胺、氘代多巴胺、氘代多巴胺衍生物或其药学上可接受的盐的剂量。
当作为滴眼剂局部地施用时,本发明的组合物可以以在从每只眼睛1滴至每只眼睛6滴(以及其间的所有整数)的范围内的量被施用,这可以等于例如在从每只眼睛约0.04ml至每只眼睛0.24ml(以及其间的所有整数)的范围内的量。可以将滴剂每天从1次至4次地应用于每只眼睛。当本发明的组合物被配制成凝胶时,提供等效剂量。技术人员将知道用于局部应用本发明的组合物的合适的分配器。
当通过注射施用时,本发明的组合物可以以在从0.001ml至0.5ml(以及其间的所有整数)的范围内的量施用,特别地约0.01ml。本发明的组合物可以以每周一次至每天一次的频率施用。
为了本发明可以易于理解以及付诸实践,现在将通过以下非限制性实施例的方式描述特定的优选实施方案。
实施例
实施例1-多巴胺组合物的制备
为了制备150mm的储备溶液,将28.4mg多巴胺(呈多巴胺盐酸盐的形式,可购自sigma-aldrichco.llc)溶解在1ml的含有在l×pbs(ph约5.5)中的0.1%抗坏血酸的溶液中。将储备溶液进一步稀释在适当体积的含有在l×pbs中的0.1%抗坏血酸的溶液中,以产生0.15mm(0.0028%w/v)、1.5mm(0.028%w/v)和15mm(0.28%w/v)的溶液。
通过向1ml上文制备的多巴胺溶液添加适当量的阿托品(呈硫酸阿托品一水合物的形式,可购自sigma-aldrichco.llc)、哌仑西平(呈哌仑西平二盐酸盐的形式,可购自sigma-aldrichco.llc)或tpmpa(呈tpmpa水合物形式的(1,2,5,6-四氢吡啶-4-基)甲基次膦酸,可购自sigma-aldrichco.llc)来制备组合溶液。
实施例2-多巴胺组合物对于形觉剥夺性近视发展的作用
30只白色雄性小公鸡被随机分配到如下文定义的6个处理组中的一个(每组n=5),并且处理持续4天时间。
·在它们的左眼上装有半透明漫射体以诱导形觉剥夺性近视(fdm)的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例1制备的1.5mm(0.028%)多巴胺溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例1制备的1.5mm(0.028%)多巴胺溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例1制备的15mm(0.28%)多巴胺溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例1制备的15mm(0.28%)多巴胺溶液的雏鸡;
·年龄匹配的未处理的对照组。
对于药物处理,使用玻璃体内注射或局部施用,在轻度异氟醚麻醉(lightisofluraneanesthesia)下施用组合物。
玻璃体内注射如下进行:使用附接至hamilton注射器的30号针,每天一次地将10μl(0.01ml)的测试组合物注射到眼睛的玻璃体腔中。
局部施用如下进行:使用滴眼剂分配器将两滴40μl的(0.04ml的两滴,或总共0.08ml)的测试组合物应用至眼睛的角膜表面。每天两次地将滴剂应用至雏鸡。
为了确定眼睛生长速率和近视发展的变化,评估了轴向长度的变化。近视与眼睛相对于正常生长速率在轴向上的过度伸长相关。轴向长度、前房深度和玻璃体腔深度使用a-scan超声波检查(biometeral-100;tomeycorporation,nagoya,japan)来测量。组之间的轴向长度、前房深度和玻璃体腔深度的变化的统计学分析涉及单向anova检验,随后是具有bonferroni校正的student'st检验。所有数据都以平均值±平均值的标准偏差(sem)表示。
结果
结果在图1中呈现。经由玻璃体内注射施用多巴胺溶液显著抑制与形觉剥夺性近视相关的轴向伸长(fdm;9.12±0.05mm)(anova,f(3,23)=6.934,p=0.002;图1)。相对于在仅用漫射体处理的对应者中所看到的情况,两种研究的多巴胺浓度(1.5mm和15mm)均显著抑制与形觉剥夺性近视相关的轴向伸长(1.5mm:8.82±0.02mm,78%保护,p<0.05;15mm:8.82±0.11mm,78%保护,p<0.05)。此外,用两种浓度的多巴胺处理的眼睛的轴向长度与年龄匹配的未处理的雏鸡的眼睛在统计学上没有差异(8.74±0.04mm,两种浓度p=1.000)。在所有条件中,前房深度(anova,f(3,23)=0.348,p=0.791)或晶状体厚度(anova,f(3,23)=2.613,p=0.077)没有显著差异。相反,与漫射体磨损和多巴胺的玻璃体内注射相关的轴向长度的变化代表玻璃体腔深度的变化(anova,f(3,23)=6.112,p=0.003)。
当多巴胺溶液以每天两次局部滴眼剂施用时,与漫射体磨损相关的过度生长(anova,f(3,23)=14.978,p<0.000;图1)被抑制。具体地,与形觉剥夺性近视相关的过度生长以剂量依赖性方式受到抑制,其中在15mm的浓度观察到显著作用(8.84±0.07mm,相对于仅fdm有72%保护,p<0.01),此时经漫射体处理的眼睛在轴向长度上与未处理的对照眼睛在统计学上没有差异(p=0.191)。在所有测试的条件中,前房深度(anova,f(3,23)=0.348,p=0.791)和晶状体厚度(anova,f(3,23)=2.613,p=0.077)没有显著差异。相反,与漫射体磨损和多巴胺的局部施用相关的轴向长度的变化代表玻璃体腔深度的变化(anova,f(3,23)=9.811,p<0.000)。
实施例3-多巴胺与阿托品、哌仑西平和tpmpa的共同处理对于形觉剥夺性近视发展的作用
70只白色雄性小公鸡被随机分配到如下文定义的14个处理组中的一个(每组n=5),并且处理持续4天时间。
·在它们的左眼上装有半透明漫射体以诱导fdm的雏鸡;
·年龄匹配的未处理的对照组;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例1制备的0.15mm(0.0028%)多巴胺溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射0.25mm(0.018%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例1制备的0.15mm(0.0028%)多巴胺和0.25mm(0.018%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射17mm(0.72%)哌仑西平溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例1制备的0.15mm(0.0028%)多巴胺和17mm(0.72%)哌仑西平溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射18.6mm(0.29%)tpmpa溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例1制备的0.15mm(0.0028%)多巴胺和18.6mm(0.29%)tpmpa溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例1制备的1.5mm(0.028%)多巴胺溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用50mm(3.5%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例1制备的1.5mm(0.028%)多巴胺和50mm(3.5%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用18.6mm(0.29%)tpmpa溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例1制备的1.5mm(0.028%)多巴胺和18.6mm(0.29%)tpmpa溶液的雏鸡。
通过将硫酸阿托品一水合物溶解在含有在1×pbs中的0.1%抗坏血酸的溶液中至0.25mm(0.018%w/v)或50mm(3.5%w/v)的最终浓度并且将ph调节至7来制备阿托品溶液。通过将哌仑西平二盐酸盐溶解在含有在1×pbs中的0.1%抗坏血酸的溶液中至17mm(0.72%w/v)的最终浓度并且将ph调节至7来制备哌仑西平溶液。通过将tpmpa水合物溶解在含有在1×pbs中的0.1%抗坏血酸的溶液中至18.6mm(0.29%w/v)的最终浓度并且将ph调节至7来制备tpmpa溶液。
根据实施例2中描述的进行测试组合物的施用和眼参数的测量。
结果
结果在图2和图3中呈现。通过玻璃体内注射单独施用或与多巴胺(0.15mm)组合施用阿托品,一种毒蕈碱乙酰胆碱受体拮抗剂;哌仑西平,一种ml毒蕈碱乙酰胆碱受体拮抗剂;和tpmpa,一种gabac受体拮抗剂;显著抑制与形觉剥夺性近视相关的过度轴向伸长(anova,f(8,53)=7.894,p<0.000;图2)。重要的是,与单独施用这些化合物时相比,将多巴胺与三种化合物中的任何一种组合,在形觉剥夺性近视被抑制的程度上引起小但显著的改善(多巴胺与阿托品:8.76±0.02mm,p<0.000;多巴胺与哌仑西平:8.76±0.03mm,p<0.000;多巴胺与tpmpa:8.60±0.07mm,p<0.000)。在所有测试的条件中,前房深度(anova,f(8,53)=0.426,p=0.900)或晶状体厚度(anova,f(8,53)=1.349,p=0.241)没有显著差异。相反,与漫射体磨损和测试化合物的玻璃体内注射相关的轴向长度的变化代表玻璃体腔深度的变化(anova,f(8,53)=7.561,p<0.000)。
单独的或与阿托品或tpmpa组合的多巴胺(1.5mm)的局部施用显著抑制由形觉剥夺性近视驱使的过度轴向伸长(anova,f(6,61)=7.357,p<0.000;图3)。由于前房深度(anova,f(6,61)=0.624,p=0.710)或晶状体厚度(anova,f(6,61)=1.534,p=0.183)两者均没有因处理而改变,所以轴向长度的变化代表玻璃体腔深度的变化(anova,f(6,61)=6.703,p<0.000)。如图3中可以看到的,多巴胺和阿托品的组合(多巴胺:8.97±0.08mm,p=0.448;阿托品:8.79±0.09mm,p=0.030;多巴胺与阿托品:8.67±0.05mm,p=0.001),以及多巴胺和tpmpa的组合(tpmpa:8.85±0.05mm,p=0.062;多巴胺与tpmpa:8.69±0.03mm,p<0.000)与单独的每种化合物相比,显著增加形觉剥夺性近视被抑制的程度。
实施例4-多巴胺-1,1,2,2-d4组合物的制备
为了制备150mm的储备溶液,将29mg多巴胺-1,1,2,2-d4(呈多巴胺-1,1,2,2-d4盐酸盐的形式,可购自sigma-aldrichco.llc)溶解在1ml的含有在l×pbs(ph约5.5)中的0.1%抗坏血酸的溶液中。将储备溶液进一步稀释在适当体积的含有在l×pbs中的0.1%抗坏血酸的溶液中,以产生0.15mm(0.0029%w/v)、1.5mm(0.029%w/v)和15mm(0.29%w/v)的溶液。
通过向上文制备的1ml多巴胺-1,1,2,2-d4溶液添加适当量的阿托品(呈硫酸阿托品一水合物的形式,可购自sigma-aldrichco.llc)或tpmpa(呈tpmpa水合物的形式,可购自sigma-aldrichco.llc)来制备组合溶液。
实施例5-多巴胺-1,1,2,2-d4组合物对于形觉剥夺性近视发展的作用
30只白色雄性小公鸡被随机分配到如下文定义的6个处理组中的一个(每组n=5),并且处理持续4天时间。
·在它们的左眼上装有半透明漫射体以诱导fdm的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例4制备的15mm(0.29%)多巴胺-1,1,2,2-d4溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例4制备的1.5mm(0.029%)多巴胺-1,1,2,2-d4溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例4制备的15mm(0.29%)多巴胺-1,1,2,2-d4溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例4制备的1.5mm(0.029%)多巴胺-1,1,2,2-d4溶液的雏鸡;
·年龄匹配的未处理的对照组。
根据实施例2中描述的进行测试组合物的施用和眼参数的测量。
结果
结果在图4中呈现。玻璃体内施用多巴胺-1,1,2,2-d4溶液显著抑制与形觉剥夺性近视相关的轴向生长(anova,f(3,22)=13.562,p<0.000;图4)。如图4中可以看到的,相对于仅用漫射体处理的动物中看到的轴向伸长,所测试的两种浓度的多巴胺-1,1,2,2-d4(1.5mm和15mm)展示出类似水平的保护(1.5mm:8.77±0.11mm,92%保护,p<0.001;15mm:8.72±0.06mm,103%保护,p<0.001)。以两种浓度的多巴胺-1,1,2,2-d4,漫射体处理的眼睛的轴向长度与其年龄匹配的未处理的对应者没有差异(1.5mmp=0.686,15mmp=0.707)。在所有测试的条件中,前房深度(anova,f(3,24)=0.646,p=0.594)和晶状体厚度(anova,f(3,24)=1.627,p=0.213)两者均没有显著差异。相反,与漫射体磨损和多巴胺的玻璃体内注射相关的轴向长度的变化代表玻璃体腔深度的变化(anova,f(3,24)=9.592,p<0.000)。
局部应用多巴胺-1,1,2,2-d4溶液显著抑制形觉剥夺性近视(anova,f(3,24)=5.346,p=0.006;图4)。与多巴胺一样,通过局部应用多巴胺-1,1,2,2-d4,以剂量依赖性方式抑制与形觉剥夺性近视相关的过度生长,在15mm的浓度观察到显著的作用(8.85±0.14mm,相对于仅fdm有71%保护,p<0.01),此时漫射体处理的眼睛与未处理的对照眼睛在轴向长度上在统计学上没有差异(p=0.407)。在所有条件中,前房深度(anova,f(3,24)=0.303,p=0.823)和晶状体厚度(anova,f(3,24)=0.436,p=0.730)两者均没有显著差异。相反,与漫射体磨损和多巴胺的局部施用相关的轴向长度的变化代表玻璃体腔深度的变化(anova,f(3,24)=4.379,p=0.015)。
实施例6-多巴胺-1,1,2,2-d4与阿托品和tpmpa的共同处理对于形觉剥夺性近视发展的作用
60只白色雄性小公鸡被随机分配到如下文定义的12个处理组中的一个(每组n=5),并且处理持续4天时间。
·在它们的左眼上装有半透明漫射体以诱导fdm的雏鸡;
·年龄匹配的未处理的对照组;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例4制备的0.15mm(0.0029%)多巴胺-1,1,2,2-d4溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射0.25mm(0.018%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例4制备的0.15mm(0.0029%)多巴胺-1,1,2,2-d4和0.25mm(0.018%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射18.6mm(0.29%)tpmpa溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天玻璃体内注射根据实施例4制备的0.15mm(0.0029%)多巴胺-1,1,2,2-d4和18.6mm(0.29%)tpmpa溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例4制备的1.5mm(0.029%)多巴胺-1,1,2,2-d4溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用50mm(3.5%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例4制备的1.5mm(0.029%)多巴胺-1,1,2,2-d4和50mm(3.5%)阿托品溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用18.6mm(0.29%)tpmpa溶液的雏鸡;
·在它们的左眼上装有半透明漫射体并且每天两次局部施用根据实施例4制备的1.5mm(0.029%)多巴胺-1,1,2,2-d4和18.6mm(0.29%)tpmpa溶液的雏鸡。
根据实施例3制备阿托品和tpmpa溶液。根据实施例2中描述的进行测试组合物的施用和眼参数的测量。
结果
结果在图5和图6中呈现。经由玻璃体内注射的与阿托品或tpmpa组合的多巴胺-1,1,2,2-d4的施用,或者经由玻璃体内注射的这些化合物中的每一种的单独施用,显著抑制与形觉剥夺性近视相关的过度轴向伸长(anova,f(6,44)=16.918,p<0.000;图5)。重要的是,与单独施用这些化合物时相比,将多巴胺-1,1,2,2-d4与tpmpa组合,在形觉剥夺性近视被抑制的程度上引起小但显著的改善(多巴胺-1,1,2,2-d4与tpmpa:8.61±0.05mm,p=0.014)。与单独施用这些化合物相比,将多巴胺-1,1,2,2-d4与阿托品组合,在形觉剥夺性近视被抑制的程度上产生小但不显著的改善(多巴胺-1,1,2,2-d4与阿托品:8.73±0.07mm,p=0.068)。在所有条件中,前房深度(anova,f(6,44)=0.508,p=0.809)或晶状体厚度(anova,f(6,44)=0.626,p=0.708)没有显著差异。相反,与漫射体磨损和测试化合物的玻璃体内注射相关的轴向长度的变化代表玻璃体腔深度的变化(anova,f(6,44)=12.758,p<0.000)。
单独的或与阿托品或tpmpa组合的多巴胺-1,1,2,2-d4(1.5mm)的局部施用显著抑制与形觉剥夺性近视相关的轴向生长(anova,f(6,57)=4.616,p=0.001;图6)。前房深度(anova,f(6,57)=0.615,p=0.718)或晶状体厚度(anova,f(6,57)=0.866,p=0.526)没有显著差异,相反,轴向长度的变化是由玻璃体腔深度的变化引起的(anova,f(6,57)=5.485,p<0.000)。虽然在多巴胺-1,1,2,2-d4和tpmpa的组合的情况下观察到形觉剥夺性近视的增加的抑制(多巴胺-1,1,2,2-d4:8.88±0.10mm,p=0.105;tpmpa:8.85±0.09mm,p=0.062;多巴胺-1,1,2,2-d4与tpmpa:8.80±0.03,p=0.015),但在多巴胺-1,1,2,2-d4与阿托品的组合的情况下未观察到相同的作用(阿托品:8.79±0.09mm,p=0.030;多巴胺-1,1,2,2-d4与阿托品:8.80±0.11mm,p=0.070)。
本文所引用的每个专利、专利申请和出版物的公开内容据此通过引用以其整体并入本文。
本文中的任何参考文献的引用不应当被解释为承认这样的参考文献可用作本申请的“现有技术”。
在整个说明书中,目的是描述本发明的优选实施方案,而不是将本发明限制于任何一个实施方案或特征的特定集合。因此,本领域技术人员应理解,根据本公开内容,可以在例示的特定实施方案中进行各种修改和改变而不偏离本发明的范围。所有此类修改和改变意图被包括在所附权利要求的范围内。
- 还没有人留言评论。精彩留言会获得点赞!
- SPNP‑I在制备Nav1.7通道工具试剂中的应用的制造方法与工艺
- SPNP‑I在制备Nav1.2通道工具试剂中的应用的制造方法与工艺
- SPNP‑IX在制备Nav1.3通道抑制剂中的应用的制造方法与工艺
- SPNP‑IX在制备Kv4.2通道工具试剂中的应用的制造方法与工艺
- SPNP‑IX在制备Kv4.3通道工具试剂中的应用的制造方法与工艺
- SPNP‑27在制备Nav1.5通道抑制剂中的应用的制造方法与工艺
- SPNP‑27在制备Nav1.3通道抑制剂中的应用的制造方法与工艺
- 一种多肽在制备Nav1.3钠通道工具试剂中的应用的制造方法与工艺
- SPKP‑XI在制备Kv4.2通道抑制剂中的应用的制造方法与工艺
- SGLT‑2糖尿病抑制剂及其中间体的制备方法